oi oi gente tudo bom então hoje a gente vai ver a nossa unidade 4 atividade que não aguentam os metais alcalinos e os metais alcalinos eles são compostos por um grupo de álcool de seis elementos chatos cobertos em são lítio sódio potássio rubídio e césio e fácil o nome alcalinos ele vem da palavra álcool o que significa cinzas por quê que esse nome porque eles eram encontrados principalmente componentes das cinzas de árvores queimadas a característica principal do grupo a camada de valência terminando em s1 normalmente ele é um grupo bastante homogêneo como assim as propriedades
variam regularmente entre os elementos do grupo todos eles são natais e a grande característica do grupo é que eles são bastante reativo porque eles têm porque eles têm o elétron fracamente ligada ao no vamos agora falar um desses elementos o primeiro elemento descoberto foi sódio e potássio o descobridor foi um químico famoso conhecido como hum verdade ele isolou os dois elementos através de um processo conhecido como a eletrólise ígnea o que é o processo de eletrólise ígnea é quando você pega no sal e aquece a pele fundir uma vez que o sol atinge o estado
líquido você passa uma corrente elétrica por dentro desse sal e você vai gerar os alimentos a partir do composto ou no caso o elemento gerado foi sódio e potássio o próximo elemento a ser descoberto foi o lítio em 1817 ele foi isolada a partir de análise quantitativa de um mineral chamado de pé talita e ele é um alumínio silicato de lítio os próximos elementos a ser descoberta por uma dupla bastante famosa o banco ser que fez aquele tubinho de gás que a gente utiliza no laboratório e e aí chefe também é famoso por algumas equações
e leis dentro daquele então em 1860 o sesi ele foi só lá e ele foi reconhecido como elemento a partir de linhas espectrais ou seja usada se a ionização de chama do composto composto absorver energia da chama se esse tava produziu uma cor essa cola é composta cada elemento ele tem uma sequência de linhas de cores diferentes então foi descoberto o alimento que não tinha um padrão conhecido devido as linhas espectrais azul celeste se ela é bem ficou conhecido como sérgio um ano depois outra vez foi descoberto pelo mesmo processo quero que o vídeo esse
nome que o vídeo ele vem a partir das linhas espectrais do elemento no caso às vezes até que traz vermelho o último elemento do grupo o frâncio ele só foi descoberto em 1939 ele existe por um pequeno intervalo de tempo através do e o radioativo do latim quartinho de massa 225 ele vai dar cair emite uma partícula alfa e vai formar o francílio o tempo de minha vida dessa reação é de 10 dias o que vai acontecer o france logo em seguida ele sofre um novo da caimento onde ele vai se converter em rádio emitindo
assim uma partícula beta negativo então o tempo de meia-vida do frâncio é de 22 minutos por isso que esse elemento isso existem na ordem de trás e pequeníssima quantidade vamos agora falar das propriedades físicas dos metais a primeira propriedade física que a gente vai falar energia de quais anos o que que esse energia de coesão é como se fosse a força da ligação na clínica ou seja quanto maior for a cirurgia de correção mais forte a ligação e o quê que isso afeta as propriedades físicas do elemento vai afetar é chamado tem na cidade que
a capacidade de resistir a fortes não ama esses elementos têm uma baixa tenacidade o que que eles têm uma baixo até na cidade porque ele só tem 1 elétron na camada de valência então a ligação metálica deles é fraca tanto que esses elementos eles conseguem ser cortados por uma faca comum como é que varia essa energia ao longo do grupo quanto menor o raio mais forte a ligação então essa energia de ligação ou a dureza do metal vai aumentar do césio até o lítio como vocês estão vendo aqui com relação a cor dos elementos acordo
um composto ele vai ser a soma da cor do cátion com a cor do ano todos os cátions dos elementos da família um ar eles não tem cor ou seja eles tendem a formar compostos branco o pessoal ele sempre vai formar compostos brancos não porque também depende da cor do union são alguns anos e por resenha o ânion o dicromato o ano cromato e o ano permanganato o cromato formas compostos laranjas o cromato amarelo arte e o permanganato de cor violeta escuro agora a gente vai verificar as propriedades químicas desses metais então vamos começar com
a reação com a atmosfera todos esses elementos eles vão reagir com o oxigênio ou o de oxigênio da atmosfera a reação com um de oxigênio ela é rápida e esses alimentos rapidamente eles vão perder o brilho o que vai diferenciar é o tipo de produto formado em cada reação no caso do lítio ele vai formar majoritariamente o óxido de lítio no caso do sódio ele forma majoritariamente o peróxido de sódio e os demais elementos eles tendem a formar super opus o hidrogênio uma molécula de dois ela normalmente aí né no entanto os metais alcalinos que
são muito o que que vai acontecer ela acaba reagindo com quem com o lixo então se o lítio ele ficar exposto com nitrogênio nitrogênio deixa de ser né elas político para formar o nitreto de leite você é muito reativos eles reagem violentamente com água e você colocar eles em contato com a água e tende a excluir a explosão ela vai aumentar de intensidade de acordo com a reatividade do elemento ou seja vai ser menos reativo no leite e acaba sendo mais reativo no sesi inclusive esses elementos eles conseguem reagir com a umidade do ar então
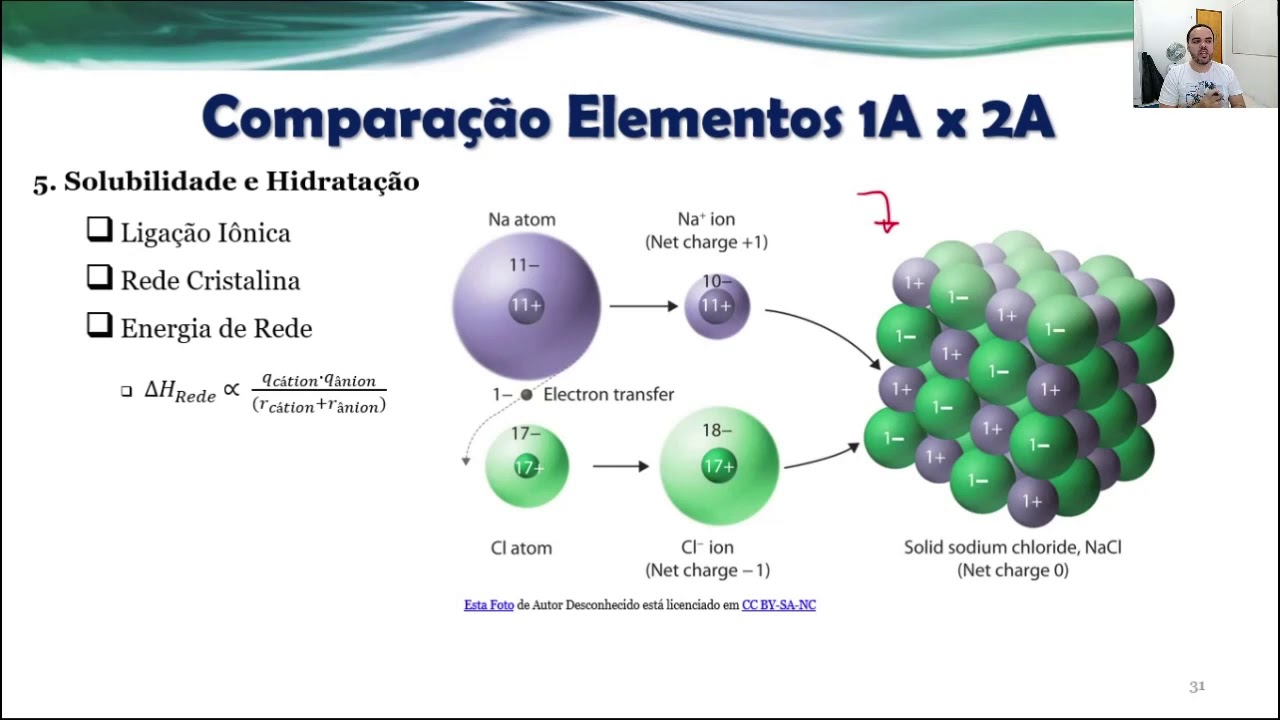
o armazenamento de um metal alcalino no laboratório ela tem que ter o máximo de cuidado inclusive esses elementos a gente tem que ser guardados dentro de um solvente orgânico como querosene para evitar o contato com a umidade do ar vamos começar a falar agora dos compostos e as propriedades desses compostos começando pelo sido e os hidróxidos de alarme essa família saudades fotos em geral são higroscópicas que que significa higroscópica ela absorve a umidade do ar no caso dos elementos da família a eles absorvem tanto a umidade que chegam a dissolver na própria unidade acabei de
solteiro dentre esses produtos os produzidos em maior quantidade estão a soda cáustica que é produzida em média 38,7 tão levar furando e a potassa cáustica que é o hidróxido de potássio a solubilidade dessas malas quanto maior raio nessa alcalino mais solúvel vai ser a base e também mais forte próximo sou a gente aprenda a química geral que todos os bases natal localização fotos são forte sim mas existe uma mais forte que a outra a medida que você desce no grupo a força da base fica maior então o hidróxido de césio ele é mais forte do
rubídio é mais forte do que eu de potássio que é mais forte por de sódio que por fim é mais eu pude vídeo agora a gente vai ver as reações dos idosos a ração que a gente está mais acostumada é chamada de reação de neutralização o hidróxido como é base ele tende a reagir com a função aposta ele que a funcionar no caso aqui a gente tá exemplificando colocando uma base genética esse m pode ser qualquer um dos metais alcalinos e reagindo com o ácido clorídrico ao reagir com ácido clorídrico ocorre uma reação de dupla
troca aonde vai formar um cloreto do metal alcalino e no final você vai ter a professor essa é a única relação que tem não tem várias outras por exemplo os hidróxidos metais alcalinos eles são capazes de reagir com o gás carbônico produzido o carbonato que é o m2 co3u nesse n pode ser qualquer um dos metais alcalinos e água além dessas relações eles conseguem reagir com sais de amônio o amônio o pato mais em caixa positivo e durante quando você coloca e presença de um hidróxido o hidróxido ele tira o hidrogênio através de uma reação
ácido-base de bronsted-lowry produzido o gás amônia um sal e água uma raça muito importante para o nosso cotidiano é uma reação chamada de saponificação eu só que significa uma saponificação significa uma reação de produção de sabão como é que é feito o sabão professor você pega normalmente uma gordura ou óleo pode ser um óleo vegetal e esse óleo você vai reagir com o hidróxido de sódio o óleo ele é um triglicerídeo seja e vai ser um triester orgânico o hidróxido ele vai quebrar a cadeia desse triestre formando com o produto a glicerina que esse composto
aqui e vai formar três moléculas de sabão o professor qual é a diferença do samu que o sabonete o sabão ele vai ser o sal de as carboxílico que é só essa parte aqui se você quiser colocar um pouquinho de glicerina para tornar o produto pouquinho mais hidratante o sabão para glicerina e já muda de nome ele é chamado de sabonete agora a gente vai ver os superóxidos e o super ó fiz aqui eu coloquei só umas propriedades mais básicas para gente ser mais objetivo com esse copo então vou falar do peróxido de sódio ele
é um poderoso oxidante ou seja ele vai entender a oxidar algum material nessa oxidação ele normalmente leva ao branqueamento do material por isso que ele vai ser bastante utilizado no branqueamento da polpa de madeira podem ser utilizado na indústria têxtil para branquear tecidos e também para bloquear papel outro produto importante é o superóxido de potássio o superóxido de potássio ele é bastante utilizado na máscara dos bombeiros o que o que é o superóxido de potássio ele tem a capacidade de reagir com o gás carbônico o bombeiro quando ele entra na região onde está tendo incêndio
se ele entrou no recinto fechado a quantidade de oxigênio naquele recinto é muito baixa para uma pessoa conseguir te esperar então ele desmaiar e se alimentar sem máscara e qual é o papel do superóxido de potássio ele vai produzir oxigênio a partir do céu dois então ele reage com o céu dois vai produzir o carbonato de potássio e vai produzir oxigênio para o bombeiro respirar um produto importantíssimo dos metais alcalinos o bicarbonato de sódio o bicarbonato de sódio aqui também é vendido como fermento químico por que que ele é vendido como fermento químico porque uma
vez que misturar na massa na hora que você vai aquecer o bolo ou pão ele vai sofrer uma decomposição térmica e os bicarbonatos como se deco com eles vão produzir três produtos o carbonato de sódio a água e o gás e o gás carbônico ele vai ser formado na forma de pequenas bolinhos que vai fazer com que a massa xixi que você quando corta o pão ou bolo você vai perceber pequenos buraquinhos lá dentro é justamente a região onde o céu dois foi formado além disso o bicarbonato de sódio ele um sal com características básicas
então ele pode ser utilizado como antiácido ele também vai ou ser utilizado em produtos farmacêuticos no caso dentista ele também utiliza na higiene bucal na parte de remoção de placas bacterianas quem vai fazer limpeza no dente espécie de vez em quando o dentista dá um jato uma coisa muito salgada na boca quando ele vai fazer a escovação e se essa coisa salgada que o dentista usa é o bicarbonato de sódio ele também é utilizada em extintores de incêndio cerca de 10 por cento da produção global dele é voltada para esse fim mas a maior parte
ainda é utilizada na produção do fermento químico e a gente vai ver os métodos de obtenção desses alimentos esses alimentos eles vão ser obtidos a partir de eletrólise e ou seja você pega a matéria-prima desse composto converte no cloreto porque um cloreto porque os coleção aumente eles têm baixo ponto de fusão então faz a eletrólise passa para o estado líquido passa corrente elétrica separa a história de um lado como a gente tá vendo aqui o equipamento o gás for ele vai subir aqui e do outro lado você vai ter o metal alcalino na forma líquida
e logo em seguida ele volta para o estado só o sódio ele vai ser produzido a partir do cloreto de sódio o potássio ele pode ser produzido a partir desses dois minerais é o ortoclase e a sil vita no caso do rubídio ele pode ser obtido a partir de três minerais valeu cita apolo cita e assim maldita o sérgio ele vai ser produzido a partir da onu cita que esse composta aqui um papo cita pesado ela tem basicamente césar ainda tem que pequenas doses de rubídio é por isso que ela também é utilizada para produzir
um convite agora a gente vai ver as principais aplicações desses alimentos o lítio ele pode ser utilizado em farma certa ele vai age no sistema nervoso combatendo sintomas de depressão da doença de alzheimer e também pode ser utilizar no transtorno bipolar ele também é utilizado muito em baterias eletrônicas essas baterias são utilizadas em computadores notebooks tablets e calculadoras também e também pode ser utilizado como reagente de partida para síntese orgânica próximo elemento é só as utilidades do sódio em vai ser utilizado na regulação da pressão osmótica do sangue tem que está relacionado com a pressão
começou a sentir desmaio a pressão está baixa é normal a gente pegar um pouquinho de sódio colocá la boca que a pressão volta a subir ele também está presente na atividade mus e ele também vai ser utilizado na iluminação pública então se você tiver andando na rua e vê perto lá no terceiro aquela lâmpadas e amarela acendendo aquela lampada ali é vapor de sódio e ele também pode ser utilizado na fabricação de detergentes vamos agora o potássio o potássio como sódio ele também está relacionado com a regulação da pressão sanguínea e da atividade muscular através
de um processo biológico chamado de bomba de sódio e de potássio além disso ele é um componente importante para as plantas sendo utilizado como fertilizante na forma de nitrato de potássio ele também vai ser utilizada material de limpeza formação de cristais também pode ser utilizado na fabricação de sabão e creme de barbear e o rubídio ele tem um papel importante na medicina ele vai ser utilizado no tratamento da epilepsia ele pode ser utilizado no processo de separação de ácidos nucleicos e vírus e também pode ser utilizado na medicina nuclear na forma de um isótopo radioativo
no combate ao câncer com relação à aplicação tecnológica do rubídio objeto pode ser aplicado em síntese de materiais para a tecnologia de fibra ótica que é o que a gente utiliza para internet ficar mais rápida além disso agora a gente vai para o sesc a última lamenta o sesi é muito utilizado na medicina no tratamento do câncer na forma de um isótopo radioativo e também é utilizado na tecnologia de relógios atômicos e da produção de energia nuclear a e em células fotoelétricas o césio ele ganhou uma certa notoriedade através de um acidente que ocorreu em
goiás e o hospital de fechou e os resíduos de seus artigos utilizados pelo hospital eles foram jogados no lixão a população foi lá começou a mexer conseguir um abrir a bomba e viu aquela coisa verde brilhosa que é que eles fizeram começar a passar no corpo então nessa negócio de passar no corpo acabou que muitas pessoas acabam contraindo cansa então coisa a gente termina o nosso resumo básico de metais alcalinos









![Tudo Sobre Química Inorgânica - Elementos de Simetria [Módulo 3]](https://img.youtube.com/vi/5tX-ejQ-Rt0/maxresdefault.jpg)






![Tudo Sobre Química Inorgânica - Retículo Cristalino [Módulo 5]](https://img.youtube.com/vi/aBm4F2UlVI0/maxresdefault.jpg)



