e na aula de hoje nós vamos aprender sobre a construção da tabela periódica e Imagine que você seja um professor no fim do século 19 e você tem a importante missão de ensinar química para os seus alunos naquela época já eram conhecidos os 63 elementos mas não havia ainda uma forma lógica de organizá-los como então trabalhar com tantos elementos de forma que os alunos pudessem compreendeu uma tarefa desafiadora não é mesmo demitri Ivanovich mendeleev foi um químico e físico Russo e ficou seriamente empenhado em resolver esse impasse é dito que mandalas disse algo como o
edifício da ciência requer não apenas material mas também um plano e necessita do trabalho de preparar estes materiais colocá-los juntos elaborar os planos e proporções simétricas das várias partes e enfim o que média leve quis dizer é que deveria haver um sistema de organização que facilitasse o estudo EA compreensão da química o mangá leve era um grande fã de jogos de cartas em especial o chamado paciência em que as cartas são organizadas em várias colunas respeitando a ordem de grandeza e as cores das cartas Mega leve resolveu então criar uma carta para cada um dos
63 elementos conhecidos cada carta com tio símbolo do elemento a massa atômica e suas propriedades dizem que mendelev carregou essas cartas para todos os lugares durante 3 exaustivos dias ele conta que ficou tão cansado que caiu no sono enquanto trabalhava e foi então que ele sou eu com uma tabela onde cada elemento se encaixava em lugar exato assim que acordou nem de leve começou o seu trabalho de ordenar periodicamente os elementos no que mais tarde seria o seu trabalho mais famoso e para entendermos o raciocínio de mendelev Vamos fazer um exercício de simular como ele
organizaria apenas essas 21 cartas vamos começar por organizar as cartas em fileiras horizontais e em ordem crescente de massa atômica temos então lítio com massa de 6,94 o berílio com 9,01 o boro com 10,81 e assim por diante até chegarmos o elemento sódio e é aí que está grande sacada de mendelev em vez de darmos continuidade a esta fileira Vamos colocar o sódio logo abaixo do lítio já que estes dois elementos apresentam propriedades muito parecidas assim como o magnésio apresenta propriedades muito similares ao brilho dessa forma daremos continuidade a distribuição de e respeitando além da
ordem crescente de massa atômica nas linhas horizontais a similaridade dos elementos em cada coluna na terceira fileira temos o potássio depois do cálcio e no nosso exemplo o próximo elemento que possuímos é o Arsênio de massa igual a 74,90 e dois e é então que mendelev faz a sua Jogada de mestre em vez de colocar o Arsênio na coluna do poro ele coloca o Arsênio na coluna do nitrogênio Pois é com os elementos desta coluna que o Arsênio se assemelha e os próximos elementos são o selênio e o bromo que se encaixam perfeitamente nas colunas
do oxigênio e do flúor respectivamente e agora você deve estar se perguntando e esses espaços em branco bem Manda ela me disse que os espaços em branco indicavam os elementos que não haviam sido descobertos ainda Ele propôs Então qual seria a massa aproximada destes elementos e como deveriam ser as propriedades dos mesmos mais tarde esses elementos foram descobertos o que confirmou suas previsões em alguns cientistas contemporâneos de mendelev já haviam constatado que havia uma correlação entre a massa atômica e as propriedades de alguns elementos mas foi mendelev que criou uma correlação sistemática e detalhada que
permitiu inclusive prever os elementos que ainda seriam descobertos agora vamos ver algumas características da Tabela Periódica atual no início do século 20 o número atômico de vários elementos foi descoberto e logo os químicos perceberam que era melhor organizar os elementos por número atômico e não por massa repare que para cada número a um elemento químico correspondente para o número atômico um temos o hidrogênio dois o Hélio 3 o lítio 4 o berílio cinco oboro seis o carbono sétimo nitrogênio e assim por diante e repare que os elementos químicos estão organizados de acordo com o número
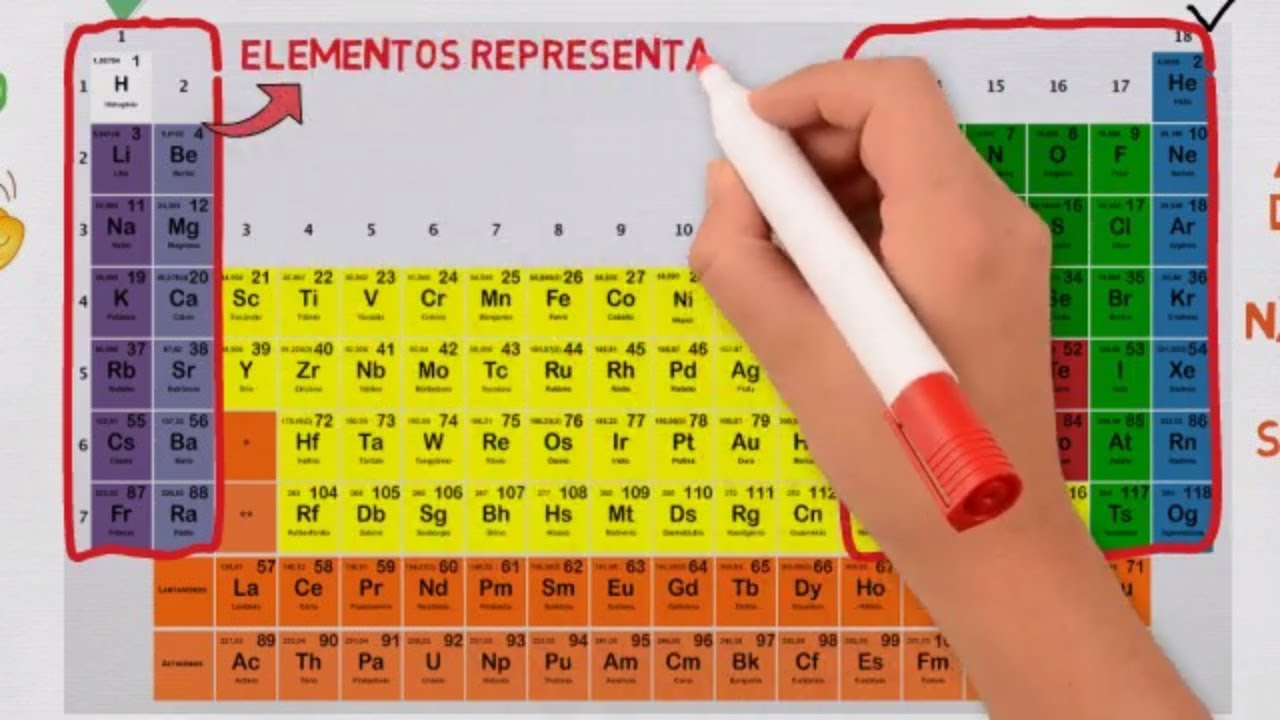
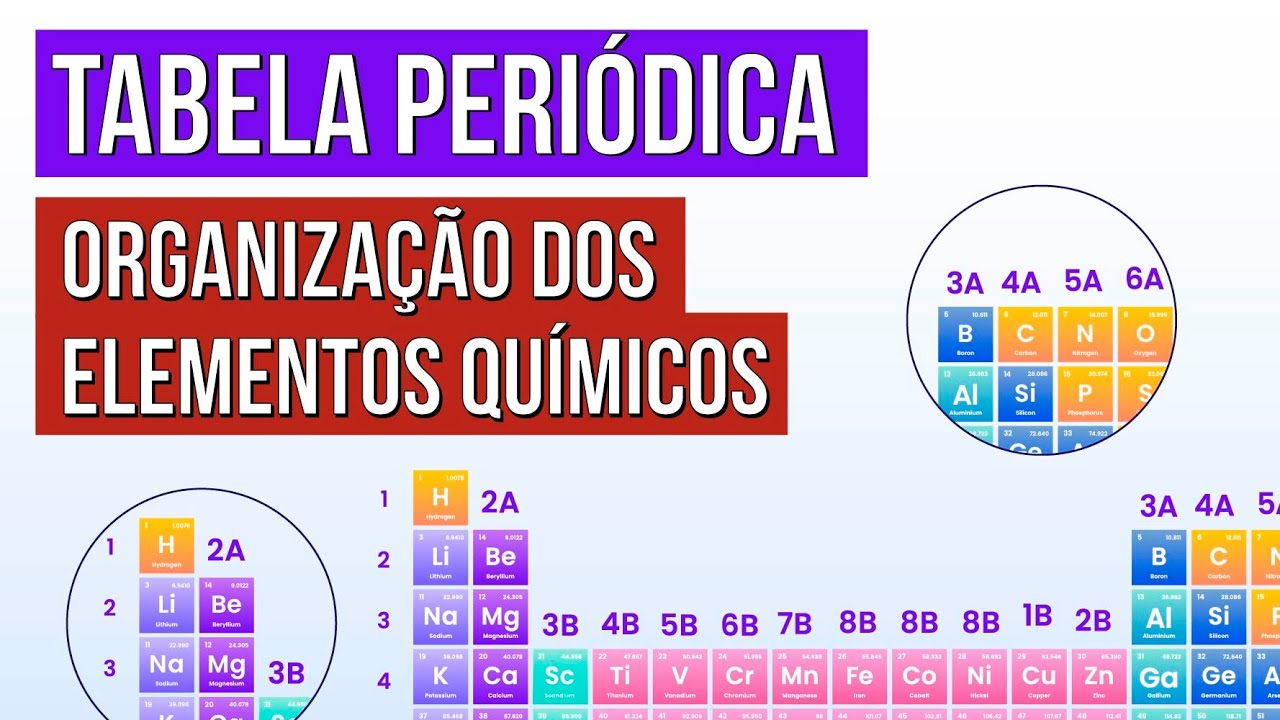
atômico da esquerda para a direita e de cima para baixo uma coluna da Tabela Periódica corresponde a uma família ou grupo de elementos químicos sendo que os elementos pertencentes ao mesmo grupo apresentam propriedades similares esses grupos são numerados de 1 a 18 e alguns grupos recebem ainda um nome específico o grupo um por exemplo é o grupo dos metais alcalinos o grupo dois é o grupo dos metais alcalinos terrosos 16 são os calcogênios 16 são halogênios e o grupo 18 é o grupo dos gases nobres e os elementos pertencentes aos grupos 1 e 2 e
de 13 a 18 são denominados de elementos representativos e os grupos de 3 a 12 que estão aqui representados com uma cor rosa são os elementos de transição temos ainda em azul os lantanídeos e actinídeos que são conhecidos como elementos de transição interna fazendo uma escadinha começando pelo alumínio até o radônio passando pela estado dividiremos a tabela periódica entre os elementos metálicos e os não metálicos e agora que já sabemos como são organizados os elementos na tabela periódica Estamos prontos para um novo mundo de possibilidades Então é isso e até mais [Música]















![Tabela Periódica [Mapa Mental] [COMPLETO] - Mapas da Química](https://img.youtube.com/vi/BsOF-zHi2H4/maxresdefault.jpg)



