e fala galera essa Mais uma aula do nosso top dentro de estrutura atômica Hoje a gente vai falar um pouquinho mais sobre configuração eletrônica e também sobre a tabela periódica para acompanhar bom a nossa discussão anterior a gente estava falando dos Estados eletrônicos ou seja né os valores de energias que são permitidos para os elétricos que a gente terminar agora a forma segundo o qual esses estados são preenchidos com os elétrons a gente tem que fazer fazer o uso do princípio da exclusão de Pauli o princípio de exclusão de Pauli eles pula Cada sabe eletrônico
ele pode convocar número máximo de dois elementos os quais devem possuir espinho Posso então se a gente tem que subir camada PDI é a gente pode acomodar em cada uma dela número total de 26 10 e 14 um outro conceito importante que a gente estudar a configuração desse homem que eu decidi o que ele determina na teoria como que deve ser a distribuição dos elétrons acamados você já deve ter visto ensino médio que a gente faz uma setinha do senhor nesse sentido E aí bom então só tenho um e levo eu tenho um átomo com
certo número de Leco Teoricamente ele vai seguir essa minha aqui para fazer o preenchimento das camadas todavia acha que o modelo teórico Eu tenho algumas exceções o princípio de aula e por exemplo o cobre o cobre por exemplo e o cobre por exemplo a entender outono 2019 é ele que hora o Flamengo estão princípio de altura deveria ter as seguintes a seguinte configuração é um S2 então Authentic dois elétrons mais 2 mais seis mais dois é porque eu já tenho 10 12 + 6 + 26 mais dois já tenho que seis 10 6/29 correto do
homem a configuração final teria que ser um s 2 2s 2 2p 6 3S 2 há 66 Eu tenho 19 4S 2 é correto mas na prática ao invés de último 1942 esses últimos são invertidos eu tenho 3S 2 3P seis eu tenho aqui um texto D10 c14 S1 ou seja Apesar que são Príncipe de ar ele existe ele possui algumas exceções como é o caso do Fábio um outro assunto importante que a gente vê sobre configuração eletrônica é exatamente e o elétron de Valência e que o elétron de Valencia elétrons de Valência eles são
os elétrons da última camada no meu aqui por exemplo ter que o magnésio fiz uma distribuição aqui eletrônica nele o alumínio e o silício a minha última casinha aqui a minha última Vital ele vai possuir esse número de elétrons aqui esse aqui é para submissão de Valência e eu vou ter que uma Valência doesto não fez S2 no Valência 316 s261 uma Valência para a valência ele é muito importante que ela vai muitas vezes no digitar nos digitar Como que o meu meu o elemento ele vai reagir em contato com os elementos qual o tipo
de ligação que ele vai fazer como que ele ele vai interagir com outras forças atômicas então muitas propriedades químicas e físicas dos solos elas são baseadas nos elétrons de Valência então existiu a minha camada que tiver completamente preench em um átomo sagu como a gente chama né quando existe uma camada por exemplo o a gente tava fazendo uma distribuição aqui se a gente tira a camada 2p 2s 2 2p 6 conhecida a gente fala que o nosso átomo ele tá eletricamente estável o seu cargo haste do neném até que eu botei aqui embaixo o aviso
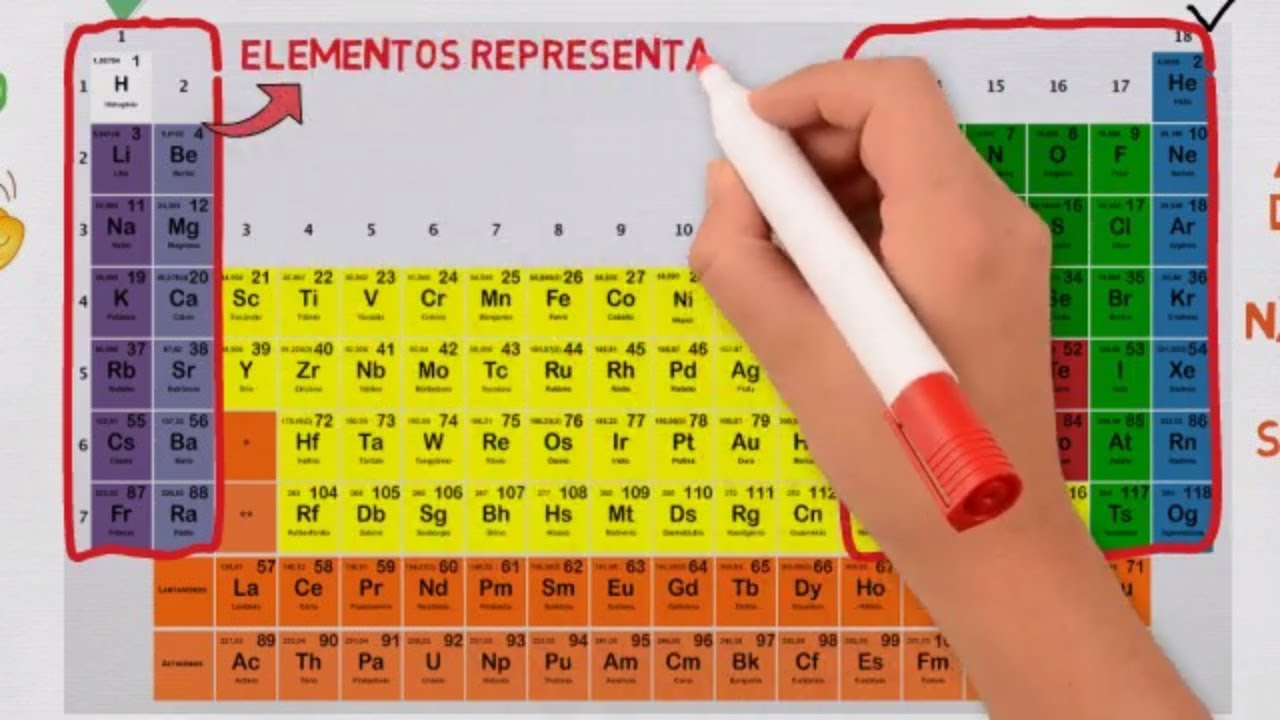
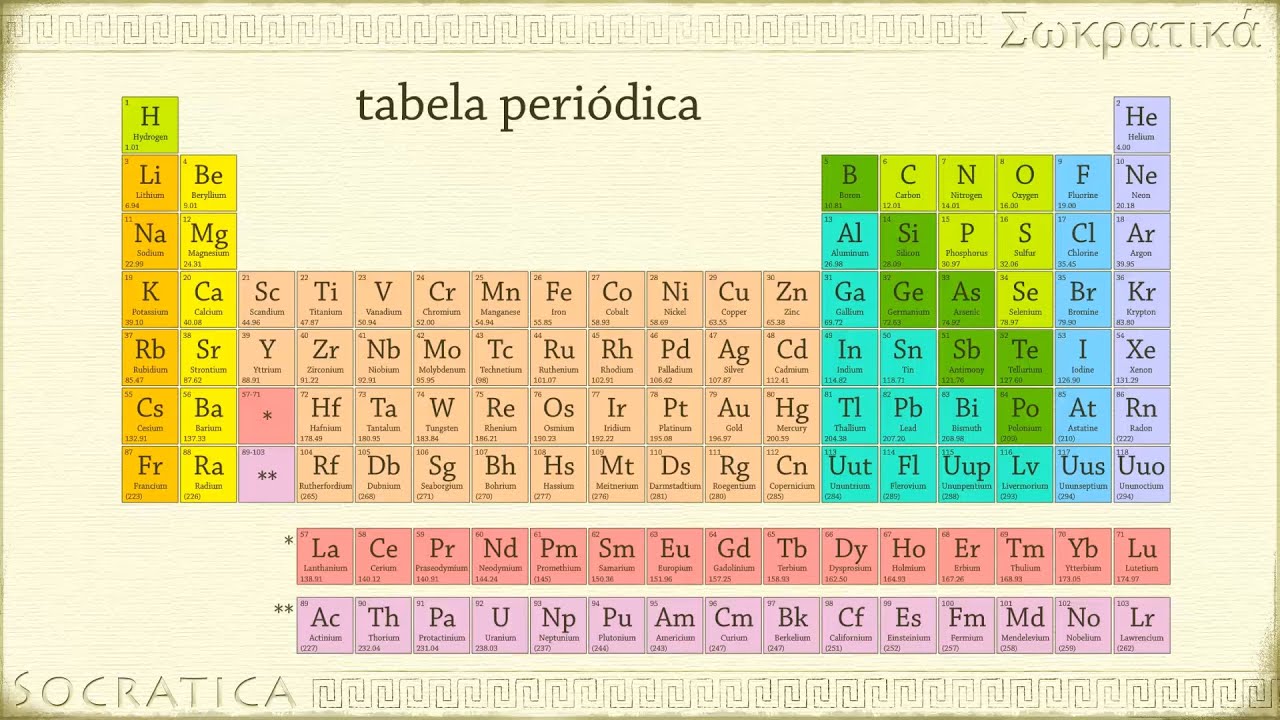
dos gases nobres que a gente vai vir mais para frente então se eu tenho uma camada o número de elétrons por exemplo colocar lado preenchida o número de Valência aqui ele é considerado zero bom é isso que a gente vai analisar um pouquinho essas questões dentro de uma tabela periódica Olá gente agora vamos dar continuidade à nossa aula voltamos aqui para nosso cliente comprou o presente fazer algumas análises e algumas observações importantes sobre a tabela periódica primeiro. Se observar que os elementos eles são é os elementos eles são funcionários de uma forma e tal todos
os elementos de uma mesma coluna por exemplo aquilo hidrogênio lítio sódio borough lugar todos eles que são vários na coluna e tem algumas propriedades semelhantes isso ocorre principalmente Pois todos eles possuem o número de Valência que ele tinha estudado é igual exemplo de valência do carbono é igual silício e germânio todos acaba resultando em propriedades semelhantes nos dentes mas parecidos os elementos no grupo zero aqui o jogo do cruzeiro-são respectivos direitos são as elementos são os gases inertes e eles possuem a camada preenchida por exemplo ele aqui tem dois elétrons esse aqui o número atômico
do elemento esse aqui é o é o nome do elemento né o símbolo aqui é o nome de quatro e aqui eu vou peso atômico do elemento tem um resumo aqui o caso que vamos ver certinho então nesse grupo 03 - gases inertes as inertes Já possui uma camada de valência preenchida por exemplo ela ele tem dois elétrons se eu quiser mesmo então depois de como fazer aqui não S2 beleza Depois chego nem óleo a gente fez um exercício anterior o argônio lá botei um S2 sentido 2s 2 2p 6 e PS2 há 66 o
metal amarelado agora isso vai ter Oi Ernesto também aqui eu posso dirigir os meus as versões vindos né que eu tenho lá os A6 A4 a lá sei lá 7 a 0 e aqui o tem os meus nossos posição que eu tenho fez v4b e assim sucessivamente né vamos falar algumas características de alguns grupos destes os grupos 6 ar e o set a eles possuem respectivamente faltando a distribuição eletrônica deles um elétrico ou seja têm 7 elétrons 6 e 7 elétrons na camada de valência bom por outro lado e existe um grupo um aro dois
aqui é o grupo dos metais metais alcalinos e alcalino-terrosos que eles têm um e respectivamente além da camada preenchida então a camada de valência possuem dois elétricos além da estabilidade em contraposição aos 16 e 17 a gente me chamou os elementos nesse período mais bons do seis dedos ver eles são chamados de metais de transição de metais de transição são 3B e aqui eu eu 2B e eles possuem status eletrônico DP parcialmente preenchido e o grupo fez a quatro a em cinco a eles possuem propriedades intermediárias entre os metais e dos ametais e até tanto
que se a gente quer para fazer uma classificação aqui a quem que é metal aqui que é a metal a gente considera aqui como metal alumínio para baixo aqui o galho também é você será do Metal o índio estranho ou antimônio desce aqui para o mesmo outro e depois O Colono né e eu que a gente considera o grupo dos metais daqui eu tenho alguns que a gente chama de intermediário que vai ser inclusive o Bora o carbono e silício eo germânio o Arsênio o selênio e o seguro esse grupo aqui está os intermediários Ah
tá aqui intermediários esses aqui são considerados os metais minhas todas aqui a e do outro lado eu tenho que eu só consigo que eu considero os não metais ou a metal então agora zerando aqui a nossa tabelinha a gente pode vir com a maior parte do dos ossos dos Ossos elementos e se enquadram nos grupos dos metais né em algumas vezes se lembranças são chamados de eletropositivos o que indica que são capazes ceder alguns elétrons de Valência pressionar em íons carregados positivamente de forma adicional os elementos estão situados do lado direito da tabela então para
cá e eu vou possuir aqui os meus elementos eletronegativos como funciona a identidade na lateral à medida que o para direita a medida quando o pé direito e para cima mais eletronegativo te disse o material a obviamente aqui nos do Grupo Zero Não É frontal o meu material mais Atrativa ou fungos e a camada mais era ou na mais Atrativa essa E à medida que eu vou deslocando para a direita voltando elementos mais eletronegativos a eletronegatividade é uma propriedade importante que a gente teria depois como que funciona algumas ligações entre materiais é outro ponto importante
que a gente pode avaliar aqui ainda pela tabela periódica uma curiosidade tá na parte dos metais de transição ou seja só esse grupo 2,3 ver esse grupo aqui eles têm os materiais são condutores de eletricidade e de calor também um pobre com um ótimo tua carta nutrientes. Enquanto os ametais que vocês vão se tomam nosso biquíni aqui da pontinha mais ou menos aqui eu tenho os meus a mentais eles vão ser materiais isolantes e só nos Pontos importantes em que tô características gerais não necessariamente só que ele tá nesse grupo e ele vai ter esse
tipo de característica ou por por hoje é só essa nossa geral nosso geralzão sobre a tabela periódica eu espero que vocês tenham gostado dessa aula qualquer dúvida que tenha ficado pode botar embaixo e aqui em cima também a gente vai colocar os dentes de alguns exercícios e exemplos que a gente vai fazer sobre essa última aula que a gente deu está com alguma dúvida até querendo exercitar o assunto é uma conferida do nosso vídeo dos exercícios sobre o quê E aí [Música]