o Olá pessoal sejam todos bem-vindos aí se nosso primeiro vídeo né do nosso curso de química inorgânica da graduação em química da UFMG é como eu me apresentei para quem não esteve na nossa aula Inicial lembra o nome Guilherme eu vou ser o professor de vocês nesse curso como eu expliquei é esse nosso os vídeos que eu vão fazer eles são vídeos completamente amadores né não tem iluminação adequada não tem nada na verdade tem boa vontade só termina na boa-vontade boa-vontade não resolve muita coisa mas enfim é o que eu consigo fazer nesse primeiro momento
tudo bem bom hoje o nosso vídeo é um vídeo de revisão e esse vídeo de revisão ele vai passar por alguns pontos Pode ser que tem alguns buracos aí que a gente vai ter que resolver na hora das dúvidas mas ele vai eles vão passar por alguns pontos Oi e Eu esperaria que vocês soubessem lá da química geral Ok é basicamente eu vou falar hoje um pouquinho sobre estrutura eletrônica de átomos que opção pontos bastante importantes Ok bom como eu comentei na na nossa aula da Live né na primeira aula cada aula minha vai ter
uma kanekinha diferente eu tenho uma coleção Essa foi a caneca que eu usei na Live né é uma caneca da Starbucks de time vai me Nessa idade que eu morei na Alemanha pode fazer meu doutorado sanduíche no teste que eu tenho um carinho muito grande então tem aqui alguns monumentos na praça central lugar lindo aqui é o ponto turístico né é dizem que nos contos dos Irmãos Grimm fala muito dessa cidade fala disso eu pessoalmente não conheço esses desconto Ah mas não tem uma função pedagógica não tá gente é só para aparecer mesmo mostrar minha
coleção não tem nenhum significado Além disso não tá joia só chega de conversa chega de sória a nossa aula começa agora você fecha todos os seus todas as abas desliga o celular tá na hora de concentrar vamos lá em pó então como eu tô comentando a aula hoje uma aula de revisão de alguns aspectos que Eu esperaria que você já soubessem da química geral mas que eu vou revisar com vocês bom nós vamos estudar a boa parte do nosso curso ligação química usando a modelos baseados na mecânica quântica tão teoria igual a primeira que nós
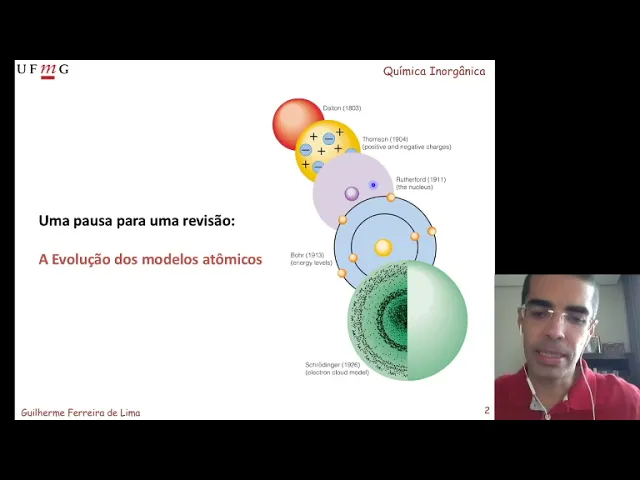
vamos usar a teoria do orbital molecular é uma teoria que é fundamentada na mecânica quântica Então essa figura aqui ela ilustra um pouco a evolução dos modelos atômicos desde o primeiro modelo atômico da era científica vamos dizer assim até o que é mais próximo do que a gente considera atualmente então modelo atômico de Dalton lá do do século 19 ele é baseado naquelas leis ponderais né lei da Conservação da massa lei da proporção definida lei da adição volumétrica de gases e como essas coisas e vim e experimentais né É O que diferencia o modelo de
Dalton dos modelos filosóficos lá de antes de Cristo a o detalhe que esse modelo ele considerou a tão como sendo uma esfera maciça fazer uma hora de uma partícula pequenininha de visível que tenha massa a pessoa esse modelo ser muito arcaico é gente quando a gente trabalha com fenômenos envolvendo apenas massas como por exemplo cálculos estequiométricos você não precisa de nada mais elaborada do que esse modelo então modelo tem essa característica tá gente ele se ajusta para aquilo que você quer explicar se você quer explicar apenas fenômeno de massa o modelo de Dalton modelo mais
sobre suficiente bom porém a a estrutura da matéria Ela tinha algo muito ela tem alguma interação com efeitos envolveram cargas né cargas elétricas e aí essas cargas elétricas precisarão ser incorporadas ao lado Thomson descobre o elétron usando aquele um tubo de raios catódicos e com base nisso Ele propôs um modelo onde você tem umas partículas negativas encontradas e uma distribuição positiva de carga que faz esse contrabalanceamento porque ao final da história o seu átomo deve ser neutro bom a a evolução do modelo vai para o modelo de Rutherford né ou até four faz um experimento
bastante famoso né que é o espalhamento de partículas Alfa colidido com quatro de ouro né E aí Com base no padrão de espalhamento culto é four propõe que o núcleo é o o átomo é composto por um núcleo esse núcleo vai ter praticamente toda a massa do átomo e as cargas positivas e uma região externa que é conhecida como eletrosfera esse modelo de Rutherford ele ele é interessante o modelo que explica apenas a existência do núcleo atômico você não consegue colocar os elétrons aqui de nenhuma forma que eles vão ficar estável então o modelo atómico
de Rutherford ele não consegue explicar absolutamente nada de estrutura eletrônica a evolução o seguinte né o modelo de Bohr esse modelo já é que no século 20 então a mecânica quântica já estava começando a ser desenvolvida então o momento de pó ele combina alguns elementos da física clássica com física quântica então é assumir que os elétrons eles vão estar nessa região da eletrosfera né derrotar só só que eles não podem estar em qualquer lugar mas apenas em algumas órbitas definidas E aí quando eles estão nessa obra eles vão ficar aqui indefinidamente e eles podem fazer
transições eletrônicas desde que eles recebam e eu que eles emitam energia ao sair de uma horta de energia mais alta para uma de energia mais baixa com isso ele consegue explicar o experimento né do da das raias do átomo de hidrogênio né é que eram uma das coisas que não se tinha explicação com base nos modelos anteriores bom no entanto esse modelo né com a evolução da física quântica esse modelo mostra-se um modelo bastante limitado e aí nós vamos discutir hoje alguns aspectos relacionados ao modelo moderno que é nada mais nada menos o que uma
nova forma mesmo que a gente poder enxergar Esse ato bom a primeira coisa então é que esse modelo ele vai explorar bastante o comportamento um ambulatório da matéria bom tem todo uma o desenvolvimento da física da época não os detalhes eu tô fazendo apenas uma revisão bastante resumida mas de broglie mostra que todas as partículas elas vão ter associadas a ela um comprimento de onda então eu quando eu ando eu vou ter uma onda associada é esse meu movimento essa um eu possa realizar o meu movimento considerando a minha partícula ou eu posso analisar esse
movimento analisando a onda associada aí bom tem uma tem umas equações tão por exemplo o comprimento da onda associado a uma determinada partícula pode ser dada H sobre o momento né H sobre IP o momento dessa partícula Então quando você vai Analisa objetos macroscópicos como eu for exemplo meu corpo é o comprimento de onda ele vai ser extremamente pequeno tão pequeno que você não vai conseguir observar por outro lado quando você vai para objetos muito pequenos de massa muito pequena e que tem uma velocidade muito grande esses objetos podem ter um comprimento de onda mesmo
tamanho razoável e apresentar esse comportamento ondulatório é o que acontece por exemplo com o ato o elétron você pode atualmente explorar o comportamento ondulatório dele para fazer várias medidas experimentais eu trago aqui dois exemplos de microscopia onde você consegue gerar imagens de vírus Como por exemplo o vírus do HIV e aqui é algumas imagens de esferas de carvão que você só consegue ver explorando o comportamento ondulatório do Eletro nessas duas situações a elétrons tá se comportando Como Uma Onda bom aqui São só alguns exemplos de alguns de alguns objetos né os corpos materiais e o
seu comprimento de onda chama a atenção que o comprimento de onda aqui está em picometro e Cometa dessa menos 12 tu é esse número vezes 10 a menos 12 então por exemplo o elétron ele vai ter aqui um comprimento de onda de sete mil quilômetros 7 mil quilômetros na verdade é sete vezes 10 a menos dez que é basicamente um tamanho de um átomo ele tem um comprimento de onda da Ordem do tamanho de um átomo bom a chamar atenção aqui agora com um objecto macroscópico pesado na uma bola de beisebol só para você ter
uma ideia bola de beisebol não sei se alguém te der uma oportunidade de pegar é pesadinho para você ver novas né se pegar dói então eu comprimento de onda disso a três vezes 10 a menos 20 x 10 a menos 12 toda a verdade ele vai ter um comprimento de onda de 10 amigos 32 metros quer dizer é pequeno demais algo tão pequeno que você não vai conseguir medir Oi vó em qual a importância de isso gente a importância disso é que quando você tem um objeto macroscópico que tenha esse comportamento ondulatório significativo não é
o meu caso mas é o caso do Eletro esse esse objeto ele está sujeito a um princípio que é o chamado princípio da incerteza de Heisenberg Já assistiram Breaking Bad Breaking Bad Heisenberg as raízes Berg o do princípio da incerteza físico extremamente importante nesse desenvolvimento da mecânica quântica então ele vai falar que esse seu objeto tem um comportamento ondulatório importante é você não vai conseguir saber com precisão O Mover ou a posição e o momento dessa sempre tem uma incerteza associada porque assim certeza porque você sempre vai ter uma interação é é da do que
você tá usando para medir com a partícula isso já vai provocar uma modificação tá beleza você quer utilizar um movimento de um elétron você vai analisar jogando foto ali logo que você jogar o foto já vai ter uma transferência de energia isso vai mudar o movimento do seu Eletro então é você sempre tem uma certeza que é associada e essa incerteza é de no mínimo H sobre quatro pe onde HQ a constante de Planck quer 6 x 10 - 34 aproximadamente que deu certeza pequena só que dentro do cenário que você tá na lizando isso
pode ser grande vamos pegar um exemplo aqui e vamo pegar um elétron que tem essa massa né de dessa - 31 essa é uma constante é que tem essa está nessa velocidade aqui de 5 x 10 a 6 vamos supor que eu consegui medir essa velocidade só com um experimento tem uma incerteza de um por cento ao mês certeza razoável só um por cento disso é dessa a quarta certo então agora eu quero calcular a incerteza na posição desse Alerta vou aplicar direto aquela fórmula toque A incerteza na minha posição ela vai ser a constante
de Planck / 4 PI aqui e me ver é o certeza no momento né mas é uma constante então aí certeza tá apenas da velocidade bom substituindo constante de placa 6 vezes 10 anos 34 a massa do elétron tá aqui e qual que é a incerteza na velocidade é um por cento é desse número aqui então a 10 a quarta quando você faz essas contas aqui você chega numa certeza de 10 a menos nove metros qual o significado disso significado disso gente é o seguinte um átomo ele tem o tamanho de 10 a - 10
Ben 10 - 9 é dez vezes maior do que isso então você basicamente é sua interferência na posição do elétron é dez vezes maior do que isso tamanho do ato também uma coisa que você fazer um experimento onde você vai ter como resultado dessa mais ou menos tem você não tem a menor ideia de qual é esse número que você tá trabalhando tá ok então é isso então a conclusão que a gente chega a partir desses nesse princípio da incerteza de Heisenberg é que usar essa abordagem determinística né Onde está o elétron que é um
que os outros modelos vem fazendo ela não faz sentido quando eu vou de escrever o Eletro porque o elétron está sujeito uma física nova uma física completamente diferente que a mecânica quântica então eu não posso mudar mecânica clássica para descrever o alerta para abordar isso eu vou precisar entrar É nesse mundo louco aqui que é o mundo da mecânica quântica nesse mundo louco a gente vai trabalhar com uma entidade que a chamada função de onda que para nós vai o que é o que significa a função de onda é o orbital onde esse Eletro vai
está mais a função de onda é uma função matemática tenha sempre em mente eu tô falando aqui de matemática é uma função matemática que tem toda a informação do meu elétrico e eu posso extrair essa informação desde que eu conheça a operador matemático adequado então aqui isso aqui é um daqueles Doodle do Google esse aqui foi uma curiosidade na primeira vez na minha vida que eu tava preparando a aula sobre esse tema lá em 2013 eu vou fazer uma pesquisa de alguma coisa digitei Google apareceu isso aqui por curiosidade isso aqui é o famoso gato
de schrodinger né que ele faz o que que se você tem um gato dentro de uma caixa e Esse gato é está na caixa fechada tá sem nenhum interação e tem um veneno aqui dentro ah esse gato até você abrir e interagir com ele ele vai ser uma mistura de duas coisas ele vai estar vivo e ele vai estar morto ao mesmo tempo Claro tem que ir normalizar Porque no final de contas é só um gato né por isso que tem essa raiz de 2 aqui isso aqui na organização mas ele só vai definir se
ele tava ver você tá morto na hora que você abrir interagir com ele essa ideia do experimento de do gato de schrodinger não é um experimento Imaginário esses experimentos imaginários são muito comuns no cenário da mecânica quântica Tá bom então o cara que mudou essa história foi Joaninha lá em 1926 ele ganha prêmio Nobel em 1933 só para destacar tá gente Scherzinger tem um papel importante principalmente na resolução da equação todo o arcabouço teórico né da física quântica já estava sendo estabelecido por Planck por tirar que Poupo de dormir todos Esse cara tem uma contribuição
muito importante no desenvolvimento da mecânica quântica mas a pessoa que sabe usar matemática para resolver o problema era o sangue Ok então e a equação Ranger né Essa equação aqui que aparentemente uma equação muito simples né que é a gapi-si igual apps e na verdade isso aqui é o que a gente chama de uma equação de autovalor e autovetor que ele já passou aí né todo mundo já passou espero né por áudio para eu desenhar nela Pelo Grau deve ter estudado essas equações já os valores autovetor então aqui eu tenho um operador matemático essa operadora
que ele é representado por esse chapeuzinho ele atua sobre uma função de onda e me dá com o resultado uma energia que é o alto valor x essa função de onda de novo aqui que é o meu alto vetor ok que que é um operador gente uma operador é um a gente matemático que executa uma ação tão por exemplo ou mais é um operador ele soma uma coisa a outra uma derivada o operador então vocês já conhecem alguns operadores eu vou precisar conhecer os operadores específicos que vão atuar sobre a minha função de onde detalhe
que eu não conheço minha função de óleo Então eu não sei operador não te acusando de Ó tem nada mas eu consigo ficar uma resposta que legal aí e aí eu chego um alto valor e tem de volta a minha função de ó Então tá aqui só um exemplo né de um operador tô pensando aqui é um sistema simples é onde vou ter o meu Eletro em movimento sujeito a um potencial Então esse primeira parte aqui é um operador que um operador de energia cinética e aqui eu vou ter a informação da minha do Meu
termo potencial bom gente se eu resolver eu posso resolver uma equação de chover em qualquer situação então por exemplo se for um elétron em torno de um núcleo esse termo potencial aqui eu tenho tipo Kombi é uma atração Eletrolux Lu E se for um átomo de um elétron né na presença de um campo magnético eu posso calcular aposto Eu só preciso saber o operador que descreve esse campo magnético campo elétrico que você quiser basta você colocar aqui dentro desse tempo potencial então se for meu átomo de hidrogênio como eu comentei né um átomo tipo hidrogênio
né Poderia você também só pode ter um Eletro vai ser um potencial dessa forma que onde vai ter a carga positiva ver aqui é o número atômico tá então é a carga positiva multiplicado pela carga do elétron né Esse é aqui aquela constante fundamental 1,6 vezes 10 menos 19 dividido pela distância tá ok Tá bom mas o que importa muito para gente é o que nós vamos discutir aqui é essa função de onda porque essa função de onda é o que traz a informação do meu sistema e é ela que nós vamos chamar de orbital
então cada função ela vai estar associado a uma energia quando eu resolvo aquela equação a vou ter a energia relativa aquela função ela não tem significado físico Na verdade essa função é uma função imaginária tem um ali que complica tudo para a gente tentar o significado físico no entanto é eu esqueci o nome do pesquisador Born mostra a steinborn mostra que o quadrado nessa função de onda ela vai ter um significado de probabilidade então agora Observe como tá tudo relacionado eu não sei aonde está o meu elétron porque o princípio da incerteza me proíbe de
saber o Porém quando eu sei a minha função de onda e eu levo ela o quadrado eu passo até informação acerca da probabilidade de eu encontrar o meu horário Tá ok então essa é isso que eu vou chamar do meu o Vital é isso que importa o que que são um exemplo né Se eu pegar para um átomo de hidrogênio né A Val probabilidade de encontrar o elétron mastersysfer aqui em torno do meu número que é o que a gente conhece como orbital S né e eu não vou entrar em detalhes com relação a resolução
da equação de schrodinger você já vão chorar muito que eles estudar muito isso é Quando vocês tiverem lá na frente estudando mecânica quanto eu vou deixar o sofrimento quer dizer na verdade eu quero dizer a trazer do aprendizado mas sua frente agora só vou apresentar os resultados deixa para vocês sofrendo depois vai resolver esse problema na equação de schrodinger eu preciso fazer um truque truque matemático é que é fazer uma troca de uma troca de coordenadas todo mundo que aprovou aí em calculo1 né Tem certeza que são todos é perfeito isso em algum momento para
resolver algumas derivadas mais cabulosos lá mesmas integrais cabulosos na verdade né você faz uma troca de variáveis Ah é Então na verdade a gente tá tá muito acostumado a trabalhar em coordenadas cartesianas x y z você definir qualquer posição é de um de alguma coisa usando um conjunto de parâmetros x y z então se eu falar x y z eu pego no espaço tridimensional consigo indicar qualquer lugar que eu quiser mas existem outras formas de você fazer isso uma das formas é usar essas coordenadas esféricas polares então ao invés de xyz que eu tenho eu
tenho aqui um vetor R que ele pode assumir qualquer tamanho de 0 até infinito e eu tenho um ângulo testa e pode ir de 0 até 180 e eu tenho um ângulo fica aqui você pode dezero a o 360 então Observe gente que se eu definir é Rita e fim eu consigo cobrir o meu espaço inteiro tridimensional assim como eu faria se fosse x y z e dá uma olhada nessa função aí dá o nessa nessa figura e convenção sim que eu posso definir o espaço assim como definir os anos xyz usando essas coisas às
vezes é importante e Qual a vantagem disso bom Se eu tentar resolver a equação de schrodinger usando coordenadas cartesianas x y e z eu chego no momento um problema que eu não consigo fazer uma separação de variáveis bom então eu chego um homem que eu paro mas não é problema físico problema matemático eu vou bater mais trabalho não tem ferramentas matemáticas para resolver agora quando eu escrevo a minha função dessa forma eu posso pegar minha função de onda e escrever ela como um produto de duas funções esse uma técnica bem estabelecida na matemática na chamada
de separação de variados onde eu tenho uma função que depende só da parte Radial e eu tenho uma outra função que depende apenas da parte angular e aqui só para vocês e os trabalho né quem tiver curiosidade ver algumas dessas funções né eu tô mostrando aqui para vocês o que são essas funções radiais e o que que são essas funções angulares tudo isso para o átomo de hidrogênio e o átomo de hidrogênio gente é o único átomo que eu consigo resolver de forma exata tudo bem Tá bom eu vou colocar aqui nos resultados quando eu
resolvo essa equação de schrodinger para o átomo de hidrogênio eu vou surgir com três números quânticos o primeiro número corte que é chamado de número quântico principal e a gente chama ele de Ênio Qual a função desse número quântico principal bom ele vai me dar o valor ele vai me dar a energia daquele estado é por isso que ele é chamado de principal ele surge quando eu resolvo a parte Radial um outro significado que muitas vezes a gente acaba negligenciando o dele é que ele vai dar o tamanho do meu orbital Então o meu orbital
ele pode ser pequeno se ele tiver online pequeno mas ele pode ser grande se ele tiver um aí grande Tá ok é bom quando eu resolvo na parte de energia a energia ele vai as penas do esse número pode com o principal bom ele pode assumir qualquer valor inteiro tod0 até infinito dependendo o que você quer Ok mas só que desculpa Vera não quer ele é de um até infinito que são os valores que ele pode assumir quando eu parto para resolução a angular né da minha função de onda eu vou surgir com outros dois
orbitais dos outros dois números quânticos o primeiro número quântico L chamado de Momento Angular Nesse Momento Angular é esse é meu né ele vai me trazer informação acerca do Momento Angular do meu elétron e isso na verdade gente ele está relacionado com a o formato daquele meu avental então ele é uma esfera a forma de um o ter ele na forma de um lobo isso é o que vai formação com ele me dá o l ele assume valores que vão desde zero Aí sim é zero até em menos um Então quem define todos os valores
possíveis do ele é o n e aquelas pessoas costumam ter um cometer um erro que é o seguinte fala assim o n = 2 então o Hélio ele não é apenas um que é o valor de 2 - um ele é zero e ele pode ser um também então são todos os valores possíveis Que bom de 0 até ele menos uso ok e esses valores né DL eles por origens por razões históricas eles recebe uma letra associado então por exemplo é igual a zero é chamado de S O L = uma chamado de p o
l = 2 chamado de d o l = 3 é chamado de S muitas pessoas acabam cometendo o erro tá achando que estão só esses valores de L possível não eu posso ter o é igual a quatro que seria o orbital Gi eu posso ter um L = 5 que seria um ovo e tal H depois do F gente Segue o ordem alfabético G H I Box nenhum elemento no estado fundamental né de um átomo usa esses orbitais para colocar os seus elétricos E no entanto nós lá nos cálculos né quânticos né gente usa na
Química teórica a gente precisa considerar esses orbitais para quando a gente quer fazer alguns tipos de cálculo Então esse é o que tá hoje não existe existe vamos lembrar né gente que esses orbitais são apenas funções matemáticas que para nós tenho significado físico Ok bom o último número quântico que importa para nós aqui nessa parte é o ML o ML tem uma definição que estranha que é o seguinte é a projeção do l em um eixo arbitrário basicamente que que eu tô falando o l me dá informação sobre o sobre o formato o ML e
me dá a direção Então se aquela forma tá indo numa direção se ela tá em outra isso ao ml que me dá essa informação ele vai assumir valores que vai desde - L até mais l variando de um passando pelo Zap Tá ok bom orbitais aí eu tô pensando em átomos com mais de um elétron tá é que tenha o mesmo é que tem o mesmo que tem um é mesmo ele varia só o ML todos esses ambientais que variam só o ML eles têm a mesma energia eles são degenerados ele só mudou essa energia
na presença de um campo magnético se o campo magnético for Zero eles têm todos a mesma energia então a gente só um resuminho aqui um desses números quânticos então eles podem ser é o número quântico principal ele vai assumir valores de um até infinito ele vai me dar informação da energia mas também do tamanho o Momento Angular ele vai dizer ó até - n - 1 ele me dar informações a cerca ela Afonso num magnético ele vai de menos dela e até mais velho e me dar informações da orientação para o descrever o elétron e
isso só vai surgir quando eu resolver a equação de dirac né que a equação relativística ela eu ainda preciso de mais dois números quânticos o primeiro deles é chamado de número quântico de spin que é meio com um elétron tem um respingo amei é isso esse Spin ele é um momento é Um Momento Angular intrínseco do elétron com elétron tem um Momento Angular E aí eu posso projetar Esse Momento Angular que é esse momento de spin que é mais meio ou menos meio Tá ok então para definir o meu elétron no átomo eu preciso de
a verdade quatro números quânticos o principal Momento Angular o magnésio e um momento de sim porque o espinho uma constante Tá ok E aí vai vir né quando a gente vai fazer no as distribuições eletrônicas vai vir um parâmetro importante né que é o chamado princípio de exclusão de Pauli que ele vai falar que um átomo nenhum Eletro pode ter esses quatro números iguais Então ele pode até tá no mesmo orbital quer dizer tem o mesmo e no mesmo lml mais um momento de espinho dele tem que ser diferente tá ok então Gente o que
que é um orbital né o pessoal costuma ter problemas com relação a isso um orbital é uma combinação de um n com l e um ml vou pegar alguns exemplos aqui então se meu n = 1 e qual que é o valor de L possível l é de 0 a TN menos um só que esse meu n = 11 o único L possível é zero Ok Google enviar e possível o ML ele vai de menos dela e até mais lok0 então essa combinação aqui 100 isso é um orbital é o hospital S e isso era
igual a 2 cm ou n = 2 Eu tenho dois elles possíveis 001 já que um é o n menos um bom Quais são os quais são os ml possíveis Suelen igual a zero o único ml possível é zero Oi Suelen igual a um o ML pode ser mais 10 - Então essa combinação aqui 01200 isso é um orbital essa combinação 21 mais um isso é um outro orbital 210 é um outro orbital 21 e menos um é um outro ouvi tal então eu tenho aqui um homem tal 2s mas eu tenho três orbitais 2p
tudo bem Tá bom fui assim vai ver todos os outros Observe que aqui quando eu vou para o m = 3 os velhos possíveis são 012 Suelen igual a dois olha só eu tenho cinco orbitais possíveis que são os cinco orbitais desde que nós vamos trabalhar muito nesse curso aqui tranquilo gente bom então agora nas minhas aulas não tem vários desses momentos aquela hora que você vai dar um pause no seu trabalho e vai responder essas perguntas daqui a pouco eu volto para poder ajudar vocês com a resposta tá bem pausa E aí o meu
filho você tem que pausar se você não pausar não tem jeito Querido vamos lá pausa por favor Oi tá esperando né ela gente tem jeito não bom claro que vocês causaram fizeram atividade agora nós vamos responder né basicamente Então olha só quando n = 2 Quais são os valores possíveis DL se n = 2 l pode ser zero ele pode ser um e quando ela igual a um quais os possíveis valores de m l = 1 seria mais 10 e menos um Qual que é a letra que representa Esse é igual é o p quando
o L2 Qual que é a letra que representasse subir camada é a letra de né é igual a dois são os orbitais e tipo B e quando uma subcamada denominada s qual o valor do L nesse caso ole0 e qual o valor do ML também é zero quando o nosso bicamada denominada P quantas outras sub-camadas existem dentro dela bom sua sub camada é p significa que o l golo isso é igual um o ML vai ser menos 10 e mais um quando uma subcamada denominada F quantos são os valores de ML bom o f ele
= = 4 então ele vai ter os valores de ML - 4 desculpa é igual L3 Então vai ser - 3 a menos 2 menos 1 0 ou dois três são os valores possíveis Ok bom aqui somos algumas curiosidades tá gente que só função Radial né assim a função de onda Radial essa função de onda é ela é Ela vai sumir valor ela ela vai ter né uma dependência exponencial que a gente pode observar aqui é um pouco até tranquilo disse você se lembrarão ela mostrei lá no Zap lá atrás que a minha função né
Ela é o meu hamiltoniano é uma derivada segunda né no operador uma derivada segunda qual a função matemática que você deriva duas vezes e tem como resposta ela mesma né já que a derivada da função de onda gera energia EA própria função de onda bom no função que você deriva gerar ela mesma função exponencial da função de onda até o tipo de uma função exponencial mesmo e é o que importa que eu quero mostrar que é o seguinte né que essa função ela tem esse decaimento exponencial mas Observe que seu aumentar o valor do n
ela de carne anos tá vendo eu tenho umas posições aqui onde essa minha função ela é igual a zero para essa função aqui isso aqui é o que a gente chama de um nó é Radial e toda vez que eu passo por um nó essa minha função ela vai mudar de sinal ok bom então isso aqui é uma função que a gente chama de uma função de distribuição Radial que que é isso eu tô pegando essa função de onda aqui isso aqui gente é o PC vamos lembrar que o psi ele não tem significado físico
tá OK assim é uma função imaginária eu vou pegar esse levar o quadrado que é o que tá acontecendo aqui essa função de distribuição Radial só que aqui tá aparecendo uma coisa nova que é esse é o 14 pe desculpa TV e de errado aqui na verdade você pegar uma borracha é o que eu quero chamar atenção é esse quatro pia aquilo E aí 14 Pierre desce com é roubada Pode perguntar o que você simplesmente não pegou e elevou a função Radial ao quadrado O que que a função é de alta gente ela é uma
função que está longo de uma linha é só como é o átomo ele é um átomo que é na verdade uma distribuição esférica certo então que tá fazendo aqui o que eu tô fazendo é considerando não só uma posição mas a esfera que definir aquela posição Então o que eu tô fazendo é pegando essa minha função ao trocar a caneta é o que eu tô pegando é o r E aí é o que eu tô pegando né aquele r Ah e Tô considerando o elemento de volume em torno de Sr Mas e se ele menos
volume e o volume de uma esfera então o volume de uma esfera ela é quatro terços de Pi a r e Ao Cubo certo letra ficou feia gente porque é muito difícil escrever com mouse nesse negócio aqui então se eu pegar o elemento de volume eu vou ter que ir ver em baixo aqui então passa o três para frente então vai ficar quatro PE a r e ao quadrado então quando eu multiplico disso aqui que eu tô falando eu não tô na andando mas apenas ao longo de uma linha Mas Eu Tô considerando a casca
esférica que é determinada por aquele raio então quando eu faço isso né gente eu vou chegar nessas funções aqui então tô pegando isso aqui o elevou não quadrado e multiplicando o quarto Pierre os dois então só chamar atenção aqui Observe que a função é se ela começa lá no infinito só que quando eu levo ela o quadrado ela começa do zero Tá mas como assim como que eu levo uma coisa O infinito ao quadrado e a resposta é zero ele não é zero por causa disso aqui ele é zero por causa desse R aqui esse
R Aqui é zero então a função ela aumenta depois tem José a oferta algumas funções em gente tinham um nó esse Loki tá gente eu consigo calcular ele e esse nó ele é dado por n - l -1 o certo é naquele número quântico principal que o hospital dois s o n = 2 u l é o valor to S então é zero tô aqui fica 2 - 0 - 1 Então significa que ele tem um Nord au que é o que aparece aqui ó Tá certo bom então tá aqui você vai lá mas o
que significa sinal Radial bom se você se eu pedir para você desenhar o orbital é se você vai desenhar para mim assim Tá certo e onde vai ter um sinal aqui que é um sinal positivo ou negativo tanto faz né esse número essa essa esse sinal não tem nenhum significado físico para gente né é simplesmente um sinal de uma função matemática e se fosse ou pedir para vocês aqui um orbital 1s e Se eu pedisse para você um homem tal dois é como você desenharia E aí vocês aqui ó e é uma esfera dentro da
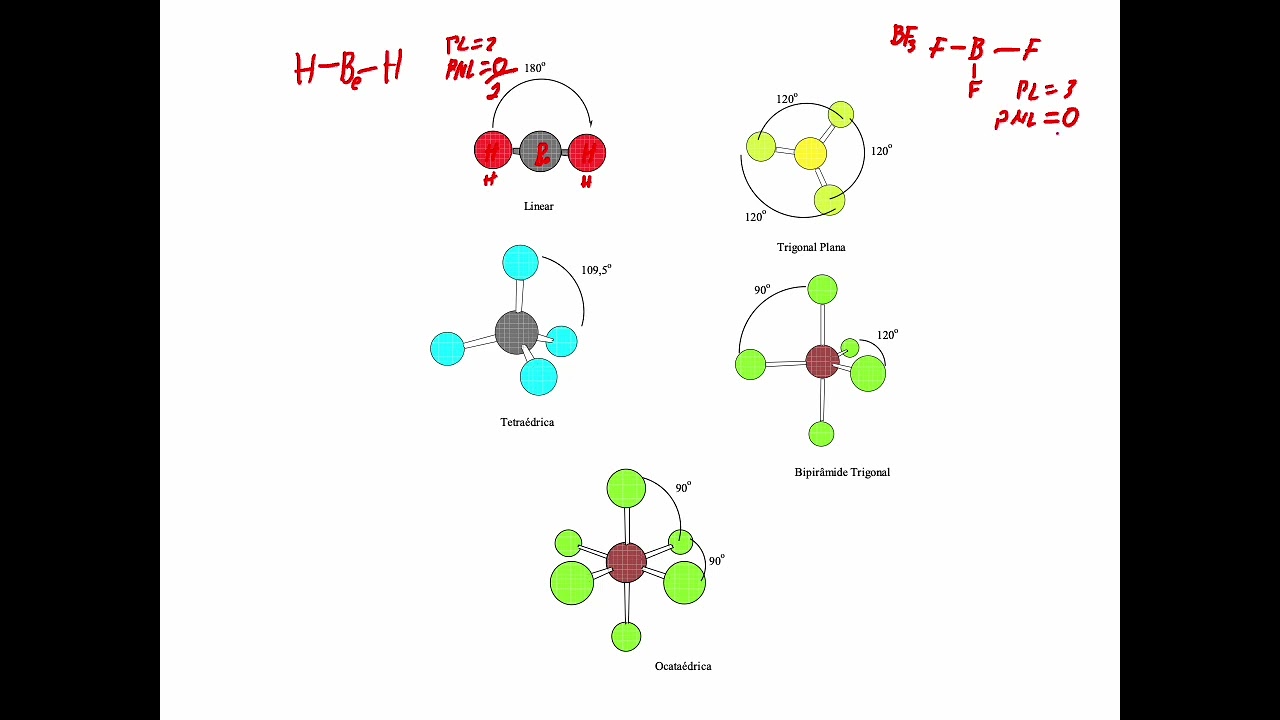
outra onde eu tenho aqui ó o Nó e sinal é o que a gente chama de um ó radial tá ok bom aqui tá uma curiosidade né Eu imagino vocês tenham visto isso em lado a química geral bom Assunção Estagiários tem essa forma aquilo vou entrar em detalhes mas o que me importa é que a gente chama atenção de vocês a gente vai ficar muito disso são os formatos então quando o seu L = 0 o seu formato é de uma esfera esse tranquilo E se o seu orbital foi um orbital do tipo P esse
orbital ele vai ter esse formato de lóbulo sendo que os orbitais p são três né eles estão apontados ao longo do meu eixo de coordenada gente saber a orientação de um orbital é extremamente importante quando a gente vai trabalhar é com teoria do orbital molecular você tem que saber para onde esse orbital a ponta tá ok então tá aqui ó Orbital que a gente chama de peixes ele está ao longo do eixo X o p y está ao longo do eixo Y e o pz está ao longo do meu eixo Z tá bom as pessoas
costumam perguntar mas qual que é a que os 10 o mais um e o menos um né relacionado com ml e não tem como você saber tá gente porque porque se você se lembrar do meu definição eu falei isso a definição fala que é uma projeção e o eixo arbitrário então você pode colocar o eixo onde você quiser e aí você não vai conseguir definir o que é x quem é isso 15 Tá bom quando ela é igual a dois eu tenho cinco orbitais possíveis três desses orbitais apontam nas bissetrizes dos eixos de coordenadas que
quer dizer triste bissetriz é um eixo que corta um ângulo meio então aqui eu tenho um ângulo de 90 graus entre os eixos eu tenho aqui uma bissetriz que está passando aqui para 35 graus bom então eu tenho desses três que vão estar ao longo dessas bissetrizes Observe Quando muda de cor tá relacionado ao sinal da minha função de onda tá então por exemplo esse Orbital que está entre o eixo Y e o eixo Z é chamado de desde pronto e e esse aqui que está entre o eixo X e Y ele é o dedo
xy&o que está entre o eixo x e z ele é o mês de x de além disso eu tenho dois orbitais que apontam na direção do meu eixo de coordenada que é o de dizer dois então ele tem uma parte maior aqui no eixo Z e tem essa rosquinha aqui né é o rostinho porque a maior parte falou que passou a quarentena comendo engordando Então deve estar deve ligar o nome à pessoa ou uma rosquinha aqui e o homem tá o dele esses dois menos de dois ele vai estar ao longo do eixo X e
o lixo isso tá ok gente novamente a gente vai usar muito disso aqui então se tem que saber onde estão os seus comentários não existe não consigo fazer nada teoria do orbital molecular tudo bem do pop nós vamos trabalhar mas apenas de curiosidade para vocês né eu tenho aqui os hospitais F sobre Tais genes que são vitais mais complexo vou botar os dias não tem nenhum elemento da tabela periódica atualmente conhecido que precisa né dele o hospital F mon seus lá os lantanídeos actinídeos que tem uma química bastante peculiar a gente não vai entrar em
maiores detalhes tranquilo bom pessoal era isso essa aula ficou um pouquinho mais longa mas era um pouco esperado porque é uma revisão de vou fazer uma pequena uma aula bem pequenininha com uma outra parte da revisão mas era basicamente isso que eu queria mostrar para vocês tá bom bom eu sugiro que vocês Leiam lá no livro do ar ou não tem algumas informações acerca disso Isso vai ajudar um pouco vocês aprenderem mais sobre isso tá bom gente um forte abraço eu volto em breve com mais um vídeo