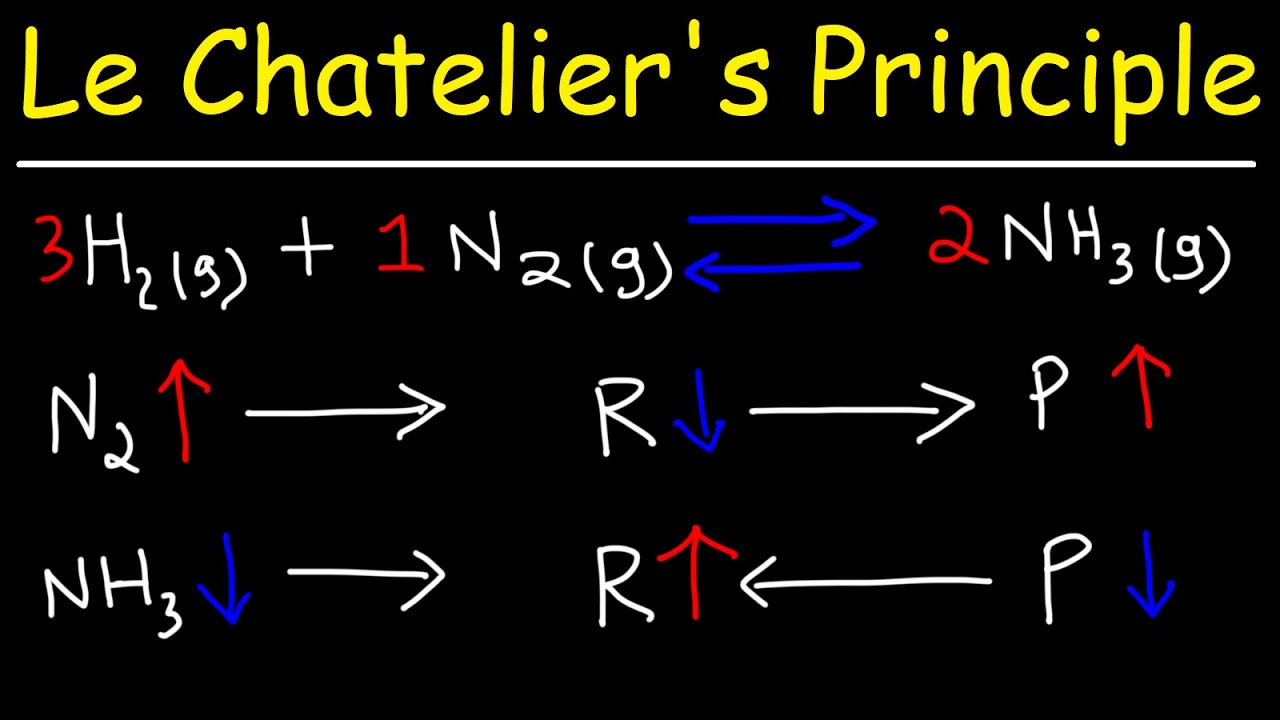
Olá no vídeo de Hoje iremos fazer vários experimentos testando o deslocamento de equilíbrio de leite atelier onde iremos aproveitar o cloreto de Cobalto 2 que foi obtido no experimento das baterias de íon-lítio e vamos observar os efeitos da concentração temperatura e pressão no deslocamento de equilíbrio o primeiro iremos observar o efeito da concentração no Equilíbrio e para isso vamos colocar um pouco de solução de cloreto de Cobalto dois nesses tubos de ensaio aqui o Cobalto dois participa do seguinte equilíbrio onde temos o ion Rosa hexaaquocobalto dois-mais-quatro íons cloreto e equilíbrio com iam Azul tetracloro Cobalto
dois mais seis h2oh como temos muita água a espécie é que saco Cobalto dois está em quantidade gigantesca na solução em relação ao eo Azul tetracloro Cobalto dois por isso sua cor é rosa e o equilíbrio pode ser afetado pela mudança da concentração de qualquer espécie do Meio reacional iremos adicionar o ácido clorídrico pois ele libera muitos irão CL menos no meio E aí [Música] nós vemos que qual adição docinhos ali menos o equilíbrio se desloca para a direita com a formação de mais e uns tetracloro Cobalto 2 que azul que fica em excesso em
relação ao e eu hexaaquocobalto dois que é Rosa só que acabei resolvendo adicionar o ácido muriático fazendo a mudança de coloração ficar mais visível e sempre que adicionamos uma espécie de um lado do equilíbrio o equilíbrio se desloca no sentido a formar espécies do outro lado do equilíbrio nós podemos também adicionar ácido clorídrico até tornar a cor da solução como a mistura do azul com rosa agora vou afetar o equilíbrio novamente adicionando água a solução Azul O que faz o equilíbrio se deslocar para o lado contrário da equação para a esquerda com a predominância do
complexo Rosa e agora iremos ver o efeito da temperatura nesse equilíbrio utilizando a água gelada e água quente Primeiro vamos colocar a amostra que contém a cor da mistura das cores dos complexos na água quente [Música] vemos que o equilíbrio se desloca para a direita com a predominância do complexo Azul isso ocorre pois a reação nesse sentido é endotérmica e agora colocamos A solução do tubo com água fria [Música] E aí E aí E aí vemos o equilíbrio se deslocar para a esquerda com a predominância do complexo Rosa isso ocorre pois a reação nesse sentido
é exotérmica e dessa vez Vamos adicionar uma solução de nitrato de chumbo 2 a solução Azul a fim de informar o precipitado de cloreto de chumbo 2 retirando os íons CL - do meio reacional E aí E aí E aí vemos que quando diminuição da concentração dos íons CL - a solução se desloca para formar uma maior quantidade do complexo Rosa sempre que retiramos uma espécie química do meio reacional o equilíbrio se desloca para o mesmo lado onde está essa espécie química e pronto agora chegou a hora de testar o efeito da pressão sobre o
equilíbrio para Isso peguei uma garrafa PET e construiu uma tampa improvisada com a válvula de câmara de ar a fim de bombear gases para a garrafa aumentando sua pressão e para a reação Vamos colocar vinagre na garrafa PET e vamos fazer a reação do ácido acético do vinagre com carbonato de cálcio da casca do ovo [Música] e essa reação acaba por formar o ácido carbônico e participa do seguinte equilíbrio químico nesse caso temos mais gases do lado direito da equação com o CO2 e sabemos que ao aumentar a pressão o equilíbrio se desloca para o
menor volume com a predominância do ácido carbônico aquoso e agora vamos bombear o ar para dentro da garrafa aumentando a pressão E aí E aí nós vemos aí claramente que temos menos CO2 liberado pois o equilíbrio se deslocou para o menor volume ou seja para a esquerda e mais ao liberar o ar retirando a tampa e consequentemente diminuindo a pressão vemos o equilíbrio se deslocar para o maior volume e consequentemente para a formação do CO2 Agora vejo o equilíbrio se deslocando com as variações de pressão em um maior ângulo E aí E aí E aí
E aí [Música] E aí E aí E aí E aí