fala galerinha do me salva estamos começando mais um módulo sobre ligações químicas e nesse módulo a gente vai falar de duas ligações químicas que são as ligações covalentes e as ligações metálicas nessa primeira aula a gente vai falar um pouquinho sobre as ligações covalentes quando é que elas ocorrem e quais as características desses compostos bem primeiro lugar né ligação covalente é aquela ligação que vai ocorrer entre elementos que tem eh baixa pouca diferença de eletronegatividade certo são eles ametais então quando a gente tiver ligação entre um ametal com outro ametal a gente vai ter uma
ligação chamada de ligação covalente é muito importante vocês lembrarem né com muita imaginação se isso aqui for a tabela periódica que os ametais aqui tem meio que uma escadinha né os metais são aqueles elementos que ficam mais aqui mais acima e mais à direita na tabela carbono oxigênio nitrogênio e não esqueçam que am metal significa não metal então tudo que não for metal vai ser am metal então o hidrogênio por exemplo o hidrogênio não é um metal ele pode então ser chamado de ametal então aqui né Entra o hidrogênio também hidrogênio com hidrogênio ou hidrogênio
com am metal também quem faz ligação covalente é claro que existem algumas exceções né regras de ligações químicas Existem várias exceções Então a gente vai aqui focar né Principalmente no que mais aparece que são metal com am metal ligação covalente e aí qual é a característica dessa ligação covalente se a gente for lembrar né a ligação iônica ocorre com troca de elétrons um elemento do elétrons o outro recebe aqui não aqui a gente tem o que a gente chama de compartilhamento Então a gente tem um compartilhamento de eletrons não tem nem uma espécie doando nem
outra recebendo e sim compartilhando elétrons os compostos que formam ligações covalentes eles formam estruturas que a gente chama de moléculas certo então aqui de fato todos os compostos que forem covalentes são os únicos que vão formar moléculas se a gente observar lá na ligação iônica não são moléculas é um retículo cristalino na ligação metálica também a gente tem uma rede de átomos então aqui de fato são as moléculas compostos covalentes formam de fato Então as moléculas e como é que isso acontece bom eu peguei aqui o exemplo do hidrogênio né se a gente colocar dois
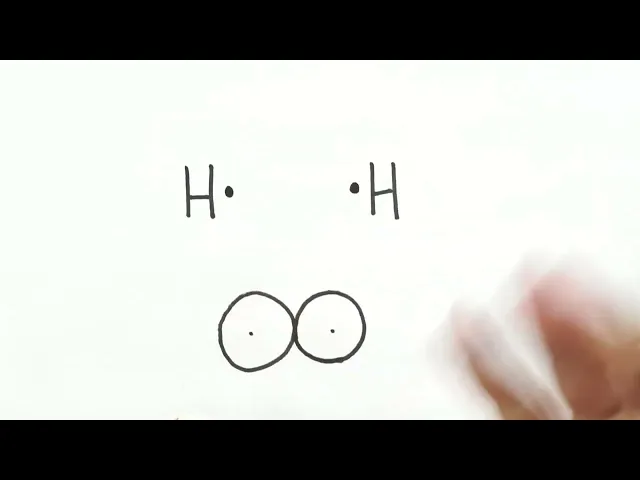
átomos de hidrogênio a gente sabe que eles têm um eletroninho lá só só na camada de valência e que o hidrogênio é um dos poucos elementos assim como o Hélio que fica estável com dois elétron somente na camada de valência Se cada um tem um ao invés de um doar e o outro receber né um vai ficar sem e o outro vai ficar com dois não o que que eles fazem eles compartilham esses elétrons Então se a gente fosse representar né a gente vai pensar lá esse é o núcleo desse hidrogênio aqui aqui e aqui
seria a última camada né ã que na verdade o hidrogênio só tem uma camada né e o elétron Zinho aqui e o núcleo desse outro hidrogênio tá aqui do lado direito e o eletroninho dele também fica girando em torno dele só que o que que acontece quando eles compartilham que que acontece esses elétrons ficam girando ao redor os dois né ficam girando ao redor dos dois núcleos por isso que a gente diz que há um compartilhamento de elétrons na ligação covalente e aí quais são as características desses compostos as características dos compostos covalentes bom primeiro
lugar a gente pode encontrar compostos covalentes nos estados sólido líquido e gasoso nos três estados físicos é claro Nas condições ambientes né só para lembrar que compostos iônicos e metálicos em geral a gente encontra Nas condições ambientes somente no estado sólido aqui não aqui a gente pode encontrar em todos os estados físicos certo os pontos de fusão e de ebulição dos compostos covalentes geralmente são baixos mas são baixos se a gente comparar eles em relação aos compostos iônicos e metálicos então compostos iônicos e metálicos TM pontos de fusão e ebulição mais altos em geral do
que os compostos covalentes os compostos covalentes também não conduzem eletricidade a gente só tem uma são aqui tá que são os ácidos os ácidos quando eles estão eh em solução aquosa eles sofrem o que a gente chama de ionização E aí eles podem conduzir eletricidade mas sen não todos os outros compostos covalentes né não vão conduzir eletricidade e por fim quando eles estão no estado sólido essa característica só vale para os compostos covalentes sólidos eles têm em geral baixa dureza eles não são duros e baixa tenacidade ou seja né a gente não consegue deformar ele
sem que haja uma ruptura ali do material muito cuidado aqui né com alguns compostos covalentes Como por exemplo o carbono diamante carbono grafite a sílica né que é o dióxido de silício presente lá na areia esses compostos vejam tanto carbono quanto silício quanto oxigênio são ametais eles fazem ligações covalentes só que a gente tem que cuidar porque são os únicos que a gente vai chamar eles de substâncias covalentes a gente não pode chamar eles por exemplo de substâncias moleculares porque esses compostos aqui são os únicos que apesar de serem formados por ligações covalentes são os
únicos que não formam moléculas eles formam uma rede de átomos os átomos Ficam todos interligados É bem interessante vocês procurarem na internet a estrutura aí do carbono de amante carbono grafite e da sílica para vocês entenderem que forma uma rede de átomos e são os únicos aí que T ligações covalentes mas não formam moléculas pessoal sobre os compostos covalentes eras isso espero que tenha ficado Claro e até a próxima