E aí pessoal do me salva vamos para mais uma aula aqui de oxirredução tá E nessa aula aqui nós vamos ver algumas regrinhas para determinar o nox tá para ficar mais simples Existem algumas regras para determinar o nox das substâncias Então nós vamos ver essas regrinhas nessa aula tá bom vamos começar aqui então com a primeira regrinha que é a regra de substância simples tá então substância simples sempre terá nox igual a zero tá então o nox da substância simples é zero por exemplo o nox do oxigênio aqui vai ser zero ele não tem esta
carga elétrica por que isso porque eu só vou ter átomos do mesmo tipo né então não vai haver diferença de eletronegatividade portanto não vou ter Separação das cargas e vai ser zero Se eu tivesse por exemplo um pedaço de ferro aqui átomos de Ferro como só tem átomos de Ferro eu também vou ter Nox zero Ok não há diferença de eletronegatividade aqui Como assim por exemplo vamos usar como exemplo aqui h h a eletronegatividade dos dois são iguais Então ninguém puxa os elétrons nem para um nem para outro portanto não há separação e o nox
fica zero Ok bom segundo caso segunda regrinha aqui o hidrogênio o hidrogênio ele geralmente possui nox igual a mais um então o hidrogênio tem nox igual a mais 1 exceto quando ele esti em um hidreto metálico o que que é um hidreto metálico é um hidrogênio ligado a metal Ok bom nesse caso aqui ele não está ligado no metal Portanto ele tem nox mais um que é o nox usual do hidrogênio certo o c aqui vai ter nox menos um mas geralmente o nox é mais um na água também óxido do hidrogênio é mais um
o que que é um hidreto metálico então aqui no caso do hidreto metálico por exemplo na h o que acontece é que o hidrogênio é o cara mais eletronegativo Portanto ele vai ficar -1 Ok então ele vai ficar com esse elétron então em hidretos metálicos tem que cuidar que a exceção o nox do hidrogênio será -1 e não mais um que é o nox usual dele tá mas em grande parte dos compostos o nox dele é mais um bom vamos ver o próximo carinha aqui o próximo carinha é o oxigênio o oxigênio ele possui os
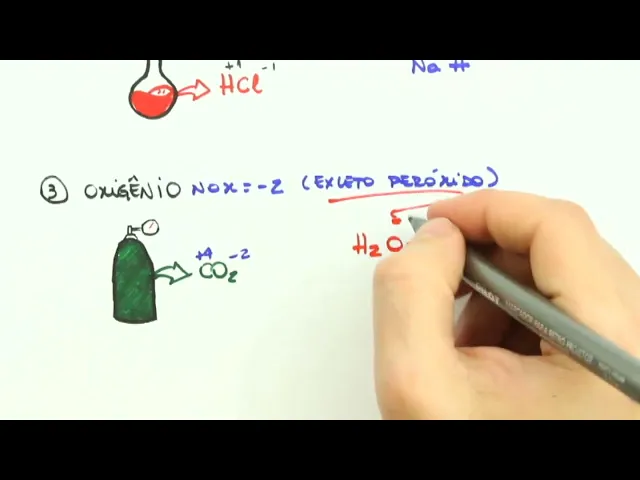
geralmente nox igual a -2 tá exceto quando ele for um peróxido bom Então nesse caso aqui é um caso comum o CO2 o nox dele vai ser -2 Ok por enquanto não Vimos a regrinha mas o do carbono vai ser mais 4 Nós já vamos ver em seguida como é que a gente faz o do carbono aqui bom o nox dele geralmente é -2 quando que não será -2 quando ele for um peróxido então um peróxido aqui de exemplo seria água oxigenada H2 O2 que aqui o nox dele vai ser nox Men 1 ok então
em peróxidos oxido oxigênio é -1 isso aqui tem relação à configuração do peróxido certo O peróxido ele tem esta forma aqui portanto a diferença de elidade de oxigênio com oxigênio não existe então ele só fica com o elétron daqui e o elétron daqui portanto cada oxigênio tem só uma carga men-1 certo então vem aqui vem aqui cada oxigênio fica com uma carga apenas menos um uma outra observação um outro caso tá é um caso bem especial aqui é quando ele tá ligado ao flur Ok então uma observação aqui é quando nós temos esse cara aqui
o flur ele é mais eletronegativo tá então esse é um caso bem particular onde o fluro vai ter carga men1 e o oxigênio carga mais 2 tá então é o único único caso onde o oxigênio vai ter um nox mais do quando tiver ligado ao flur beleza bom vamos ver então a nossa quarta regra aqui alguns elementos possuem nox usuais nox que geralmente acontecem com o mesmo valor quais são eles bom nox usuais primeiro então o grupo um da Tabela Periódica geralmente o nox é mais um o grupo dois geralmente o nox É mais do
certo outros carinhas que o nox também se mantém o valor a prata mais um nox o zinco mais do o o alumínio mais 3 outro carinha aqui o flur menos 1 o resto as tabela periódica eles acabam tendo variações maiores no número de oxidação portanto a gente acaba não generalizando mas esses casos aqui é é isso que seguia os em azuis sempre são assim tá E os em vermelho também grande parte das vezes sim então a gente acaba dizendo que praticamente sempre eles são esse valor bom qual que é o próximo aqui o próximo é
esse caso aqui aonde nós temos que a soma do número de oxidação em uma espécie eletricamente neutra esse nox aqui tá então o número de oxidação em uma a soma deles então tem que ser igual a zero Ok então aqui ó o somatório dos números de oxidação tem que ser igual a zero vamos ver um exemplo né como é que funciona imagine então o caso do ag n três Qual são os nox fixos aqui os nox que acontecem bom o do oxigênio ele não é um peróxido então portanto é Men 2 a prata é o
caso aqui de cima prata mais 1 ok e o do nitrogênio o do nitrogênio a gente usa essa regrinha cinco como então cada prata possui inox mais um quantas pratas eu tenho eu só tenho uma prata aqui ok portanto 1 x 1 mais 1 a o noxo nitrogênio eu não sei então eu vou dizer que é mais x o oxigênio cada oxigênio tem carga -2 eu tenho três oxigênios portanto duas x 3 eu tenho - 6 a regra aqui nos informa que a o somatório dessas cargas tem que ser zero então eu posso resolver esse
cálculo bem simplesinho aqui para x certo e nós vamos ter uma carga que x vai ser igual eu passo vocês para lá para cá + 5 certo quantos mais C seria o total Ok quantos nitrogênios eu tenho Então eu tenho que pegar esse valor aqui que eu achei e dividir pelo número de nitrogênios Ok então 5 dividido por 1 vai dar mais 5 ok porque se eu não tivesse só um nitrogênio aqui eu teria que dividir por um valor diferente Ok Isso aí vale para diferentes casos tá sempre tem que ser o somatório igual a
zero Ok então só tem que cuidar que quando tu achar esse x aqui tu tem que dividir pelo número de átomos Bom sexta e última regrinha é que o somatório dos nox em ion então o somatório do nox em um ion agora não num substância eletricamente neutra vai ser a própria carga do íon então por exemplo se eu tiver um ion R Cromo mais 3 CR + 3 o nox dele já tá definido é + 3 Ok mas se eu tiver diferente um ion composto aqui so4 - 2 Men -2 como é que eu faço
isso bom é a mesma ideia de cima só que agora tem que ser igual ao a carga do ion então cada oxigênio é -2 o enxofre eu não sei eu vou chamar de X então + X cada oxigênio é -2 eu tenho 4 então eu multiplico - 8 Isso aqui vai ter que ser igual a carga do ion que é -2 eu calculo o x aqui então passo o -8 para lá x vai dar igual a mais 6 quantos enxofroso por 1 meu nox Vai ser + 6 utilizando essas regrinhas de Nox fica mais fácil
para nós determinarmos a carga de cada átomo nas substâncias e nós vamos poder inferir várias coisas para as reações de Ox redução Certo muito obrigado e até a próxima