olá pessoal me salvar vamos ter mais uma aula do nosso modo de entropia nessa aula então a gente vai desenvolver a desigualdade de clausius a desigualdade de klaus é né a expressão matemática como a gente chega na expressão matemática da entropia e aí infelizmente pessoal a gente não consegue parte né daquele conceito abstrato que a gente tratou de dispersão de energia chegará mais precisão matemática porque a gente não tem muito muitos dados para trabalhar então a gente vai fazer isso da maneira que clausius chegou a ele fez isso a partir do estudo de máquinas térmicas
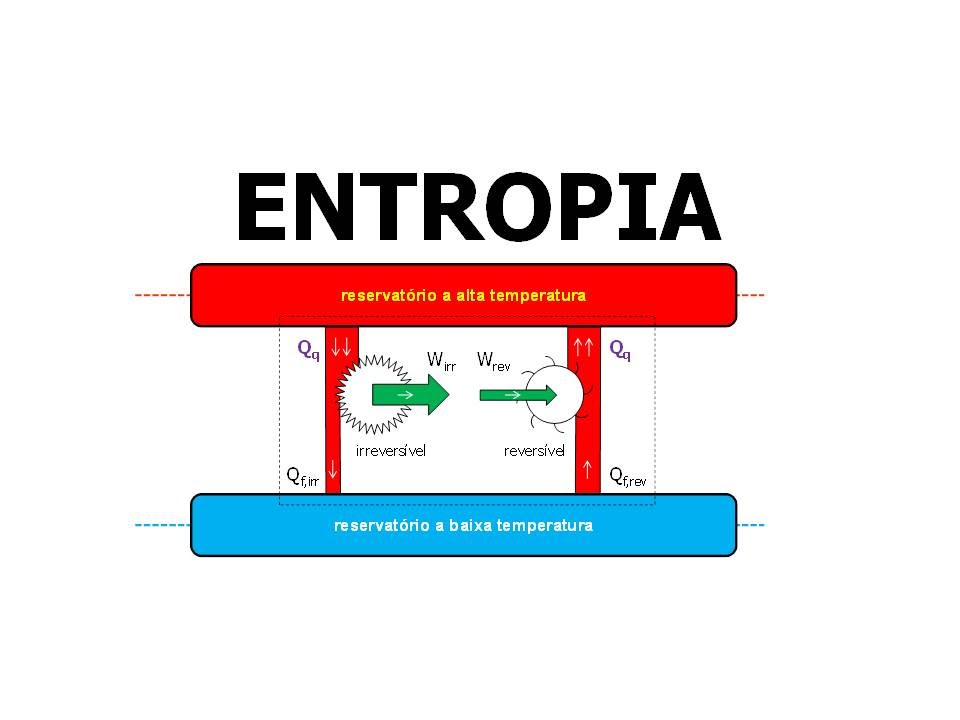
que a gente já está bem familiarizado com a gente vai ver como é que a gente chega nessa expressão de entropia a partir dessa desigualdade de klaus está a gente pensar então o nosso sistema que é de máquina térmica a gente tem é um ciclo que está aqui é inserido então a gente tem nosso ciclo em contato com a fonte quente uma fonte fria e ele está aí produzir um trabalho tudo aquilo que a gente já viu né a gente vai dizer que esse ciclo é um ciclo de carne ou então esse nosso ciclo ele
é reversível certo bom se a gente fizer então uma análise das transferências de calor para esse nosso ciclo reversível aqui a gente fizer então o somatório de todas as ilhas de calor a gente tem duas netas de pensar que a gente tem o calor da fonte quente o calor da fonte fria então agora foi de quem está entrando positivo eo calor da ponte preta saindo negativo nesse nosso balanço é do nosso calor que está entrando e saindo agora se a gente fazer fizeram uma uma questão matemática aqui pessoal de dividir a essas calorias pela temperatura
considerando que essa temperatura é a temperatura na fronteira onde está acontecendo a transferência de calor lembrando que a transferência de calor a gente né calcula ela na fronteira então a gente vai ter que essa expressão vai ficar desta maneira a temperatura da fonte quente e aqui temperatura da frente fria partindo então agora dessa expressão e lembrando qualquer a expressão é pra processos irreversíveis é da nossa escala kelvin a gente tinha essa relação aqui que a gente desenvolveu nas aulas passadas para processos irreversíveis que é o nosso caso nosso ciclo de cannon essa relação aqui ela
era válida e então a gente vai substituir esse valor a gente vai no caso aqui inverter é os nossos os nossos coeficientes aqui ea gente vai chegar numa expressão pra essa daqui ea gente vai substituir na nossa expressão ea gente vai ficar então com uma expressão que nós integral da transferência de calor sobre a temperatura vai ser então o calor da fonte quente sobre a temperatura da fonte quente - o calor a fonte quente sobre a temperatura da fonte quente certo se a gente quer usar aqui os nossos índios e é isso que obviamente é
igual a zero a gente vai cortar este com esse então pra processos irreversíveis a gente tem que essa expressão aqui da integral do calor sobre a temperatura é igual a zero então aqui isso aqui é válido para processos irreversíveis agora a gente vai fazer a mesma coisa pra um processo irreversível então para um processo irreversível a gente vai ter lá né pensando no processo irreversível sendo que o nosso calor de entrada que é o calor da fonte quente vai ser igual ao que a gente tinha lá processo irreversível a gente está considerando que esse calor
vai ser igual então que se que o calor de entrada lembrando também que para um processo irreversível né a gente sabe que a eficiência do reversível é sempre maior do que a eficiência do irreversível aqui todos são conceitos que a gente viu em algumas passadas no outro modo e então lembrando que em que a expressão da nossa eficiência da máquina térmica é o trabalho sob o calor de entrada que no nosso caso o calor da fonte quente a partir então dessas relações aqui a gente encontra né a gente conclui o trabalho do irreversível é menor
do que o trabalho do reversível obviamente então o nosso quando o nosso ciclo opera de forma irreversível a gente consegue produzir mais trabalho que a gente consegue produzir menos trabalho justamente por causa das nossas irreversibilidades questão dispersando né a nossa energia em forma de calor tá e aí então se a gente fechar o nosso balanço de energia para o sistema a gente vai encontrar que o calor da fonte feia irreversível é maior do que o calor da fonte fê reversível isso aqui também pessoal quer dizer que a gente está dispersando mais calor ou seja a
gente tá né transferindo mais calor para fonte fria justamente porque a gente está produzindo menos trabalho a gente tá perdendo maior quantidade de energia na forma de calor ea então continuando aqui na nossa expressão a gente vai substituir isso a nossa integral que a gente tinha inicialmente a nossa integral lembrando né ela essa variação é do calor na temperatura ea expressão original o kindle só escrevendo pra gente não esquecer ter esta daqui a gente vai então substituir né o nosso calor lembrando que o calor da fonte quente é o mesmo mas o calor da fonte
fria é diferente e odair irreversível é maior do que a de irreversível substituindo então nessa expressão a gente vai ficar com este aqui permanece igual e aqui então a gente vai ter o calor onde fica irreversível sobre a temperatura aqui e aí então pessoal lembrando né se a gente for comparar então esse aqui é a nossa expressão do nosso processo irreversível se a gente comparar a ela como o processo reversível é onde este aqui era menor isso quer dizer que a nossa subtração dos termos que esse termo aqui no irreversível é maior no reversível a
nossa subtração vai ser maior não sei se vocês conseguirem então vou botar aqui matematicamente pra gente tentar explicar melhor esse aqui é o nosso balanço para o processo irreversível certo esse termo aquino reversível ele é menor do que esse termo aqui então na subtração necessariamente essa situação tem que ser maior do que essa e lembrando que esse resultado que a gente encontrou processo irreversível é igual a zero então se a gente simplificar tudo isso não é pra um processo irreversível a gente vai ter que a expressão dessa integral ela vai ser menor do que 0
então este que é o resultado de um processo e irreversível certo e se a gente juntar os dois então considerando processo irreversível e irreversível a gente chega na expressão de que esta integral é menor ou igual a zero menor quando for irreversível igual quando for reversível essa expressão aqui é o que a gente chama então de desigualdade de cálcio certo e aí a partir daqui a gente consegue fazer alguma reflexão lembrando só então o pessoal que se a gente tiver o resultado integral como maior do que zero quer dizer que nosso processo é impossível certo
vamos agora refletir um pouco em cima dessa desigualdade eu trouxe aqui pra nossa se a gente considerar agora o processo irreversível onde a gente tem que o valor da integral é igual a zero tá pra reversível o valor da nossa integral é igual a zero essa integral de ciclo é como a gente viu já estava realizando um ciclo termodinâmico vamos lembrar quem são assim todas integrais de ciclo que a gente conhece lá a gente tratou da integral cíclica de trabalho integral significa de calor ea gente viu né que essas integrais aquela são sempre diferentes de
zero e essas são tão propriedades né que dependem não são propriedade são quantidades que dependem do caminho que a gente lembra que a gente viu elas dependem do caminho são aquelas diferenciais exatas né do caminho do processo mas a gente tinha integrais cíclicas que eram iguais a zero se vocês lembram as integrais cíclicas por exemplo do volume quando a gente completa um ciclo tá pessoal a gente está falando de graus técnica é igual a zero porque ela depende somente do estado inicial e do estado final e aí o estado inicial estado final de um ciclo
são iguais depende do estado inicial e final e não depende do caminho então se a gente parar para analisar né essa integral aqui ela tá né com um comportamento igual ao do volume e o volume é uma propriedade de estado justamente uma característica da propriedade do estádio tudo é que num ciclo integral ele vai ter 10 então chegou klaus quando estava analisando essa expressão para um processo irreversível ele viu que este valor aqui time que representará uma propriedade do estado porque isso aqui é uma característica da propriedade do estado e então ele escolheu nem chamar
essa quantidade de entropia então foi assim que surgiu né a entropia justamente qual se definiu então que a entropia é matematicamente seria definido como o resultado aqui da nossa integral que no caso está na forma diferencial para um processo irreversível e então comunidade né pra isso a gente tem energia por temperatura então ela vai ser em que elogiava eles porque é o vim aqui a gente vai usar a escala absolutas temperatura escala kelvin que a gente trabalhar ainda na forma de variação de entropia é como a gente tem pra energia por exemplo a gente vai
ter que vai ser resultado né da entropia do estado final - entrou pelo estado inicial isso vai ser integral então dessa expressão então o pessoal essa expressão matemática né que a gente obtém para a entropia a partir da desigualdade de klaus porque a gente viu que ela se comporta e como uma integral de propriedade do estado então o próprio klaus né definiu que essa seria a propriedade chamada entropia quando a gente analisa assim só matematicamente né a gente não consegue relacionar isso indiretamente aquele conceito de dispersão de energia e tal mas essa aqui é a
expressão matemática entre o quilo e essa foi a maneira que ela foi desenvolvido é quando ela foi descoberta digamos assim a gente vai continuar trabalhando com essas expressões matemáticas sempre tentando né é relacionar um pouco com essa questão significado mais físico e mais real disse mas realmente entropia é um conceito bastante abstrato e ela vai continuar sendo assim um pouco abstrato ao longo do curso mas espero que seja um pouco mais claro então essa a gente viu né como é que se chega a desigualdade de klaus a partir de ricos lembrando que a gente está
aplicando isso aqui pra ciclo e aí depois a gente a partir das igualdades desenvolveu o conceito de entropia que é uma propriedade de estado certo espero vocês nas próximas aulas tal