hoy hablaremos acerca de los conceptos generales de temperatura y calor al igual que sus unidades de medida y características principales iniciemos por el significado que comúnmente le damos a la temperatura de acuerdo a nuestra experiencia cotidiana podríamos decir que la temperatura mide qué tan frío o qué tan caliente se encuentra un cuerpo o sustancia de tal forma que si éste se encuentra muy caliente decimos que tiene alta temperatura mientras que si se encuentra muy frío decimos que tiene baja temperatura de cierta forma esto es correcto sin embargo se aleja mucho del concepto real de temperatura
para entenderlo mejor veamos lo siguiente aquí tenemos un vaso con agua y supongamos que lo dejamos en reposo por unas dos horas en este caso de forma macroscópica podríamos decir que el agua se encuentra totalmente estática sin embargo si observamos a nivel microscópico las moléculas del agua se encuentran en constante movimiento impactando unas con otras constantemente ahora claramente esto es una manifestación de energía sin embargo es energía a nivel microscópico es decir dentro del propio sistema esto es lo que conocemos como energía interna y es que como ya dijimos a nivel microscópico las moléculas de
todo cuerpo o sustancias se encuentran en constante movimiento y como ya sabemos la energía que se manifiesta en forma de movimiento es conocida como energía cinética ahora es importante aclarar que las moléculas no solamente se mueven de un lado a otro sino que éstas también pueden rotar en torno a su propio eje o también pueden vibrar siendo todas estas formas de energía cinética ahora teniendo esto en cuenta también podemos decir que las moléculas de un cierto cuerpo o sustancia pueden moverse rotar y vibrar más rápidamente o más lentamente si lo hacen de forma lenta decimos
que tienen una menor energía cinética mientras que si lo hacen de forma rápida decimos que tienen mayor energía cinética ahora habiendo visto todo esto podemos ahora sí dar la definición exacta de temperatura y es que la temperatura es el promedio de la energía cinética de las moléculas de un cuerpo o sustancia es decir que entre más rápido se muevan rotten y vibren las moléculas mayor será la temperatura y viceversa por lo tanto entonces también podríamos decir que la temperatura es una especie de medida del grado de agitación que tiene las moléculas de un cierto cuerpo
o sustancia ahora decimos que la temperatura es un promedio de esta energía ya que dentro de un mismo cuerpo o sustancia pueden haber moléculas que se muevan más rápidamente que otras es por eso que el concepto de temperatura tiene más sentido a nivel macroscópico ahora ya que entendimos el concepto de temperatura veamos que es el calor el calor en esencia es una forma de energía y podríamos decir de forma muy resumida que es la suma de la energía cinética de todas las moléculas de un cuerpo o sustancia es decir que en comparación con la temperatura
ya no estamos hablando de un promedio de la energía cinética de esas moléculas sino la suma de esa energía total ahora para ser exactos técnicamente lo que acabamos de decir se denomina energía térmica o energía calorífica mientras que el calor como tal hace referencia más al proceso de la transferencia de esa energía térmica sin embargo para el propósito de esta explicación podemos asumir que son lo mismo ahora hasta este punto podríamos tener un poco de confusión con los conceptos de calor y temperatura que hemos dado por eso para entender mejor la relación entre estos dos
términos veamos los siguientes ejemplos supongamos que aquí tenemos dos recipientes ambos con la misma cantidad de agua en este caso 10 litros sin embargo la diferencia es que el recipiente contiene agua a 20 grados centígrados de temperatura mientras que el recipiente b contiene agua a 70 grados de acuerdo entonces con los conceptos que ya hemos visto el agua del recipiente ve tiene mayor energía cinética en promedio ya que sus moléculas se mueven más rápidamente la pregunta entonces es cuál de los dos reciben tiene más calor pues bien ya que ambos contienen la misma cantidad de
agua y el recipiente be tiene una mayor energía cinética en promedio significa que el agua del recipiente be tiene más calor que la del recipiente ahora este ejemplo pudo haber resultado bastante intuitivo para nosotros ya que en nuestra vida cotidiana estamos acostumbrados a relacionar una mayor temperatura con un mayor calor pero veamos el siguiente ejemplo aquí nuevamente tenemos dos recipientes en este caso el agua que contienen se encuentra a la misma temperatura 70 grados en ambos casos sin embargo la diferencia es que el recipiente contiene 100 litros de agua mientras que el recipiente b contiene
10 litros la pregunta es entonces cuál de estos dos tiene más calor pues bien antes que todo debemos decir que la energía cinética promedio de las moléculas del agua en ambos casos es la misma ya que tenemos la misma temperatura sin embargo el calor no es el promedio de esta energía sino la suma total y ya que el recipiente tiene mayor cantidad de moléculas significa que a la final tiene una mayor cantidad de energía por lo tanto decimos que el recipiente tiene más calor que el recipiente ve a pesar de que se encuentren a la
misma temperatura en este orden de ideas entonces podríamos ver el siguiente ejemplo tenemos una taza de café a 60 grados de temperatura y tenemos por el otro lado el océano con una temperatura promedio de 15 grados la pregunta entonces es cuál de los dos tiene más calor pues bien obviamente el océano tiene muchísimo más calor que una simple taza de café ya que tiene muchas más moléculas y recordemos que el calor es la sumatoria total de la energía de cada una de esas moléculas con lo cual aquí demostramos que mayor temperatura no necesariamente significa más
calor y viceversa tanto así que retomando este ejemplo a pesar de su temperatura relativamente templada la gran cantidad de calor o energía térmica que contiene el océano es capaz de generar fenómenos atmosféricos violentos tales como los huracanes y esto claramente no se debe a su alta temperatura sino a su alto contenido de energía térmica ahora entendiendo esto veamos el siguiente ejemplo aquí tenemos nuevamente dos recipientes con diferente cantidad de agua pero se encuentran a la misma temperatura en este caso 20 grados centígrados ahora supongamos que exponemos ambos recipientes a una fuente de calor externa después
de un cierto tiempo digamos cinco minutos observaremos lo siguiente en el recipiente ve la temperatura aumentó 20 grados centígrados y llegó a los 40 grados mientras que en el recipiente a la temperatura sólo aumentó un par de grados y es que esto sucede porque en el recipiente el calor se tiene que distribuir en los 100 litros de agua que contiene lo cual representa un incremento pequeño en el promedio de la energía de cada molécula mientras que en el recipiente ve ya que el calor se debe distribuir en una menor cantidad de agua la temperatura aumenta
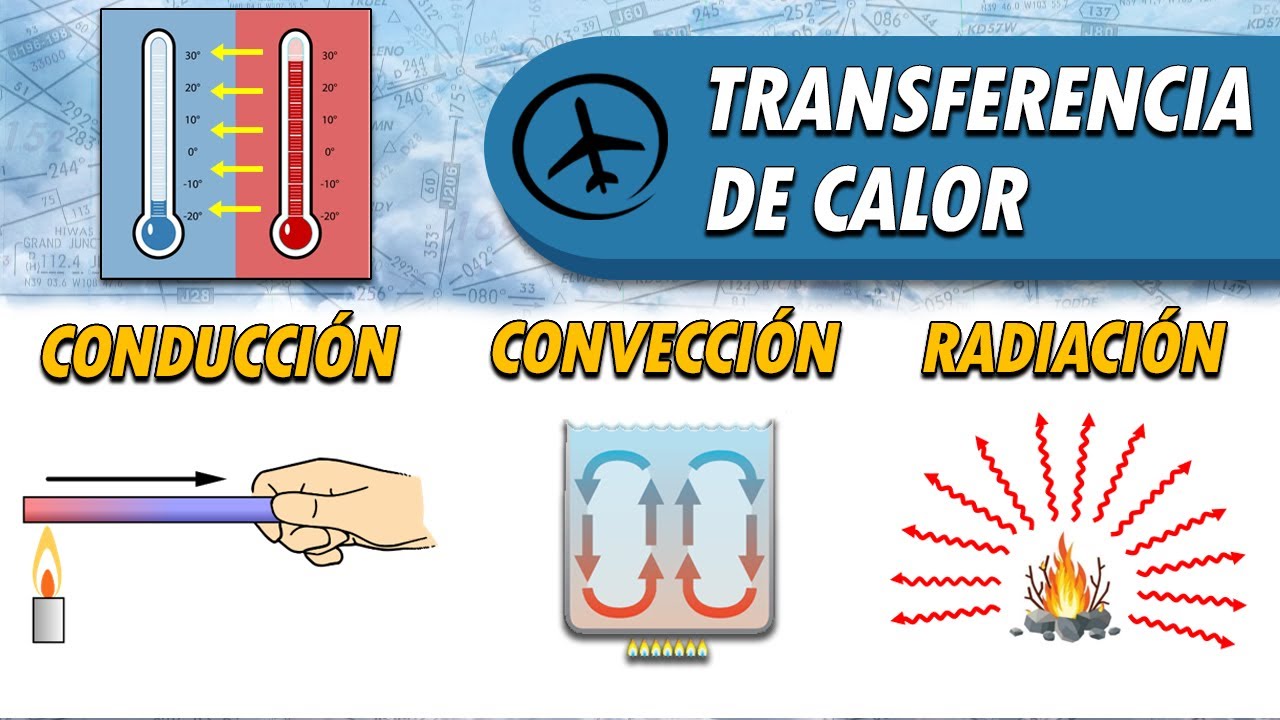
mucho más ahora aquí hay que destacar que se está produciendo una transferencia de calor y es que una de las características del calor es que se puede transformar de un cuerpo a otro si estos tienen diferentes temperaturas por regla general de la termodinámica el calor siempre fluye del cuerpo de mayor temperatura al de menor temperatura hasta que se alcanza el equilibrio térmico lo cual significa que ambas sustancias u objetos alcanzan la misma temperatura en tal caso la transferencia de calor se detiene ahora esta transferencia de calor puede producirse por diferentes procesos específicamente existe en la
conducción la radiación y la convección de los cuales hablaremos más en detalle en el siguiente vídeo ahora bien en este punto podríamos preguntarnos qué pasa si un cuerpo pierde todo su calor pues bien en este caso sus moléculas no se moverán ni vibran en lo absoluto es decir que en otras palabras no tendrán energía cinética como podemos observar en este ejemplo en esta situación en particular decimos que ese cuerpo o sustancia ha alcanzado la temperatura del cero absoluto la cual obviamente constituye la temperatura más baja posible habiendo entendido todo esto pasemos a ver las unidades
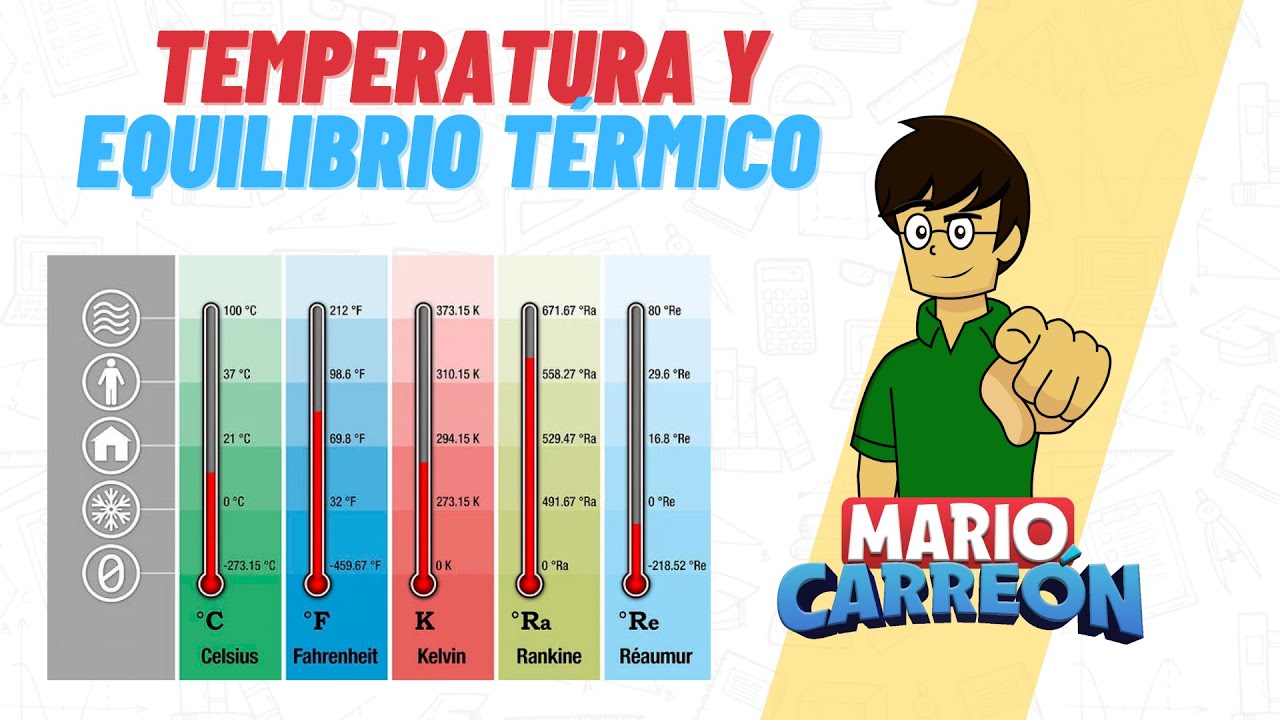
de medida de la temperatura existen diferentes escalas pero las más famosas son la escala de grados fahrenheit celsius y kelvin normalmente para comparar estas escalas se utiliza como referencia el punto de congelación y ebullición del agua al igual que el cero absoluto de acuerdo a esto el cero absoluto se representa como 0 grados kelvin o menos 273 grados celsius o menos 459 grados fahrenheit por otro lado el punto de congelación del agua es representado como 273 grados kelvin o cero grados celsius o 32 grados fahrenheit y finalmente el punto de ebullición del agua está representado
por trescientos setenta y tres grados kelvin o 100 grados celsius o 212 grados fahrenheit a continuación podemos ver los diferentes factores de conversión que debemos utilizar para cambiar de una unidad a otra como podemos observar en la parte inferior la relación de grados kelvin y grados celsius es bastante sencilla simplemente corresponde a una diferencia de 273 unidades mientras que por otro lado la conversión de grados fahrenheit celsius o viceversa es un poco más compleja esta puede representarse utilizando fracciones como podemos ver aquí con 9 quintos o 5 novenos o también podemos utilizar un factor de
18 si nos resulta más sencillo como podemos ver aquí ahora el instrumento utilizado para medir la temperatura es el termómetro y existen diferentes tipos dependiendo de su principio de operación en meteorología y aviación normalmente se utilizan los termómetros bi metálicos los termómetros de mercurio y los termómetros de resistencias eléctricas sin embargo hay que aclarar que aparte de estos tres existen otros tipos de termómetros utilizados para diferentes propósitos como por ejemplo el termómetro infrarrojo o el termómetro de gas o el termo para ahora en meteorología a parte del termómetro se suele utilizar otro instrumento conocido como
el termógrafo este se utiliza para registrar el comportamiento de la temperatura en el tiempo utilizando un papel que se encuentra en constante movimiento muy similar álvaro grafo del cual hablamos en vídeos anteriores y al igual que sucedía con este se utiliza para analizar el comportamiento de la temperatura y así poder predecir cambios futuros ahora es muy importante que tanto el termómetro como el termógrafo obtengan una lectura adecuada de la temperatura real es por eso que estos instrumentos se instalan dentro de una garita meteorológica o en inglés stevenson screen esta es una estructura especialmente diseñada para
asegurar una medida adecuada de la temperatura ya que ésta evita que la lectura se vea alterada por la radiación solar la precipitación o el calor emanado por la superficie terrestre para esto la garita debe diseñarse de tal forma que los instrumentos se encuentren a una altura de entre 12 y 2 metros sobre la superficie y alejados a unos 4 metros de estructuras que puedan afectar la medida de la temperatura ahora esta es la forma en la cual se mide la temperatura en la superficie para poder medir la temperatura a diferentes altitudes se utilizan dispositivos conocidos
como radio sondas que se elevan desde la superficie hasta aproximadamente 65.000 pies de altitud estas radios ondas se componen de un globo meteorológico que es el que permite que asciendan un reflector de radar y la radio sonda como tal el reflector de radar se instala en los modelos más antiguos para que un radar en la superficie pueda detectar la posición exacta de la sonda en todo momento sin embargo en los modelos más actuales se utilizan una antena gps para monitorear la posición de la sonda ahora hasta el momento hemos visto cómo se mide la temperatura
pero veamos cómo se mide el calor pues bien el calor al ser una forma de energía puede medirse como tal y por lo tanto en el sistema internacional podemos medir el calor por medio de los judas sin embargo también debemos decir que también se puede medir el calor en función de la cantidad de energía necesaria para cambiar la temperatura de un cuerpo de acuerdo a esto obtenemos una unidad de medida conocida como la caloría una caloría se define como la cantidad de energía necesaria para elevar la temperatura de un gramo de agua en un grado
centígrado específicamente corresponde a la cantidad de energía térmica necesaria para elevar la temperatura de un gramo de agua de 14 a 5 grados centígrados a 15 5 grados centígrados asumiendo condiciones de presión estándar a nivel del mar para hacer una equivalencia una caloría es igual a 4 mil 186 jules ahora derivado de esto debemos decir que no todos los materiales necesitan la misma cantidad de calor para cambiar su temperatura es por eso que entramos al concepto de calor específico esta es la cantidad de calor necesaria para que la temperatura de un cuerpo o sustancia aumente
en un grado centígrado para entenderlo un poco mejor veamos el siguiente ejemplo aquí tenemos dos materiales a ibm y tenemos la misma cantidad de masa en ambos casos un kilogramo para este ejemplo vamos a asumir que ambos se encuentran a la misma temperatura inicial de 15 grados centígrados y el objetivo será aumentar la temperatura de ambos materiales en un grado centígrado es decir que alcancen los 16 grados ahora de acuerdo a las características de estos materiales resulta que el material necesita menos calor que el material be para incrementar su temperatura en un grado debido a
esto podríamos decir que el material a tiene menor calor específico que el material ve ahora este concepto del calor específico está muy ligado a la capacidad calorífica en términos simples la capacidad calorífica es la capacidad que tiene un material de absorber calor sin cambiar mucho su temperatura de tal forma que diríamos que el material tiene menor capacidad calorífica que el material ve habiendo entendido esto debemos decir que cada material o sustancia tienen un cierto calor específico el cual determina que tan fácilmente cambia su temperatura de acuerdo al aporte de calor aquí por ejemplo en esta
tabla podemos ver el valor del calor específico para diferentes sustancias veamos un ejemplo con esta información podemos observar que el agua tiene un calor específico de 1 mientras que el hierro tiene un calor específico de 0,11 es decir que el hierro tiene un calor específico casi 10 veces menor que el agua de acuerdo con esta información si tuviéramos la misma cantidad de agua y hierro en este caso un kilogramo a la misma temperatura en este caso 15 grados y les añadimos calor por ejemplo 1000 calorías su temperatura cambiará de forma distinta ya que tienen diferentes
valores de calor específico en el caso del agua que tiene una mayor capacidad calorífica está solamente cambiará su temperatura en un grado centígrado mientras que el hierro que tiene una menor capacidad calorífica aumentará mucho más su temperatura en este caso en nueve grados centígrados ahora de acuerdo con lo que hemos visto resulta natural pensar que cuando se le aporta calor a un cuerpo su temperatura siempre va a aumentar y la verdad es que en la mayoría de los casos sucede de esa manera a este calor utilizado para aumentar la temperatura de un cuerpo se le
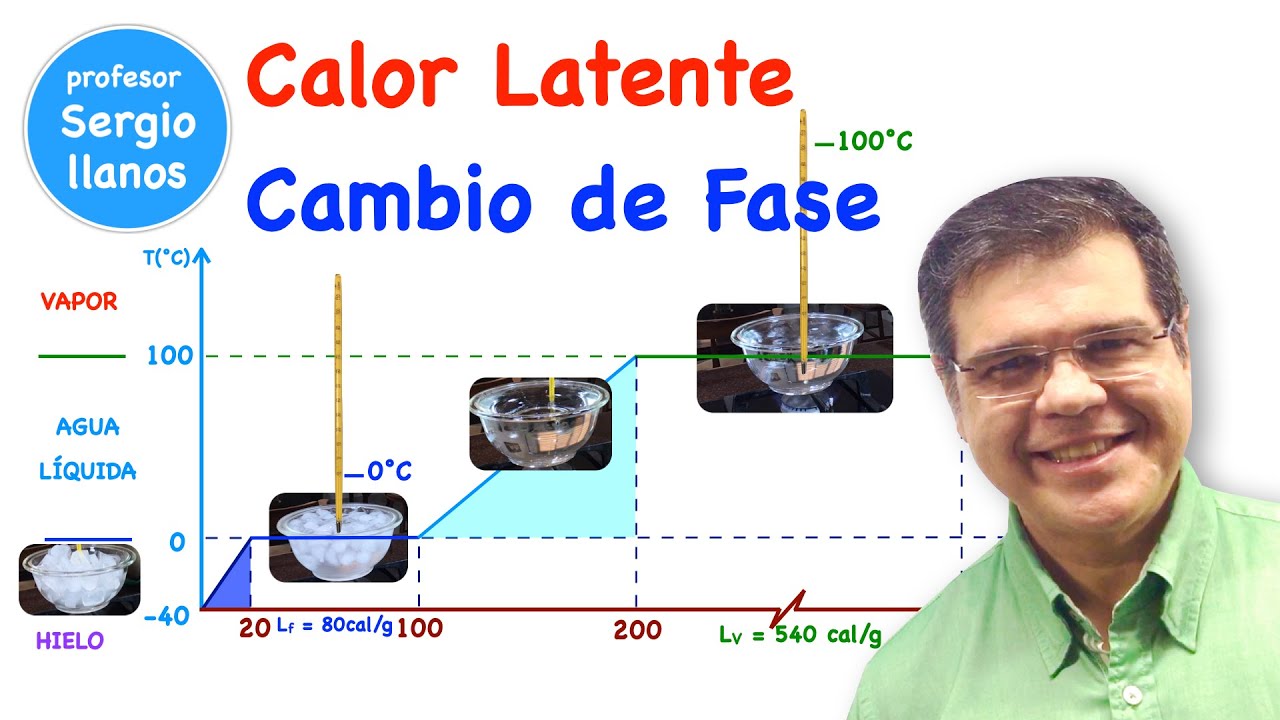
conoce como calor sensible sin embargo existe otro efecto que puede producir el aporte de calor a un cuerpo y es el cambio de estado en este caso la temperatura del cuerpo permanecerá constante a pesar de que se le está aportando calor lo que sucederá en cambio es que ese material o sustancia va a cambiar de estado al calor utilizado para cambiar de estado se le conoce como calor latente este calor latente se define como el calor que es liberado o absorbido por un cuerpo o sustancia durante un cambio de estado manteniendo la temperatura constante por
ejemplo para que el agua pase de estado sólido a estado líquido se requiere calor latente y ya que el proceso de cambio de estado sólido a líquido se denomina fusión esto se conoce como calor latente de fusión de la misma forma para que el agua pase de estado líquido a estado gaseoso se requiere también calor latente que en este caso se denomina calor latente de vaporización ahora ya que este calor latente no afecta como tal la temperatura del cuerpo o la sustancia este permanece de alguna forma oculto hasta que se libere en el proceso contrario
es decir para pasar del estado gaseoso al estado líquido ahora se requiere liberar calor latente este se conoce entonces como calor latente de condensación y de la misma forma para pasar de estado líquido a sólido se requiere liberar calor latente de solidificación de tal forma que podríamos decir que el calor latente es energía que se utiliza para cambiar de estado en lugar de cambiar la temperatura y éste se libera o se absorbe dependiendo del proceso que se esté llevando a cabo veamos por ejemplo la relación entre el calor latente y el calor sensible que ya
vimos supongamos que tenemos un cubo de hielo a menos 30 grados centígrados que sería agua en estado sólido y a este le empezamos a aportar calor lo que sucederá inicialmente es que la temperatura del hielo empezará a aumentar es decir que en este caso ya que el calor se está utilizando para aumentar la temperatura del cuerpo lo llamamos calor sensible esto sucede hasta alcanzar los 0 grados centígrados que es el punto de congelación del agua a partir de este punto el calor que se le aporte ya no se va a utilizar para aumentar la temperatura
es decir que durante este proceso la temperatura permanecerá constante a 0 grados centígrados y ese calor se va a utilizar para cambiar del estado sólido al estado líquido por eso lo llamamos calor latente ahora cuando el hielo se derrite completamente y quedamos únicamente con agua en estado líquido el aporte de calor va a producir un aumento en la temperatura nuevamente con lo cual lo llamamos calor sensible esto sucederá a los 100 grados centígrados donde encontramos el punto de ebullición del agua aquí entonces el calor que se le aporte al cuerpo se va a utilizar para
cambiar de estado líquido a estado gaseoso no para aumentar su temperatura con lo cual lo llamamos calor latente y una vez todo el agua se encuentre en estado gaseoso y le sigamos aportando calor su temperatura ahora comenzará a aumentar siendo este calor sensible esta fue una explicación sencilla de lo que es el calor latente y el calor sensible al igual que cómo se producen los cambios de estado sin embargo esto lo veremos más en detalle en el vídeo acerca de la humedad y el ciclo hidrológico espero que la información de este vídeo te haya resultado
útil si fue así dale al botón de me gusta suscríbete y activa la campana de notificaciones para que estés al tanto cada vez que se publique un nuevo vídeo [Música]




![Diferencia entre CALOR y TEMPERATURA en 5 minutos [FÍSICA]](https://img.youtube.com/vi/96Lku_Sd7vY/maxresdefault.jpg)







![ENERGÍA TÉRMICA 🔥| TEMPERATURA y CALOR 🧪[Definición y Diferencias]](https://img.youtube.com/vi/y_fIXAgHlBA/maxresdefault.jpg)