oi oi turma tudo bem hoje a gente tem a segunda aula de enzimas falando de cinética e inibição o da primeira aula a gente falou sobre conceitos gerais de enzimas fala um pouco da estrutura do fato de que as enzimas são na sua maioria proteínas e por isso vários dos fatores que alteram o seu funcionamento a gente fala um pouco de cofatores falou também sobre a influência de ph temperatura e concentração de enzima e substrato sobre a sua velocidade hoje a gente vai falar então um pouco mais sobre cinética enzimática e também sobre mecanismos de
regulação de atividade das enzimas nas nossas células começamos então pela cinética enzimática a atividade de uma enzima é medida através da velocidade da sua reação e lembrando que a equação geral da reação enzimática tem no início enzima mais substratos depois da formação de um complexo enzima-substrato a transformação do substrato formando um complexo em cima produto e depois da liberação dos produtos e a gente pode a falhar velocidade ou atividade de uma enzima por duas maneiras diferentes medindo a quantidade de substrato que a transformado ou consumido ou então medindo a quantidade de produto formato através da
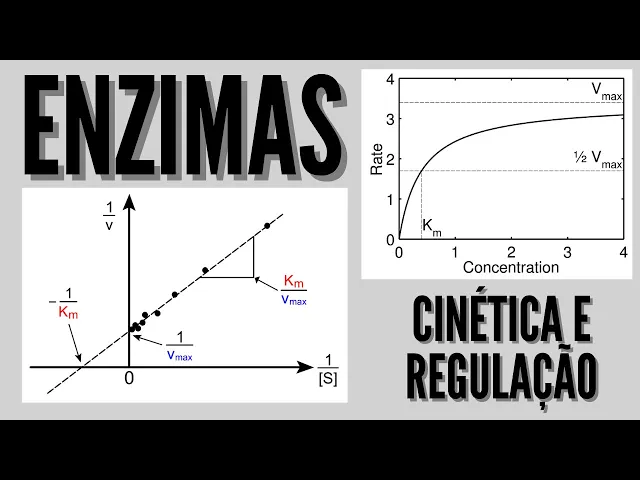
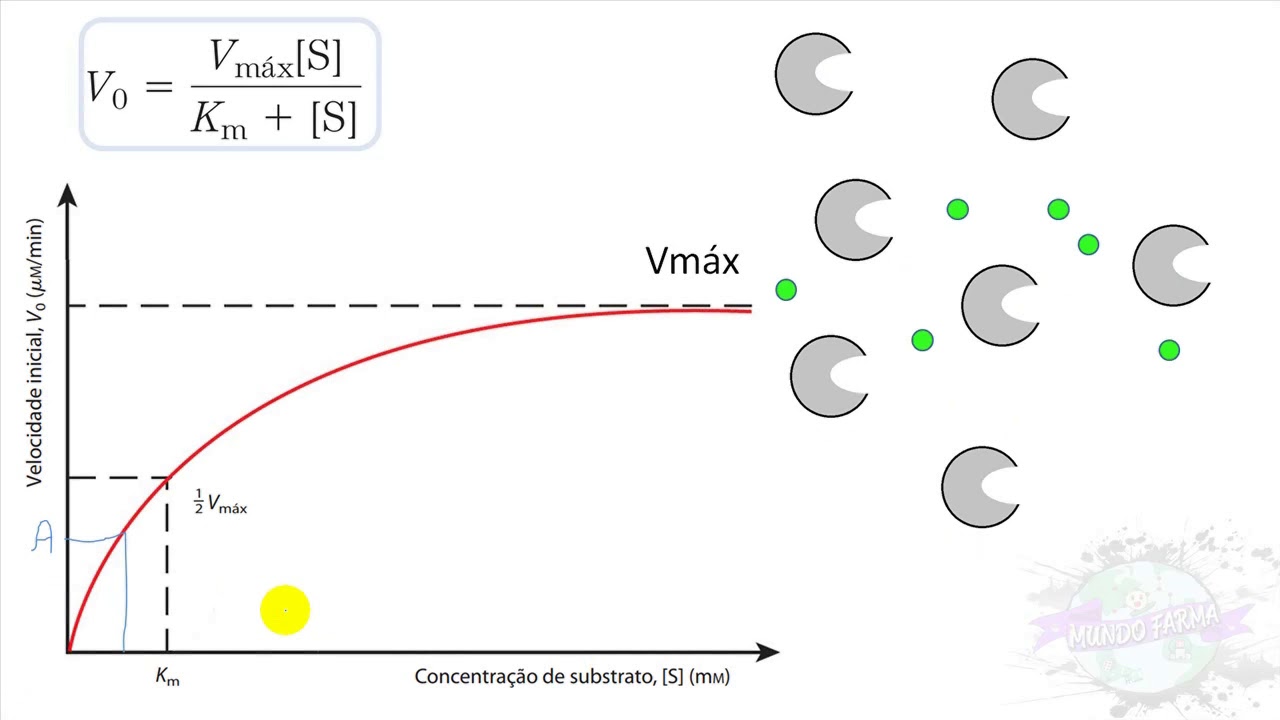
variação da velocidade dessa reação por unidade de tempo a gente pode determinar a atividade de uma enzima dois pesquisadores se destacaram no estudo da cinética enzimática michaelis e mantém-se dois pesquisadores trouxeram vários conhecimentos importantes sobre cinética enzimática ou seja sobre como a concentração de enzima e também principalmente a concentração de substrato afeta a velocidade das enzimas na outra aula a gente discutiu como a concentração de substrato pode afetar a atividade de uma enzima oi e o gráfico que a gente viu era parecido com esse que esse gráfico quer dizer que eu tendo condições fixas de
temperatura e ph e uma quantidade fixa de enzima à medida que eu vou aumentando a quantidade de substrato a concentração de substrato eu tenho um aumento na velocidade da enzima também em algum momento eu vou atingir a velocidade máxima que significa velocidade máxima é aquele ponto a partir do qual eu posso adicionar mais substrato e a velocidade não vai mais ser alterado então através de vários estudos cálculos esses pesquisadores trouxeram um cálculo de uma constante que a gente chama de km matematicamente o km pode ser expresso pela concentração de substrato necessário para que a gente
atingir a metade da velocidade máxima na reação enzimática então km também é chamado de constante de michaelis menten e essa constante é flash o poder catalítico da enzima em alguns autores sugere que o km pode também refletir a afinidade da enzima pelo seu substrato essa constante é específica para cada enzima e para cada substrato e esse gráfico mostra uma consideração interessante também que foi discutida na outra aula que avaliação da atividade enzimática à medida que a gente tem uma alteração na quantidade de moléculas de enzima então por exemplo a gente pode ter uma velocidade máxima
com um número x de molécula de enzima e se a gente tiver três vezes esse número de moléculas a gente vai ter três vezes a velocidade máxima ou seja uma coisa que pode acontecer fc a célula precisar de mais velocidade numa reação ela pode introduzir mais moléculas de enzima então a atividade de cada molécula permanece a mesma no entanto a velocidade da reação vai ser proporcional à quantidade de moléculas dessa enzima e como foi falado na outra aula a velocidade uma atividade da enzima vai depender da presença de com fatores ciência sem precisar além disso
km que reflete o poder catalítico da enzima outros fatores que podem alterar atividade das enzimas como também o previsto são variações de ph e temperatura além disso a presença de inibidores afeta a atividade das enzimas agora a gente vai falar um pouco sobre os tipos de exibição enzimática primeira forma de classificar a inibição enzimática é através da inibição inespecífica ou inibição específica em um caso de uma inibição inespecífica a gente tem uma redução da atividade de todas as enzimas e um determinado sistema por exemplo o inibidores inespecíficos seria um agente desnaturante considerando que as enzimas
são proteínas a desnaturação da sua estrutura faz com que elas pegam a sua atividade no caso agora de inibidores específicos a gente vai ter como o nome sugere a inibição de uma enzima ou a pulga estrito de enzima a edição específica ainda pode ser dividida em inibição irreversível ou inibição reversível na inibição irreversível o inibidor vai ligar na enzima de forma estável isso é um inibidor vou fazer uma ligação covalente com a enzima nesse caso no momento em que eu tenho a inibição irreversível aquela molécula de enzima tá fervida para que a célula consiga recuperar
a velocidade dessa reação ela vai precisar produzir novas moléculas de enzima um exemplo muito comum é bem importante de inibição irreversível é inibição da ciclooxigenase uma enzima importante que produz mediadores de inflamação dor febre pelo ácido acetilsalicílico já na inibição reversível a gente tem uma ligação mais fraca entre inibidor enzima e nesse caso a inibição não envolve uma modificação covalente e também a gente tem tipos diferentes de inibidores reversíveis e a gente tem ainda tipos diferentes de inibidores reversíveis os inibidores competitivos não competitivos ou mistos na inibição competitiva o inibidor tem uma semelhança estrutural com
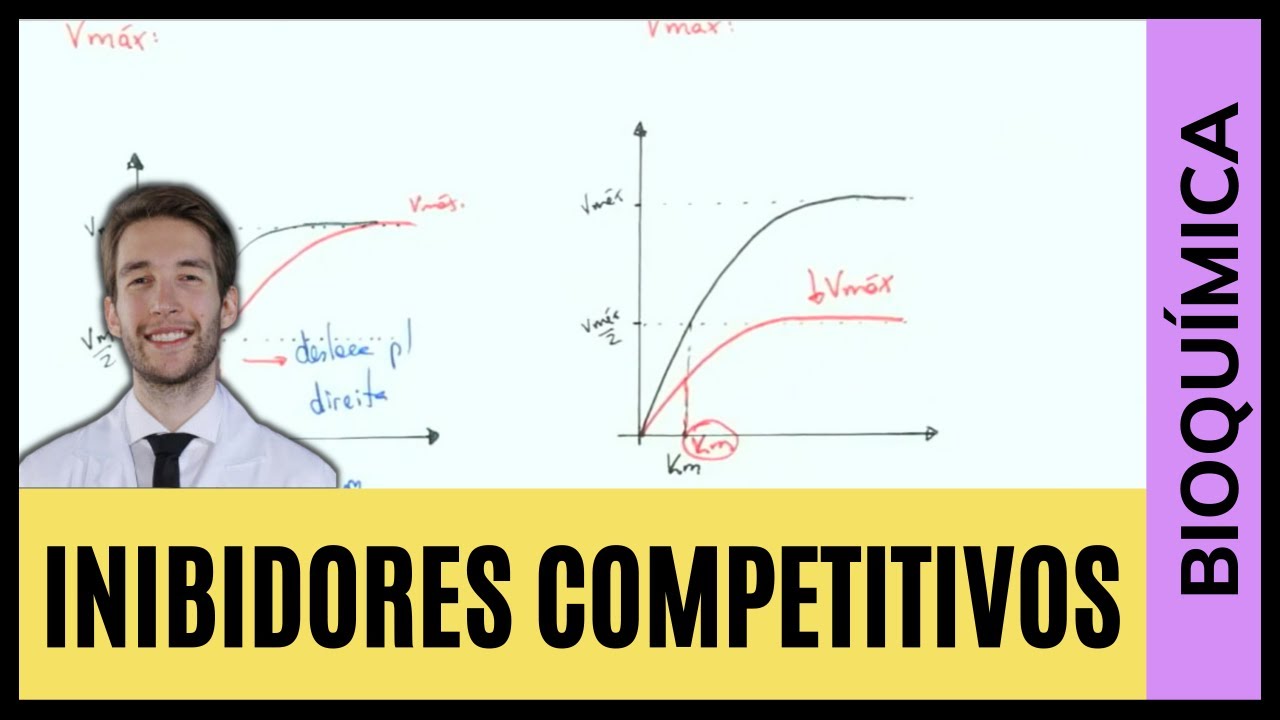
o substrato isso faz com que ele ligue no sítio ativo da enzima dessa forma lhe bloqueie o acesso do substrato da enzima como demonstrado nesses dois esquemas o inibidor desloca o substrato do sítio de ligação pois eles estão competindo e em relação à inibição competitiva existe o outro detalhe importante na presença de inibidor competitivo a gente pode aumentar a concentração de substrato isso vai fazer com que em cima possa voltar a funcionar normalmente porque depois eu aumentar a concentração de substrato eu começo a deslocar o inibidor do sítio de ligação e dessa forma consigo fazer
a velocidade da enzima aumentar ou seja como vocês podem observar esse gráfico se a gente adicionar o excesso de substrato uma grande quantidade desse subtrato a gente consegue atingir a velocidade máxima o que vai mudar é o km que aumenta o que significa isso que eu vou precisar de uma quantidade maior de substrato para chegar na metade da velocidade máxima o nome de salmão competitiva a gente tem algumas diferenças a primeira delas é que exibido não tem semelhança estrutural com o substrato e ele não vai ligar no sítio ativo da enzima então na inibição competitiva
[Música] [Aplausos] e olha só desculpa se eu quis dizer na inibição não-competitiva tá corrigindo a gente tem a interação do inibidor com o complexo enzima-substrato como vocês podem ver nesse esquema que a esquerda também como vocês podem ver nos dois desenhos o substrato vai ligar no sítio ativo da enzima no entanto a enzima funciona na velocidade mais baixa o que de novo o inibidor liga-se em um sítio diferente do sítio ativo que é onde o substrato vai ligar é por causa desse perfil diferente da inibição não competitiva em relação a competitiva na presença de inibidor
não competitivo não adianta o aumentar a quantidade de substrato isso não vai alterar o perfil de inibição da enzima já que inibidores substrato não estão competindo pelo sítio ativo da enzima ou seja a gente não tem uma alteração do km posso colocar um monte de substrato que eu não vou chegar na velocidade máxima que eu teria sem a presença de inibidor no caso então da inibição não-competitiva velocidade máxima diminui e o km não é alterado talvez vocês estejam se perguntando por que que ele tá falando tanto de enzimas inibição enzimática onde é que eu vou
usar isso as enzimas não participam somente do metabolismo energético aquele que nos fornece energia principalmente na forma de atp mas elas estão presentes em várias vias metabólicas vias de síntese por exemplo de alguns compostos importantes para o funcionamento das nossas células é bastante comum as enzimas serem alvo é lógico então a gente tem vários e vários e vários exemplos de fármacos que atuam inibindo a velocidade de enzimas e dessa forma regulando alguns processos que podem estar alterados em algumas doenças quando essas enzimas também estão alteradas existindo um terceiro tipo de exibição que inibição mista onde
o inibidor também não tem semelhança com o substrato mas nesse caso ele pode ligar tanto ao complexo enzima-substrato como é o caso da inibição não-competitiva mas também a enzima somente sem o substrato então agora a gente vai falar sobre mecanismos de regulação da atividade enzimática e quatro mecanismos que vão ser abordados nessa relação enzimas alostéricas modificação covalente clivagem proteolítica de enzimas e controle higiênico que são as enzimas alostéricas são um grupo bastante importante de enzimas que a gente possui e elas são principalmente enzimas regulatórias que não tem o comportamento micaele ano no caso das enzimas
alostéricas a gente tem a sua velocidade ajustada pela ligação reversível de um modulador ou também chamado um efetor alostérico em um determinado o sítio da enzima que não é o sítio ativo esses moduladores podem ser inibidores ou ativadores as enzimas alostéricas apresentam o fenômeno chamado cooperatividade positiva é que esse fenômeno quando a gente tem a ligação de um substrato em uma subunidade ocorre a facilitação da ligação de substratos em outras subunidades ou seja à medida que o primeiro substrato liga aumenta a afinidade da enzima por mais substrato o caso então como funcionam as enzimas alostéricas
elas estão em constante equilíbrio entre o que a gente chama de estado te ou tenso e estado r relaxado no estado te a enzima está com uma velocidade menor gente pode considerar que ela tá inativa no estado ela está com uma atividade maior ou seja a gente pode considerar que ela está mais ativa assim mas na lotéricas estão sempre em equilíbrio entre os estados te inativo e r ativo e essas duas figuras a gente pode observar o comportamento das enzimas alostéricas então na figura da esquerda nós temos a enzima em estado te ou seja atividade
menor inativa no momento em que esse equilíbrio tende pro estado r ela vai ligar no substrato e no momento em que ela liga o primeiro substrato ela aumenta a afinidade para ligar mais moléculas de substrato oi e o gráfico da direita mostra a curva da enzima lotérica do como vocês podem ver não é uma curva igual àquela descrita por michaelis-menten no início afinidade é menor o substrato pela enzima à medida que o substrato liga essa afinidade aumenta ah e também vocês podem observar qual é a curva na presença de um ativador e na presença de
um inibidor alostérico e assim mas a lotérica são muito importantes principalmente na regulação de vias metabólicas uma segunda forma de modular a atividade das enzimas e através de ligações covalentes então a gente pode adicionar alguns grupos nas enzimas fazendo com que elas alteram em a sua atividade é uma forma muito comum de modular a atividade de enzimas e aplicações de fosforilação então a gente tem por exemplo substrato proteico né uma enzima com resíduo de serina treonina ou tirosina que são resíduos que contém hidroxilas livres e nessas hidroxilas a gente pode ter ação de quinases que
são enzimas que vão fosforila os seus substratos do contrário a gente tem outro grupo de enzimas chamadas e fosfatases que podem desfosforilar o seu substrato ou seja retira esse fosfato e deixa em cima novamente na sua forma inicial outros tipos de modificação incluem a acetilação onde a gente pode adicionar assertivas lá em cima um exemplo é de novo a sigla com ácido acetilsalicílico e a gente também pode adicionar mente las tradição de mentiras também mudou uma atividade de enzimas bom então o que a gente viu até aqui um grupo de enzimas que tenha comportamento micaele
ano que podem ser exibidas de forma irreversível ou reversível e dentro da reversível competitiva não competitiva e mista dependendo do perfil do inibidor em relação ao fato de ligar ou não no sítio ativo da enzima a gente também falou sobre as mesmas ao lotéricas ela tem um comportamento um pouco diferente das enzimas microbianas e elas são importantes reguladoras do metabolismo e a gente falou também de como as enzimas podem ser alteradas através de modificação covalente esses tem mais dois mecanismos importantes o primeiro desses mecanismos ea clivagem proteolítica de enzimas e a gente produz muitas enzimas
na forma de próximas ou zimogênios que é isso são enzimas que não têm atividade então quando elas são produzidas elas não têm atividade e no momento em que elas sofrem clivagem proteolítica ou seja elas perdem um pedaço da sua estrutura elas vão perder uma sequência de aminoácidos elas se tornam ativas existem vários exemplos importantes desses processos enzimáticos que são ativados por clivagem proteolítica como exemplo a gente pode citar as enzimas digestivas lá são produzidas na forma de zimogênios momento que são privadas se tornam ativas e fazem principalmente a digestão de proteínas o outro exemplo muito
importante que é todo mediado por proteínas produzidas de forma inativa como zimogênios é a cascata de coagulação do sangue e uma outra aula a gente vai falar especificamente desse processo de coagulação do sangue mas a gente tem aqui uma sequência de reações e onde a gente tem ativação de proteases ou seja uma protease e a uma enzima que vai atuar sobre uma outra proteína que forma fazendo essa clivagem quando a gente tem um sinal de coagulação do sangue tem que calcular a gente começa uma cascata de reações onde uma protease e vai ativando a outra
isso combina com a produção de fibrina a partir de fibrinogênio essa fibrina vai formar um polímero e uma rede que vai ajudar no processo de coagulação é porque a gente produzem enzimas como se mo gênios ou seja enzimas que não são ativas estão inativas e vão ser ativadas mediante algum determinado estilo trazendo de novo exemplo da população a gente precisa ter esses fatores de coagulação essas proteínas todas circulando no nosso sangue o momento que a gente tem uma população eles têm que estar prontos para g então da mesma forma que a gente não pode esperar
ter uma hemorragia ou sangramento ou uma lesão do tecido para dar tempo do fígado produzir todos esses fatores de coagulação a gente também não pode ter esses fatores fazendo a população quando não houver um estímulo da lesão ea última estratégia que a gente vai falar na aula de hoje é sobre o controle em nível genético então as células elas podem modular a quantidade de moléculas de enzima que elas têm presentes isso geralmente acontece quando eu tenho uma maior disponibilidade de substrato ou seja uma situação em que o aumento a quantidade de substrato vai fazer com
que a célula produza mais moléculas enzimas um exemplo a gente pode citar as enzimas do ciclo da ureia quando eu tenho uma ingestão maior de proteínas eu vou ter uma degradação maior de aminoácidos e uma necessidade também maior do funcionamento do ciclo da ureia então o nosso corpo consegue sentir isso e produzir mais enzimas para essa via metabólica ao contrário se não tiver uma ingestão menor de proteínas o corpo sente que não precisa ter tantas moléculas das enzimas desse ciclo e vai diminuir a sua produção então nessa aula a gente falou sobre o funcionamento das
enzimas e cinética enzimática e começa as regiões podem ser reguladas bom valeu boa aula a evolução de cada um oi oi turma tudo bem a aula de hoje é sobre enzimas não vamos tentar não gravar a aula com gatos de gatos de fundo oi oi é você que tem gatos e não sabe o que fazer sugestão quem tem gatos sabe whiskas me patrocina foi só pegar aqui ó e vem cá semana vem cá um vem cá para as pessoas que conhecer vem cá e essa é a fiona se trata mais fofa que vocês vão ver
na vida né o carro perfeitamente comprar as coisas sachê podemos voltar a aula em pó os principais tá cara que é o mario não está atrapalhando a aula a briga com ele e não né e aí e agora para divulgar senão vai aparecer no áudio e por favor para de roubar eu não posso pegar contigo porque senão ninguém para presta atenção na bioquímica é muito mais interessante ver química quem é e aí o que se faça já tá acabando toda a figura da esquerda a gente tem inicialmente a enzima no estado de ou seja e
nativo e a janela bateu eu acho que não ficou claro né