o Olá tudo bem com você Estou mais uma vez de volta que é o nosso canal para te ensinar um pouquinho mais de química e a aula vai tratar agora sobre um tema relacionado com a atomística atomística gente é a parte da química que estuda o átomo por isso nosso tema hoje vai ser delineado especificamente para tratar sobre os modelos atômicos Mas antes você já sabe se inscreva aqui no nosso canal deixa a sua curtida aí e ativa o Sininho de notificação vamos lá começar então quando a gente fala na política de modelos atômicos nós
queremos trazer para você a ideia de queixar como nunca foi visto a olhou e atualmente através de todo desenvolvimento científico e tecnológico temos nas áreas experimentar ainda é muito difícil se definir realmente como é a estrutura deste arma por isso foi criada as ideias aí suposições o modelo de como realmente é este aqui mesmo e o primeiro modelo atômico está associado ao modelo puramente filosófico trazido por dois filósofos gregos chamados de Demócrito e leucipo onde aproximadamente por volta do ano de 450 antes de Cristo esses dois filósofos começaram a se questionar de como a matéria
era constituída a gente começaram a quebrar sucessivas vezes ver o que eles encontravam no interior daquela matéria e conta a história que eles pegaram cadastro de rocha que quebraram quebrado que brava Até que chegaram a menor partícula não menor pedaço dessa pedra que eles não conseguiam mais quebrar Então imagina aí o grãozinho de areia e quando ele se encontraram esse grãozinho de areia não conseguiu mais quebrar esse grown in deduziram filosofia o rio era a menor partícula da matéria e chamaram essa menor partícula de átomo onde este a significa um prefixo de negação que significa
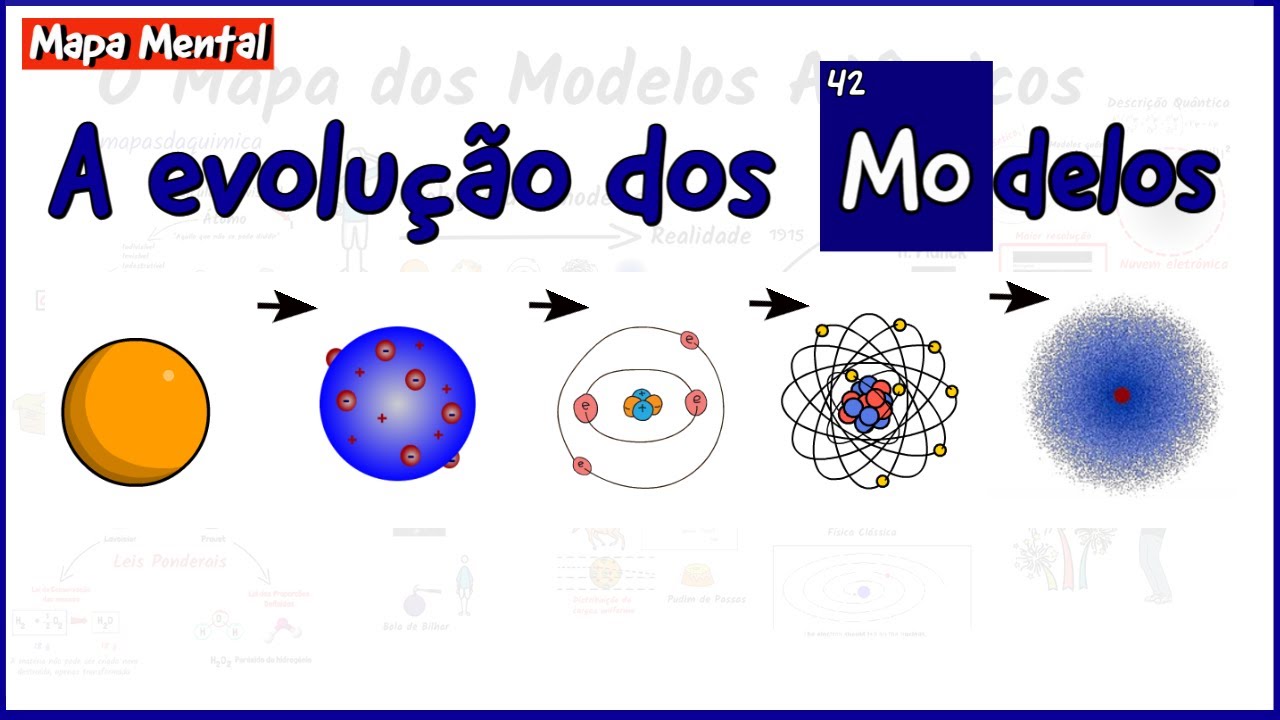
não e Thomas está relacionado com o significado de parques então se eu posso definir para você o que seria átomos segundo Demócrito e leucipo é a parte da matéria que a gente não consegue mais quebrar que não pode ser mais dividida partindo dessa ideia hoje agora o segundo modelo atômico está relacionado ao cientista álcool onde dá o com disse que o seu modelo atômico era muito parecido com uma bola de bilhar porque ele era indivisível e indestrutível homogêneo e maciço e indivisível e indestrutível está muito relacionado o cômico de Demócrito e leucipo não pode ser
dividido não pode ser destruído novidade do modelo atômico de Dalton está relacionado a eles e homogêneo e maciço onde esse mas está associado com a ideia de que tem massa e com essa ideia de que o átomo É mássico e tem massa nós vamos partir agora para o terceiro modelo atômico onde alguns experimentos já haviam sido realizados E torça ou propôs que o átomo seria parecido com o modelo pudim de passas maciça modelo pudim de passas porque partiu-se da ideia da bola de bilhar ser uma esfera essa espera seria positiva e teria encrustado seja grudado
na sua superfície partículas negativas e Isso está muito é a ideia que próximas teve em relação ao pudim de passas a massa positiva do átomo seria a massa do pudim E as falsas que estão enfeitando esse pudim seriam as partículas negativas na superfície deste a beleza no quarto modelo atômico nós já temos um desenvolvimento mais significativo das experiências em surge Rutherford com a ideia de que este arrumou agora Seria tipo o sistema solar ele começa a partir das experiências dizer eu assumo ele é divisível e vai apresentar duas regiões uma central muito pequena onde caracteriza
a massa do átomo chamado de núcleo e outra região muito espaçosa do lado de fora do ar no de uma região periférica chamada de eletrosfera e onde você tem a ideia do sistema falar justamente porque na eletrosfera estaria ou as partículas negativas e girando ao redor desse núcleo assim como os planetas assim girando ao redor do sol por isso o modelo de Rutherford ficou conhecido como modelo planetário ou modelo do sistema solar uma coisa que eu quero te chamar a atenção é que essa eletrosfera era formada por obter circulares segundo o modelo atômico de Rutherford
ok e como quem tu modelo temos a sequência do estudo do modelo atômico de Rutherford porém agora em para os postulados que o seu ajudante vó conseguiu prosseguir nos estudos e ele afirmou o seguinte E essa eletrosfera era formada por camadas onde essas camadas apresentavam níveis de energia assim como entre essas camadas existiam subníveis de energia em relação a criança a esses níveis de energia e subníveis de energia nós vamos deixar para ver um pouquinho mais lá na frente quando falarmos de distribuição eletrônica e números quânticos Por Enquanto no modelo atomico de rutherford-bohr eu preciso
apenas que você saiba se essa eletrosfera é formada por essas duas divisões e em vez de energia e entre os níveis de energia nós temos os subníveis de energia como se fosse uma escadinha até chegar lá no nível mas é bom voz também postulou o seguinte que se eu levo está circulando está se movimentando em uma camada Em um nível de energia tem ganhar ou perder energia ele vai continuar nessa camada e nunca vai sair dali isso é chamado de estado estacionário ou fundamental Então o que é o estado estacionário ou fundamental é aquele que
o elétron não ganha e nem perde o que energia por isso é que vai permanecer lá de forma indefinida tá bom porém Gente esse elétron um belo dia ele vai ganhar ou perder energia e quando ele ganha a energia quando a energia fornecida aí você leva ele salta para uma camada mais energética ou seja ele se afasta do núcleo quando isso acontece a gente diz que o elétrons entrou no estado excitado ou O porém ele é instável e o certo dia que vai perder essa energia Só que essa energia que perde na forma de luz
e calor e retorna para uma camada Myles energético ou seja de retorna para mais próximo do núcleo como mostra a sua animação aí tá bom outro ponto importante que eu quero frisar para você é que quando ele recebe essa energia entrando no estado ativado ou excitado a energia pode ser qualquer tipo de energia energia solar energia eólica no Goiás tipo mas quando ele perde a energia porque ele fica no estado energético muito alto de forma instável essa energia ele só libera na forma de luz ou calor tranquilo a sequência dos modelos atômicos tem como explicação
este essa questão dos saltos quânticos né de receberem ganhar e perder a energia através da a queima de fogos de artifícios que a gente ver muito aí nas festas de finais de ano junto com a pólvora em hospitais e de determinado elemento químico que quando eles fazem essas transições eletrônicas ele Zidane perde energia soltando a coloração específica de cada onde casa átomos de cada elemento químico temos também a questão do modelo atômico de rutherford-bohr presente nas pulseiras de neon muito utilizado aí nas festas nas baladas da vida e também no processo de bioluminescência dos vagalumes
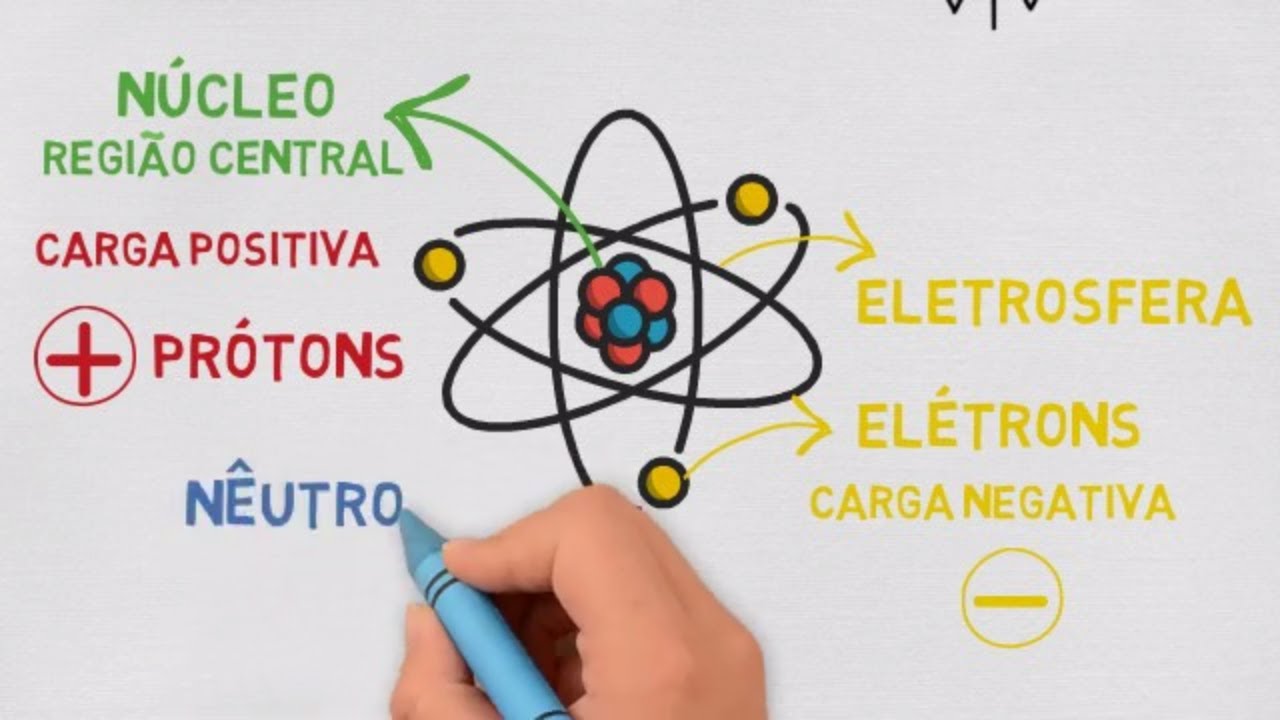
então a gente vê relações com o nosso cotidiano onde os modelos atômicos estão bem presentes no nosso dia-a-dia tá bom tempo apresentação dos modelos atômicos para você chegou o momento agora de tia apresentar as partículas sub atômicas Porque até então eu só tava falando em partículas negativas e positivas as partículas sub atômicas elas são divididas em três e até esses modelos atômicos Tá ok as partículas positivas elas vão ser chamadas de prótons e elas estão localizadas no núcleo são as bolinhas em vermelho aí na sua animação já as partículas negativas elas são chamadas de elétrons
são elas que estão girando aí na sua eletrosfera na forma de bolinhas azul na sua animação e temos também uma outra partícula que está em verde que são os neutros e são as partículas neutras são bem localizado no seu núcleo e agora você começa a relacionar quando eu disse no slide anterior porque o lucro apresenta né a característica da massa do aro O que é Latte nós vamos encontrar os próprios seus neutros não é exatamente o aspecto da massa da Constituição deste a outra característica G e o núcleo ele apresenta propriedades positivas porque os próximos
que estão neste núcleos são positivos assim como as eletrosfera A sua eletrosfera também tem propriedades têm características negativas porque os elétrons que estão naquela eletrosfera eles são o que negativos e os neutros não consegue tantas né são meus Qual que é o nome daqui não é nem positivo nem negativo ela não influencia em nada nas questões elétrico de trás aí para você agora vocês o modelo atômico que está relacionado ao cientista homem Field onde eficiente Vista ainda faz parte leva em consideração a esse 10 do modelo atómico de Rutherford boa porém a única diferença é
que ele diz agora que as órbitas dessa eletrosfera deixe a elas são elípticas como Aparece aí na sua animação Então se tem uma relação de diferenciação em eu devo ter Fireboy somente hoje é essa lá e voltei fora ó as obras são que circulares lembra-la dos planetas girando ao redor do sol da animação que também eu coloquei para você e já aqui no modelo de comer Field as obras elas são elípticas tem esse formato aí mais oval como você vê na sua animação tem outros modelos atômicos tem tem um modelo por exemplo de tireóide e
diz que o átomo apresenta nuvens eletrônicas ao redor do núcleo em cima para você a nível de Ensino Médio na preparação do seu Enem basta você saber até o modelo de subsídio às vezes nem um modelo de só venceu de entra na questão da elaboração dos itens das questões mas se você entendeu Essa diferenciação entre cada um dos modelos você está bem preparado para realizar qualquer tipo de questão de prova se relaciona com o conteúdo e modelos aqui tá bom a criança muito obrigado Mais uma vez porque você teve preferência assistir nossos explicação o nosso
conteúdo você sempre é muito bem vindo aqui tudo que eu produzo para você é especialmente para você para te ajudar o seu estudo facilitar na sua vida e qualquer dúvida você já sabe onde me encontrar aí né gente ficou sociais meu e-mail basta tá mesmo e comunicação não tenha vergonha entre em contato pergunta e é isso Até a próxima aula 1