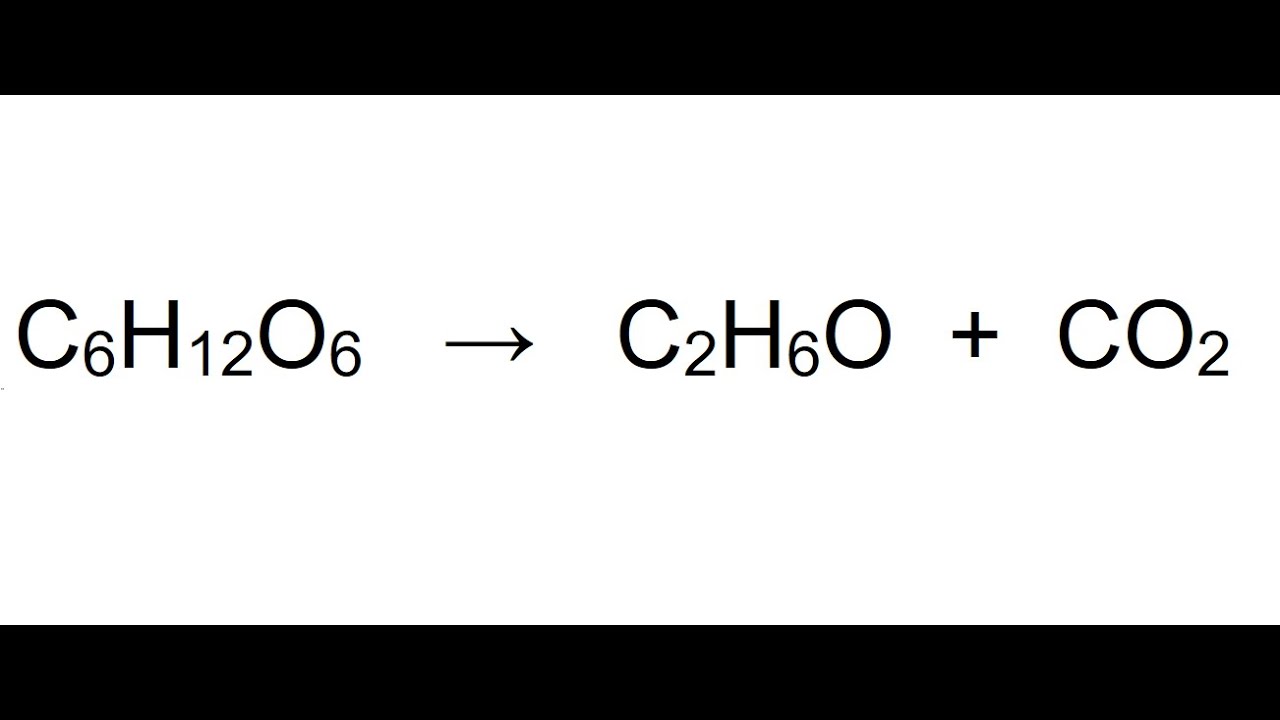o Olá eu sou a Inês e vou ser atual se nesta série de vídeos de química Neste vídeo vamos falar sobre reações químicas e equações químicas e cálculos estequiométricos Bora lá as substâncias sofrem transformações químicas que dependem da própria estrutura atômica e molecular e também das substâncias com que reage a estas transformações damos o nome de reações químicas à medida que uma reação química que ocorre a formação de novas ligações químicas ocorre a quebra de ligações entre os átomos das substâncias iniciais os reagentes que levam a obtenção de novas substâncias os produtos da reação assim
numa reação química os reagentes são as substâncias consumidas e os produtos da reação são as substâncias que se formam Por exemplo quando cozinhamos os alimentos no fogão a gás está a reação química de combustão entre o gás por exemplo tem e o oxigênio danos à formação de dióxido de carbono e vapor de água esta reação química pode traduzir simbolicamente por uma equação química que esta as reações químicas traduzem-se por equações químicas que indicam os reagentes utilizados e os produtos formados apresentados pelas respectivas fórmulas químicas em que a seta indica o sentido da reação química e
as proporções em que se combinam os reagentes e em que se formam os produtos de reação estas proporções são indicadas pelos números escritos antes das formas químicas que se designam por coeficientes estequiométricos que neste caso são os números dois 13 8 e 10 podemos ver esta equação química considerando a quantidade de matéria em Londres assim o modo moléculas que C4 H10 reagem com 3 modos de leque do 2 original oito módulos Marcos de CO2 e 10 mol de moléculas de H2 o na equação química podemos ainda referir os estados físicos reagentes e dos produtos Reação
em abreviaturas entre parentes como esse para o estado sólido para o estado líquido e e para o estado gasoso e aqui para a solução aquosa a lei lavo agir ou Lei da conservação de massa ser que em qualquer reação química a nossa Tolle reagentes é igual a massa total de produtos da raça não existente perder matéria deste modo o número de átomos de cada elemento químico existente no início da reação tem que ser igual ao número de átomos desse elemento nos produtos reação Por isso as equações químicas devem sempre ser acertadas a serem sempre escritas
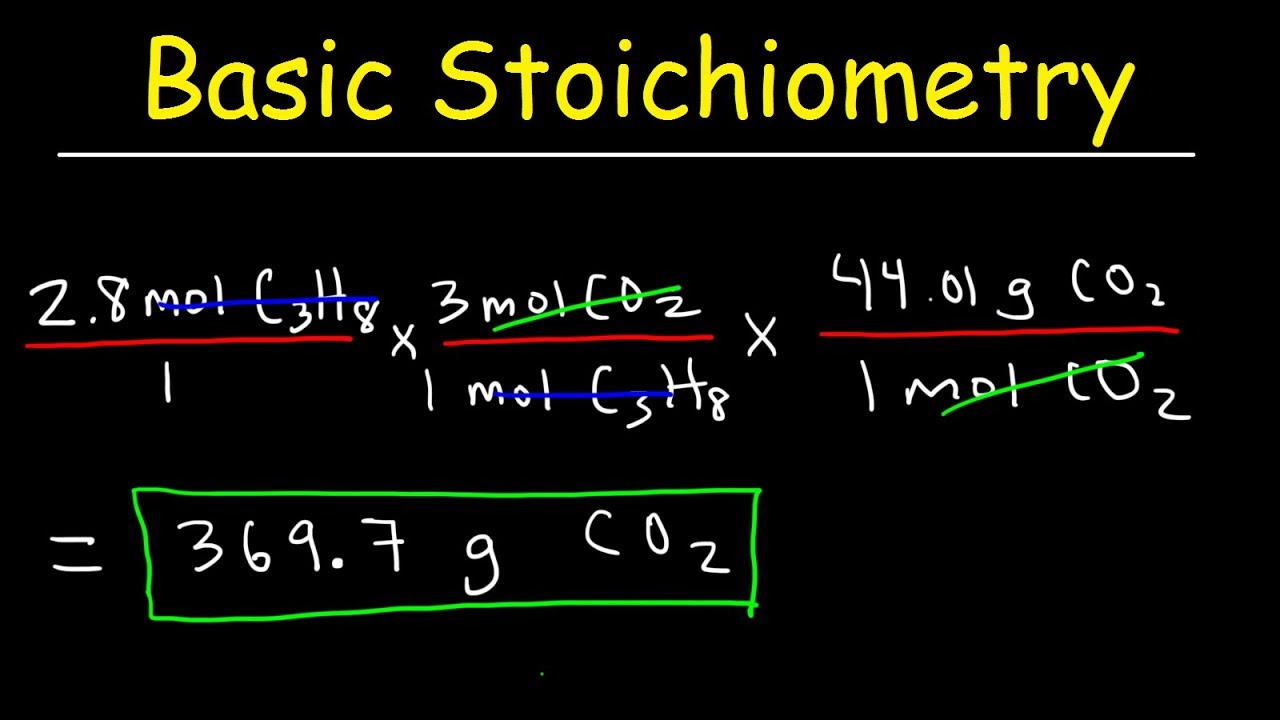
com os coeficientes estequiométricos que garante igualdade entre um gatos de cada elemento nos reagentes e os produtos de reação para perceber melhor esta parte que vem a seguir deve-se rever os conceitos quantidade de matéria volume molar massa molar número de entidades e constante de avogadro Que destino 10º ano como deves compreender numa fábrica um laboratório é absolutamente necessário fazer previsões sobre as quantidades de reagentes que se Gastão ou sobre as quantidades de produtos de reação formatos estas previsões tem com base os carros estequiométricos ou seja os cálculos baseados nas equações químicas conforme informação e vamos
a um exemplo você tem que saber o volume de vapor de água produzir a condições PTN a partir da combustão completa de uma botija de pressão com massa de 3 Kg tendo em conta a informação da equação química apresentada no início após proceder ao cálculo várias formas mas o mais fácil determinar a quantidade de botar na botija e depois trabalhar com as proporções estequiométricas em quantidade de matéria ou seja em morre a primeira etapa a ser realizada é o cálculo da quantidade de matéria em destaque para isso vais utilizar uma forma objeto o conhecida em
que a quantidade de matéria n = massa a dividido pela massa molar e sempre em conta que tem uns 13.000 gramas de botar e a massa molar 58,4 de grama por mole quase obter o valor de 220 e 3,6 molde Gotham a segunda etapa é o cálculo da quantidade de matéria de água tendo em conta as proporções estequiométricas sabes que duas modo butano corresponde a 10 mol de água assim pode-se concluir que 223/16 modo butano o valor se deu na primeira etapa corresponde a1118 molde água por fim a terceira etapa é o cálculo do volume
de água formado a condições PTN sabes que o sumo é igual a volar vezes a quantidade de matéria Como regular estas condições é 22,4 centros públicos por mol obténs para o volume de água um valor de 25 mil 43,25 públicos e se no final ainda quiseres saber a quantidade de oxigênio necessária para a combustão da botija de preço quilogramas portanto percebe-se de forma análoga sabes que duas modo butano corresponde a 13 molde oxigênio assim sabes que 220 e 3,6 modo de Tam correspondem a 1.450 e 3,4 molde ou 21 E aí G1