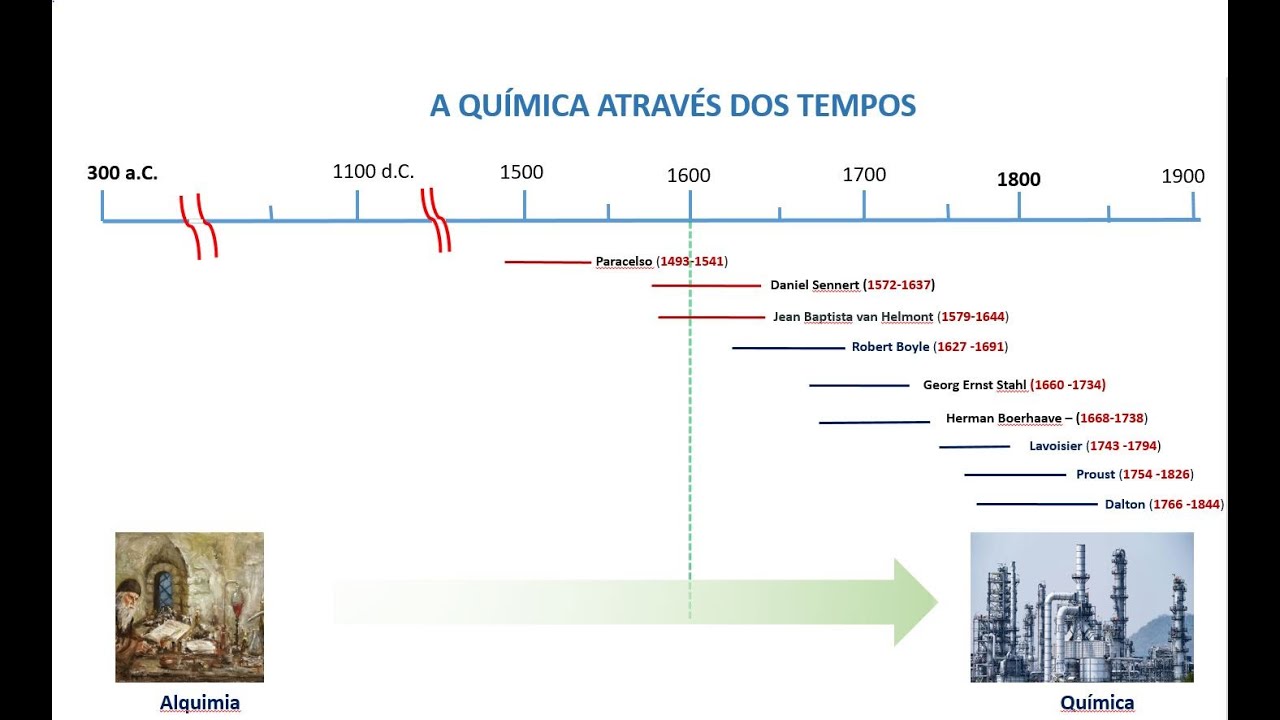
O Olá pessoal vamos continuar nosso estudo sobre história da química Nesta aula nós vamos falar sobre a desenvolvimento da físico-química no século 19 uma das trataremos jogos aspectos relacionados ao nascimento da físico-química no século 19 falaremos um pouco sobre a natureza do calor é bom química gases EA teoria cinética Cinética de reação em equilíbrio químico e faremos algumas considerações ao final o nascimento da físico-química do século 19 durante o século 19 área de físico-química se desenvolveu paralelamente às áreas de química orgânica e inorgânica E essas duas áreas nós tivemos vídeos anteriores nós tratamos com bastante
detalhes sobre diversos aspectos relacionados a evolução EA consolidação da química Orgânica bem como a organização da química inorgânica e os principais Progressos ocorrerão nos campos da cinética e termodinâmica e eletroquímica além desses estudos e além disso desses estudos de fotoquímica ecológicos também tiveram início Neste período mas os avós dessas áreas somente vieram a ocorrer no próximo século o desenvolvimento da teoria cinética da termodinâmica ocorreram de forma paralela tiveram suas bases na física do Século 19 esse período os químicos estavam preocupados muito mais preocupados com as descobertas qualitativas na área da química orgânica desconsiderando as leis
matemáticas físicos por outro lado empregavam materiais químicos e tentavam fazer generalizações a partir dos resultados obtidos e substâncias específicas para casos Gerais gases ideais líquidos sólidos cujas propriedades poderiam ser explicadas por leis Gerais nos vemos em Vídeos anteriores sobre toda a evolução EA consolidação da química orgânica e todo aquele trabalho foi realizado sem qualquer fundamentação matemática e os que estavam preocupados com substâncias específicas e com base naquela substâncias eles criaram todo um arcabouço e combinou com a teoria estrutural orgânica os físicos por outro lado e nessa área vamos incluir depois os físico-químicos né estavam preocupados
em estudar as substâncias Mas olhando assim de uma forma diferente tentando entender e o comportamento geral dos gases comportamento geral dos líquidos e sólidos e não casos específicos a procurando sempre encontrar leis mais Gerais É mas eu não menti químicos faziam alguma observação que era apropriada pelos físicos que investigavam mais detalhes todavia outros químicos não prestavam muita atenção na descoberta um exemplo disso que acabamos de falar Tentamos observação feita por gay dos aqui que era um químico de um gás ao se expandir no vácuo e aqui o destaco que desse processo o gás não realiza
trabalho é esse caso não sofre mudança de temperatura essa informação foi utilizada pelos físicos quando começaram a estudar o comportamento dos gases mas não durou outros químicos Apesar desses aspectos aos poucos a área de físico-química se consolidou como um Ramo da química isso estamos falando do século 19 e outras palavras enquanto vários químicos estavam trabalhando no sentido da consolidação da área de química orgânica esse outro grupo de químicos e tinha interesse também no entendimento dos processos de uma forma mais quantitativa em Santa matemática na descoberta de teorias equações que explicasse comportamento geral dos gastos fixos
e dos sólidos esse grupo Também estava atuando e nesse sentido a data de nascimento da físico-química é sempre tida como sendo 1887 ano que apareceu a primeira edição do jornal de físico-química estequiometria e teoria da afinidade o nome desse jornal é Originalmente e o nome alemão tá aqui embaixo aí eu coloquei uma tradução em português para dar uma ideia do significado de curica essa revista tratava essa primeira Revista de disco química era editada por Friedrich Wilhelm ostwald que Jacobs rende henricus vant Hoff conta com o apoio irrestrito Oi Augusto arreios químicos físico-químicos nós trataremos de
trabalhos deles ao longo desta apresentação é que você tem uma imagem Osvaldo nasceu 1853 morreram e 32 típico alemão um dos fundadores como eu acabei de dizer da físico-química e fundador deste jornal e foi laureado com o prêmio Nobel de química em 1909 observa que Ainda com 55 56 anos de idade é a natureza do calor todos os partidos momento falar de vários aspectos várias Ramos Associados com Associados né com que veio a ser cunhado de físico-química nós vamos começar a nossa apresentação então falando sobre a natureza do calor desde os tempos antigos a humanidade
especulava sobre a natureza do calor O fogo é um dos quatro elementos nós já Vimos que estes elementos eram o fogo a terra a água eo ar e o fogo deles eram mais quente e o período da revolução científica que ocorreu essencialmente Centralizado em do século 17 acreditava-se que o fogo era uma substância e para alguns era composto de átomos e para rodas de boi ing filósofo natural irlandês existiam partículas de fogo e sim Impregnava nos corpos durante a calcinação e para Robert hooke quinto inglês que trabalhou durante muito tempo juntamente com Robert Boyle o
calor se originava do movimento das partículas dos corpos Observe que como nos veremos o decorrer dessa apresentação objetiva uma visão bem mais avançada tava pensando que o calor estava relacionado com o movimento de Partículas E durante o século 18 Joseph Black médico e químico vocês que nós vimos deu grande contribuição para o desenvolvimento da química pneumática é o descobridor do gás carbônico ele estabeleceu também os fundamentos da calorimetria para ele o calor era um fluido que podia ser absolvido pelos copos ou sair deles Black introduziu o conceito de calor Latente imaginando que o gelo ao
se fundir combinava com o calor a água ao se combinar o mais calor chegava um ponto que entrar em ebulição black friday bastante Pioneiro Estava bastante à frente de seu tempo quando ainda na segunda metade do século 18 não apenas contribuiu para o desenvolvimento da química pneumática mas também para Olá tudo sobre a natureza do calor o outro cientista que foi um dos Pioneiros no estudo do calor Lavoisier do qual nós falamos bastante em um vídeo anterior Lavoisier io a teoria do surto incluiu em sua tabela dos elementos publicado em seu líquido o elemento que
ele chamou de calor e esse calor e lhe deu o nome de calórico para Lavoisier elementos tal como o oxigênio é um compostos de calórico combinado com que ele chamou de base alimentar do gás ou seja o calor era um elemento e o Oxigênio é o elemento oxigênio não eram algo simples era formado pelo calórico mais uma base alimentar seja o elemento oxigênio era algo mais complexo que o conceito de elementos que nós temos hoje isso para Lavoisier é a primeira vidência experimental sobre a natureza do calor foi fornecida por Benjamin Thompson também conhecido como
Conde de rumford e não físico e inventor britânico que nasceu em Massachusetts ele observou que Uma grande quantidade de calor era gerada durante o processo de fabricação de canhões beija bem Thomson civil como Conselheiro do governador da Baviera e durante a guerra de sucessão da Baviera que ocorreu entre 1778 1779 ele supervisiona fabricação de canhões e observou que o atrito gerado durante esse processo liberava calor conforme então em 1798 e planejou o experimento em que um pedaço de Ferro o outro metal Utilizado para fazer um canhão foi colocado dentro de uma caixa e submetida a
perfuração o calor gerado durante a perfuração a broca conectado um torno Foi meticulosamente medido o torno era no ouvido com auxílio de dois cavalos ele então correlacionou o calor gerado o trabalho realizado pelos cavalos um dos seus experimentos com Ford concluiu que "parece-me extremamente difícil senão impossível Formar qualquer ideia de tinta de qualquer coisa sendo excitada ou comunicada de maneira como o calor foi comunicado nesse experimentos a menos que seja movimento a selva que Como pode Clara diz mostra aqui na sua na sua conclusão que para ele o calor tá relacionado ao movimento de alguma
coisa é na máquina material um forte continua por anos a defender a ideia de que o calor tinha natureza dinâmica Apesar de seus esforços dos seus resultados da seus trabalhos publicados muitos de seus contemporâneos não se convenceram de sua teoria John Dalton do pau nós já falamos bastante de uma importante contribuição à teoria atômica por exemplo ele escreveu seus átomos de gases como sendo esferas rodeados de calórico que era responsável pela repulsão entre as partículas Dalton que era um cientista natural filósofo natural muito importante a sua Própria e ainda bonitinho calórico e somente na década
de 1840 você Avaí já quase na final da primeira metade do século 19 é que teoria do calórico foi finalmente descartada Essa época conceito de energia estava começando a se desenvolver de uma forma mais concreta de uma forma mais com base de mais científicas e as principais contribuições desses nesse Campo vieram de Julius Robert Von Mayer o físico alemão e James prescott Joule físico e matemático inglês e o Julius Maia contra uma relação do América de equivalência entre o trabalho mecânico realizado no calor produzido o seu trabalho entretanto não chamou a atenção de outros pesquisadores
da época basicamente passou e quase que despercebido Todavia o trabalho de Shaolin que havia sido aluno de Dalton e ele investigou o efeito Da passagem de uma corrente elétrica sobre o aquecimento de um corpo então realizou experimentos com Dinamo e demonstrou a equivalência de calor e outras formas de energia ou seja o calor e outras formas de energia estavam relacionados era possível encontrar uma relação ele estabeleceu então o princípio da Conservação da energia e finalmente defendeu a teoria Mecânica do calor sendo feito várias determinações muito precisas sobre o equivalente Mecânico do calor tem essa imagem
é o equipamento utilizado por Giulia para medição de equivalente mecânico do calor neste equipamento nesse durante essas medidas a o trabalho é realizado por um peso em queda e ele movimenta essas paz e converse tem esse essa queda né esse trabalho né de queda no movimento de rotação das pás e agitando a água aquece a água ou seja já aula fez medidas muito precisas com esse equipamento Mostrando que um peso ao cair a realiza trabalho e o trabalho é convertida em calor e vamos falar um pouco sobre termoking e eu comentei anteriormente que os pioneiros
no estudo da termoquímica foi o médico e químico escocês Joseph Black recordando mais uma vez um dos Pioneiros importantes nomes do estudo da química pneumática a black além de introduzir o conceito de calor Latente mostrou que a quantidade de calor pode ser estimada medindo a quantidade de gelo EA fundida esse príncipe foi empregado por Lavoisier e Laplace que utilizaram um calorzinho de Gelo e seus experimentos vocês têm nessa imagem aqui a direita um calorímetro de gelo de Lavoisier e Laplace Lázaro matemático e essa parceria é uma parceria que durou durante muitos anos No estudo da
calorimetria trabalhos de Lavoisier nesse canto foram realizados em colaboração grande básico Laplace Esse é seu imagem retirada de um dos últimos livros do Lavoisier desenho feito por Marie Lavoisier observa os detalhes desse calor a onde colocava aqui dentro tanto de gelo com água e recolher a água que era formada pela fusão do Gelo a daí ele fez as várias medidas ou seja entre 1782 em 1784 Lavoisier e Laplace empregado isso Favorito que eu mostrei pra vocês para medir a quantidade de calor produzida por muitas transformações químicas estabelecendo assim o fundamentos da termoquímica ou seja realizarmos
transformações químicas essas transformações liberavam calor este calor um dia o gelo função da quantidade de água é formada que sabia se relacionar o ex com tanto de calor liberado na reação E o calor latente o calor de transformação uma grandeza física que designa a quantidade de calor recebida ou cedida por um corpo enquanto seu estado físico se modifica é dado por essa equação aqui que que a quantidade de calor em caloria o sol é igual a massa em grama o quilo vezes ele é o calor latente tá tô na fase Laplace realizaram vários experimentos também
sobre a respiração humana a e eles concluíram que Respiração é um tipo de combustão onde o oxigênio é convertido em dióxido de carbono novamente aqui é direita vocês podem apreciar uma desenho também feito por Marie Lavoisier e ela própria se representa na cena dos experimentos conforme já comentamos anteriormente ela teve participação ativa todos os trabalhos de Lavoisier aqui agora um trabalho sobre a respiração um tipo de combustão você observa o assistente aqui De Lavoisier essa imagem é pequena mas ele está com a máscara e todo o ar que ele respirava era recolhido experimento feito de
uma forma muito controlada a E aí o índice de experimentos ele colocou uma cobaia dentro do calorímetro de gelo por 10 horas Coitada da cobaia né mas enfim é eles depois fizeram um experimento controle e realizando a combustão de uma amostra De carvão o e mostrou o resultado mostrou que era necessário realizar a condução de 10 onças e meia uma onça que a unidade usada na época corresponde a 28,35 gramas aproximadamente aí umas 300 gramas de carvão para fundir a mesma massa mesma quantidade de gelo que a que foi fundida pela cobaia durante as 10
horas ou seja a cobaia durante o processo de respiração tá liberando calor e o gelo Está subindo e ao queimar o carvão E também o gelo fugiu medindo a quantidade de dinheiro que foi fundido ou seja de água que ele recolheu ele observa que durante dez horas ela pequena cobaia ela produz lá ela capaz de fugir tanto gelo quanto a queima combustão e aproximadamente 300km de carvão lá roseila plástico então concluíram seguinte " e a respiração é um tipo de combustão reconhecida a net muito lenta mas de Outra forma exatamente igual a combustão do carvão
obter cacheados observe a perspicácia de Lavoisier e Laplace na conclusão da análise dos resultados de seus experimentos experimentos muito bem planejado um experimento muito bem executado em um experimento muito bem interpretado nós estamos falando esse experimento de Lavoisier ocorreram o século 18 no final do século 18 ainda tá tanto a mais de 200 anos em os tonicos 230 240 anos e olha a interpretação precisa que Ltda e é muito importante que nos dias de hoje e onde nós realizamos experimentos tô fazendo aqui um parênteses não só que experimento seja bem feito você já tem planejado
seja bem conduzido mas ele você tem que gastar tempo para interpretar para analisar as consequências dos resultados Que você obteve e Lavoisier nós já havíamos mencionado antes ele era muito preciso Nesse tipo de análise é o Lavoisier com loja descemos teve uma vez extremamente ativa realizando trabalhos dos mais diversos e muitas pesquisas e pouco antes de morrer em 1794 eles retomou seus experimentos e mostrou que a combustão do oxigênio aumentava durante o processo de digestão bem como durante a realização de exercícios observa naquele experimento que nós mostramos a imagem anterior ou o indivíduo que estava
sendo objeto de Estudo por uma máscara ele recolhia todo o CO2 que era liberado no processo de respiração e já vi associado o terror é a combustão né do carvão com a quantidade de CO2 produzidas durante a respiração e ele observou que esse indivíduo estava em jejum os indevido e onde estava no processo de digestão a a combustão do oxigênio era mais intensa bem como durante a realização de exercícios esse trabalho de Lavoisier Eles foram você trabalhos nessa área de termoquímica muita coisa pouca coisa foi feita até o início lá até os anos é 30
década de 1830 quando este físico e médico juízo Germano a festa iniciou uma intensa série de trabalhos nessa área os resultados do trabalho de restos culminaram em 1840 uma lei que recebe seu nome que a lei de resto que é assunto estudado por todo o aluno que faz uma disciplina de físico-química química geral A segunda lei de Regência avaliação do calor de uma reação depende apenas dos Estados inicial e final sendo independente do caminho de reação Ou seja você parte do reagente a b para produzir um produto CD me interessa Quais são os compostos intermediários
interessa apenas é de onde você parte e o produto final e nas teclas de 1850/1860 outras pesquisas nessa nessa área foram Realizadas pelo químico dinamarquês Julius pão e pelo francês marselan detê-lo detê-lo inventou a bomba calorimétrica nós usamos e punham os temos endotérmico e exotérmico são dois termos comuns a qualquer estudante de química seja química geral seja físico-química nós empregamos esses termos endotérmico quando uma transformação resulta na absorção de calor e exotérmico quando a transformação resulta na produção da Eliminação de calor berthillot sugeriu ainda que reações espontâneas ocorrem sempre com liberação de calor essa conclusão
Possivelmente se mostrou errônea hoje nós sabemos disso que a espontaneidade da e ela está associada o outro parâmetro chamado energia livre que está assim relacionada com calor o entalpia da reação a E aí e Vamos falar agora o outro aspecto relacionado aí com o objeto de investigação da área de físico-química que são os gases EA teoria cinética dos gases Esse assunto também o importante e foi estudado extensivamente o século 19 mas nós devemos lembrar que um dos Pioneiros no estudo experimental das propriedades dos gases foi roda esse bolo isso ainda no século 17 ele investigou
a relação entre a pressão e o volume de uma quantidade fixa de ar Esse É o tema do trabalho de Boyle bastante conhecido por estudante de química até mesmo nível médio Ah mas isso foi no século 17 mas até um bando de 1802 pouco trabalho foi feito nessa área até que então O químico francês Gay Lussac investigou a expansão dos gases em função da temperatura trabalho de games aqui envolveu a medida do volume ocupado por uma certa quantidade de gás mantido na temperatura De fusão do Gelo bem como da temperatura de ebulição da água ou
seja pegou um determinado das tudo certo volume de gás colocou no recipiente com água e gelo gelo fundindo-se gás Ocupa um certo volume imagina bem e pega esse recipiente agora coloca em água em ebulição das span span did uma certa porcentagem e o que você é fofo de todos os gases expandiam uma mesma porcentagem do volume que tinham na temperatura de Fusão do gelo ou seja se o gás o volume e temperatura de fusão de gelo tem um volume v0 ao ser colocado a 100 graus a temperatura aqui no motor de 100 graus é da
temperatura de ebulição da água é esse gás em vez de v0 tinha por exemplo 1,50 seja comentou cinquenta por cento volume aumentava de uma certa porcentagem ele observou todos os gases sempre expandir de uma mesma porcentagem do volume que tinha 0° ele fez então extrapolação dos resultados e estimou Que se ele fizesse o contrário se ele resfriar se o gás em vez de elevar sua temperatura Então você de reduzir a temperatura o volume do gás EA de beber e por extrapolação ele concluiu que o gás o compadre um volume 0 a - 273 graus Celsius
em seu artigo e do sax referiu aos resultados obtidos por Jack Alexander César Charles do voltas falamos em vídeo anterior Sales havia mostrado que gases como Oxigênio nitrogênio hidrogênio Panda em uma mesma fração é uma mesma temperatura há muitos anos depois em 1848 William Thomson também conhecido como Lord Kelvin propôs o uso de termômetro a gás no qual a expansão do gás uma medida do aumento da temperatura como uma referência para calibração de outros termômetro essa que a proposta acabou sendo aceita em 1887 e Sonso não físico matemático Engenheiro britânico nascido em Belfast e ele
é muito conhecido por ter desenvolvido essa escala de temperatura absoluta conhecido como escala Kelvin onde o zero absoluto e definido como 0 ou seja que alguém deu a importância o contribuição tão grande para o desenvolvimento da ciência do estudo dos gases que em função desse desse seus trabalhos da importância de seus trabalhos E recebendo o título de nobreza acetona ser conhecido por Lord Kelvin em 1829 uns anos antes aí nesse nesse trabalho de Thomson tenho que vocês Palmas/ e ele iniciou uma série de experimentos também sobre difusão de gases e descobriu uma lei que leva
o seu nome é a lei de carro segunda lei de barra as velocidades relativas de difusão de gases são inversamente proporcionais a Raiz quadrada de suas identidades eu ponho aqui no canto tá bem pequeno mas realmente vocês podem observar que a velocidade R2 né velocidade taxa de difusão do gás um dividido pela taxa de fusão do gás 2 = raiz quadrada da massa molar do gás dois dividido pela massa molar do gás a garra descobriu essa lei recebeu o seu nome e não artículo que Ele publicou em 1833 ele começa aqui "a lei não está
prevista pela teoria Corpuscular de hoje ou seja está muito ciente de que essa descoberta esse comportamento de difusão dos gases é algo extremamente novo o Denilson 848 grava continuo estudando esse tema por muitos anos Ele mostrou que a taxa difusão de gases em dessa dente proporcional a raiz quadrada da massa molar É de fato é a equação que eu mostrei anteriormente aqui eu vou fazer apenas uma parêntese para dizer o seguinte aí é Fusão botei o conceito aqui para vocês e a difusão é a propriedade de dois ou mais gases se misturarem espontaneamente EA efusão
é a passagem de um gás através de pequenos poros aquela equação que eu mostrei no slide anterior tá tratando a taxa de fusão que é inversamente proporcional a raiz quadrada da massa molar dos gases e ele passou a estudar e fusão de substâncias em solução e no processo descobriu algumas soluções aparentes Na Verdade são Suspensões de partículas grandes demais para passar por um filtro de pergaminho os poros esse fio lá ele chamou esses materiais de coloides termo que ele procurou e que passou a denotar uma classe importante de materiais finamente divididos esses colares são estudados
até hoje é uma área de estudo muito importante na época em que gravam fazia o seu trabalho conceito de peso molecular tava sendo amplamente estabelecido por meio de Emissões de gases a Drogaria corpuscular já havia sido aplicada os gases antes e neutro dia mostrado que era possível explicar a pressão de um gás EA lei de Boyle em termos tá e a lei de Boyle isso tudo inteiros da repulsão entre as partículas ou seja no entanto a lei de Boyle quanto à questão da pressão dos gases era possível explicar conforme Nilton pela considerando a redução das
Partículas Davi o modelo de New Era estático e a primeira pessoa que propôs um modelo dinâmico ou cinético foi danial Bernoulli e se tornando aí um pouco antes né 1738 Cruzeiro faz um século Antes vão dar um pulo para trás aí para a gente falar do desenvolvimento dessa teoria cinética dos gases nesse nessa data Daniel Bernoulli assumiu que os gases consistem de um início número de partículas de tamanho negligenciável Essas partículas em movimento rápido não exercem força umas sobre as outras exceto quando elas colidem a pressão é causada pelas partículas bombardeando as paredes do vaso
e as contém ele mostrou que a lei de Boyle podia ser derivada desse modelo o desenvolvimento matemático completo da teoria cinética dos gases foi feito mais de um século depois pelo físico alemão rudolph clausius Rodolfo Julius Emanuel clausius nasceu 1822 e morreu 1888 físico e matemático alemão e um dos fundadores da Ciência da termodinâmica e Essa época em que consegue energia já havia sido desenvolvido e sabia-se que a temperatura de um gás estava relacionada a energia cinética média das moléculas causa então foi capaz de levar as leis do Movimento dos gases O que são familiares
hoje é comumente encontrada nos livros de físico-química o nome de Cláudio sempre aparece nos livros de físico-química modernos ele descreveu o movimento caótico das moléculas introduziu o conceito de caminho médio livre caminho percorrido pela molécula aí é que ela não sofria choque a outra contribuição importante de clausius foi ter mostrado para moléculas monoatômicas a razão dos calores específicos a pressão e volume constantes deve ser 1,67 válvulas 67 o outro lado para moléculas poliatômicas Esse valor é menor isso teve implicação muito importante porque quando determinação experimental dessa razão para gases elementares itens encontrados valores abaixo de
1,67 ele apresentou uma evidência física isso posta a hipótese de avogadro você Jean os gases como nitrogênio oxigênio eram moléculas diatômicas o que passou a ser ou seja sem posso advogados passou despercebido até o congresso de cálculo e é sobre o qual Nós falamos amplamente em vídeo anterior o modelo simplificado de clausius todas as moléculas tinham a mesma velocidade elas eram pequenas que o velocidades se chocavam e desenvolveu esse modelo aí mas modelo matemático Mas Ela assistiu a mesma velocidade esse modelo foi posteriormente desenvolvido pelo físico escocês James clerk Maxwell que considerou que existe uma
distribuição Das velocidades das moléculas m859 Max aplicou técnicas estatísticas para resolver o problema se você tem aqui uma imagem à esquerda do tempo para macho o físico escocês e logo embaixo fique Eduardo woltmann físico austríaco posteriormente 1871 dos anos mais tarde no futebol timão foi capaz de generalizar e as lei distribuição estatísticas de Março para casos Onde existe forças atuando sobre as moléculas e observem as causas começa a desenvolve modelo matemático mas considera que as moléculas têm a mesma velocidade Maxwell n considera agora que as moléculas têm uma distribuição de velocidades Nem todas as moléculas
têm a mesma velocidade algumas são mais velozes outra menos e para cada faixa de velocidade existe uma certa porcentagem de moléculas iludir futebol Sentimental mais tarde faz uma generalização e leva em conta as forças que atuam sobre as moléculas O tempo como é que a ciência avança são são décadas de estudo os primeiros estudos quantitativos sobre gases para investir identificar a relação entre pressão e volume de um gás começa com uma obra deboyu o século 17 e vai avançando o século 18 e quase já no final do século 19 bolo de cima ainda É mais
uma melodia nesses modelos ciência assim determinadas áreas nós temos visto ao longo deste curso vão sendo vão avançando ao longo das décadas e em muitos casos os modelos propostos são totalmente descartados em outros casos o meu caso que nós estamos vendo aqui agora os modelos são aprimorados e vão sendo cada vez mais sofisticados de moda explicar melhor comportamento do sistema sobretudo a que Vocês estão vendo e Diferentemente dos químicos que estavam muito ativos químicos orgânicos estavam muitas vezes preocupados com a estrutura com a propriedade de uma molécula em particular Os físicos o físico-químicos agora estão
preocupados com descrever o comportamento geral de uma classe no caso aqui nós estamos falando de gases o Max continua então os seus estudos a Embora tenha sido aprimorado por última aquelas equações Marcos levou uma equação que associa a viscosidade do gás com sua densidade e o caminho livre médio e a velocidade média das moléculas lembro que nós estamos falando que o modelo de Março agora Leve em conta uma distribuição estatística de velocidade das moléculas com isso realizando medidas experimentais de viscosidade ele conseguiu estimular o caminho médio livre essas moléculas com esse valor foi Possível estimar
o número de moléculas por unidade de volume desde que diante das moléculas fossem conhecidas a outro químico e físico austríaco que deu uma contribuição importante nessa área curiosa José próximo que 1865 sugerir um método para determinar o diâmetro das moléculas em função disso A Malévola por centímetro cúbico sua conhecido como o nome de rosto it em 1869 E aí Victor Renault nós comentamos Brevemente sobre ele quando falamos do congresso e causou e tô vendo ele é via é vou trabalhar um pouco com Renault e nessa época aqui junto Renault juntamente com Emily ler a largar
demonstre que todos os gases em certa extensão tem comportamento que se afasta do ideal o comportamento ideal é dado por essa equação que vocês conhece todos conhecem bem né que pressão vezes volume = nrt ou às vezes essa como relação Moderna e às vezes era dado para o PV = nrt a em 1873 e o Randy de Rick wanderhouse físico Holandês desenvolviam coração para descrever o comportamento dos gases reais a equação agora é bem mais complexa envolve outros parâmetros Ah mas aí você tem uma relação entre pressão e volume algumas constantes e igual à RTP
no trabalho de wanderhouse os esse desvio do comportamento Ideal da assistência sob determinadas condições são devidas as forças de atração entre as moléculas muito dessas forças são conhecidas inclusive como forças Diva Aderbal E aí e aqui aparece um outro personagem pouco conhecido mas eu gostaria de destacar a presença dele aqui nesse nesse nessa apresentação quer Thomas Andrew Thomas Andrews nasceu 1813 Rio 1885 é um químico e físico irlandês Ele Nossa habilitou-se para o trabalho sobre transição de fases há entre gases e líquidos em 1869 Thomas Andrews estudou Poupatempo de gases sob pressão e desenvolveu o
conceito de temperatura crítica como a temperatura acima da qual um gás não se liquefaz então estamos muita atenção nesse aspecto Porque já era possível Bora muito antes disso muitos gases haviam sido De que é feito por Faro por exemplo e outros pesquisadores Só que alguns gases como nitrogênio eram chamados de gases Permanente em função da impossibilidade de ele quer fazer os aquela época um conceito de temperatura crítica desenvolvida por Thomas Andrews e fica claro que e seria possível ele quer fazer cinco outros gases desde que a temperatura fosse é abaixo dessa temperatura crítica no caso
do nitrogénio a temperatura crítica e depois descobriu-se é - 141, um graus Celsius Ou seja você ele quer fazer um gás ele deve ser comprimido alguns casos por exemplo se essa temperatura crítica só cima da temperatura ambiente basta que você cumprir uma num dado momento ele vai se ele quer fazer mas se essa temperatura crítica foi muito baixa quanto a temperatura do sistema não for reduzida abaixo desse ponto crítico o gás não se de que faz esse conceito muito importante foi desenvolvido por esse químico e físico irlandês Os últimos trinta anos do século 19 e
há os últimos últimos trinta anos do século 19 e fato correspondem a um período de muitos debates sobre a existência ou não de átomos simples orgânicos como nós temos estavam envolvidos na síntese de diversos compostos e a maioria tomava por certo na existência dos átomos tava muito preocupado em provar ou não existência aceitava a existência dos átomos para muitos químicos o atomismo era apenas uma hipótese Para a qual não havia qualquer evidência experimental esse tema não quer tornaremos esse tema do atomismo é em dado momento até que vamos mostrar como ele finalmente aceito a fala
de um pouco mais sobre a questão do atomismo as evidências experimentais para a comprovação da existência dos átomos começaram a surgir apenas no início do século 20 Note que John Dalton havia proposto a Sua teoria no início do século 19 e durante todo o século 19 até o seu final multiclix não aceitavam a existência dos átomos achava que era apenas uma hipótese rápidos ensino no existiram temos orgânicos como eu disse aceitava mano estavam muito preocupados com a natureza dos átomos e no início do século 20 JJ Thomson identificou os raios catódicos como sendo o partículas
de eletricidade Joseph mohr só de explicar o fenômeno da radioatividade em Termos atómicos e enquanto esse pintar scoppio decrux permitiu a detecção de desintegrações atômicas individuais esse equipamento inventado por Cruz a muito no início do século ele já não tem a absolutamente mais aplicação alguma também de fora é de uso mas foi o aparelho importante em 1905 Albert Einstein explicou o movimento o efeito browniano em termos moleculares e desenvolveu um tratamento matemático Para o fenômeno alguns anos mais tarde o dono de 1909 1911 ie11 jean-baptiste perrin o físico francês estudou o movimento browniano e foi
capaz inclusive de conheci estudos estimar o valor do número de avogadro serve que a hipótese de advogado foi lançada por advogado em 1811 Um século depois Berlim e é capaz então de determinar o número que ver esse chamado né que é então chamado de advogado o Valor para esse número obtido o peru estava em concordância com o encontrado por Joseph mohr and wood em 1811 1911 existe uma imagem Ferri sua meia-idade aí Tá ele foi laureado com o prêmio Nobel de Física em 1926 é um professor muito importante na sua área é e nessa nesse
slide nós temos aqui duas imagens retiradas da Wikipédia desse spinthariscope you que como eu disse é um dispositivo que praticamente não tem uso nos dias atuais ele era destinado a Observar integrações desintegrações do cread causadas pela interação de radiação ionizante com sentido como se cintilador ele foi inventado em 1903 por William krooks a continuar então em seus experimentos brother volte mudo a contar um número de partículas alfas emitidas por uma mostra de rádio e também medir o volume de Hélio que era produzido no intervalo de tempo partir para salta só mentiras e produzir Hélio É
com estas informações considerando que todos os átomos de Hélio sobre um das partículas Alfa for possível calcular o número de átomos de Hélio de um determinado volume Com todas essas evidências a oposição a teoria atômica finalmente convencida e até mesmo Osvaldo que eram muitos físico aqui um dos fundadores da físico-química e era cético em relação à existência de átomos acabou se convertendo ao atomismo Ah é então estamos previamente alguns Desses fatos porque a físico-química umas outras áreas da ciência começaram a se desenvolver de uma forma muito complexas nos complexa com muitos experimentos sofisticados e aqui
rapidamente demos um salto no início Zinho do século 20 estamos falando do século 19 principalmente mas no início do século 20 não mostrar aqui toda essa evolução da teoria cinética dos gases acaba que combina com esses últimos experimentos que eu mostrei para Vocês a a teoria do movimento browniano com as medidas experimentais de movimento avaliando os trabalhos de Rutherford volte sobre desintegração de partículas radioativas terminando então com vários tipos de medida é do número de átomos é tudo aquilo lado volume e essa ele dessas todas estavam dando suporte a existência de átomos basicamente início do
século 20 o atomismo ele deixa de ser uma hipótese para muitos e mesmo os mais Cépticos como eu disse Osvaldo acaba se convertendo e vamos tratar agora do outro tema é assunto da área de físico-química que é cinética de reação e equilíbrio químico quando nós tratamos de cinética Estamos tratando na velocidade do tempo necessário para uma reação a correr é um assunto que sempre preocupou muitos químicos foi a natureza da afinidade química sobre isso nós tratamos em vários momentos e em um vídeo em Particular tratamos sobre o início dos estudos sobre afinidade química embora nos
Tenhamos nos últimas aulas tratados de outros temas quando química orgânica e inorgânica afinidade química ela continuou sempre preocupando vários químicos dessa forma os primeiros estudos sobre a cinética tiveram como motivação o entendimento EA quantificação das forças de afinidade os primeiros estudos nesse sentido deve ser alquímico frederich wiesel que Realizava estúdios do sentido de medir a afinidade por meio da observação da os detalhes ouviu em ácidos Frederico nasceu 1740 morreu em 1793 todo time e metalurgia esse animal ele foi o primeiro anunciar a noção de equivalente grama EA publicar uma tabela de pesos equivalentes de ácidos
e bases posteriormente de ideias venham existe ter Composto uma tabela mais extensa de pesos equivalente a tabela delícia ficou bastante mais conhecida né porque aí os próprios trabalhos de UEL e agora o resultado esperado por vezes eu não tenha sido alcançado Esse estudo corresponde talvez a primeira investigação relativa a velocidade de reações de seus dados experimentais o exopodito time os metais podiam ser arranjadas em ordem de afinidade por um determinado Ácido e ele ainda observou que ao variar a quantidade do ácido e reduzindo a concentração pela metade o tempo de dissolução do Metal Ficou duas
vezes maior observa que aqui nós temos os primeiros estudos sobre cinética Ou seja a velocidade com que a reação acontece que faz um experimento coloco metal e ver na presença de uma certa quantidade de ácido e Verifica quanto tempo que aquele mental gasto para ser dissolvido e faz medidas para Vários metais para vários ácidos e verifica que alguns metais reagem mais rapidamente que outros sejam metal de acordo com o réu teria mais afinidade pelo ácido outro experimento importantes foi esse que eu acabo de mencionar ele põe uma determinada quantidade de metal uma quantidade de ácido
gasta um tempo para que ele seja dissolvido quando ele reduz a concentração pela e a dissolução fica mais lenta tempo é duas vezes maior Agora seja esses são os primórdios dos Estudos sobre cinética química e há tempos era sabido dos químicos que muitas reações não se completavam já era de conhecimento misturava-se dois reagentes a mais pipa produziu e a gente ser feliz tem que saber o que aconteçam nem sempre Ela completa foi isso pensava-se que seria possível medir a afinidade por meio da medida da extensão da reação em outras palavras se o Regente a Kombi
Completamente convertido em ser é porque Eles teriam a maior afinidade um pelo outro e a quantidade de ser produzida fosse uma pequena é porque afinidade de a com B seria menor Essa é a ideia e lembremos aqui dos trabalhos de texto lê que nós já mencionamos anteriormente e ele também endividou muitos esforços do sentido de sem sucesso medir as afinidades seus estudos envolveram essencialmente investigação das condições de Equilíbrio sobre Substâncias reagentes nós mencionamos muito sobre o trabalho de Victor e dá algum tempo atrás os seus trabalhos ficaram esquecidos por conta de uma série de controvérsias
de uma série de outros dados que não foram aceitos trabalhos de ver Toledo sentido é nas investigações sobre equilíbrio químico eram de fato na época trabalhos inovadores mas ficaram esquecidos por 60 anos um químico e Imaginologia isso alemão Henry Rose que vocês podem apreciar a imagem dele sua meia-idade em mei dormi ou gente descobriu e nome o nome Óbvio químico e ele realizou o doutorado sobre do exército muito influência de BFF e Rose é é um dos personagens e realizou estudos nessa área da década de 1840 e também na década de 1850 e seus estudos
Rose reagir um sal insolúvel sulfato de bário uma solução em ebulição de carbonato de sódio ele observou que o Uso de quantidades equivalentes dos sais resultado em apenas 10 por cento de obtenção dos produtos e o pegar um excesso 15 vezes carbonato de sódio ele obteve sem por cento de conversão do sulfato de bário em carbonato de bário Serra nós estamos falando de 1840 1.850 e agora já começa o estudos mais quantitativos Rose pega uma solução sofá pega uma amostra de sulfato de bário e insolúvel em água e põe em uma solução de carbonato de
Sódio carbonato de sódio totalmente surgiu e em ebulição parte do sulfato de bário é convertido no também insolúvel desculpe parte de sulfato de bário é convertido no também insolúvel carbonato de bário pessoal dez porcento o dele usa excesso de carbonato a 15 vezes mais carboidratos de Deus o fato agora todos sulfato embora seja Insolúvel acaba que é convertido em carbonato de bário isso porque do conhecimento que nós temos hoje essas reações e sais insolúveis o nós dizemos que um sal insolúvel na realidade existem equilíbrio pequena quantidade solúvel a Essa época não se sabia disso Este
é um dos primeiros estudos quantitativos quando você se lembrar isso se Recordar dos estudos Que você fez sobre solubilidade constante de solubilidade de um determinado composto saiba que estes trabalhos Pioneiros de Rose são os primeiros na verdade de Toledo e Estudos nesse sentido mas as quantificações mais detalhadas vieram correr agora muitos anos depois com o o divórcio e do ponto de vista da cinética na aí você tava cheiroso e estava relacionado com equilíbrio químico não com cinética o primeiro trabalho de Cinética de uma reação é considera-se que foi realizado pelo pouco conhecido ainda né químico
alemão viu Realm notifix ser ginásio Realm no seu 1812 e morreu relativamente jovem é em 1864 Agora se a imagem parece aqui ele tem até um pouco mais de idade e em 1850 eles dou a Hidrólise da sacarose na presença de ácido para quantificar o processo Progresso da reação que produzir glicose + frutose ou seja sacarose na presença de ácido ela Hidrolisada existe uma quebra da ligação e resulta na formação de glicose e frutose acompanhar este processo de Hidrólise e lhe Entregou um polarímetro como sinal de rotação ótica da sacarose positivo enquanto da mistura da
relação ao negativo o progresso da reação pode facilmente ser seguido pela variação deste parâmetro é o colar indo já era conhecido você mede nós chamamos de rotação específica a rotação específica Da sacarose ela um valor positivo e da mistura de glicose frutose e tem um valor negativo na medida em que a Hidrólise vai ocorrendo o ângulo de desvio dessa o e na luz polarizada ela Ele vai reduzindo tô pela redução deste parâmetro Que nós conhecemos como rotação Ótica ele acompanhou o progresso da reação de deslocamento mostrou que para cada concentração para uma dada concentração se
de sacarose seja você Começa com a concentração z existe um certo valor de concentração de rotação específica tá na medida que a reação vai teorizando a concentração de sacarose e vai reduzindo por uma taxa que nós chamamos aqui de dese no intervalo de tempo DT e que essa redução podia ser expresso por essa equação menos de Z dividido por d t = k é uma constante vezes a concentração Inicial Este É de fato um dos primeiros trabalhos de cinética realizados de forma Quantitativa com isso eu vi helmer pouco como viveu era pouco conhecido que eu
acabei de dizer o seu trabalho não chamou muita atenção da comunidade química apenas 30 anos após a publicar chuva obrigação é que o outro físico-químico Osvaldo teve sua atenção voltada para os trabalhos de vida real Mas eles se interessa o crédito por esse estudo pioneiro da velocidade de Hidrólise da sacarose em Meio ácido o trabalho de vir Realm permanece esquecido como eu acabei de dizer o 30 anos trabalho não chamou muita atenção outros químicos começaram a realizar estudos nessa área também de cinética nesse Campo destacam-se os trabalhos de Taylor e Leo Peão de santilli não
confundi aqui perder low um bertholet que como eu disse também realizou estudos sobre equilíbrio químico cujos resultados não foram aceitos Percebidos da época e o décadas ele não teve o crédito por esse tipo de trabalho Léo Leon obtê-lo é um dos times franceses mais importantes de sua época e Leo a pena sanjay's químico francês morreu de tuberculose estreou três importantes memórias em colaboração com besteira ou em 1862 1863 observa um período que nós estamos Nós estamos aqui já na segunda metade do século 19 o que eles fizeram foi investigar a velocidade da reação entre ácido
acético e etanol para produzir acetato de etila essa reação de hoje em dia nós conhecemos muito bem né também assunto estudado é o estudante de química em nível médio e curso de química em nível superior você pega o ácido e pega um alto na presença de uma certa quantidade de ácido é ocorre uma reação e produz um Éster nesse caso específico USA o processo e etanol Western é o acetato de etila eles mostraram que a velocidade da reação é proporcional à quantidade dos reagentes e inversamente proporcional ao volume do sistema em outras palavras se o
volume diminui para uma mesma quantidade de reagente nós estamos falando que a concentração aumenta tão rephrase Anísio basicamente o que eles mostraram é que a velocidade é Proporcional à concentração seja se você tá trabalhando com a solução mais concentrada de ácido a reação ocorre mais rapidamente ou se você aumenta a concentração do álcool a velocidade também aumenta a reação é mais rápida eu espero ter ficado Claro esse ponto Porque é importante que aqui tô falando que a velocidade é proporcional à quantidade e inversamente proporcional ao volume ou seja para o mesmo volume é De sistema
se você põe mais quantidade se aumenta a concentração ou se você tem uma mesma quantidade de a gente vê dois o volume dos sistema reacional você aumenta a concentração também e eles realizaram estudos e voltar a quantidade de Éster formada É depende da proporção dos reagentes por exemplo ao empregado um equivalente de ácido Ed álcool ou seja quantidade Equivalente de Aço de alto o equilíbrio da reação é alcançado com a formação de 66,5 por cento do Oeste da reação avançava tem um ponto atingir-se o equilíbrio e o máximo de essa cirurgia era 66,5 por cento
de coleção aí ao empregar um excesso de 12 vezes de álcool em relação ao ácido a conversão deste esta alcançava 93,2 por cento observa agora nós dois estamos tratando aqui de velocidade Estamos tratando de Equilíbrio você põe usando o palavreado moderno 1 mol de ácido e um molde alto você obtém quando sistema atingiu aquele há 66 0,66 5 mol do Oeste mas se você emprega um molde o ácido 12vol do álcool você obtém Gero 93,10 932 Ball do Oeste RO seja 93,2 por cento do Astro é convertido não é ser obviamente aí com esse excesso
de álcool Infelizmente esses trabalhos também eram pioneiros da rua e já no sentido de resultar em descobertas fantásticas Eles foram interrompidos com a morte prematura de Santiago como eu acabei de mencionar ou tuberculose aos 31 anos ele veio a falecer e não se tem notícia que besteira ou tenha continuado trabalhos nessa linha é preciso observam que os estudos sobre equilíbrio estava avançando é O meio dos trabalhos de vaso cientistas mais dois desses se destacam estão mais conhecidos nos dias de hoje são comuns de encontrar estes nomes dos livros de química geral físico-química e ele se
devem a Catho maximillian good time e matemático norueguês e o Peter Berger um time norueguês e vocês podem observar nessa figura os dois juntos a esquerda tudo bem E a direita o vag e eles eram cuidado e do Outro e esses quilos também estavam interessados em quantificar as afinidades terra que nós começamos falando que um dos motivos que inspiraram que motivaram a investigação de como que essas reações se davam era essa procura já tentativa de quantificar essas forças que agiam entre as substâncias chamadas de afinidade os é gudiberg Wagner publicado em 1864 vocês Têm aqui
uma referência e esses estudos relativos afinidade olho título do trabalho deles Este trabalho foi publicado na academia no mercado de Ciências e Letras tá bom eles iniciaram seus estudos em 1861 publicaram parte desses estudos 1864 mais em 1867 veio uma publicação muito importante e nesta publicação de disseram " e Nós pensamos que deve ser possível Encontrar valores numéricos para as magnitudes das forças químicas Nós também pensamos que seremos capazes de encontrar para cada elemento e para cada composto químico certos números que devem expressar suas afinidades relativas da mesma forma que os pesos atômicos expressam seus
pesos relativos observa aqui a descrição as conclusões a que chegaram good good bug mais Chamando essas interações de afinidades O Berg Wagner realizado então estudos com sistemas que podiam atingir um estado de equilíbrio dinâmico como os resultados como os estudados por tê-lo betoneira 600 ácido acético etanol Rose sulfatos e carbonatos de baile potássio quando eu quero quando eu digo aqui equilíbrio dinâmico significa o seguinte escolheram sistemas em que por exemplo o ácido mais o álcool produz o Éster mas o Extra vai ser hidrolisado Produzido Astro e Álcool essa relação acontece numa direção ou da direção
reversa até que o equilíbrio seja atingido você já não progride em uma outra direção a reação não deixa de ocorrer continua ocorrendo mais existe esse estado é chamado de equilíbrio dinâmico o mesmo ocorre com Sulfato seca Nós já mostramos é e estão codec vaga com sistemas de si mesmo tipo de comportamento um Pouquinho mais sobre de trabalhos de Goldberg que e acaba que foram os trabalhos que são se tornaram mais conhecidos e eles são mais reconhecidos é de um modo geral pelo estabelecimento desses estudos dessa lei de Equilíbrio eles estabeleceram esse duas substâncias A e
B reage uma com a outra para formar duas novas substâncias a linha e de linha a força que age sobre a e b é dada por essa expressão k p e que onde cai uma Constante chamada de constante de afinidade coeficiente de afinidade eu podia ser outra coisa estão procurando essa afinidade a reagir com de Ah tem uma certa afinidade Konder e nesse caso pq são os q eles a massa chamaram de massas ativas ou seja estamos falando aqui das concentrações dos reagentes a expressão Cap que corresponde a massa de aipim e são transformadas em
galinha e bellinha por Unidade de tempo o segundo esses resultados quando o sistema atingir o equilíbrio Ou seja a mais ver forma a linha mais velhinha mas a linha e ver linha a linha reage com de linha formando AB é um sistema atingir o equilíbrio a reação tem uma velocidade numa direção igual a velocidade na outra ou seja no pó de Equilíbrio as concentrações dessas espécies do mundo segundo esses resultados quando o sistema atingir o equilíbrio as forças Que agem na direção de informação de a linha e bellinha são iguais às Forças que agem na
direção oposta ou seja na formação de ATP e outras palavras E essas forças que estão expressas aí por cá de que seria igual a força que age no sentido oposto da linha Kelinha Kelinha essas conclusões ficaram conhecida como lei da ação das massas todos que já estudaram um pouco de química deve se lembrar de ter estudado Essa lei da ação das massas esses dois químicos são os pioneiros que chegaram nessas expressões as conclusões goodback vague correspondem e ao que é chamado hoje lei do equilíbrio é E aí que eu te ligo time Claro e como
é comum no desenvolvimento da ciência conforme caso que nós já discutimos anteriormente Comunidade que me da época e não deu muita atenção a publicação de Goldberg Wagner nós temos vários exemplos ao longo desse custo de ideias inovadoras resultados importantes que passaram despercebidas pela comunidade química e foram redescobertos décadas depois também aconteceu com o goodback Wagner que 1864 tinha mostrado anteriormente divulgar os seus resultados de uma revista norueguesa esse trabalhos passaram percebidos o que não é de Estranhar Pois é uma língua e poucos pouco conhecida não é uma língua que tem importância científica Então esse trabalho
ficou restrito à comunidade química do mesa Ah e não foi divulgado não teve nenhum impacto da Comunidade Internacional m877 eles publicaram novo artigo que Eu mencionei parte das conclusões deles anteriormente só que dessa vez eles publicaram em francês porque a época já não era tão dominante no campo Científico Como foram algumas regras nós estamos lá na segunda metade do século 19 e quando nós estudamos sobre o congresso de cálculo i e ocorreu em setembro de 1860 nós comentamos aquela época que grande parte dos times participantes eram alemães já estava Evidente A Supremacia da química alemã
ciência alemã estava ficando já dominante daquele período a França era importante e ele tá realmente assim como ainda é importante hoje mais aquela Época a o alemão já estava e se tornando uma língua muito mais o dominante no campo científico especialmente no campo da química em função da pujança do desenvolvimento da química nesse nesse país segue que ainda não era o país né ela Alemanha só foi Estado alemão só foi criado em 1870 novamente com a publicação em francês não houve grande impacto o fornecimento tempo pode goodback Wagner continuava as suas pesquisas Outros químicos como
o sol enquanto Hoff trabalhavam na mesma área identificando casos específicos de equilíbrio químico essas palavras um tema um determinado tema de investigação científica é vai ocorre que as pessoas se comunicam de uma forma ou de outra esses resultados de uma forma de outra é chegam a pesquisadores de diversos países e ele vários pesquisadores começam a investigar o mesmo tema mas Segundo Robson o nosso autor que nós tamos Seguindo para essa apresentação Osvaldo e vant Hoff não tinham conhecimento dos trabalhos dos noruegueses esse ciclo do Radisson não não consegui outras fontes não sei até que ponta
e são estes trabalhos eram absolutamente desconhecidos até porque eles publicado em francês em francês embora não fosse a língua dominante uma língua era uma língua importante muitos químicos importantes Lyon francês Bom mas essa informação nos dada o Robson há alguns anos mais tarde em [Música] 1879 bug bug publicaram agora um artigo em alemão passaram-se aí uns anos é mais de uma década onde eles então resolveram publicar um trabalho e Alemão neste meio tempo vários trabalhos já haviam sido publicado por outros o que eles fizeram então nesse trabalho alemão foi Reafirmar suas conclusões iniciais inclusive indicando
que elas haviam sido confirmadas por trabalhos mais recentes de outros químicos a partir desse momento eles receberão crédito por suas descobertas e seus trabalhos passaram ser reconhecidos por todos o barco de Berg Wagner considerado as forças de afinidade como sendo responsáveis pela combinação química essas forças foram introduzidas na formulação da lei da ação das massas Apenas com constantes tiveram pouca relação com o trabalho deles a importância da teoria desenvolvida está no reconhecimento de que as concentrações das espécies reagentes constituem as massas ativas e determina o equilíbrio resultante da reação em uma direção ou na direção
reversa outras palavras eles o consideraram que essa força de afinidade existia o posto lá tem uma facilidade por um composto dele e essa Afinidade ela era de alguma forma é expresso naquela constante mas mil houve nenhuma Avanço No entendimento dessa questão de afinidade importante o grande reconhecimento é que o que ele chamava de massa ativa ou concentração é que determinava a direção da reação e no sentido ou no numa direção anotei a mais ver forma Aline de linha ou a linha e de linha forma Abrir sentido reverso quem importante destacar o Reconhecimento da importância da
concentração e o conceito de equilíbrio dinâmico proposto completa o trabalho de bertholet de seis décadas antes que havia sido que não havia sido reconhecido de tô lê-se já tinha realizado trabalhos nesse sentido a usando o sistema de Equilíbrio mais é a época de seus trabalhos foram descartados quem é e não foram reconhecidos agora 60 Anos depois reconhece-se a importância dos trabalhos de bertholet mas goodbag Wagner foram os que deram maior contribuição neste sentido e os nomes deles sempre aparecem nos textos atuais e além dos trabalhos de Gude lague Claro estes investigações ocorria em outras partes
e na Inglaterra trabalhos no sentido de realizar a estudante ativos do campo da cinética vinham sendo realizados por Auguste George inverno acode acode nasceu em 1834 morreu 1919 físico-químico inglês professor da universidade de Oxford eu chamo atenção aqui que ele era amigo do matemático também noxo Charles dodgson que era conhecido mais conhecido como New Style II o famoso poder escrito quanto Alice no País das Maravilhas Eles eram muito amigos nos diários de Charles John Dodson existem vários registros dos encontros dos dois Isso é uma informação paralela é a chamar atenção de que esse físico aqui
em inglês juntamente com outros matemáticos também leis William Edson E ele disse o trabalho sobre cinética química ou seja tudo sobre velocidade das reações também fomos Pioneiros nessa área nome dele é pouco conhecido goodback vale é o nome Talvez isso aí conhecido Da maioria de vocês mas aqui o outro não enquanto os pesquisadores estavam investigando reações reversíveis raspou de Edson escolher investigar uma reação Irreversível conhecê-los concentrado seus esforços no estudo das velocidades das reações nos palavras concentraram no estudo da cinética química é destaca que o trabalho de vácuo em função da diferença com relação aos
trabalhos de Gutenberg Wagner Roberto Wagner outros como nós Mencionamos escolheram os sistemas em que as reações estavam equilíbrio em cima de sua Carlos equilíbrio na direção direta ou reversa em função das concentrações dos reagentes das espécies envolvidas are Cold fez diferente estratégia dele por escolher uma reação absoluta é Irreversível a reação produzia formavam um produto mais o reverso não ocorria com isso ele podia focar sua atenção Todo seu tratamento matemático e análise dos seus resultados não da questão da influência das da concentração dos reagentes no equilíbrio a quantidade de produtos formato mas na velocidade no
tempo necessário para a reação ocorrer eles exploraram vários sistemas e por final é encontraram esse sistema que agora eu coloquei numa representação moderna para vocês tá H 2 o 2 mais 2 h i i 12 H 2 o mais de dois agora representa Para ficar até mais fácil quando você enxerga uma representação moderna né teve estado fazer isto ao longo da Apresentação mas é a sua reação né são plástica em que o iodeto com água oxigenada todos aí dois e pela coloração da solução é possível você avaliar Inclusive a extensão e medir o tempo gasto
aí quando esse li essa cor aparece e vocês terem uma ideia da persistência desses dois desse químicos matemático Durante mais ou menos 30 anos eles realizaram mais de 30 mil experimentos e de forma muito rigorosa e estabelecer a dependência da velocidade com as concentrações dos reagentes observa é muita persistência você pega um projeto desse uma reação relativamente Simples boa noite estamos falando de uma época que não se conhece não se sabe como é que as transformações ocorre eles estavam interessados em descobrir a a essência do que ocorre durante uma Transformação Quais são os fatores que
afetam a velocidade do processo Quais são as leis que guiam a que regem aquele processo passaram durante 30 anos mais ou menos 30 mil experimentos é muita persistência eu é isso porque tem realiza pesquisa Hoje existe muito imediatismo a sempre a busque de querendo resultados e mesmo resultados em completo são publicados observa que resultados importantes Surgem de um trabalho persistente como esse e eles estabelecendo então essa dependência entre a velocidade da reação EA concentração dos reagentes para que isso possa de fato ser feito é importante você tenha dados confiáveis no ano de 1895 e aqui
o recorde que o trabalho de Goldberg Vargas foi publicado o livro da primeira versão lá em francês navio norueguês M864 ou seja 30 anos depois aí 31 anos depois eles descreveram como a velocidade da reação também depende da temperatura Esse é um outro aspecto muito importante claro com 30 Minha experiência vocês podem imaginar que eles investigaram muitos parâmetros fizeram muitas reações de várias condições e eles descobriram que a velocidade da reação Dobra a cada aumento de 10 graus claro isso tudo por meio de Experimentação como é que chegaram ao 10° e os dados se aumenta
a temperatura Verifica que o tempo de reação EA reação ocorre mais rapidamente uma vez e identifique aqui existe o efeito da temperatura você passa agora então fazer experimentos mais bem planejados fazendo variações sistemáticas de temperatura e com isso descobrir o que a cada dez graus a velocidade de dobra ou seja o tempo para Reação ocorrer aí dou a metade fazer uma extrapolação desses dados eles concluíram que a menos 270 e 2,6 graus não correria copiar transformação e a nós falamos do zero absoluto na escala Kelvin Em outro momento o o bom e isso daí Olha
é basicamente próximo lá do zero absoluto o resultado de impressionante que eles obtiveram atingindo o zero absoluto não existe transformação que a sua conclusão deles não chamou de zero Absoluto lá muitas das ideias fundamentais sobre cinética foram também desenvolvidos por outros químicos destacamos sair o trabalho enquanto Roche em Amsterdã que na imagem off químico Holandês bastante conhecido já tratamos dos trabalhos dele quando ele fala o pai da sua publicação de importante sobre a natureza do carbono de gente que o cartão dela Tetraédrico quanto rock começou trabalhando com química orgânica e depois passou a ser mais
conhecido por seus estudos de físico-química e dentro desses estudos enquanto os estudos sobre cinética em uma é de 84 com apenas 32 anos fantoche fez uma revisão dos trabalhos inéditos realizados por ele já era o bastante e produtos químicos e publicou o livro estudo da dinâmica química desse livro discute a relação entre Cinética e mecanismo de reação bem como a dependência da velocidade com a temperatura ou seja vant Hoff faz aqui nesse nesse vídeo a revisão do que se sabe a época e já destaque aqui um outro conceito que eu chego da atenção aqui agora
que a questão do mecanismo da reação tá a continuar os seus estudos é 1887 pontos altos definiu várias ordens direção e contribuiu para o entendimento do mecanismo de reações é claro que pode Surgir contribuiu foram os primeiros estudos de mecanismos de reação E especialmente as reações orgânicas ele se desenvolve largamente já começa a se desenvolver na primeira metade do século 20 o outro químico Sueco muito importante ganhador do prêmio Nobel de química em 1903 E aí bate August arrhenius na 6.859 e faleceu 1927 A tese de doutorado de Janeiro quase reprovada tá tanto a parte
escrita Ou seja a teoria quando a própria defesa ele teve notas no limite da aprovação quase reprovado era uma teses pela tese inovadora e não teve muita aceitação pela banca mais arrhenius fez um trabalho intenso para divulgar o seu trabalho e acabou recebendo depois do apoio de Que importante e seu trabalho foi reconhecido e em 1889 Rendas começou a discutir o motivo pelo qual um pequeno aumento da temperatura resultava em um grande aumento da velocidade da reação wunderland rossi.rar Cold havia mostrado é que a temperatura influenciava mais foi a reino que começa a observar esse
assunto com começa a investigar isso de uma forma mais detalhada ele destacou que a teoria cinética caso teoria cinética dos gases ela não era capaz de dar uma explicação satisfatória para os Resultados observados ser a teoria então disponível você ficava que aumentando a temperatura aumentava a velocidade e com isso se deveria aumentar a velocidade da reação mais para reinos a explicação não era satisfatória no caso dos gases o aumento previsto da frequência de colisões da e com o aumento da temperatura era muito pequeno para explicar o aumento observado nas velocidades e o que levou a
reinos a considerar que O mesmo deveria estar ocorrendo em solução eu estava aqui que a renda que começa agora é analisar os resultados da teoria dos gases começa a fazer uma inferência a respeito de soluções trabalho de arrhenius é muito importante da área de soluções e a gente então considerou que nem todas as colisões moleculares mesmo envolvendo reações biomoleculares resultava em reação com base nessa ideia Ele propôs o conceito de moléculas ativas e energia de ativação aqui aparece um conselho e é do Conhecimento hoje né de muitos estudantes de química é que eu sei de
energia de ativação da revista de gelo é o seguinte numa reação bimolecular duas moléculas as moléculas colidissem e xó tão tá dizendo que nem todos os choques vão resultar em reação é apenas alguns desses choques ou resultar na transformação do produto Essa fração de moléculas tá e ao se chocarem se transforma no produto ele chama de moléculas ativas EA energia para esse processo ocorrer ele chama de energia de ativação começa a surgir agora e x se conceito novo e apenas vai desenvolver oi povo lindo qualquer área de conhecimento os avanços E as novas descobertas de
modo geral lá sempre ocorre o base em trabalhos anteriores A a rede estava ciente Claro dos trabalhos De seus antecessores e ainda em 1867 O químico e físico austríaco Leopoldo San Andreas Zombie Rider on e propôs que apenas moléculas possuíam as moléculas que possuíam energia cima de um certo valor que ele chamou de valor crítico podiam sofrer transformação química ou seja esse conceito de que nem todas as moléculas ao e se encontrarem vão sofrer ou transformação já eram com efeito município já havia sido proposto por vão A demo sabermos a ou seja e ele define
Inclusive essa energia quando você não valor crítico se a energia das moléculas tiver a parte desse valor crítico não tem transformação química por outro lado Maxwell James clerk Maxwell em seu trabalho sobre a distribuição de velocidades moleculares ele havia sugerido que a fração de moléculas que possuem energia consideravelmente Acima da Média a temperatura normal E aumenta significativamente com o aumento da temperatura seja nós vimos que Maxwell começa a fazer um tratamento estatístico para esses temas desde que existe a temperatura ambiente uma fração de uma existe uma distribuição de energia dessas moléculas e sua curva de
distribuição a existe uma fração de moléculas que tem energia acima do valor médio mas à medida que se aumenta a temperatura essa fração aumenta esse é um outro Conceito e trata aqui agora dessa distribuição de energia das moléculas as redes por sua vez Ele propôs que apenas as moléculas altamente energéticas eram ativas está com esse ativos e nem todas as moléculas serão ativas em todas as moléculas vão reagir as moléculas ativas são tão capazes de participar e efetivamente de transformações químicas e série de diarreia mas essa ideia vocês observam já estava no ar por meio
de trabalhos de outros pesquisadores como a Dermor Maxwell e a rede então encontra uma relação entre duas constantes de velocidade que é caseiro e k1 e são constante de velocidade medida nas temperaturas t0 e T1 ou seja em cada temperatura Você tem uma constante de velocidade e aqui você tem uma expressão que eu incluo para vocês expressão desenvolvida pela renews onde a constante de velocidade da temperatura T1 = constante de velocidade na temperatura t0 aqui exponencial elevado Né a que T1 - t0 / 2 [Música] xt1630 a gente oração que arranjos deduziu é de onde
você se encontra essa mesma expressão dado por essa equação que é conhecida como equação de arrhenius onde a constante de velocidade é igual uma constante exponencial elevado né a menos é que energia façam R constante que a temperatura seja essa equação a condição conhecida e permite por meio de estudos experimentais Determinado Inclusive a energia de ativação de um determinado é transformação anti conceito de energia de moléculas ativas espécies nativas energia de ativação Eles são amplamente de o desertos que combina com essa equação que é uma equação comumente encontrado em livros texto de hoje E como
eu havia mencionado antes Microsoft havia escrito esse livro estudo de dinâmica química né E nesse Livro ele faz um resumo do que se sabia é a época sobre equilíbrio e cinética e discutir essa questão da cinética Mas além disso ele indica as condições para o estabelecimento porque ele dinâmico ele dele vou expressões para constante de equilíbrio empregando os dados de bertholet e berthillot e Sandy Johns para esterificação do ácido acético ele mostrou que os seus resultados eram consistentes com a fórmula concentração Do ácido acético vezes concentração de etanol é igual a um quarto da concentração
de é certeza concentração de água nas rochas reconheceu que uma mudança na temperatura sempre afeta o equilíbrio ele anunciou o princípio do telemóvel dizendo Hoje sabemos bom né que o aumento da temperatura favorece uma reação endotérmica e nesse tempo o tempo O químico Metalúrgica francês ouvir o hino Chantilly e estava também investigando equilíbrio químico a enquanto o fantoche tinha e publicado o seu livro seja e o mais um personagem entre aqui em cena e a Rio e Russel terrier King Metalúrgica francês tava que junto dos seus trabalhos uma lei do equilíbrio químico a que fica
conhecido como princípio de le chatelier e ele contribui muito para o desenvolvimento da termodinâmica É como eu disse lixa ele enunciou enunciou o princípio que leva o seu nome e é conhecido de todo estudante de química nos dias de hoje segundo Esse princípio quando uma mudança imposta um sistema em equilíbrio dinâmico o sistema responderá de tal maneira a minimizar a mudança imposta ou seja só recordando você tem composto a mais um composto B é em equilíbrio tomando o composto cê no sistema está em equilíbrio se você aumenta a Concentração de bebê por exemplo sistema o
equilíbrio se desloca no sentido de formar mais ser Ou seja você entende minisal o aumento imposto na concentração de B se você aumenta a concentração de ar o sistema também ele se desloca no sentido de formar mais ser por quê E aí se a concentração de aqui você aumentou na reduzir a e dessa forma foi mostrado que o princípio dinâmico de vant Hoff trata-se de um caso especial do princípio de le Chatelier seja quando nós tratamos de equilíbrio químico na sempre é mencionamos o princípio de bruxa ele em função do fato de que ele é
um princípio Mais amplo ou seja Qualquer mudança imposta no sistema o equilíbrio seja estabelece de modo a minimizar essa essa essa essa alteração imposta ao sistema isso então o princípio dinâmico de voto Rafa era apenas um caso especial do princípio de le chatelier os estudos Sobre cinética e termodinâmica envolveram muitos outros cientistas celestes uma longa história quantas vezes tudo estavam sendo realizados muitos químicos sabia que algumas reações ocorrida em forma mais rápida na presença de pequenas Em certas substâncias essas investigações resultaram na área da química que nós chamamos de catálise foi descoberto todo um uma
série de Substâncias que na presença das quais mesmo em quantidades Muito pequenas a transformação era acelerada nome para essa aceleração tá é cartazes e o nome dado a essas substâncias que aceleram a reação são catalisadores Mas essa é uma outra história que nós contaremos no os momentos em nós estamos chegando ao final farei algumas considerações e além dos temas aqui discutidos a físico-química se desenvolveu e muitas Outras subáreas e como exemplo podemos citar os estudos sobre mecanismos de reações que tiveram a contribuição Pioneiro de arte lápis Wars que 1903 estudou adição de hcn a compostos
carbonílicos estudo sobre o terror dinâmica química química de soluções contribuições importantes de arrhenius e Osvaldo de outros estudos o propriedades físicas estrutura molecular muitos desses avanços continuaram no Início do século 20 e no final do século 19 os jogos clássicos da química que conhecemos hoje como química orgânica química inorgânica e físico-química já estavam bem estabelecidos certa forma eram áreas quase que Independentes umas das outras E conforme Veremos em outros momentos nos séculos 20 com os grandes avanços ocorridos nas várias áreas da química e de outras ciências como física e Biologia existe passou a existir uma
tendência ao estabelecimento de uma maior interação entre os diversos Ramos da química de modo que hoje em pleno século 21 química orgânica por exemplo se beneficia muito da físico-química nativo da computacional e da física nos dias de hoje ter uma visão compartimentalizada química colups estabeleceu ao final do século 19 constitui a meu ver uma visão retrógrada E não contribui para o avanço da ciência em uma dimensão mais alto E aí nós terminamos por aqui não perca o próximo vídeo A História Continua muito obrigado pela sua audiência e até a próxima E aí E aí