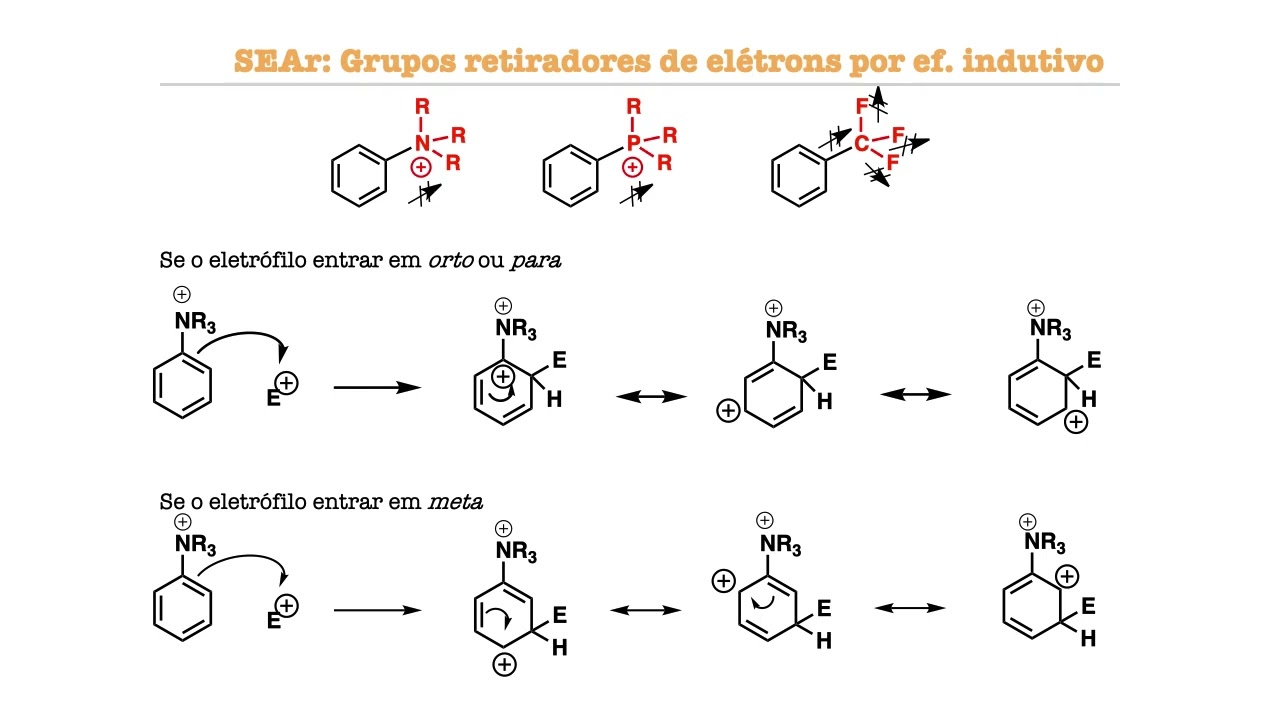
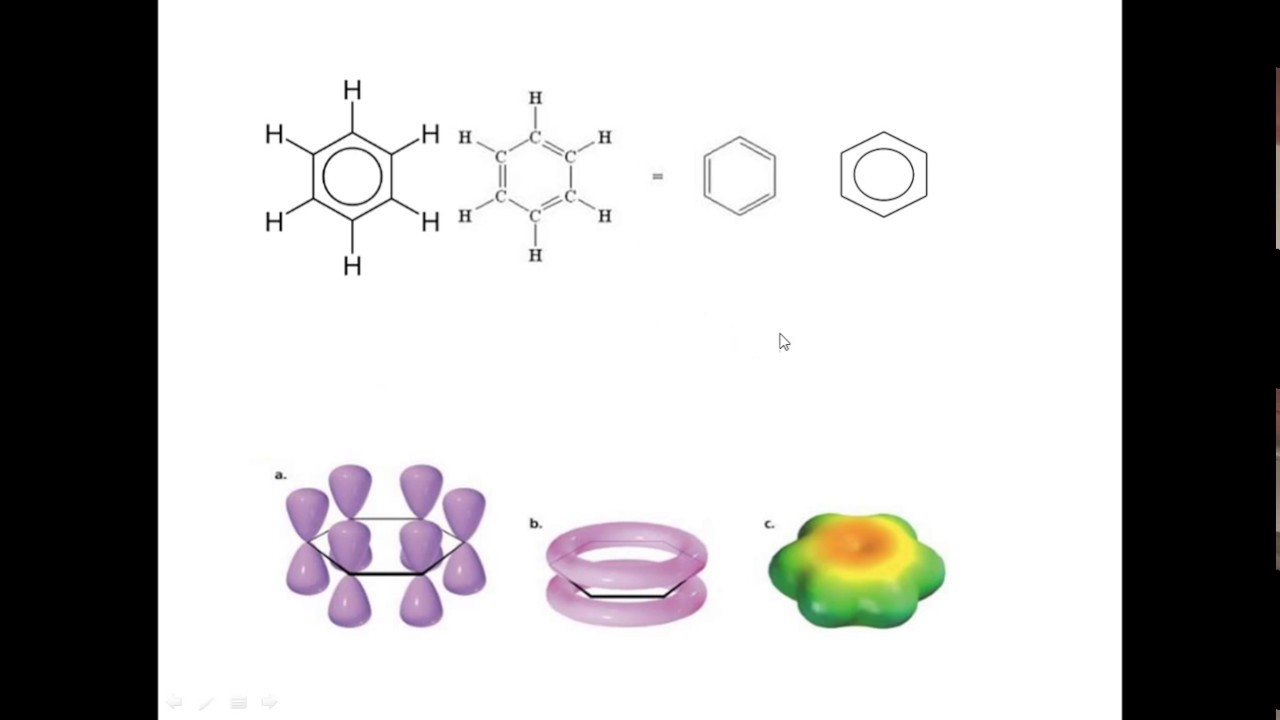
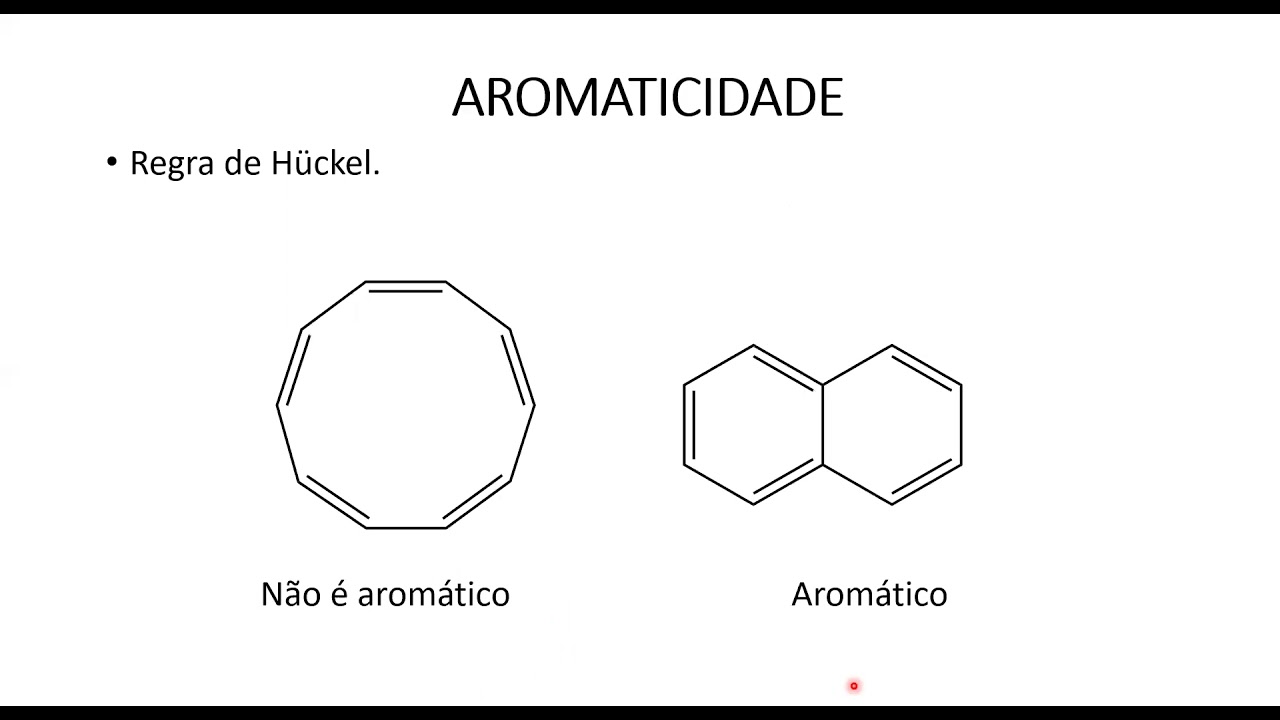
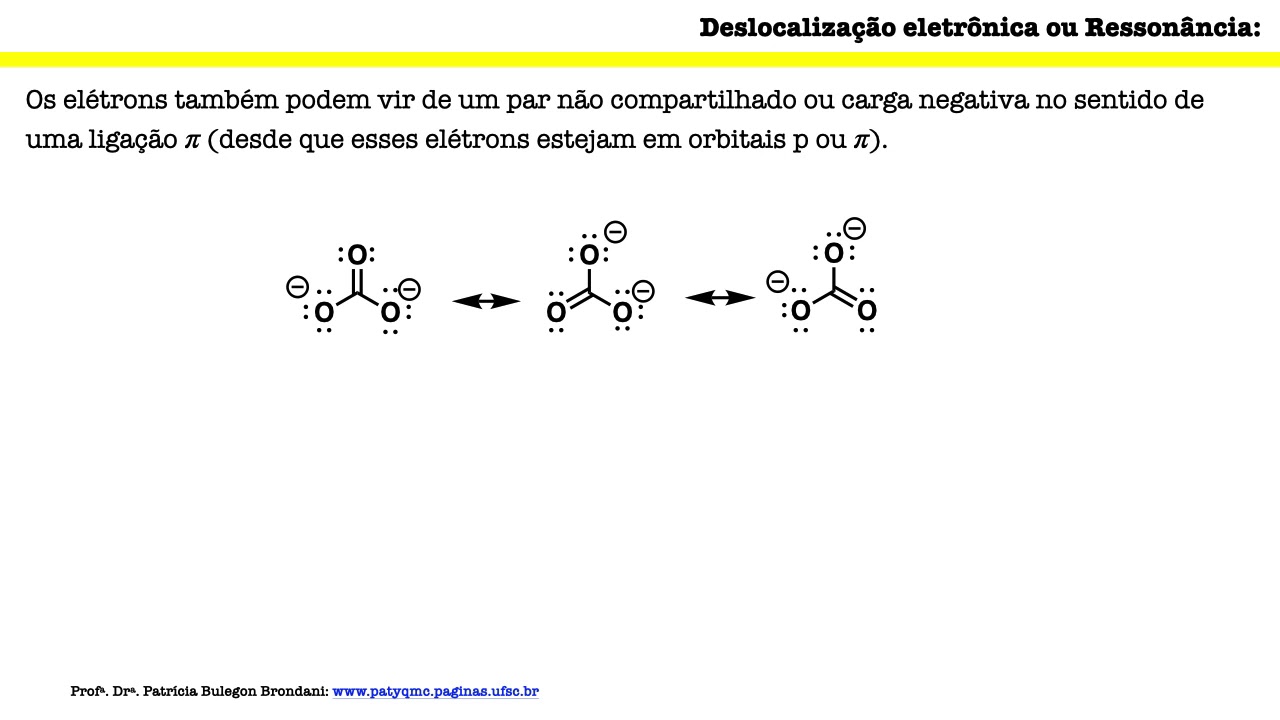
o Olá meu nome é Patrícia e nesse vídeo falaremos sobre o conceito de aromaticidade os compostos aromáticos possuem uma estabilidade especial aromaticidade é uma propriedade associada com a estabilidade Extra apresentada somente por certos tipos de sistema fica por exemplo alguns tipos de alunos bem anulenos são hidrocarbonetos monociclos que contém ligações duplas e simples alternadas e os compostos que são classificados como aromáticos possuem uma reatividade diferenciada nós iniciamos falando do benzeno que é o exemplo mais clássico de composto aromático o benzeno pode ser representado dessas três formas ele tem uma estrutura planar e possui seis átomos de carbono hibridizado SP2 e portanto seis por vitais percurso essa característica estrutural faz com que o benzeno tem uma deslocalização total dos elétrons pi e com que todas as ligações tem um mesmo tamanho e tem mas não são todos os anulenos que são aromáticos e para entendermos as razões para alguns demonstrarem essa estabilidade especial e outros não devemos falar de modelos que expliquem a aromaticidade e para classificar um composto em aromático é comum se aplicar a teoria de orbitais moleculares de rukia que é um dos modelos que explicam uma cidade Talvez o mais comum e muitas vezes essa teoria simplificada em regras diretas que funcionam para classificação dos sistemas aromáticos simples a teoria dos orbitais moleculares de hooke o fala que monociclos planares e completamente conjugados que possuem 4 n + 2 igual ao número de elétrons pi sendo que n é um número inteiro tem uma camada fechada de elétrons todo o senhor vitais ligantes e são excepcionalmente estáveis e esses sistemas são chamados de aromáticos e o benzeno por exemplo possui 6 elétrons pi devido a três ligações duplas Cada uma com 2 elétrons cada sendo assim 4 n + 2 = 6 e n = 1 ou seja um número inteiro para a fórmula citada Além disso vem sendo é cíclico planar e completamente congelado ele era o mágico os sistemas análogos que contém 4 n igual ao número de elétrons pi com n inteiro são chamados de antiaromaticos e são extremamente instáveis para entendermos a origem das formas 4 n + 2 pi e4n devemos olhar para os orbitais moleculares das espécies novamente iniciamos com o benzeno e o benzeno possui seis orbitais P que se combinam formando seis orbitais moleculares se aqueles orbitais formados em Sistemas conjugados já falamos em outros vídeos o orbital molecular de mais baixa energia deriva da combinação em fase de todos os seis orbitais p e chama-se orbital molecular fiz um e o segundo nível de orbitais moleculares de mais baixa energia tem um plano nodal a divisão simétrica de seis átomos de carbono com um plano nodal pode acontecer de duas maneiras através dos átomos ou através das ligações levando a dois orbitais moleculares PSI Ops 2 e o PS3 os dois orbitais moleculares sse2 sse3 tem a mesma energia ou seja são degenerados e os próximos orbitais possuem dois planos nodais e novamente Existem duas maneiras para fazer isso levando a dois orbitais moleculares degenerados se quatro e psíquico e o orbital molecular de mais alta energia possui três planos nodais O que significa que todos os orbitais P se combinam fora de fase e é o orbital molecular pieces e os orbitais moleculares pi 1 2 e 3 São coabitais moleculares ligantes os demais são antiligantes e e para mais detalhes sobre os orbitais moleculares do benzeno o material complementar é inscrito pode ser encontrado no meu site da w w ponto prática Mc. Páginas. Ufsc.
br e o benzeno como falamos possui 6 elétrons pi e eles ficam alocados nos orbitais se um se2 ep13 é e os orbitais antiligantes ficam vazios sendo assim o orbital molecular PS2 e PS3 são os ombros e os orbitais P se quatro cinco os alunos e percebe-se que a camada de orbitais moleculares ligantes está completamente preenchida levando uma alta estabilidade é disso que se trata calcular n inteiro em 4 n + 2 = o número de elétrons pi se n for inteiro significa uma camada fechada de orbitais moleculares ligantes O que é extremamente estável é uma maneira fácil de prever os orbitais moleculares de ciclos conjugados é desenhar um círculo em volta do Círculo o círculo defrost em cada ponto de intersecção desenhar um orbital molecular o diâmetro horizontal do Círculo a linha pontilhada vermelha representa o nível de energia dos orbitais atômicos P originais do carbono e se algum orbital estiver nessa linha ele será não ligante os orbitais moleculares que estiverem abaixo da linha pontilhada serão elegantes e acima antiligantes e deve-se notar no entanto que esse método somente prediz o nível de energia para orbitais moleculares de monociclos e quando planares e também devemos notar que os orbitais moleculares aparecem em pares degenerados com exceção do mais energético e do menos energético se o número de átomos do ciclo for para lá e agora que os orbitais moleculares do benzeno foram apresentados e que se conhece o modo de prever os orbitais moleculares pi se de outros ciclos uma comparação pode ser realizada deve-se ter em mente que não é qualquer anuleno que vai apresentar estabilidade Extra de um sistema aromático comparando o ciclo-octatetraeno o corte com benzeno por exemplo percebeu-se que o Cot se comporta como um polígono ou seja um alqueno simples com várias ligações duplas e não como um aromático e a explicação para esse fato reside nos orbitais moleculares ao montarmos como na figura mostrada na tela os possíveis orbitais P se para o Cot e compararmos com o benzeno e colocarmos os orbitais pirica da sistema nós temos que por exemplo o benzeno tem 6 elétrons o que significa que todos os orbitais moleculares ligantes estão preenchidos levando a uma estrutura de camada fechada que falávamos e por outro lado cote tem 8 elétrons pi seis deles preenche os orbitais moleculares ligantes mais dois elétrons sobram esses elétrons que sobram devem ir para os dois orbitais não-ligantes que são degenerados um em cada orbital ou seja para esse modelo o Cot possui dois elétrons desemparelhados em orbitais de Alta Energia O que é extremamente instável portanto uma estrutura planar do Cot não tem estrutura de camadas fechada que tem bens é e esta é uma das razões para a diferença de estabilidade desses compostos e se repito se o corte fosse planar ele seria antiaromatico porque ele teria 4 n = 8 elétrons e portanto igual a 2 ou seja inteiro para fugir da antiaromaticidade o corte adotam uma estrutura tubular que não é claro dessa forma ele não tem ligações conjugadas ele tem ligações localizadas e ele não forma mais orbitais P se e como ele não fica planar ele é somente não aromático ao invés de antiaromatico Oi e ele faz isso claro porque é mais estável não aromático do que antiaromatico como ele tem a escolha e os graus de liberdade para distorcer a planaridade Ele o faça o outro exemplo de anuleno é o cyclobutadiene um ciclo de 4 metros o ciclobutadieno tem quatro elétrons ou seja dois elétrons ligante mas outros dois elétrons desemparelhados por causa da presença de dois orbitais não ligantes de gêneros sendo assim Se colocarmos na fórmula 4 n = 1 e o ciclobutadieno por esse modelo seria antiaromatico e o ciclo butadieno não possui os graus de liberdade que o corte possui e não consegue distorcer a planaridade para evitar a aromaticidade ele é forçado a ficar planar há evidências experimentais indicam que o circo butadieno ele é na verdade retangular e não quadrado isso modifica o contexto descrito Pelo modelo de orbitais D rukio que considera uma geometria quadrada com ligações de mesmo comprimento na verdade segundo essas evidências experimentais a molécula de ciclobuteno não é estática Existem duas formas que rapidamente sem ter converte sendo assim os dois níveis não-ligantes não seriam mais degenerados nesse modelo e o ciclo butadieno não apresentaria elétrons desemparelhados apesar disso os dois modelos concordam com a empresa dizer que o ciclo butadieno extremamente instável e com uma mulher Alta Energia e na verdade outros métodos de análise consideram um ciclo butadieno não só muito reativo como menos estável do que um dinheiro isolado então podemos dizer que o ciclobutadieno é antiaromatico e concordar com o modelo de Rubio e após seis o próximo número que levaria aí inteiro em 4 n + 2 e 10 o Porém para ser planar um ciclo de 10 membros conjugado deveria ter ângulos de 144 graus o ângulo normal de uma ligação dupla é 120 portanto 144 é longe do ideal esse composto pode ser feito mas ele não adota uma conformação planar e portanto não eram matico mesmo tendo 10 eletros contrastando com isso o 18 anuleno que também é um sistema 4 n + 2 e elétrons com n inteiro nesse caso = 4 ele adota uma conformação planar e era o médico É nesse sistema existe um arranjo trances das ligações duplas todas com ângulos de 120° isso ocorre pois como é um ciclo maior ele tem maior liberdade de organização e consegue acomodar todos os átomos no mesmo plano já ouvinte anuleno também poderia ser planar mas ele é um sistema 4n com ele inteiro ao invés de ser um sistema 4 n + 2 com ele ter sendo assim ele prefere não ser planar porque assim ele é Vita antes era uma cidade e após esses exemplos percebe-se que a regra de Ruca o modelo de Hulk ou é muito útil no entanto a importância de o ciclo ser monociclo é menos Clara o problema começa em Como contar os elétrons em ciclos fundidos por exemplo naftaleno e e deve ser considerado Dois benzenos Unidos ou como um sistema de 10 Eletros e para os químicos o naftaleno tem caráter aromático mas talvez seja um pouco menos estável do que o benzeno é isso se aplica também a outros sistemas fundidos em um sistema fundido não há seis elétrons para cada anel o naftaleno por exemplo se um anel tiver seis elétrons o outro tem 4 é uma maneira de explicar a maior reatividade do naftaleno em relação ao benzeno é considerar um dos Anéis comum benzeno e o outro como um sistema similar ao bull terrier o outro ponto a ser considerado em Sistemas fundidos é que os contribuidores de ressonância não são equivalentes podemos observar para o naftaleno que a primeira estrutura de ressonância tem uma ligação dupla Central que não está presente nas outras duas E além disso se todas as estruturas contribuírem igualmente que ocorre a ligação 12 teria maior caráter de dupla ligação do que a ligação 23 pois a dupla ligação aparece em duas estruturas entre os carbonos numerados comum e dois cálculos de orbitais moleculares mostram essas ligações como diferentes realmente em concordância com esses dados as distâncias de ligação são 1,36 Anderson para a ligação dois e 1,45 para a ligação 23 o padrão de reatividade também é diferente e a ligação 12 reagir preferencialmente com ozônio por exemplo isso não acontece com benzeno onde todas as ligações sem o mesmo comprimento e para o benzeno não substituído todas reagem de maneira similar em alguns sistemas ficam com caráter aromático ao sofrer alguma reação química e se tornarem carregados um exemplo ciclopentadieno o ciclopentadieno neutro não é aromático na sua estrutura ele tem duas ligações duplas conjugadas ele é planar mas ele possui um carbono SP3 que quebra essa conjugação no entanto o cyclopentadiene é facilmente desprotonado levando um ânion muito estável era um mágico esse ano tem 6 elétrons pi 4 das duas ligações duplas e do mais dois da carga negativa essa carga negativa pra que se composto seja aromático precisa estar em um orbital P Portanto o ânimo ou seja o carbânion tem habilitação SP2 para que esta estrutura seja então aromática e o cátion correspondente ele não é facilmente preparado porque ele é completamente conjugado e planar só que ele possui quatro elétrons pi Ao Total e Isso daria aí inteiro na fórmula 4 n e portanto ele é antiaromatico em outro caso interessante é a formação do íon tropílio que há muito estava esse um é formado através da perda de hidreto pelo ciclo é fria no ciclo original de sete membros existem três ligações duplas e portanto seis elétrons pi no entanto um dos carbonos não possuir orbital P puro pois depois está hibridizado SP3 então não conjuga com os demais por isso apesar de se encaixar na regra 4 n + 2 = eletros e com ele inteiro o ciclo não era o médico Porém quando ocorre a perda da igreja EA formação do carbocátion o carbono que antes era SP3 ele Analisa e fica SP2 e a carga positiva portanto fiquem orbital p o orbital foi vazio agora pode se sobrepor aos demais em conjugação e os seus elétrons cobrem todos os sete carbonos através da formação dos orbitais P se e em analogia ao eu tropilio um anel de três membros com uma ligação dupla pode originar um cátion aromático quando o carbono SP3 se vira SP2 o novo sistema é aromático esse sistema tem dois elétrons da dupla ligação ou seja 4 n + 2 = 2 e = 0 o ou seja inteiro e ainda tem todos os carbonos SP2 o que permite uma conjugação dos orbitais p e um sistema planar portanto é aromático compostos cíclicos contendo o outro átomo que não carbono e hidrogênio ou seja heterociclos também podem ser aromáticos um exemplo bastante conhecido é a piridina esse composto se constitui de um anel de seis membros análogo ao benzeno onde um átomo de nitrogênio está no lugar de um ch o anel ainda tem três ligações duplas com 6 elétrons PI é porque tá o Pedro nitrogênio está interagindo com os demais orbitar espelho participando da formação dos orbitais P se o par de elétrons não compartilhados do nitrogênio fiquem orbital SP2 e não é alocado Hereditárias não fazendo parte da aromaticidade como o par de elétrons não está envolvido com era uma cidade esse composto ele pode agir como base sem afetar a estabilização Extra conferida pela aromaticidade de fato acredita é muito utilizada como base em reações orgânicas e seu ácido conjugado Ou seja a sua versão Pro nada é ainda aromático o outro exemplo nitrogenada ou pirrol um ciclo de cinco membros com duas ligações duplas e um nitrogênio e nesse caso o nitrogênio está na forma de NH e os elétrons não ligantes ficam em orbital P enquanto o orbital SP2 faz ligação com o hidrogênio e esse ciclo é aromático pois tem 4 n + 2 = 6 sendo que esses elétrons 6 elétrons são dois das duas ligações duplas e mais dois elétrons não ligantes do nitrogênio orbital p e como os elétrons não compartilhados estão comprometidos com a aromaticidade esse composto não é básico ou seja o par de elétrons não pode ser utilizado para reações facilmente em outros ciclos de cinco membros com duas ligações duplas EA presença de um heteroatomo são aromáticos como Fulano em que vai ter o a tomar oxigênio e o tio feno em que o heteroatomo é o enxofre nesses casos como existem dois pares de elétrons não ligantes um para ficar em hospital p e participa da aromaticidade mas o outro fica orbital SP2 e não participa da aromaticidade podemos ser usado mais facilmente em reações químicas o pé espero que esse vídeo tem ajudado no entendimento do conceito de erva-mate cidade mais detalhes sobre esse assunto podem ser consultados em material escrito no meu site www. pat. com Mc.
Páginas. Ufsc.







![Upbeat Lofi - Deep Focus & Energy for Work [R&B, Neo Soul, Lofi Hiphop]](https://img.youtube.com/vi/THh4fT0O7IY/maxresdefault.jpg)





![Upbeat Lofi - Power and Energize Your Workday - [R&B, Neo Soul, Lofi Hiphop]](https://img.youtube.com/vi/ONcY0BM5EAg/maxresdefault.jpg)