e até o final desse vídeo você vai compreender o que que ocorre com o material à medida que mais calor vai ser fornecido a ele você vai perceber que nem sempre a temperatura vai aumentar [Música] Olá pessoal bem vindo ao vivo sentif antes de prosseguirmos dê um like nesse vídeo isso porque o YouTube vai mostrá-lo a mais pessoas quanto mais light ele tiver assim ele também o canal basta clicar nesse botão aqui e Ative o Sininho para que você possa acompanhar nosso conteúdo que sai a cada semana nós temos que quando você aquece uma água
para o chá a uma dada temperatura você precisa de duas vezes mais calor para aquecer duas xícaras do que para aquecer uma então a quantidade de calor depende da quantidade de massa além disso a experiência também mostra que para que ser uma quantidade de água e levanta a sua temperatura por 60 graus é preciso do dobro do calor que para levá-la por apenas 30 graus com isso fica claro que a quantidade de calor necessária vai depender também da variação de temperatura desejada quanto maior for o aumento desejado na temperatura maior vai ser a quantidade de
calor para promover Esse aumento finalmente a quantidade de calor necessária também depende do material elevar a temperatura de um quilograma de água requer muito mais calor que para fazer a mesma variação em uma mesma massa de alumínio por exemplo Isso tudo foi visto nesse vídeo aqui agora nós podemos juntar todas essas e eu temos vai passando geral que reafirma que a quantidade de calor necessária para promover uma variação de temperatura delta t depende diretamente da massa da substância em seu calor específico e da própria variação de temperatura para medir o calor específico de uma substância
uma amostra dessa substância é aquecida até uma dada temperatura depois ela é colocada no recipiente com uma certa quantidade de água a uma temperatura diferente quando o equilíbrio térmico é alcançado a variação da temperatura é a ferida EA temperatura final da água então obtida isso é feito usando o fato de que no sistema fechado não há perdas de calor para o ambiente a quantidade de calor que o sistema Perde é a mesma quantidade que o outro sistema ganha e para cada quantidade de calor dessa relação nós podemos empregar a equação empírica que acabamos de discutir
usar os valores adequados para cada um dos termos e assim determinar o calor específico essa técnica a famosa calorimetria o usamos o termo fácil para descrever o estado específico da matéria como sólido líquido ou gás a água por exemplo pode existir tanto na fase sólida na forma de gelo como na fase líquida como água e na fase gasosa como vapor essas fases também são chamadas de estados da matéria o estado sólido no estado líquido e o estado gasoso quando o material muda de fase digamos do estado sólido para o líquido ou do estado líquido para
o gasoso sempre há uma certa quantidade de calor envolvida nessa transformação parte dessa energia é a própria energia térmica do material por exemplo num sólido é a energia cinética dos átomos vibrantes mas a energia potencial das ligações moleculares esticadas e comprimidos e essa energia que constitui a energia térmica do material outra energia envolvida na transformação é o calor que pode ser fornecido ou retirada do material o calor é fornecido o material em quantidade suficiente seu derretimento vai ocorrer uma vez que a energia térmica será tão grande que as ligações entre os átomos ou moléculas começam
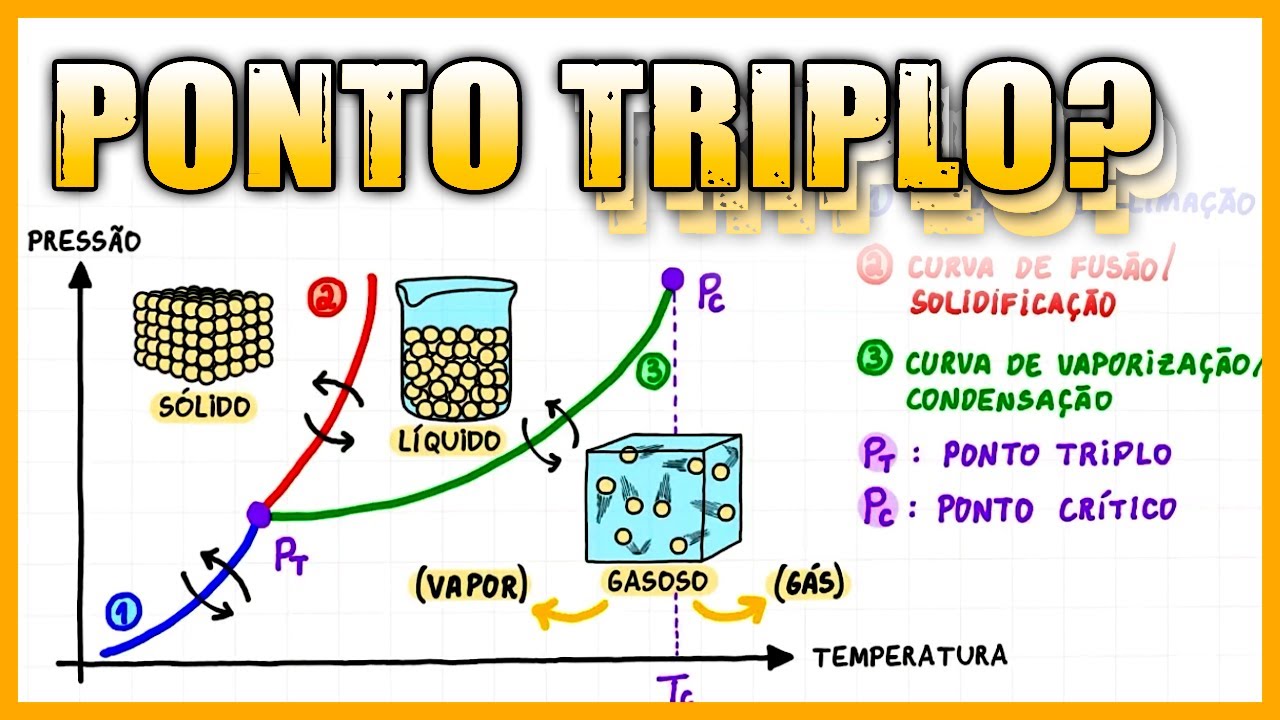
a Se romper permitindo que eles se movam mais livremente a temperatura na qual um sólido se torna líquido é chamada ponto de fusão ou temperatura de fusão por outro lado no caso onde a extração de calor ocorre o oposto a energia térmica do material será reduzida de tal forma que o líquido se solidificam a temperatura em quem socorre é chamado o ponto de congelamento e o rendimento e o congelamento são exemplos de mudanças de fase é um diagrama de Fases é usado para mostrar como as fases de uma substância variam com a temperatura EA pressão
cada diagrama é dividido em três regiões correspondentes as fases sólida líquida é gasosa as linhas de limite que separam as regiões indicam as transições de fase e cada ponto sobre essas linhas representa o estado de equilíbrio de fase que é um estado onde as duas fases diferentes que existem cruzar a fronteira sólido líquido corresponde a fusão ou congelamento depende do sentido enquanto que cruzaram a fronteira líquido-gás corresponde a ebulição ou a condensação também dependendo do sentido mas alguma outra possibilidade cruzar a fronteira do gás sólido a mudança de fase na qual o sólido se torna
um gás é chamada sublimação não é uma experiência cotidiana Mas provavelmente você deve ser familiarizado com a sublimação do gelo seco por exemplo a fronteira gás-líquido term o denominado ponto crítico abaixo do ponto crítico o líquido e o gás são claramente distintos há uma clara mudança de fase quando você passa de um para o outro mas não há distinção Clara entre líquido e gás a pressões e temperaturas acima do ponto crítico nessas condições o sistema é dito um fluido supercrítico e ele varia continuamente entre alta densidade E baixa densidade sem nenhuma mudança de fase último
ponto de interesse no diagrama de fase é o ponto triplo onde os limites da fase se encontra duas fases estão em equilíbrio de Fases ao longo dos limites ao longo das Linhas já o ponto triplo é o único valor de pressão e temperatura ou seja o único ponto no diagrama de fases do qual todas as três fases podem coexistir em equilíbrio de fase e como já mencionamos a transição de fase ocorre geralmente acompanhada por absorção ou emissão de calor por exemplo um bloco de gelo de 1 kg pode ser aquecido a uma taxa constante Esse
é transformado totalmente em água a água então pode ser aquecida até 100 graus celsius e ser transformada totalmente vapor indo além é possível continuar fornecendo calor e aquecer vapor ainda mais nesse processo quando o gelo é aquecido a partir de 20 graus Celsius a sua temperatura aumenta uma taxa de meio grau para cada quilo dyuly de calor que lhe foi fornecido isso porque o calor específico do Gelo é de 2090 Jules por quilograma por graus Celsius quando o gelo atingir 0 graus Celsius a temperatura para de aumentar mesmo que continuemos a fornecer calor nesse estágio
o gelo se converte gradualmente em água e nesse processo de transição de fase não ocorre nenhuma alteração na temperatura depois de adicionados A 160 kg de calor ao sistema a 0 graus Celsius metade do Gelo ainda vai permanecer e a outra metade já terá se liquefeito após 333 kg Julho terei sido adicionados ao sistema todo gelo terá se transformado em água ainda 0 graus Celsius essa quantidade de 336 quilos juros necessárias para transformar 1 kg de gelo a zero grau em 1 kg de água a zero grau é chamado de calor latente de fusão ou
seja para a água o calor latente de fusão ad333 kilos por quilograma a partir da água líquida a 0 graus adição continuar de calor faz com que a temperatura do sistema volte aumentar agora a uma taxa de 1 grau celsius para cada 4190 Jules de calor adicionado isso porque o calor específico da água é 4190 de Ulisses por quilograma por grau quando toda a água for aquecida a 100 graus celsius a fatura volta ficar constante na sequência todo calor adicionado é consumido na transição de fase do estado líquido para o estado vapor que é o
estado gasoso para isso são necessários cerca de 2.250 quilos de calor para transformar o quilograma de água completamente em um quilograma de vapor essa quantidade de calor necessária para transformar um quilograma de água a 100 graus Celsius em 1 kg de vapor a 100 graus celsius é o chamado calor latente de vaporização ou seja o calor latente de vaporização da água é de 2.260 kg de uso por quilograma outras substâncias seguem gráficos semelhantes a este que vivemos para a água embora as temperaturas do ponto de fusão e do ponto ebulição sejam diferentes assim os calores
específicos e os calores de fusão e de vaporização também você Diferencie os calores latentes de vaporização e fusão também se refere à quantidade de calor liberada por um substância quando ela muda de um gás o líquido ou de um líquido para o sólido assim o vapor libera dois 1260 quilos de ouro por quilograma quando ele se condensa e a água lidera a quantidade de 333 kg juros para cada quilograma quando ela se congela em todos os casos o calor envolvido em uma mudança de fase depende não apenas do calor latente Mas também da massa total
da substância Note que o calor que é adicionado ao liberado durante a mudança de fácil então ele pode ser tanto positive quanto negativo as reações químicas são análogas às mudanças de fase pois elas envolvem quantidades bem definida de calor por exemplo a combustão completa de 1 grama de gasolina produz cerca de 46 kg Jules de energia Portanto o calor da combustão da gasolina é 46 mil quilômetros por quilograma os valores de energia dos alimentos também são definidos de forma semelhante quando dizemos que um grama de pasta de amendoim contém 6 calorias nós queremos dizer que
seis que local ou 25 kg de ouro de energia são liberados quantos átomos de carbono e hidrogênio na pasta de amendoim reagem com o oxigênio com ajuda de enzimas em são completamente convertidos em CO2 e água aqui nós vimos como a calorimetria é útil para se estudar o aquecimento EA mudança de fase dos materiais esse vídeo Termino por aqui e se você gostou dessa explicação dá um like assim mais pessoas vão ter acesso a esse vídeo e não saia do canal sem antes se inscrever clique nesse botão aqui no meio da tela e tenha deve
sentir abraço e até a próxima a