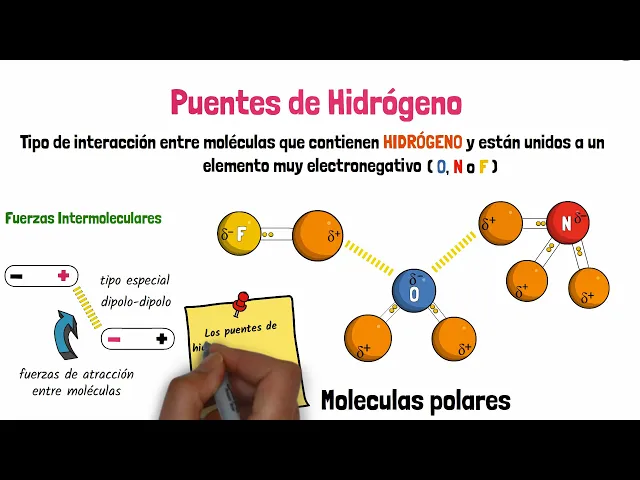
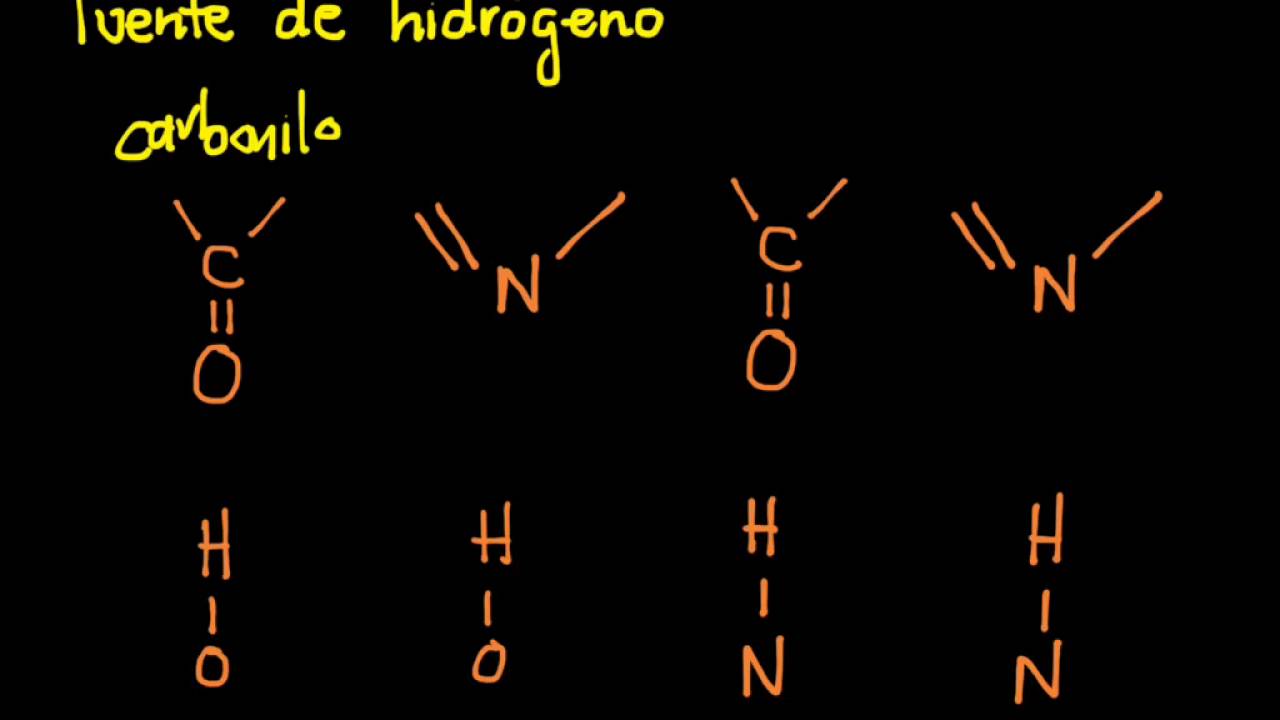
[Música] i [Aplausos] [Música] [Aplausos] fuentes de hidrógeno si queremos hablar de los puentes de hidrógeno primero debemos hablar de las fuerzas intermón cool ares y estas se definen como fuerzas de atracción entre moléculas existen varios tipos de fuerzas intermón oculares como ya hemos visto en otros vídeos sin embargo para este vídeo nos enfocaremos únicamente en los puentes de hidrógeno pues bien dicho esto podemos definir a los puentes de hidrógeno como un tipo de interacción entre moléculas que contienen hidrógeno y están unidos a un elemento muy electro negativo ya sea oxígeno nitrógeno o flúor dicho en
otras palabras las moléculas que contengan un enlace entre un hidrógeno y un elemento muy electro negativo y hasta el flúor nitrógeno y oxígeno formarán puentes de hidrógeno cuando se forman este tipo de enlaces la molécula se vuelve muy polar es decir que los electrones del enlace que dan mayor parte del tiempo cercanos al elemento más electro negativo por lo que es el lado de la molécula tiene carga negativa y los hidrógenos tendrán carga positiva bajo estas características podemos decir que estas moléculas forman puentes de hidrógeno pero como sucede esto pues bien el oxígeno nitrógeno o
flúor al ser muy electro negativos detendrán por más tiempo los padres de electrones de los enlaces y esto formará que la molécula tenga una carga parcial negativa del lado del elemento más electro negativo y una carga parcial positiva del lado de cada hidrógeno pero estas cargas van a ser muy polares como sabemos las cargas opuestas te atraen entre sí y las moléculas con puentes de hidrógeno al ser muy polares atraerán a la carga opuesta de una molécula con mucha intensidad entonces se dice que las cargas de hidrógeno con carga positiva atraerán a la carga negativa
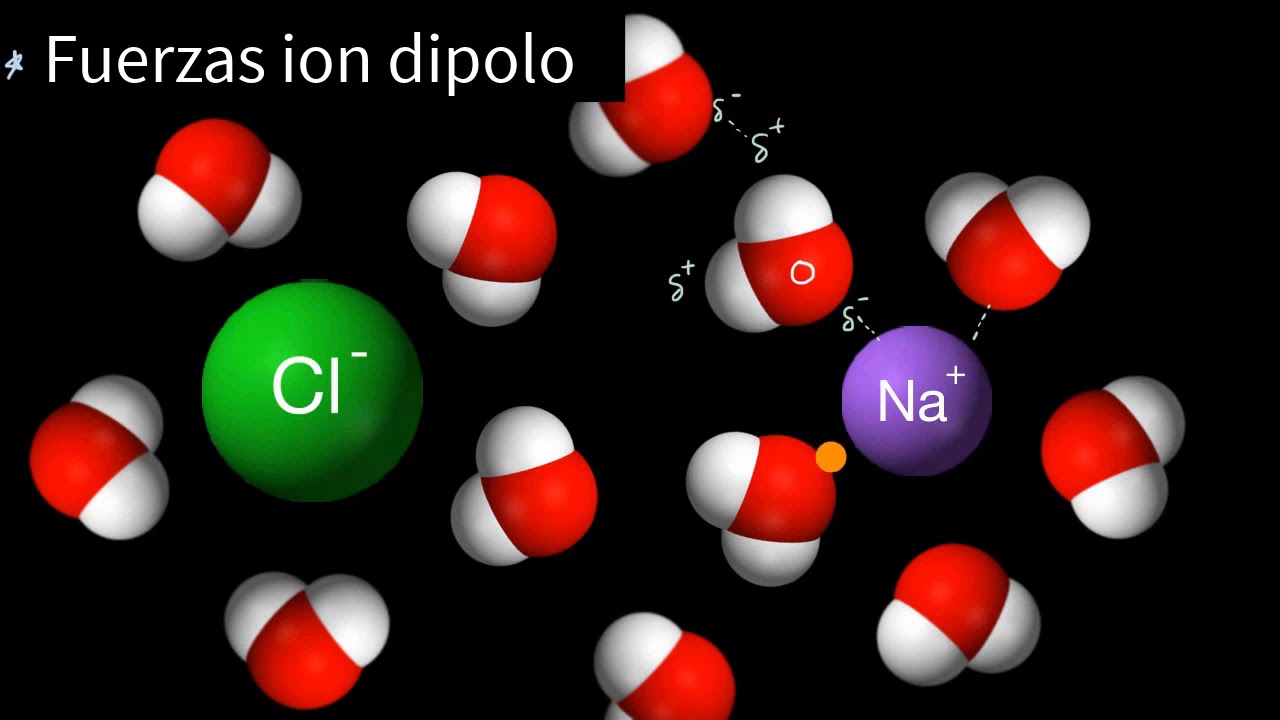
de otras moléculas y entre más polar sea la molécula mayor fuerza de atracción habrá entre las cargas la interacción que se crea con los puentes de hidrógeno es tipo dipolo dipolo que esta es una atracción entre moléculas muy polares y las moléculas acomodan de tal forma que las cargas opuestas queden más cerca para tener una mejor interacción entre sí sin embargo a pesar de que los puentes de hidrógeno tengan este tipo de interacción dipolo dipolo la diferencia es que los puentes de hidrógeno tienen una mayor fuerza de atracción ya que la polaridad de las moléculas
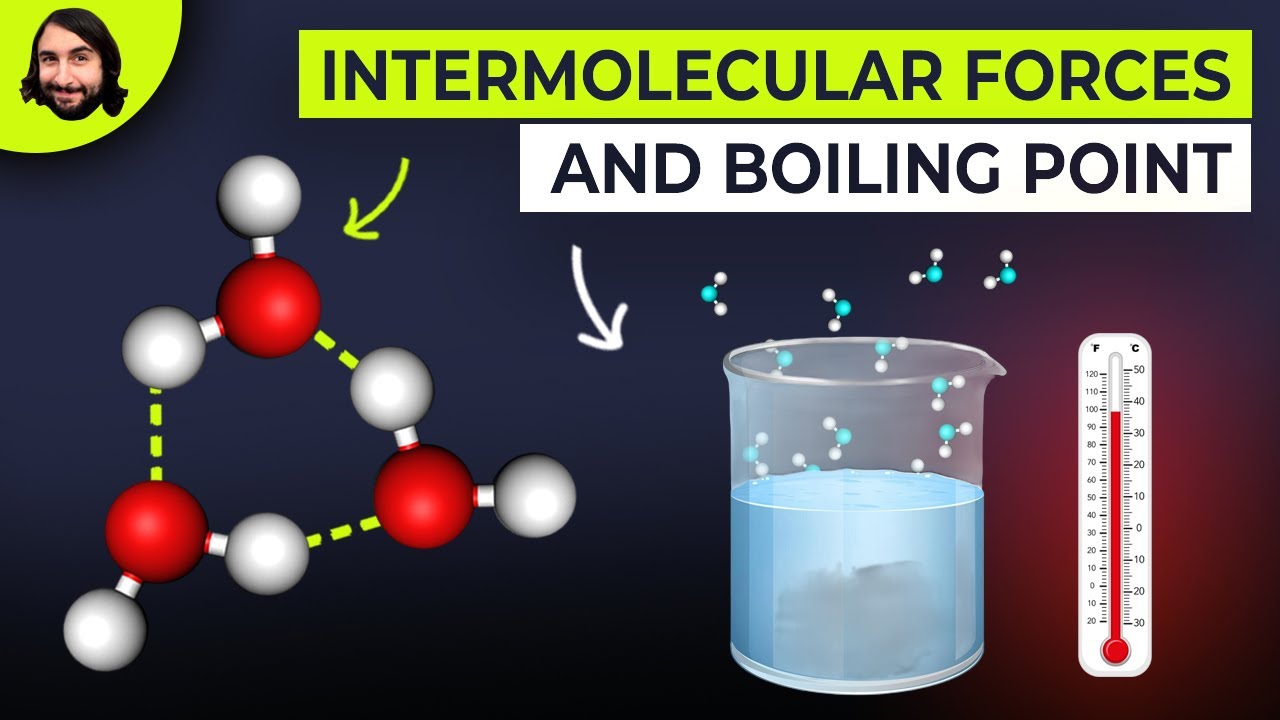
hace mayor la interacción y esto se ve reflejado en algunas propiedades físicas como el punto de ebullición pues para pasar un compuesto líquido al estado gaseoso debemos de romper estas fuerzas inter moleculares y entre más fuertes sean mayor será la temperatura para poder lograr la ebullición de estos compuestos por ejemplo la molécula del agua es capaz de formar cuatro puentes de hidrógeno ya que las cargas positivas de los hidrógenos atraerán a los oxígenos de otras moléculas y el átomo de oxígeno al tener dos pares de electrones libres atraerá a dos átomos de hidrógeno haciendo que
la fuerza de interacción entre estas moléculas sea muy fuerte si te gustó este vídeo dale like y suscríbete nos vemos hasta el próximo vídeo