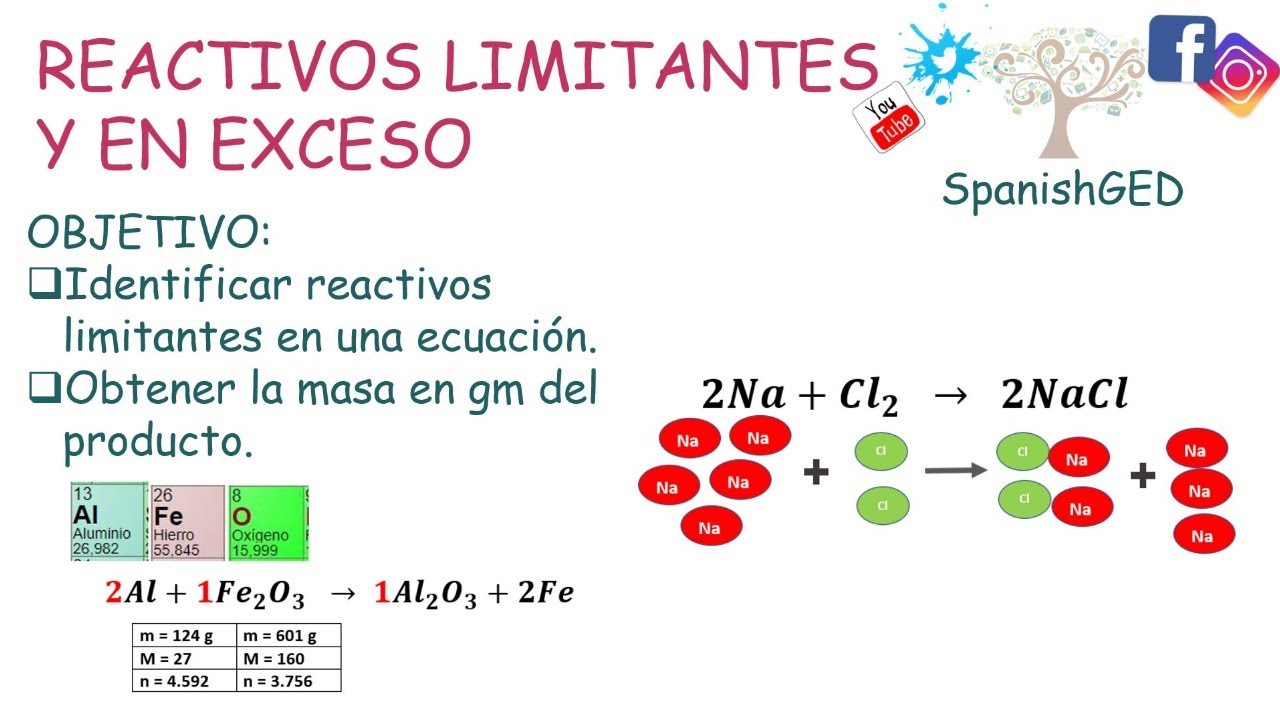
hola a todos espero estén muy bien hoy aprenderemos dos cosas en primer lugar que es el reactivo limitante y después veremos un método sencillo de como identificarlo con esto podremos resolver muchos problemas de este que me tria y sin más introducción vamos con la primera parte en todas las reacciones químicas que participan dos o más reactivos siempre hay uno que se consume primero es decir que se acaba antes que todos los demás por ejemplo imaginemos que el reactivo a reacciona con el reactivo b y eso forma un solo producto mientras transcurre la reacción ambos reactivos se van consumiendo generalmente en diferente proporción es decir a veces se necesita más de uno que del otro entonces llega un punto en que uno de los reactivos se consume totalmente en ese preciso momento se detiene la reacción aunque sobre del otro reactivo ya no se puede formar más producto porque ya no existe uno de los ingredientes y estas son las dos características del reactivo limitante es aquel reactivo que se consume primero y por lo tanto es el reactivo que determina la cantidad de producto que se puede formar esta definición de reactivo limitante es muy importante para entender cómo lo podemos identificar entonces para que quede un poco más claro vamos a hacer una pequeña analogía [Música] imagina que trabajas en un restaurante donde prepara sandwiches forzosamente cada sándwich se prepara con dos rebanadas de pan una rebanada de jamón y cuatro rebanadas de jitomate tú tienes un rato trabajando y llega al punto en que los ingredientes se comienzan a terminar y nos quedamos únicamente con iu rebanadas de pan 6 rebanadas de jamón y 12 rebanadas de jitomate la pregunta sería cuántos sandwiches más se podrían preparar siguiendo la receta al pie de la letra vamos a dar unos segundos para que intentes resolverlo mentalmente si quieres ponle pausa [Música] ok considerando los ingredientes que tenemos la cantidad máxima de sandwiches que se pueden preparar son 33 sandwiches nada más y para demostrarlo podemos pensarlo así para preparar esos 3 sándwiches se necesitan 3 rebanadas de jamón de acuerdo con la receta de jitomate se necesitarían 12 rebanadas porque la receta pide 4 rebanadas para cada uno y para el pan se necesitarían lógicamente 6 rebanadas entonces si consideramos la cantidad que tenemos de cada ingrediente y la cantidad que usaríamos para esos 3 sándwiches todavía nos sobraría jamón el jitomate es decir ya se acabó y el pan todavía nos sobran unas rebanadas entonces el ingrediente limitante es el jitomate porque ya se acabó y no podríamos hacer más sandwiches como se debe a veces los alumnos piensan que el reactivo limitante es el que se tiene menos cantidad pero no en este caso teníamos más rebanadas de jitomate y aún así es el limitante entonces no tenemos que confundir eso el limitante es el que se acaba primero no importa si tenemos mucho tenemos poco ahora hacer una tabla como la del ejemplo si nos ayuda a identificar qué reactivo es el que se agota primero pero en las reacciones químicas no es tan sencilla hacerla para mí la mejor manera para identificar quién es el reactivo limitante es hacer un cálculo para ver cuál de los reactivos es el que te produce menor cantidad de producto por ejemplo si hubiéramos querido saber el ingrediente limitante en la analogía pasada sin hacer la tabla podríamos haber hecho escenarios distintos para cada ingrediente a qué me refiero en uno vamos a calcular cuántos sandwiches se podrían preparar con las seis rebanadas de jamón en otro escenario vamos a calcular de nuevo cuántos sandwiches se podrían preparar ahora vamos a tomar en cuenta únicamente el jitomate y en el último escenario lo mismo pero con el pan el cálculo es súper sencillo básicamente es una regla de 3 por ejemplo un sándwich necesita una rebanada de jamón si se tienen 6 rebanadas de jamón cuánto se podrían preparar pues lógicamente serían 6 sándwiches en los últimos vídeos vimos mucho cómo usar la regla de 3 ahora en el caso del jitomate un sándwich necesita 4 rebanadas de jitomate si nosotros tenemos 12 rebanadas pues la regla de 3 quedaría como 12 por 1 entre 4 o sea se podrían preparar 3 sándwiches y con el pan sería igual cada sándwich necesita dos rebanadas y si tenemos diez rebanadas pues podremos preparar cinco sandwiches listo ya que tenemos el resultado de los tres escenarios vamos a analizarlo un poco nosotros sabemos que el reactivo limitante es el que determina la cantidad de producto eso es lo mismo que decir que el reactivo limitante es aquel que produciría la menor cantidad de producto entonces aquí concuerda con que el jitomate es el ingrediente limitante porque es el ingrediente con el que prepararemos la menor cantidad posible de sándwiches esta sí será una manera fácil de identificar al reactivo limitante simplemente hacemos un escenario con cada reactivo y vemos cuál produciría la menor cantidad de producto sólo que en lugar de seguir una receta le vamos a hacer caso a los coeficientes este geométricos por ejemplo vamos a hacer un problema un poco más realista pero antes de eso si te ha gustado este tipo de explicación dale like al vídeo y recuerda suscribirte para no perderte ninguna de nuestras clases que tendremos ahora si el problema dice si se hacen reaccionar 3. 6 moles de óxido de vanadio con 16 moles de calcio cuántos moles de vanadio sólido se pueden producir y aquí tenemos la reacción balanceada recuerda siempre asegurarte de que esté balanceada no te vaya a pasar como a mí que tuve que bajar el vídeo pasado porque no lo sé que muy bien jeje pero bueno antes que nada como nos podemos dar cuenta de que se trata de un problema de reactivo limitante sin que nos lo mencionen es muy fácil en cualquier problema que se especifique la cantidad disponible de más de un reactivo es nuestro trabajo encontrar el reactivo limitante porque una ley de la química es que cualquier problema este geométrico se resuelve con base en el reactivo limitante ahora sí para resolverlo vamos a plantear escenarios como en el ejemplo en uno que podemos llamar escenario as si tú quieres vamos a calcular cuántos moles de vanadio se producen con los 3. 6 moles de óxido de vanadio y aparte en un escenario b vamos a calcular los moles de vanadio que se producirían al hacer reaccionar los 16 moles de calcio cuando lo vemos así por separado no es nada complejo es como resolver dos problemas sencillos parecido a los vídeos pasados solo hay que pasar de moles de reactivo a moles de producto y para seguir el mismo hilo vamos a resolverlo con una regla de 3 que podríamos escribir siguiendo estos tres pasos el paso 1 es identificar las sustancias involucradas en el problema el 2 es indicar la relaciones tequio métrica que existe entre estas sustancias y 3 vamos a agregar los datos del problema así de fácil para cada escenario vamos con el primero en el caso a las sustancias involucradas son el óxido de vanadio y el vanadio sólido ese es el paso 1 debemos identificar la relación que existe entre estas dos sustancias básicamente debemos tomar sus coeficientes o sea en la reacción balanceada dice que un molde óxido de vanadio produce dos moles y por último tenemos que agregar los datos del problema es decir con 3.
6 moles de óxido cuantos de vanadio se producen esa es la incógnita aquí y con esto ya queda la regla de 3 sólo recuerda que se multiplican los datos cruzados y se divide entre el otro eso nos quedaría así los moles de vanadio es igual a 3. 6 por dos moles entre 1 eso es igual a 7. 2 moles listo esto es lo que se produciría en el escenario a ahora veamos qué pasa del otro lado aquí queremos saber qué cantidad de vanadio se produce con los moles de calcio entonces primero escribimos estas dos sustancias indicamos la relación que existe entre ellos o sea los coeficientes de la reacción dicen que 5 moles de calcio producen dos moles de vanadio y por último agregamos los datos del problema 16 moles que se tienen de calcio cuánto producirían de vanadio perfecto ya está la regla de 3 pues hacemos las mismas operaciones eso quedaría que los moles de vanadio equivalen a 16 moles por dos moles entre 5 y eso da 6.
4 moles finalmente ya con este resultado podemos comparar los dos escenarios en el que se produce la menor cantidad de producto es en el caso b o sea el calcio es el reactivo limitante por lo tanto el resultado del problema sería éste únicamente se producen 6.












![Estequiometría 🧪 Química [CICLO FREE]](https://img.youtube.com/vi/QdYf9WvuuY8/maxresdefault.jpg)