[Música] Hola hola qué tal espero que todo muy bien o por lo menos decentemente vamos a seguir con el tema de termo vamos a hablar de la desigualdad de klaus primero vamos a hablar de la igualdad de klaus y luego ya vamos a hablar de la desigualdad de klaus que es la que nos va a definir básicamente esto que habíamos hablado de cuando un proceso era reversible o Irreversible por desgracia se me ha borrado esa parte de la pizarra pero pero no temáis me queda aquí este trozo estupendo que era el ciclo de carnot para
gases ideales porque lo vamos a utilizar ahí en principio vamos a hacerlo para un proceso reversible vamos a bueno habíamos hablado de procesos irreversibles de transferencia de calor de rozamiento y de procesos que no sean cuasi estáticos pero necesitamos algo un poco más matemático para para saber si un proceso reversible o no y aquí es donde entra la desigualdad de klaus y en lo primero que vamos a ver que es la igualdad de klaussos quedaos con esto vamos a hacer un pequeño dibujito de esto porque lo vamos a utilizar si hacéis un poco de memoria
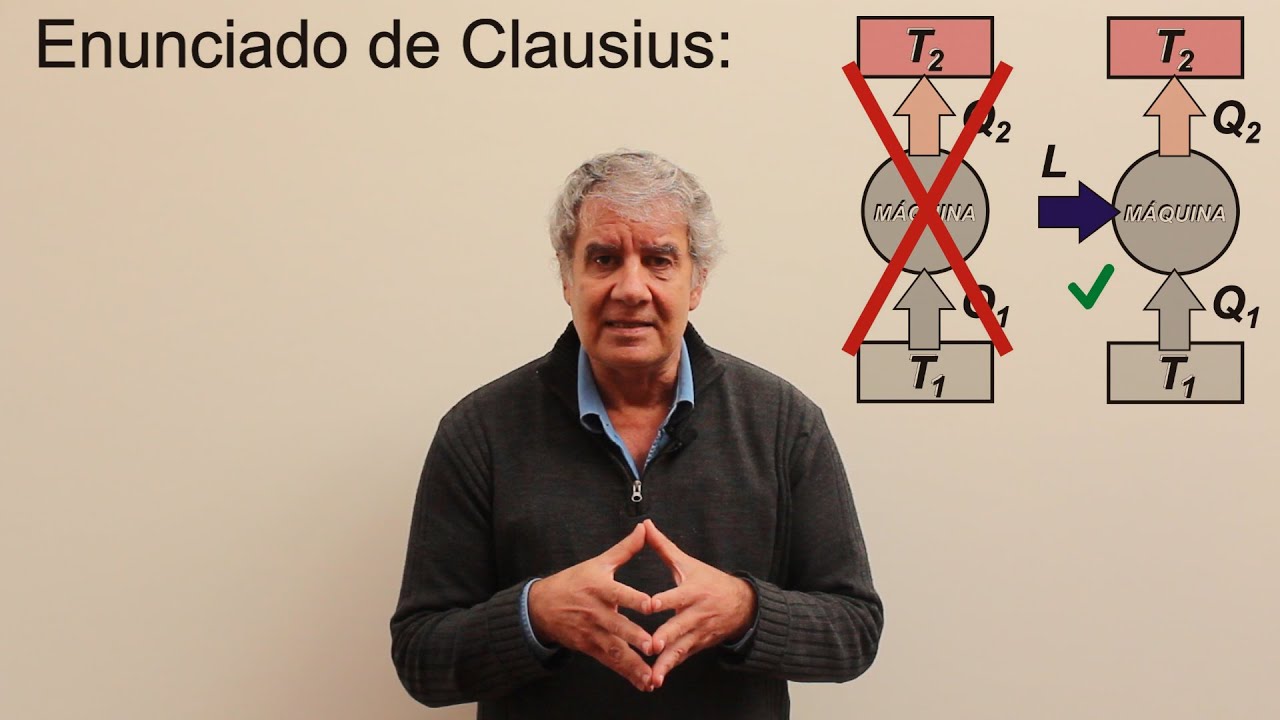
y os acordáis de la máquina de carnot y todo eso recordaréis que aquí teníamos una máquina que trabajaba entre dos focos uno caliente y uno frío que había una transferencia de calor que tratábamos de encontrar Cuál era el trabajo que podíamos realizar y lo que hacíamos era un proceso isotermo a lo largo de esta línea en una temperatura caliente extraíamos calor de alguna manera componiendo un entorno frío o lo que sea del sistema de forma diabética luego lo manteníamos en un foco frío y luego volvíamos a meter calor de forma que generábamos un trabajo ese
trabajo venía dado por un rendimiento que era esta y lo habíamos expresado de esta manera bueno vayamos a ponerle aquí Unas deltas o lo que sea para ver que son procesos entonces qué es lo que tenemos aquí aquí tenemos una máquina que funciona con un cierto rendimiento pero este rendimiento también lo podríamos expresar de esta manera en función de las temperaturas que por esto se había dicho que una máquina no podía tener un rendimiento perfecto porque un rendimiento perfecto significa perdón O como tengo la garganta significa que esta temperatura tiene que ser cero y el
cero absoluto bueno no sabemos pero todavía pero sospechamos que es algo realmente difícil de conseguir sino imposible bien Entonces qué es lo que vamos a hacer lo que vamos a hacer en lo siguiente vamos a considerar que tenemos dos máquinas térmicas dos máquinas reversibles que trabajan entre los mismos focos y fijaos donde he puesto la línea de implicación vale si trabajan entre los mismos focos van a tener en el mismo rendimiento pero ojo que yo tenga un cierto rendimiento no significa que estén trabajando entre los mismos focos vale cuidado si esta cantidad es Exactamente igual
de proporcional Por ejemplo yo trabajo entre 20 y 200 grados voy a tener una estas tf y esta tc Pero esto es lo mismo que trabajar entre dos Kelvin y 20 Kelvin vale Así que el rendimiento de esa máquina será el mismo ojo de acuerdo una vez aclarado Cuál es la línea o sea la dirección de la implicación nos quedamos con esto yo voy a tener que trabajar entre los mismos focos y por lo tanto el mismo rendimiento que va a ser el rendimiento de la máquina 1 igual al rendimiento de la máquina 2 y
lo voy a expresar de la siguiente manera el rendimiento de la máquina 1 lo voy a expresar Perdón había puesto aquí más me acabo de dar cuenta si se disculpar porque estoy haciendo máquinas que trabajan a más del 100% y eso no es posible vale el rendimiento de la máquina 1 lo voy a expresar de esta manera es decir uno menos y el rendimiento de la máquina 2 lo voy a expresar de esta otra manera por qué lo hago así porque yo lo que quiero es comparar estos o sea es decir quiero comparar qué es
lo que sucede en la relación entre el foco frío y el foco caliente o sea mi objetivo es vamos a ver como voy a trabajar dentro de una misma máquina Por así decirlo porque al fin y al cabo son iguales Quiero obtener una relación entre los focos fríos y los focos calientes bien entonces yo aquí lo que hago es que me tengo que esto es igual a esto me puedo cepillar esto cambiarlo de signo bla bla bla bla y me queda vale Y aquí es donde voy a pasar esta al otro lado y me voy
a tener que Delta c esto es igual a cero vale aquí es donde yo voy a utilizar esta relación Es decir Yo como tengo que estas negativa esto significa que menos el valor absoluto de Delta F es positivo me voy siguiendo no es decir le cambiamos le pusimos el valor absoluto para mantenerlo negativo Pero ya sabemos que es negativo por lo tanto menos con menos se nos hace positivo y por lo tanto yo me puedo cepillar estos valores absolutos y poner aquí un signo más vale Y aquí es donde tenemos ya la primera relación que
nos va a interesar qué es lo que encontramos encontramos que en un proceso reversible las sumas de las transferencias de calor divididas por la temperatura es decir la relación del foco caliente más la relación del foco frío se tiene que anular entonces aquí viene donde la van a matar cuidado qué es lo que voy a hacer yo yo lo que voy a hacer es considerar lo siguiente tengo todo esto de aquí todo esto es un proceso macroscópico digámoslo así grande yo lo que voy a hacer es dividirlo en trocitos pequeñitos vamos a dividirlo Así es
decir aquí dibujamos una diabética aquí dibujamos otra diabética entre estos dos focos y aquí dibujamos otra isoterma qué es lo que voy a tener yo aquí pues voy a tener aquí una micro máquina mini máquina de carnot miniciclo de karnot donde aquí va a entrar una cantidad de calor del foco caliente que no es la misma que todo esto sino que va a ser solo esta este recorrido de aquí voy a tener aquí un recorrido a lo largo de esta isoterma hasta este punto luego voy a sacar calor hacia allá y luego voy a volver
por esta isoterma de aquí qué es lo que va a suceder que este foco frío se va a alimentar a esta máquina que va a circular de esta manera de manera que para esta maquinita de aquí está mini máquina de carnot miniciclo de carnet el foco frío de esta Va a ser el foco caliente de esta y de esta manera Vamos haciendo lo mismo y así para todas las para todas las máquinas que tenemos aquí entonces aquí y esto es una cosa que nos sale de los diferenciales y de un montón de movidas pero solo
me interesa que os quedéis con la idea y es la siguiente fijaos que al haber esta relación entre focos calientes focos fríos esta forma de recorrerlo es decir yo aquí en mi máquina de esta de aquí lo recorro de esta manera y en mi máquina de aquí lo recorro de esta manera entonces estas caída de foco de foco frío va a contrarrestarse con esta subida de foco caliente no sé si me explico es decir como esta máquina va a alimentar a esta de forma perfecta entre comillas o pegamoslo Así o sin comillas lo que voy
a hacer es reutilizar ese calor para llevármelo a la siguiente máquina de manera que lo que nos va a quedar al final es todo este ciclo de aquí en grande qué quiero decir con esto quiero decir que yo lo que voy a hacer es repartir todo este ciclo en un montón de miniciclos y por lo tanto lo que voy a tener Es que la transferencia total de calor la voy a repartir en pequeños transferencias de calor es decir una suma vamos a poner y desde igual a 1 hasta n de miniciclos de calor pero y
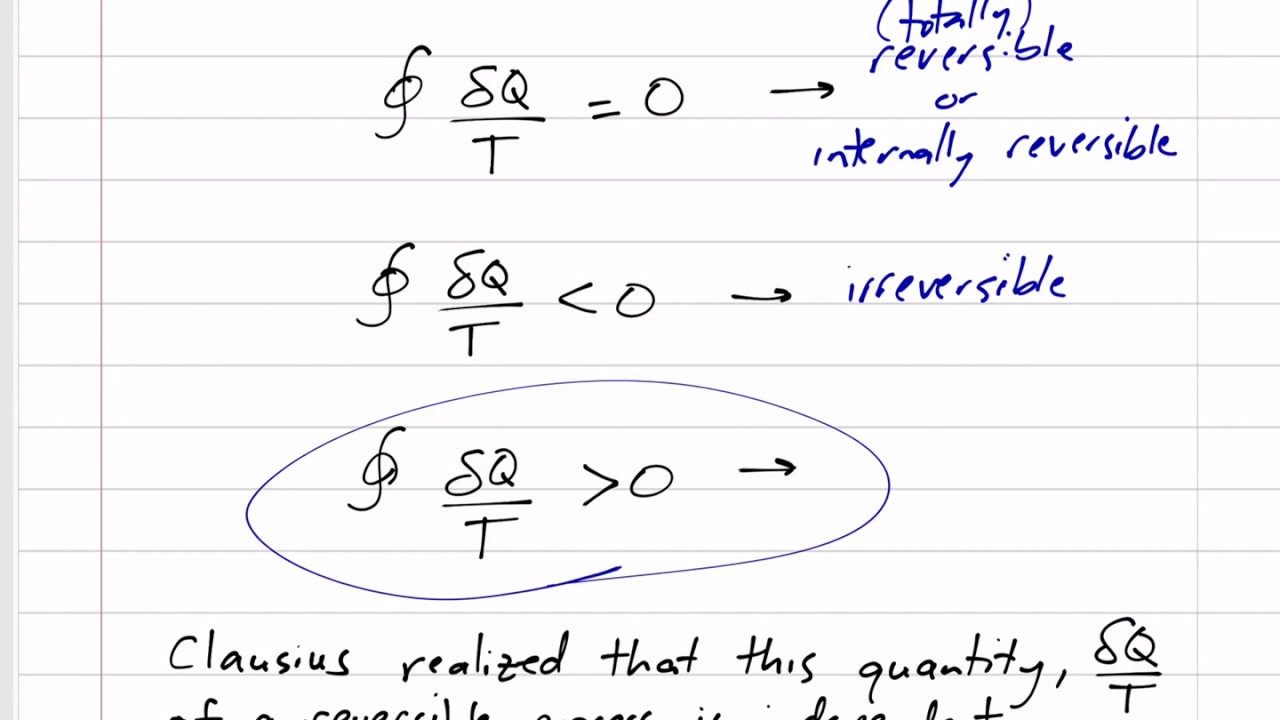
aquí es donde viene lo interesante tiene que cumplir esas relaciones es decir cada uno de los calores transferidos va a cumplir que si lo dividimos por su temperatura correspondiente me va a dar 0 al sumarlo con el con su propio foco frío y por lo tanto lo que tengo aquí es que si yo cojo y sumo todos esos calores cada uno de ellos la suma me va a dar 0 Y esto es lo que es la desigualdad de cláusus perdón la igualdad de cláusus y aquí ojo no tenemos que sacar la misma cantidad de calor
que metemos es decir esto no es cero vale lo que es cero es el cociente entre cada uno de estos calores y su temperatura correspondiente vale es decir cada una de estas mini máquinas lo que hacemos Es esta relación para cada una de las mini máquinas y luego al sumarlas todas me tiene que dar cero Vale entonces encontramos que esto es válido para un proceso reversible Qué sucede para un proceso Irreversible Bueno pues para un proceso Irreversible lo vamos a poner aquí y lo mismo que esto era para procesos reversibles Esto va a ser para
procesos irreversibles cómo vamos a hacer esto pues vamos a hacer la misma jugada pero sabiendo que el rendimiento de una máquina reversible es siempre mayor que el rendimiento de una máquina Irreversible y ahora mucho ojo con lo que vamos a hacer vamos a hacer la misma jugada que aquí es decir vamos a poner esto en función de las temperaturas y los calores pero pero aquí cuidadito con cuál ponemos y cuál expresamos en función de qué vamos a expresarlo de esta manera veréis vale Esto es para un proceso reversible esto para el proceso Irreversible por qué
lo estoy expresando así porque al final cuando hagamos nuestra magia Por así decirlo nos va a quedar una cantidad positiva por un lado vale lo que queremos es a ver al final es todo lo que nos va a salir es lo de la entropía Entonces qué es lo que hemos definido que básicamente en un proceso reversible la entropía se mantiene constante vale esto os lo adelanto ya en Primicia qué es lo que queremos qué es lo que vamos a querer aquí aquí lo que vamos a querer es que esta cantidad nos quede una desigualdad el
orden en el que nos quede la desigualdad en realidad matemáticamente nos importa un la verdad O sea nos daría igual hacerlo con el con el signo cambiado lo que pasa es que pues por convenio lo ponemos de esta manera para que la cantidad que con la que vamos a trabajar después spoiler la entropía nos quede positiva Vale entonces esto es un convenio y lo que vamos a hacer es Pues precisamente la misma magia que habíamos hecho antes es decir vamos a y vamos a empezar cepillarnos esto de aquí por lo tanto bien Ahora qué es
lo que sucede que tenemos aquí dos signos menos si cambiamos el signo a esto lo que vamos a hacer es cambiarle el sentido a la desigualdad y por lo tanto nos va a quedar esto de Aquí y ahora lo que vamos a hacer es pasamos está a este lado y esta temperatura la dejamos dividiendo y volvemos a hacer la misma jugada que hicimos antes es decir Tenemos aquí El delta partido de la temperatura del foco caliente menos el valor absoluto de delta del foco frío partido de la temperatura del foco frío y esto es menor
que cero ahora como esta sabíamos que era negativa negativo con negativo se nos va a quedar positivo borrando los valores absolutos y esto positivo y ya tenemos otra vez esto de aquí ahora qué vamos a hacer vamos a volver a hacer lo mismo pero en nuestro caso es decir para este proceso Irreversible lo que vamos a tener tenemos que esto esto de aquí sigue siendo cierto es decir el calor sigue siendo el calor que metemos el calor que sacamos etcétera y toda la suma de los calores pero ahora cuando dividamos cada uno de estos calores
por su temperatura nos va a quedar que la suma va a ser menor que cero por lo tanto vamos a tener que en un proceso Irreversible implica que la suma en y de los delta q y partido por cada una de sus temperaturas es menor que cero vale Esto sí es la desigualdad de klaus además que nos está diciendo esto ojo fijaos bien que tiene que ser menor que cero o como mucho es decir en un proceso Irreversible es menor que Cero en un proceso reversible es igual a cero por lo tanto si esta suma
Es mayor que cero tendríamos un rendimiento mayor que el de la máquina de carnot y lo que significa esto es que el proceso sería imposible no se podría llevar a cabo no podemos por la segunda ley de la termodinámica no podemos tener un rendimiento mayor que el de la máquina de carnot punto que no es posible hacer una máquina de movimiento Perpetuo coña esta máquina de movimiento perpetua que he inventado hoy es un fiasco sigue funcionando más y más deprisa Lisa hace el favor en esta casa obedecemos las leyes de la termodinámica bueno estábamos buscando
un una forma de averiguar si un proceso es espontáneo o no A ver para saber si un proceso es espontáneo o no vamos a necesitar más herramientas que se salen de lo que se va a ver este curso hablamos ya de entalpías y de cosas funciones termodinámicas muy chungas sí básicamente de derivar la mitad del alfabeto con respecto a la otra mitad y así se hace la termodinámica En qué es lo que hemos encontrado aquí aquí lo que hemos encontrado básicamente es una primera intuición realmente de lo que vamos a tener de lo que vamos
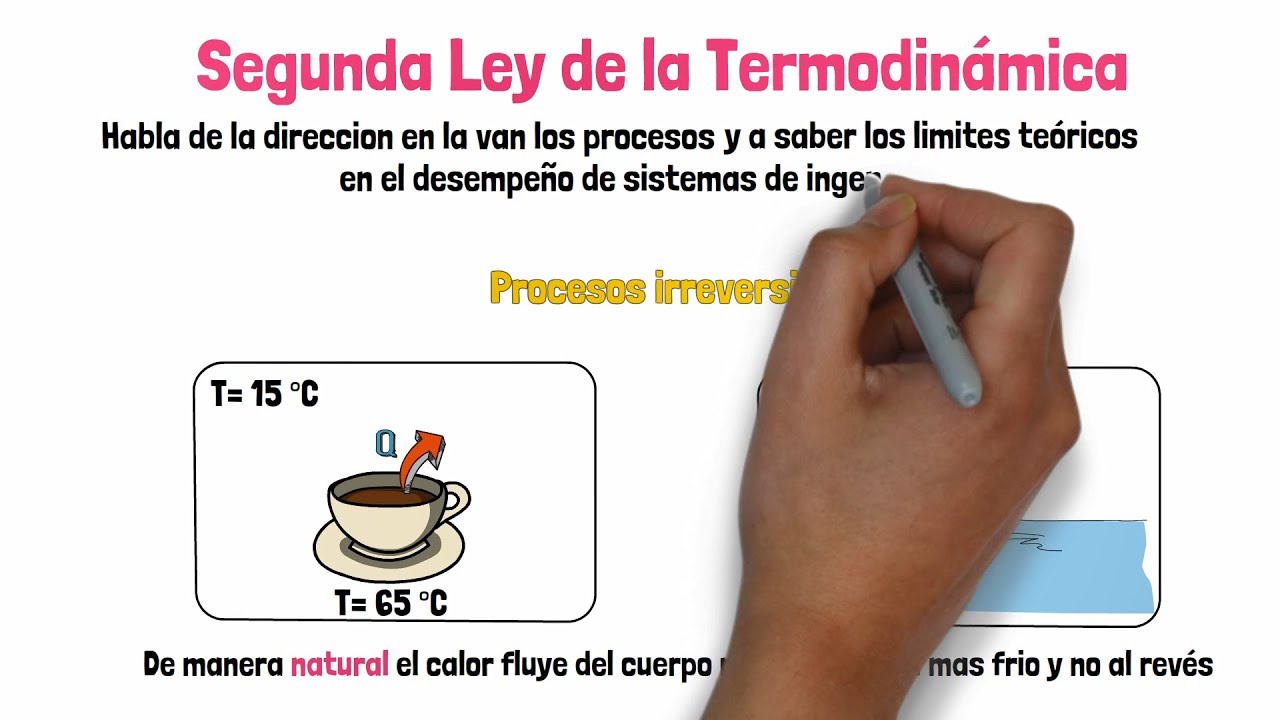
a poder ver si un proceso es reversible o Irreversible es decir por ejemplo un proceso espontáneo como la transferencia de calor es Irreversible lo por lo tanto va a tener esto de aquí que un proceso sea reversible digamos que lo hace un poco más difícil que sea espontáneo No creo que no imposible si no recuerdo mal pero más difícil bueno Y a partir de aquí ya si es donde vamos a empezar a hablar de entropía en la forma clásica Por así decirlo vamos a mancharnos bien las manos Hablando Hablando de ella y después vamos a
hablar de cómo se hace cómo se calcula ya la entropía para para algunos procesos Así que no os lo perdáis


















![👍TERMODINÁMICA. ENTRA y APRENDE TODO sobre LA ENTROPÍA (Parte 1) [👉LO QUE NUNCA TE HAN DICHO]](https://img.youtube.com/vi/0bRUIieLBSc/maxresdefault.jpg)