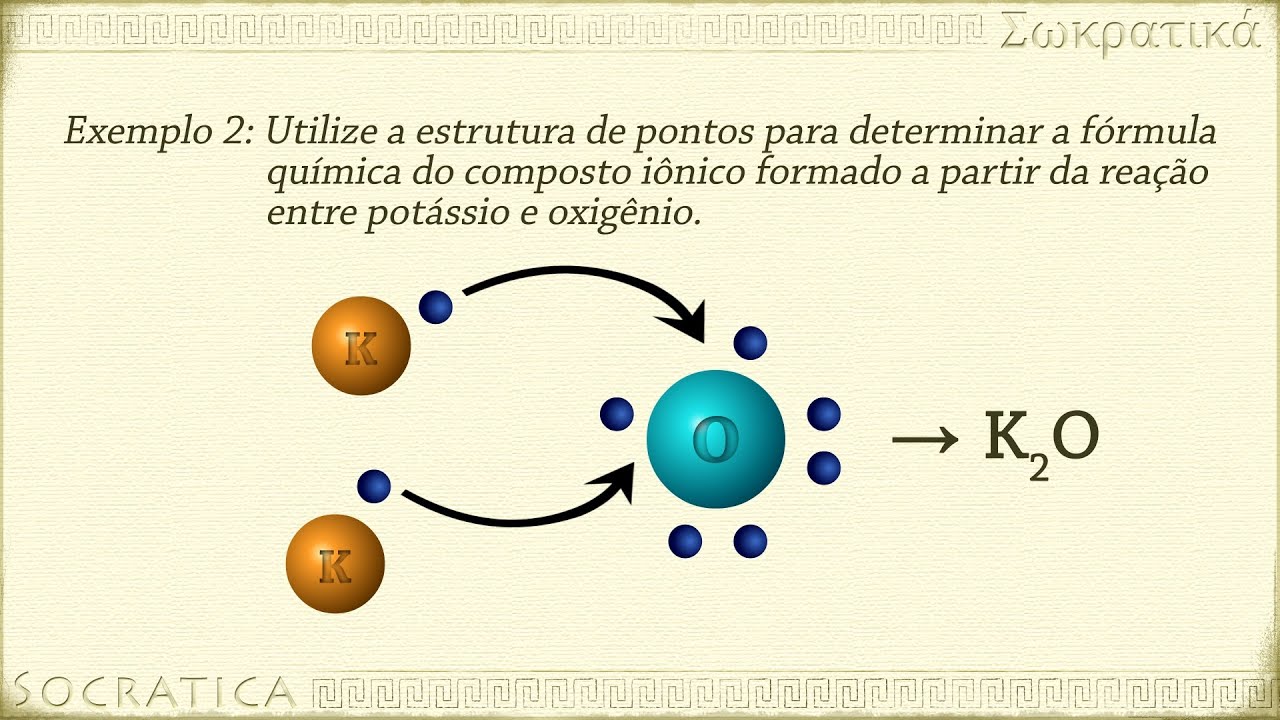
ligação iônica é a ligação que se estabelece entre dois átomos quando há a transferência de elétrons de um para o outro esta transferência se dá quando um átomo forte ou seja de grande eletronegatividade encontra um átomo fraco de baixa eletronegatividade eletronegatividade é a capacidade que um átomo tem de capturar elétrons o átomo que perde elétrons passa a ter carga positiva tornando-se Um íon positivo ou cátion enquanto que o átomo que ganha elétrons passa a ter carga negativa tornando-se Um íon negativo ou ânion como cargas elétricas Opostas se atraem os íons ficam ligados em razão da
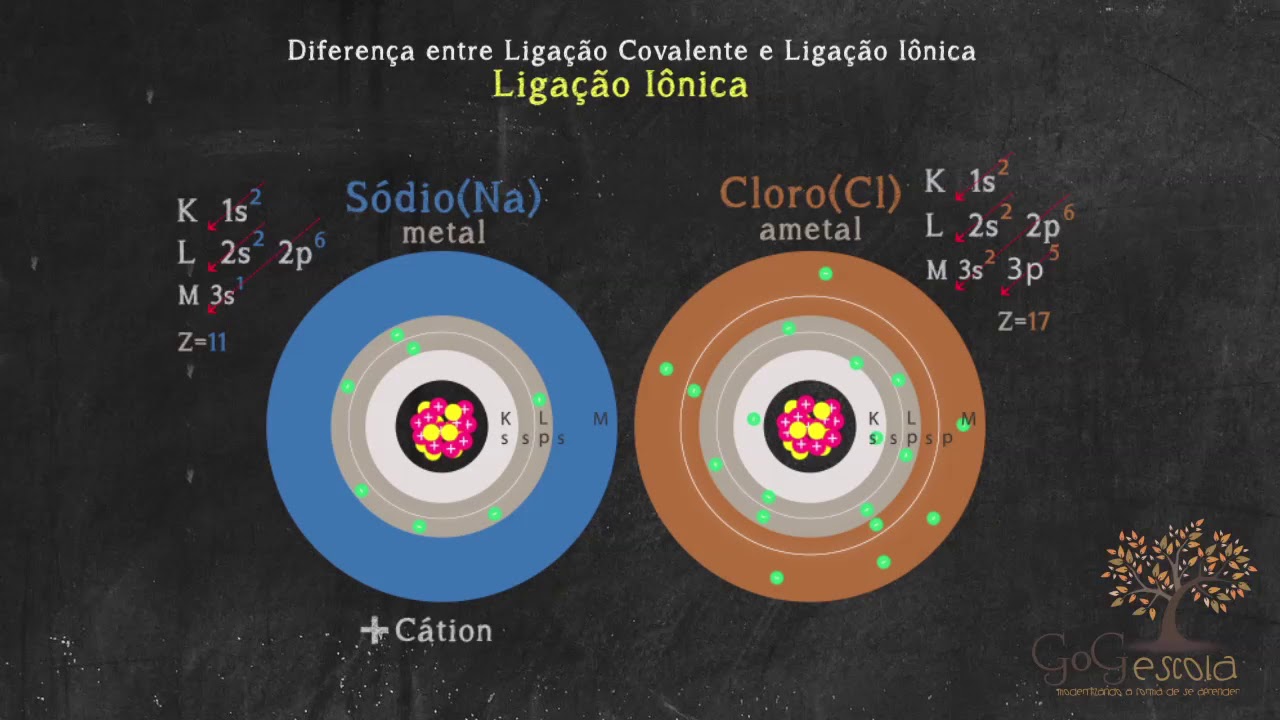
atração elétrica este tipo de ligação recebe o nome de ligação iônica e substâncias resultantes de substâncias iônicas ou sais Como por exemplo o sal de cozinha ou cloreto de sódio composto dos íons de sódio e cloro o átomo de sódio possui 10 nêutrons 11 prótons e 11 elétrons dois na primeira camada oito na segunda e apenas um na a última camada a camada de valência o átomo de cloro possui 18 nêutrons 17 prótons e 17 elétrons sendo dois na primeira camada oito na segunda e sete na camada de valência quando juntos o átomo de sódio
perde um elétron para o átomo de cloro tornando-se carregado positivamente ao passo que o átomo de cloro ao ganhar um elétron se torna carregado negativamente ocorre então a ligação iônica formando o cloreto de sódio