Olá pessoal hoje nós vamos falar então sobre as propriedades anti do baixo dos aminoácidos a gente possa entender então esses conceitos nós vamos fazer uma prega rica população em uma revisão antiácidos e baixas que vocês viram lá ensino médio certo vamos começar com a água a água ela também tem a capacidade de se ionizar olha aqui na equação ela se diz o Cia em uma gamar seu próprio em organismos tá tocando - organismos o hidróxido nós podemos nem expressar essa o seu apito dissociação matematicamente pela constante de equilíbrio mostrar aqui que é constante de equilíbrio
então Qual é a razão entre a concentração esses colchetes aqui indica concentração os produtos o Senhor nunca mais e longamente entendido pela concentração dos reagentes que nesse caso aqui água é tão Travessa constante de equilíbrio nós podemos vamos sair daqui a pouquinho também determinar a força dos ácidos nem das mulheres que serviços É essa a ionização da água é reversível vocês podem ver aqui pela certa duplo sentido é uma um processo Irreversível e ou senão assim então matematicamente resolvermos essa equação da constante de equilíbrio nós temos que a concentração né de água é 55,5 mudar
se a gente encontra pelo cálculo da molaridade vocês lembrarem a molaridade é a massa medido pelo massa molecular desde o volume tanto a gente chega nesse valor é de 55,5 molar o resolvendo né espaço esse daqui para cima multiplicando vai ficar 55,5 vezes a constante de equilíbrio igual a aquela multiplicação da concentração de própria empresa Constituição de em grossos Essa é equação nesse ponto é chamada de produto iônico da água ou kW e continuando então resolver essa equação temos o valor tá pelada que é constante de equilíbrio para a água é 1,8 dessa - 16
a 25 graus estão substituindo esse valor aqui na equação nós vamos ter que produto iônico da água parecer 55,5 é vezes 1,8 10 - 16 vai dar um valor aí de 1 x 10 a -14 é eu aprendi Tô sim reproduz iônico da água é igual concentração de próprio desde a concentração de hidróxido de Freitas ser calor né um 10 a -14 E se eu quiser descobrir aí concentração na água ou dióxido eu posso substituir a equação sabendo que outra lá primeira quais são aqui ó resolver a uma molécula de água nós vamos produzir um
nunca mais e um e um organismo então estequiometricamente um pronto então concentração de pronto vai ser igual classificação de organismos o Ou seja eu substituir aqui ó colocar próton ao invés eu H uma vez que eles têm a mesma concentração a ficar a pagar mais esse drogamais Avenida ainda mais o quadrado o seu substituiu H - aqui tá volta menos beijoca menos que tá larga menos o quadrado não resolvendo cheguei ainda mais ao quadrado = k w vou substituir tirar a raiz emendar um calor e 10 na menos 7f então a concentração de prótons né
ou íons H - na água então embora 10007 a água tem prótons Livres né provam-se sorriso assim como iOS organismo é um bom então é essa concentração é igual anda mais e organismos = 10 ou menos como é muito difícil trabalhar com esses valores negativos né E muito pequeno uma seus deduções matemáticas foram feitas aí muito tempo atrás onde nesse existia calculadoras meus computadores os matemáticos usando a escala logarítmica não tem que trabalhar com seus números negativos né Muito bem o que que é isso então nós vamos tirar né é o logaritmo de dividir pela
concentração de próprios essa concentração de próteses aí nós temos aqui dessa - 7º lugar e se resolveu não acessar passou aqui um acontecendo vocês lembram como resolver logaritmo logaritmo então aqui da divisão vai para cima certo o h mais tô aqui vai para cima aqui temos que colocar um sinal negativo na frente ou seja esse de origem a uma escala chamada de pega agradecer já ouviram falar e te pegar então Esse é o logaritmo de 1 sobre a concentração de prótons né ou menos também blog da concentração de provas a nossa então substituirmos aqui agora
a concentração de prova que a gente conhece né na água é um s10da - 7 a Chegamos no PH da água é então começa tabelinha aqui é possível ver essa transformação de todos os PH sair ó Aí sim né a concentração de próprios aqui ó tá vendo está diminuindo lembro que que 10 não instala negativa 10 a -14 consiga micro está diminuindo o PH está aumentando Então pega vai dizer a 14 a 14 Por que por causa daquele produto iônico da água e vai até 10 - 14 então máximo do PH que nós temos é
ator e a o que a recíproca é verdadeira quanto mais ou H - nos demais ou H - nós temos maior ph1 um toque eu trouxe para vocês né essas figurinhas e vocês terem uma ideia verdade algumas substâncias Então se colocar fico suco de limão refrigerantes coca-cola vinagre vinho vejam que eles têm PH ácidos suco gás vou pegar em torno de dois nosso estômago alemão e neutro nem torno de sete o leite essa lindo nosso sangue as nossas lágrimas água do mar clara do ovo e à medida aqui então apaixonar de prótons vai diminuindo e
joga vai aumentando seus não pega alto substância chamada de básicas e em se encontra aqui até gente né limpadores da base de amônia a base de alvejante não se tocou muito né conhecer como que boa e o nosso corpo trouxe aqui também ó só que o gás como falei isso é ácido taurina é uma faixa grande pode ser até Geralmente as até a geralmente alcalina aa é certa que te ver um machão Isso mesmo o nosso citoplasma das células assim como sangue veja que a faixa de pegada em controlar Dinha muito Estreita vamos ver aqui
muito perigoso dar um super aqui do sangue ganhasse dores eu aumentar em uma loja muito grave a nossa a nossa saúde e lembrando também e a escala de PH como ela está louca rítmica e se duas soluções tiverem pegar itens Por uma unidade Ou seja eu aumentei o pega as duas para três é uma unidade mas a concentração dos próprios né Daniel 10 vezes porque nós estamos trabalhando em escala logarítmica é importante lembrar e os anos esse conceito sair da dissociação da água nós podemos aplicá-las na para ácidos e bases fracos parecido porque a água
se comporta né como as tem uma base fraca vocês lembram também o quê que é o ácido segunda definição de grossa é grohe assistam substâncias que do protão fui bases são substâncias que recebem próprio então o exemplo clássico é que vocês vão encontrar os livros é uma sou cético é um ácido fraco Ele também fez o se então parcialmente desejo sentido das Plastic ele perde para o outro aí tem que mandar mais e que então aqui Will acetato com carga negativa e eu Nós vamos trabalhar sempre dessa maneira é o Astro está pronto o nado
está aqui do seu jeito Nossa Frota e ele perde seu próprio Eliel chamada base conjugado e o prato liberado Nós também podemos escrever a que bastante dente fazer a equação do constante de equilíbrio EA concentração dos produtos dividido pela concentração dos reagentes camisa maneira também podemos fazer cálculo é do pega ficar vou tá aqui bom então temos a constante de equilíbrio e cruzar é chamada de cá eu como nós fizemos propriedade nós podemos tirar organismo daqui também a escala varia de 1 a brincar ou menos logo de k1 a mesma forma nós vamos ver aqui
ó a constante de dissociação e o PK então quanto menor o PK as menores ficar mais forte eu ácido Porque você acha tem uma maior capacidade de se dissociar e perder o seu próprio tá então até mais fraco desculpa basta mais em bom então vou tá aqui quanto menor mas olha eu ácido e maior a sua capacidade de perder o próprio de se dissociar ter dinheiro pros decidi social nessa e eu Nós podemos comparar né diferentes ácidos força desse exaustos então aqui ó fosfórico tem pecado 2,12 enquanto aqui o bicarbonato por exemplo em Pecado 10
acompanhando os dois se fosse cólica muito mais forte do que o O bicarbonato em a outra mais interessante né chama atenção usar SUS eles podem ser monocromáticos ou seja só tem um própria perder por exemplo a sério como assim vai prender aqui em cima e dissociando né Você tá é atrás de conjugar e saindo próprio isso acontece então no pecado e 4.76 nós temos a SUS dipróticos Podem perder dois prótons é um aço carbônico primeiro próprio ele perde aqui no PK de três e 77 o segundo próprio ele perde no teclado 10,2 o e temos
as que são tripróticos ou seja podem PDT es pronto exemplo eu acho que o histórico o primeiro próprio ele bem ácido 2014 e o segundo próprio no pecado 6/86 e o terceiro próprio mais difícil de ser perdido nem sai no teclado 12,1 e descobre mãe no experimento experimento aumente esse valor de pecar mas podemos fazer uma situação e que a titulação nós vamos ser aqui um experimento onde nós vamos colocar não é levar o nosso ácido nós queremos descobrir o que tá fazemos colocar um indicador Universal PH eles indicadora uma molécula que muda a cor
ou forma PH né e nós vamos colocar na bureta que que vai ter então nós estamos aqui em baixo uma ácido nós vamos colocar na bureta uma base cerâmica hidróxido de sódio hidróxido de potássio que tá então neutralizar se acha que nós queremos descobrir o pk e vamos construir um gráfico assim não peixes geralmente colocamos a quantidade de base né organismos que foi adicionada ser pingado aqui a partir da bureta e não é isso colocamos o PH que está sendo medida então determinado aqui não é mais um beijo e no início do experimento né Vamos
esperar já tinha sido um acerto que eu queria o nosso exemplo nós estamos apenas o ácido acético esperado é astro-ph bem baixo nenhum 12 quando a gente começa a pingar Então abre aqui a Brita começa a pingar a base nós temos que pega vai aumentando o esperado também vai aumentando certo Observe que tá chegando um ponto aqui ó que a gente vai pingar base vai colocar aba você vai colocar a mudança de PH não é muito grande não é tão inclinada como aqui vejo que tá na vertical não Gotinha de base vou pegar muda bastante
aqui não nessa taxa em azul não acontece isso já tirei porque E aí lá no final do experimento mesma coisa coloquei um pouquinho de base e pega aumentou rapidamente Então vamos entender se comportamento aqui porque tem esse formato aqui dessa é a concessão desse gráfico né não é uma reta né gráfica fala que viu quase Messi é um beijo neste experimento o que predomina não é Maia é o Astro protonato à medida que eu vou colocando a tarde a base está aqui morrendo e pronto acabou oxilac do ácido acético É nesse ponto Central eu vou
ter uma situação onde a concentração ao sempre que eu tenho colchetes indica concentração O que é concentração do ácido do tornando é igual a concentração da base conjugada em nós temos aqui então um equilíbrio do ácido e da sua base conjugada e no final do experimento é a base Então já foi deslocando o equilíbrio dessa reação para direita eu vou ter apenas a base conjugada aqui né mas o texto protonado no final do experimento e onde que acontece o PK é k exatamente aqui nessa reflexão ficar é igual ao PH onde eu tenho esse equilíbrio
aqui onde eu Ácido é concentração laço é igual a base conjugada eu tenho valor do APK e bom então se vocês observarem nessa faixa azul eu tenho que tinha um valor de pecar mais um O que é quatro e 76 mais 15 76 ou menos um metro e setenta e seis né menos um pega 1376 nessa fecha Azul Observe que esse ácido ele que existe então a adição de base eu tô contando base e não tá modificando o pega essa chamada região de tamponamento ou seja ela resiste a variações de PH quando eu adicionar base
mas também vocês vão ver quando eu adiciono ácido bom então cada gosto fraco Ele vai ter ensaio região onde tamponamento então aqui acompanhando a série que a gente acabou de ter ele vai funcionar como um tampão nos pegar as três e 76 assim 76kg nada mais do que o pegar mais um menos um segundo aqui ó Observe que ele vai funcionar como tampão e cinco 86 a 7 86 o tampão fosfato muito utilizado em Os experimentos né que a gente trabalha com células precisa ter um PH neutro e veja o último aquele amônio ficar em
torno de 9,25 ela funcionaria como um tufão que pegar outro e 25 10 e 20 sim hein um tampão é muito importante nos sistemas biológicos e quase todos os processos dependem do pegar a gente vai vir aqui para os aminoácidos a ir a Constância né que nós queremos não ter um pega constante é de qualquer né em organismo vivo e faz uso desses tampões biológicos é o recapitulando é que tem um tampão então sistemas aquosos e tem minha resistir a mudanças de PH quando são acionados aquele ácido ou base do que que é formado um
tampão geralmente né então tampão consiste geralmente consiste de um ácido fraco e vai ser o doador de prótons e a sua base conjugada o aceptor de prótons é o tampão não O que é feito por um ácido forte somente um ácido fraco e sua base conjugar bom então recapitulando aqui nessa região de tamponamento eu tenho mas tô cético e o meu acetato que a base conjugada quando eu coloco nesse sistema base né a base neutralizada pelo ácido formando água e o pega não muda ou se eu colocar acho no sistema a base conjugada neutralizar esse
ácido também o PH não né então e não nessa região central aqui né onde a concentração do ácido a base conjugada sem iguais a força e tamponamento é máxima é bom então usando a todos esses conceitos que nós acabamos de revisar para eu acho né para água para os ácidos fracos e sua base conjugada nós vamos aplicar esses conceitos para os aminoácidos porque o amigo o hino a ele também pode perder próprio tá ele pode se e e dissociar vamos ver aqui o exemplo ela nina não acha mais simples né onde o rd vamos localizar
o r é um grupamento metil como Alfa carboxila grupamento amina e o hidrogênio que ligaram no cargo não ficar sotando risquinho e da ligação covalente aqui é bom né gente entendeu nessa figura que forma um nós temos um acho totalmente protonado ou seja o próprio da carboxila e próximo a menina estão ligadas isso acontece lá no início do experimento nesse livro tá Observe aqui a o eixo X e Y sem ter tido em relação a figura que eu mostrei que o ácido acético é porque o autor Lisa e colocou a quantidade de base adicionada no
y e o PH no eixo X faz tanto faz a interpretação é mesmo tá aqui no que nós vamos acompanha bom então nós vamos fazer a titulação da lâmina mesma maneira que a gente viu agora para nossa ciático nós vamos colocar a lâmina na guri na Telemar Vamos colocar base lá na bureta e vamos pingar tá aonde ele que a gente vai adicionando a base aumentando aqui eu pegar vai aumentando também o quê que abraço ele vai fazer ela vai fazer com que o aminoácido você disse assim o seu próprio tá o primeiro próprio que
vai ser perdido vai ser mais ácido tá vocês compararem próprio da carboxila e o próximo do Amino qualquer mais rápido é o próprio da carboxila Então é isso aí primeiro ele sair primeiro no peito um no valor de 2,3 quem é Olá hoje nós vamos ser aquela infecção né que ele fica mas estável EA região de tamponamento que o livro marcou que em vermelho tá essa região tamponamento onde a concentração de um eu Ácido é igual a concentração de 2 que seria base conjugado aí você perde aqui isso acontece em campo APK 2,3 não tem
qual pegar aqui a lâmina funcionaria como tampão do pegar um e 3 até três e três por enquanto é e é isso razão continuarmos colocando mais base né o aminoácido aqui na forma dois vai perder o seu segundo próprio tá que agrupamento Amino é uma base vai remover esse pronto tomando água e agora nós temos a forma três totalmente desse protonado Lembrando que esse próprio ligado no carbono alça não sai tá ele é bem estável e esse aqui do do pagamento metil também não foi isso acontece onde no pecado 8 9,11 aqui nesse ponto também
funciona como tampão Então pega 8 e um até dez em uma questão como tampão Aqui nós temos a Arma 2 e a forma Terezinha equilíbrio Então essa seria fama é a Cida e essa seria base conjugada em relação a essa equação aqui chata dois está presa penso a beleza tem então o nome lastro mas simples como ela menina ele é diprótico ele perde dois próprios primeiro toque da carboxila segundo próton do Amino 52 PK PK um sempre da carboxila geralmente aqui no bagulho ácido e o pecado hoje do grupamento amém e funciona como tampão em
duas faixas de PH nesses dois pecados né Mais ou menos um a outra coisa a gente tem que observar a carga a carga do aminoácido Então ela muda conforme o PH nessa primeira forma aqui ela tem uma carga e não positiva evento do grupamento Amino na forma dois Observe que tem uma carga positiva e uma negativa e se anula não tem uma carga final a 0 e na terceira que forma três carga resultante é negativo menos um né Então olha a forma predominante vai depender do PH tá no início experimento no aço tem carga positiva
e no é aqui no meio mas vamos predominar a forma dois e tem carregar líquida zero é chamada de formas wither iônica e esse ponto aqui ó e a carga é zero a chamada de ponto isso elétrico a isoelétrico porque se a gente colocar esse aminoácido no campo elétrico é o pólo positivo e polo negativo ela não esse mesmo assim não vai migrar né porque a carga final é dizer e lá no final do experimento bem comando vai predominar é a forma três o carga negativa E aí a alanina é um grupamento R não é
para não pode não perde seu próprio tá não sei ioniza agora nós temos um outro lá se o glutamato onde eu erro é uma carboxila e se ele pode ser ionizar também então vamos ver aqui ó e vamos identificar as parça reclama Alpha grupamento Amina carboxila hidrogênio e aqui ué ué tenha carboxila a mesma coisa aqui ó PH é concentração de prótons é de base adicionada lá no nossa relação e o as formas a eu coloquei aqui a forma totalmente pronto nada um troca no Amino e próprio nas carboxila certinho Ministro Experimenta né pra mamar
no PK um ela perde o seu próprio mas Ácido é o da carboxila é um perdeu É nesse ponto aqui eu tentar um nós vamos ter equilíbrio em transformar em forma Bia e é região tamponante né do aminoácido hoje não da titulação vai perder seu segundo pronto um para ambiente propondo a mina da carboxila alcoxila é mais rápida Então sai próprio a carboxila aquele documento RNA pkr e Aqui nós temos a forma predominante então querido Dhabi com a ceia né forma bem ser o que é região tamponante e continuarmos ainda mais a titulação nós vamos
perder próton do grupamento a mim no pecadores então nós temos o equilíbrio da forma seca OAB e janta não né E no final experimento afirma Então veja que o glutamato ele tem é uma raça triprótico ele vai poder 3 prótons primeiro daqui a pouco Sila Obrigado meu carbono Alta ou não ficar um depois do a carboxila do r no pkr por último vai perder o próximo do Amino né ligar o meu carbono alça não ficar 2 a Google tá mapa pode funcionar como tampão três regiões tamponantes né em volta do seu pentao É sim volta
do pkr né em volta do pk2 onde o teu ponto isoelétrico aonde que o glutamato tem carga Lula perde a final e olha aqui na figurinha onde que a carga se anula no P carga positiva ou negativa se a no eu nós vamos fazer uma média entre o pecado um e o peito é tá em volta dessa amizade ver aqui ó tentar um mais pkr dividido por 2 né quer a média aritmética legal valor de PH l322 tá se a gente colocar aqui no gráfico mais ou menos 3:22 daria um ponto isoelétrico aqui e é
entre o ficar um e o PK é é da mesma maneira e as cargas né Esqueci de comentar só ressaltando o ministro experimento nós temos o aminoácido com carga positiva né no ponto isoelétrico carga nula no é acima aqui do pkr ele tem carga negativa e no final do experimento perde o segundo terceiro pro Me desculpe também fica com carga negativa então ressaltando aí realmente a importância do PH na carga do aminoácido isso vai refletir lá tá tempo a gente estudar é um É mas esse mas né Como que o PH influencia a velocidade das
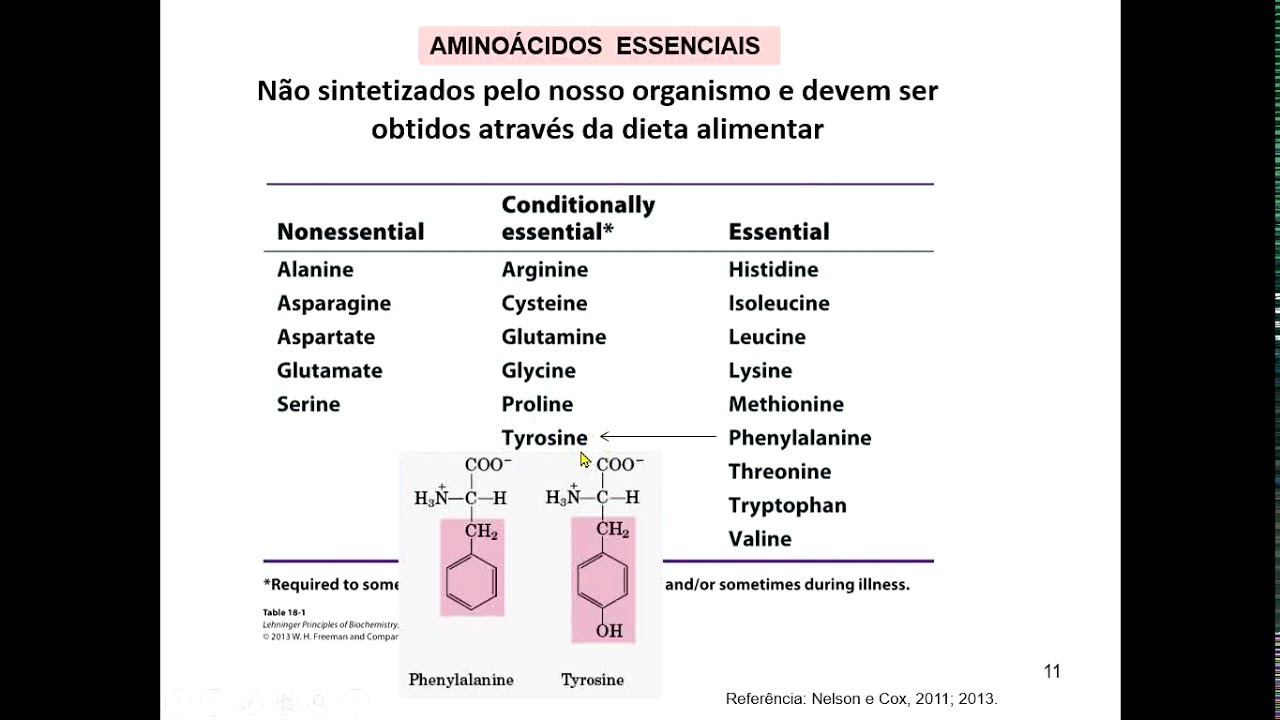
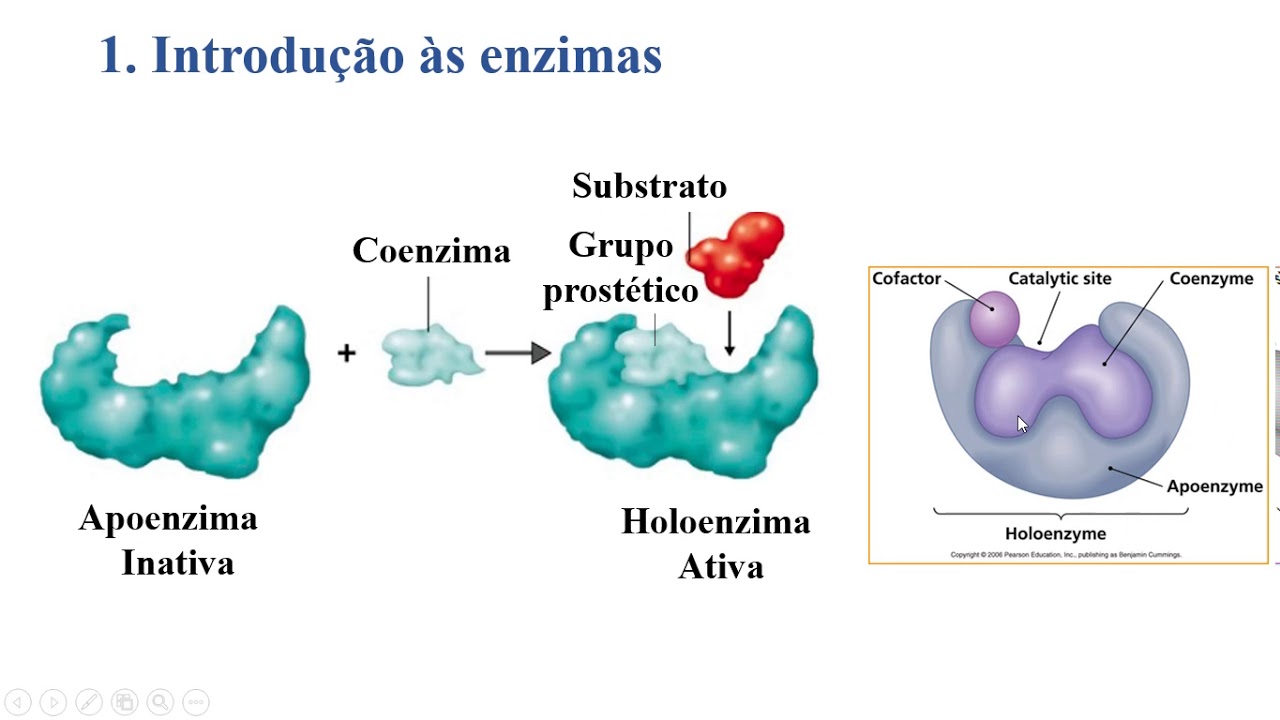
enzimas nós vimos aí que a estrutura tridimensional das proteínas é estabilizada por interações Salinas né ou contas iônicas entre as cargas dos aminoácidos então e já que é importante entender dias para verificar por exemplo que a carboxila que pode tá com carga negativa ou sem carga dependendo do PH Isso vai ser muito importante para a formação ou não das contas Salinas para estabilizar a estrutura tridimensional das proteínas eu mesmo raciocínio que a gente fez para Gruta máquinas vamos fazer para este Dina a diferença aqui é a China tem não É né aprenderam próximo é que
mas agora é meteorologia agrupamento é carregado positivamente meu mesma Pois vamos fazer a titulação vamos aumentando a quantidade de base nos engano o PH para aumentando é o primeiro próprio que sai no pk1 é o que eu para dar carga axila certo não pegar no 82 segundo troca que vai sair é o do R1 aqui em si agrupamento isso acontece no ph6 e terceiro troco que sair do grupamento Amina ligada na no carbono alta isso acontece no pk9 17 também tô incidindo o ácido aminoácido triprótico né perto três próprios três pekas E aí onde eu
compro elétrico diversas Tem que olhar aqui nessas estruturas aonde que eles têm carga final Lula então se você somar aqui em carga positiva duas positivas como negativas ainda da Positiva positivas como negativas e não tô aqui está aquela forma do interior então né fã carga assim não é lula ontem então eu conto elétrico nós vamos fazer a média pkr.com ficar dois ou seja seis mais nova 17 / 2 o ponto isoelétrico está aqui ó em torno de 7:59 é é isso já tá tabelado então para todos animados nós temos aí os valores de ficar ficar
um sempre venceu da carboxila e fica a dois do grupamento Amina um beijo aqui acabou axila bem mais um pegasse rápidos porque justamente é ácido a lâmina acontece entregar as mais básicas veja acima de 8 aí né e o pecado grupamento R varia ideia de ser mais ácido como expectativa Tomate Porque o r é uma carboxila assim como nós é plásticos ou até neutros aqui no caso deste jeito Tá certo um sonho soltando que isso é muito importante novamente né eu entendimento essa aqui é o aminoácido pode mudar a sua carga dependendo do PH no
entendimento então da estrutura tridimensional das proteínas na formação aqui ó das ligações iônicas hum estabiliza a estrutura tridimensional Isso vai ser importante Como comentei para as enzimas por exemplo na velocidade dessas enzimas hoje é só