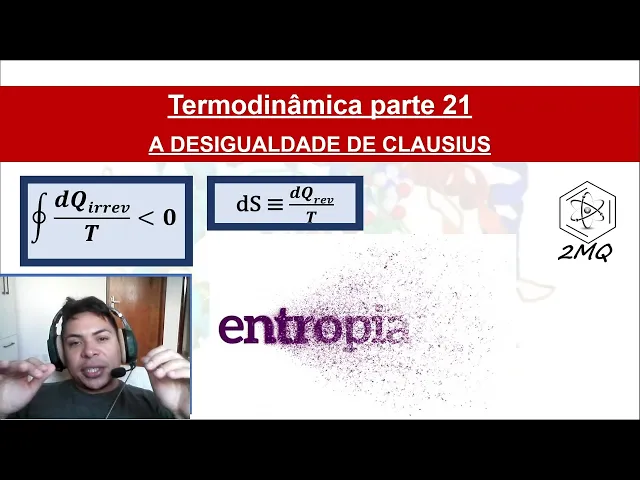
E aí pessoal beleza vamos continuar falando um pouco da nossa série de termodinâmica a gente veio falando esses últimos vídeos sobre entropia e hoje especificamente a gente vai falar um pouco sobre a desigualdade de clausius que a gente vai ter que é um padrão muito muito importante pra gente poder falar de processos espontâneos falar da natureza dos processos suas portunidades e assim por diante beleza mas vamos lá por definições desculpa primeiro considerar um ciclo no qual a sua situação ele vai irreversivelmente ser fechado então está doido tá bom depois a gente vai voltar reversivelmente no
ponto dois até o ponto um Nesse caso a nossa integral cíclica vai ficar assim nossa integral seguida de de que sobre ter vai ficar com uma integral do ponto até o ponto 2 da variação do calor e reversível dividido pela temperatura mas e a integral do ponto 2 até o ponto um da minha do meu calor temperatura isso daí vai ser menor do que zero como eu tive um vídeo anterior né Afinal o que sobre ter reversível é igual a zero mas o de que é possível sobre ter a melhor do que quiser né Beleza
então cedo a integral do ponto inicial até o ponto final do meu calor reversível dividido pela temperatura igual a minha variação da entropia a gente pode escrever assim a integral de um a dois da variação do calor Irreversível dividido pelo temperatura mas a integral do ponto 2 até o ponto um da minha entropia Vai ser menor do que zero tudo bem O curso raciocínio né e tu passo essa minha fração Irreversível para o outro lado eu posso escrever e assim ver também os limites de integração da interessante comentar isso para poder ter tudo mesmo para
na mesma base fazer o seguinte a integral do ponto até o ponto dois na minha variação de entropia vai ser maior do que a integral do Punto 1.2 da minha variação do calor Irreversível dividido pela temperatura se a mudança do Estado um até 12 ela infinitesimal eu posso resumir isso em que a minha variação da entropia será maior do que a variação do calor Irreversível dividido pela temperatura Olha só já tá chegando em alguns valores se algumas situações bem antes é pra gente poder comentar Então olha só essa é a desigualdade de clausius e basicamente
ela é um requisito fundamental para a transformação bom né lembra quando a gente fala tudo pois a falta de informações reais e de ter que devolver a entropia do processo Isso vai ser poder descrever a espontaneidade dele acusar energia liberada e assim por diante tá então essa desigualdade Ela nos permite decidir se alguma transformação ocorrerá ou não na natureza e aí é que tem o seguinte a desigualdade de clausius ela pode ser aplicada diretamente à transformações No sistema isolado porque aí avaliação da do calor reversível então assim a variação da entropia tem que ser maior
do que zero o ou seja entropia do sistema da Peneda aumentar Então olha só a condição pro transformação real e o sistema isolado é que a minha entropia cresça Ou seja que meu e avaliação daquilo que seja positiva ela sempre vai estar crescente Tá bom então a condição de equilíbrio de um sistema isolado é que a entropia atingir o seu valor máximo uma vez que a entropia chega no máximo eu sistemas equilibra e isso traz para gente uma série de observações muito antes tá olha só a forma mais simples que associar entropia é com aquela
cara de organização ou seja sistemas muito realizados eles não são naturais eles tendem a não ser em espontâneos então a tendência natural que não sistema se cada vez mais desorganizado que o aumente a minha entropia É assim nós podemos ver aqui para poder manter um sistema coeso mas o seu mexemos que despender energia gastar energia né mas olha só a observação que eu acho porta aqui em cima de falar isso aqui é o seguinte quando a gente passa para poder dizer assim a condição de Equilíbrio é que a tupia ter um valor máximo isso quer
dizer que nenhuma reação tem rendimento de 100 porcento olha só que eu tenho aqui ó olha esse primeiro quadro esse primeiro recipiente aqui que teria essas moléculas azul azul né azul azul azul azul tudo bem bonitinho Note que é um sistema bem homogêneo bem organizado dessa forma entropia é baixa do meu segundo cachec até mesmo moléculas vermelho vermelho novamente baixa com os dois reais se você quiser então eu vou querer azul e vermelho perfeito para relaxar e vermelha mas Note que todas as moléculas são azul e vermelho entropia é Baixa porque eu tenho um sistema
muito bem homogenizado Todas as moléculas são iguais às interações são as mesmas então é que a natureza faz para poder deixar entropia alta e eu ainda vou ter que a gente no meio então Note que no lugar de ter apenas um tipo de molécula no final eu tenho três eu tenho moléculas azul e vermelho moléculas Azul primeira essa bagunça que a janela aqui dentro dia essa maior entropia nessa maior desorganização tá bom E aí uma coisa que é bem interessante comentar é seus estados de agregação eles têm grau de organização de instinto Então esquece aquele
efeito sobre as distintas também então por exemplo o que é que eu me colega o meio não consegue fornecer energia suficiente a ele para deixar de morar com as coisas então ele derrete as moléculas se afastam se desorganizam E aí eu posso associar-se a tupia os estados físicos olha só e o solo ele tem um sistema muito bem organizado muito bem bonitinho de eu tenho mais uma novidade no líquido ele já é né tiro gasoso elas estão bem espalhados ou seja Note que a entropia de um sólido é menor que a do líquido EA de
um líquido é menor que a de um gás ou seja o sistema gasoso tem a maior entropia precisar os estados físicos comuns beleza e outra coisa eu gosto de lembrar é o seguinte novamente associa entropia só desordens do sistema vai estudar verdade a entropia ela o reflexo da falta de perfeição e o sistema tá imprimi essa daqui é uma das melhores definições que nós temos no qual a hidropsia ela é uma quantidade de energia perdida não mensurável uma máquina térmica Ah tá então pare e se eu colocar tanto de combustível para poder produzir energia térmica
eu devo converter isso em tanto deslocamento que a minha energia mecânica massa No final a conta não bate porque é feito da entropia alguma coisa não foi aproveitada ali no caminho marketing os pés não foi apresentada tá então a desigualdade de clausius tem para poder vai esses essas ajudas que a gente beleza então galera por hoje é isso qualquer dúvida pergunta se eles bota E os comentários espera que vai sair ainda mais vejo termodinâmica gente vai chegar até no pedágio energia de gibbs você Começa outro assunto que causa até a próxima













![O que é entropia? | Segunda lei de termodinâmica [Entropia não é desordem!]](https://img.youtube.com/vi/HhZDZXiEkq8/maxresdefault.jpg)





