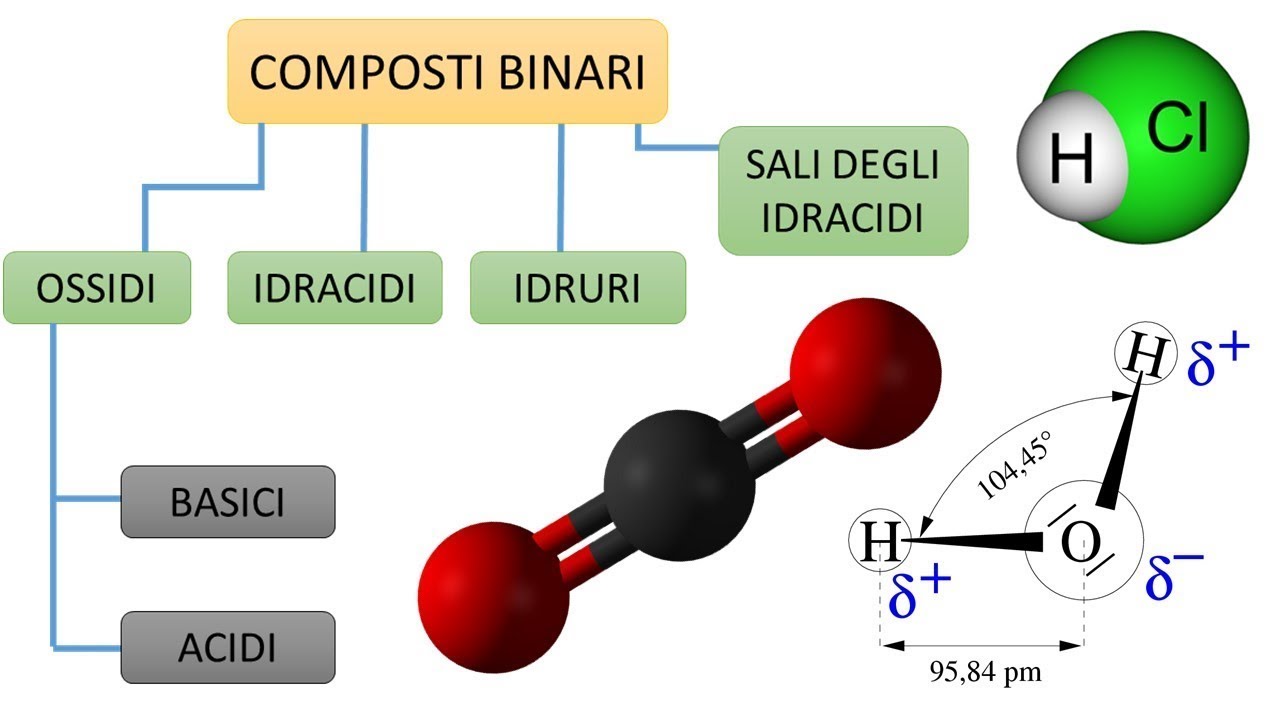
parliamo adesso dei sali i sali sono tutti quei composti che contengono sia un metallo che uno metallo e possono essere di diverso tipo in base al numero di specie chimiche diverse che possono contenere infatti abbiamo i sali binari che contengono solamente in metallo e in metallo un esempio è il cloruro di sodio il classico sale da cucina che mettiamola in serata o sulle patatine fritte poi abbiamo i sali ternari con metallo non metallo e ossigeno ed è il carbonato di calcio è quello che troviamo nelle incrostazioni della doccia oppure nel lavandino perché l'acqua soprattutto qui
a roma enrico di questo sale che poi si deposita nei lavandini o nei rubinetti quando l'acqua sta ferma o che evapora e poi abbiamo i sali quaternari metallo più idrogeno più il nome tallo più ossigeno e ad esempio abbiamo la nhs 4 l'idrogeno sul fatto di sodio in questo caso come vedete abbiamo quattro atomi in specie chimiche diverse che compongono questo sull eco ternario ora li vediamo uno ad uno ma prima vediamo come si possono classificare i sali quando non contengono atomi di idrogeno i sali sono letti neutri quindi quando abbiamo sale binario solamente col
metà leno metallo e sale è neutro se invece abbiamo sali ternario quaternari con gruppi h o gruppi waka sono rispettivamente sali acidi e sali basici si ottiene un sale ogni volta che si fa reagire un ossido acido con un ossido basico ad esempio prendiamo un ossido basico metallo più ossigeno come ad esempio l'olio di calcio è ci ho e lo facciamo reagire con l'acqua otterremo l'idrossido di calcio l'abbiamo già visto nelle slide precedenti se a questo faccio reagire un anidro con l'acqua ad esempio l'anidride carbonica con l'acqua ottengo un aussie acido h 2 o 3
anche questo lo abbiamo già visto nelle sue precedenti quando faccio reagire un idrossido che una base con ossia acido che un acido otterrò in sale se il sale finale conterrà solamente metallo metallo oppure metallo lo metallo più ossigeno il sale sarà neutro otterrò comunque o sale neutro se faccio reggere un idrossido un'idra cido invece avrò tali acidi cossali basici se da queste elezioni otterrà un sale ternario o quaternario dove ci sono atomi di idrogeno o gruppi poste thriller o h esistono poi i sal idrati che hanno molecole d'acqua nella loro struttura interna mentre i sali
doppi misti hanno al loro interno più di un metallo ognuni diversi vedremo questi sali particolari alla fine di questa lezione ma in generale si genera un sale ogni volta che facciamo leggere una sostanza basica con una acida se il sale finale non conterrà atomi di idrogeno o più h sarà neutro altrimenti sarà rispettivamente acido basico parliamo ora dei sali binari sono tutti quei sali costituiti unicamente da due specie chimiche diverse metalli e non metalli ad esempio se faccio leggere l'idrossido di sodio con lascio politico quindi una base con un acido otterrà un sale binario nhl
più l'acqua come prodotto di scarto secondo la nomenclatura iupac si aggiunge la desinenza uno alla radice del nome del metallo e poi il nome dell'altro elemento anche qui si usano i prefissi ci ha visti per numerare gli elementi della molecola ad esempio questo è di cloruro di magnesio ho messo due volte il cloro più uno desinenza dell'elemento non metallico più di magnesio perché questo dico loro forma sale con il magnesio poi abbiamo il solfuro di di potassio stavolta lo zolfo è uno solo quindi noi solo sulfuro di due volte i potassio abbiamo il 3 solfuro
di di ferro e il cloruro di rame come vedete sono tutti quanti sa liminari fatti da un aumentarle 1 metallo sono sali neutri perché non abbiamo né idrogeno nei gruppi o h l'interno questa molecola i sali binari sono sempre sali neutri perché non c'è spazio né per l'idrogeno né per il gruppo h andiamo avanti e vediamo i sali ternari sono tutti quei sali costituiti da tre specie chimiche diverse metalli nome tully così geno facciamo reagire una base nh la soda più uno si acido h no3 e otteniamo enne ha più più no3 meno che reagiscono
abbiamo l'unione metallico positivo quindi il campione e poi lo ione polemico negativo quindi l'unione che reagiscono a formare il sale ternario n an open di nitrato di sodio invece lo stesso l'unipol atomico il nitrato lo faccio reagire con un altro cattivone metallico ad esempio il magnesio otterrò che visto che questo è il 22 questo è meno uno per rendere la molecola neutra verrà fuori mg ennio 33 su due volte ovvero per ogni atomo di magnesio si legano 2 ioni polli atomici negativi no3 meno e anche questo è un sale ternario ovviamente è un sale neutro
anche il sale ternario perché non c'è spazio né per l'idrogeno nel gruppo h vediamo alcuni sali ternari qui abbiamo il suffisso dell'acido da cui provengono o so se il numero distrazione del non metallo basso e ico sei alto e poi il nome del sale da cui derivano quindi ito se il sale deriva da un acido che al numero della situazione del metallo basso ato se sale deriva da un acido che ha il numero di ossidazione del metallo alto i seri ternari si ottengono dall'elezione tra un idrossido ed uno si acido ovvero dalla sostanza basica e
da una cittá vedremo nelle prossime elezioni che cosa significa essere una sostanza acida una sostanza basica quando il numero di selezione è basso l'acido a desinenza uso ed il suo sale it all open ha detto nella tabella mentre quando il numero di ostensione è alto l'acido suffisso i coeso sale a suffisso ato questo concetto è riportato qui nella tabella facciamo alcuni esempi prendiamo ad esempio l'acido h23 l'acido solforoso un nome di upa capaci dott.ri osso solforico quindi lo facciamo reagire con lo ione metallico capione enne ha più e otteniamo la n 23 perché acquisto quando
gli togliamo i due idrogeno diventa s3 con due meno quindi per creare una molecola neutra con s 32 meno e un na1 più devo prendere due soldi per neutralizzare uno ione platonico complesso come s3 meno meno e quindi il nome del sale secondo uk che sarà trio solfato di sodio dove metto il numero 4 in numero romano secondo l'attrice di stoxx per dire che questo zolfo al numero atomico 4 prendiamo invece l'acido per clori co quindi hcl o quattro quindi acido tree of glory con nel caso della mercatura iupac dove mettiamo il numero romano 7
per specificare che cloro al numero atomico pari a 7 e lo faccio leggere con lo stagno 4 più creerà una reazione chimica che in cui lo stagno avrà carica 4 più reagisce con il cl o quattro con la carica uno meno mi servono quattro complessi pauly atomici cielo 4 meno per neutralizzare uno ione 4 più di stagno e quindi abbiamo ass.ne cielo 4 preso quattro volte tetra os sul fatto di stagno dove abbiamo il numero 7 romano per specificare che il cloro a numero della sezione 7 e numero romano 4 accanto allo stagno per specificare
che lo stagno al numero di ossidazione pari a 4 andiamo all'acido fosforico h3 to4 acido tetra osso fosforico nel caso dell'aumento dura iupac e dove metto il 5 in un romano per dire che il fosforo qui al numero di ossidazione pari a 5 lo faccio reagire con lo ione metallico ferro 2 più faccio in minimo comune multiplo tra i numerosi sezione ii è quello del pio iv meno 3 niente titolo tra idrogeno diventa più 43 meno ottengo la molecola f3 con più a 4 preso due volte quindi tre molecole di ferro 2 più ciascuna vengono
terrorizzate con 2 milioni per gli atomici complessi più 4 meno meno meno quindi tre meno ciascuno la molecola verrà chiamata tetra osso fosfato con numero 5 romano per dire che fossero a numerosi azione 5 di ferro 2 loro romano per dire che il ferro a numerose azione 2 quindi tetra osso fosfato di ferro andiamo a vedere gli ultimi due il sito nitroso h no2 acido di osso nitrico con numero 3 romano per dire che qui l'azoto a non lo stazione pari a 3 viene fatto reagire con un rame che al numero esitazione pari a 2
più quindi rcv no2 preso due volte quindi di osso nitrato 3d di ram e 2 dove i numeri romani identificano i numerosi d'azione dei rispettivi atomi infine abbiamo l'acido solforico h2so4 dove si può anche dei chiamare acido tetra osso solforico con numero 6 in un romano per dire che in questo caso il numero 2 situazione dello zolfo è 6 viene fatto reagire con l'alluminio 3 più l'alluminio ha solamente la postazione 3 più quindi non ci possono essere altri tipi di alluminio emilia è una molecola al2 s4 pesa tre volte quindi tetra os solfato 6 si
riesce subentra lo zolfo di alluminio come vedete qui non c'è in un romano perché come già detto l'alluminio ha solamente quel numero di stazione quindi non dobbiamo specificare secondo stoxx quale numero stazione e riferire a questo alluminio perché c'è solamente quello il 3 già così sarebbe giusto però se proprio vogliamo essere precisi e utilizzare lo iupac fino in fondo anche se la nomenclatura di stoxx ci permette di non essere così specifici possiamo anche specificare nel nome i numeri di atomi del metallo per esempio in questo caso trios solfato di b sodio in questo caso non
cambia nulla perché lo stagnino solo qui tetra os fosfato di 3 ferro qui ancora non cambia nulla perché ovviamente c'è solamente un atomo di rame e poi tetra osso solfato di b alluminio perché qui abbiamo due allumini quindi questa sarebbe la rotazione completa compreso di stock e iupac andiamo avanti e parliamo del carbonato di calcio perché è molto importante questo sale perché costituisce gran parte delle montagne anche dell'italia ma in particolare i calcari sono molto diffusi sulla terra sono le rocce sedimentarie e si sciolgono a contatto con l'acqua infatti l'acqua piovana quando cade dal cielo
l'acqua assorbe la co2 e genera l'acido carbonico h23 l'acido carbonico reagisce con il carcare ciaccio 3 formando fenomeni di carsismo ovvero erosione chimica infatti queste cavità le grotte sono scavate dall'acqua che letteralmente ac ficcata grazie all'anidride carbonica dell'area va a sciogliere i calcari detto questo parliamo ora dei savi quaternari sono tutti quei sali costituiti da quattro specie chimiche diverse metalli idrogeno metalli ossigeno si formano nello stesso modo dei sali ternari mata ossia cd che non hanno perso completamente i loro idrogeno come nell'esempio seguente ad esempio h2c o tre è un ossia ci dà ovviamente potrebbe
perdere un idrogeno ma ne ha ancora un altro quindi diventa uno ione pauly atomico acacia 3 meno ho anche io né ossia cito acacia 3 meno questo io non sia c dopo reagire con uno ione positivo un campione quindi ad esempio un sodio e formare nh3 questo la fa diventare una molecola neutra però abbiamo nella sesta molecola un metallo un idrogeno una meta alle 10 è un sadico ternario è anche un sale a cito perché messe in acqua questo potrebbe scindersi rilasciando ioni h più quindi possiamo dire che acide che hanno un diverso numero di
idrogeno possono formare diverse pressioni dello stesso sale quaternario vediamo alcuni esempi che lo possono fare alcuni che non lo possono fare ad esempio la h2so4 all h 2 o 3 ovvero l'acido solforico con l'acido carbonatico possono formare una sola versione di sale quaternario infatti loro possono perdere solamente un idrogeno prima di diventare uno ione senza idrogeno e quindi in entrambi i casi possono entrare o hs 4 meno o hc o tre meno posso legare questi entrambi gli oni con uno ione metallico ad esempio nel primo caso posso negarlo con il potassio e ottenere khs 4
ovvero secondo la nomenclatura iupac idrogeno solfato di potassio e secondo quella tradizionale sul fato faccio di potassio oppure nel caso del lhc o tre meno posso di carlo con il campione metallico magnesio mg2 più e avere la mg con hc3 preso due volte ovvero idrogeno carbonato di macchine sì o o carbonato acido di magnesio nella nomenclatura tradizionale è conosciuto anche come b carbonato di magnesio allora questi acidi mi possono formare solamente una sola versione di sale quaternario ma se invece come l'acido fosforico io ho più di due idrogeno e posso ottenere due tipi diversi di
ioni ovvero hp o quattro meno meno e h24 meno e legarli a loro volta con un occasione metallico e ottenere ii salì diversi il primo na2 hp o 4 e ii n a h24 in questo caso saranno il mondo idrogeno fosfato di sodio e di idrogeno fosfato di sodio o secondo la nomenclatura tradizionale fosfato mono acido di sodio fosfato b acido di sodio quindi vedete com'è possibile formare questi sali che sono salì a c perché se messi in acqua si scindono rilasciando lioni h più vediamo invece adesso quali sono i sali basici ovvero quelli che
messi in acqua si scindono rilasciando ioni o h meno un acido quaternario può presentare una composizione diversa infatti in questi sali l'ossigeno non si lega hanno un metallo ma sotto forma dello strona o gruppo funzionale o h quindi ad esempio possa avere la mg o hcl dove l'ossigeno è presente sotto forma di gruppo funzionale vacca legato con il metallo e abbiamo praticamente l'idrossido cloruro di magnesio quindi mg o h con cl ancora possa avere la lvhm o tre notate che il gruppo funzionale o h è legato al metallo così come lo ione poli atomico negativo
no3 meno meno questo è l'idrossido ritratto di alluminio ancora si può usare anche il termine basico al posto di idrossido ed evidenziare e quindi il loro numero e specificare che questo è un sale basico quindi nhs 4 si può dire come solfato mono basico di sodio oppure linea o h peso due volte cl come cloruro di basico di sodio poi dobbiamo definire anche i sali idrati sono tutti quei saldi che presentano una quantità speech di molecole d'acqua nel loro reticolo cristallino che quindi fa parte della struttura abbiamo ad esempio le nel gesto 4 con 5
molecole d'acqua vuol dire che per ogni molecola di mgs4 sono associate nel suo reticolo cristallino 5 molecole di acqua e poi le 23 con 10 molecole d'acqua il che vuol dire che all'interno della struttura cristallina accesso 10 molecole d'acqua per ogni molecola di n al 23 il primo si chiama tetra osso solfato di magnesio penta ideato con il cristo che per il sol fatto di quattro e per il magnesio di 2 oppure si può anche chiamare come solfato di magnesio penta idrato ancora il secondo si può chiamare di osso carbonato 5 di di sodio deca
idrato oppure carbonato di sodio beck ha ideato e infine abbiamo i sali doppi sono quei sali quaternari dove i due metalli sono legati a un annio nepal e atomico con metallo più ossigeno vediamo due esempi particolari come la dolomite conosciuta così col nome tradizionale ma e c amg cia 3 preso due volte secondo lupa che è carbonato doppio di calcio e magnesio oppure quell'altro minerale conosciuto col nome tradizionale all'unit e con formula k al3 s4 preso due volte con sei gruppi funzionali o h quindi solfato doppio dell'u minio e potassio e zayd rossi le in
questo altro caso il sale doppio è un sale basico perché se messe in acqua rilascia questioni o h meno questo è solamente un estratto della lezione completa sulla hanno mica dura chimica nella lezione completa descriverò tutte le sotto famiglie dei composti inorganici binari ternari e quaternari introdurrò le regole di nomenclatura dello ju pac e vedremo come si potrà dare il nome o composto chimico in modo tradizionale iupac e con la nomenclatura di stoxx inoltre parlerò anche dei numeri di ossidazione degli elementi chimici e di come questi si possono ricavare dalle formule dei composti trovate questo
e tanto altro ancora nella lezione numero 6 del mio corso di chimica facile la nomenclatura chimica sia sul mio canale youtube che sulle mie pagine instagram e facebook prof Antonioi Loiacono grazie