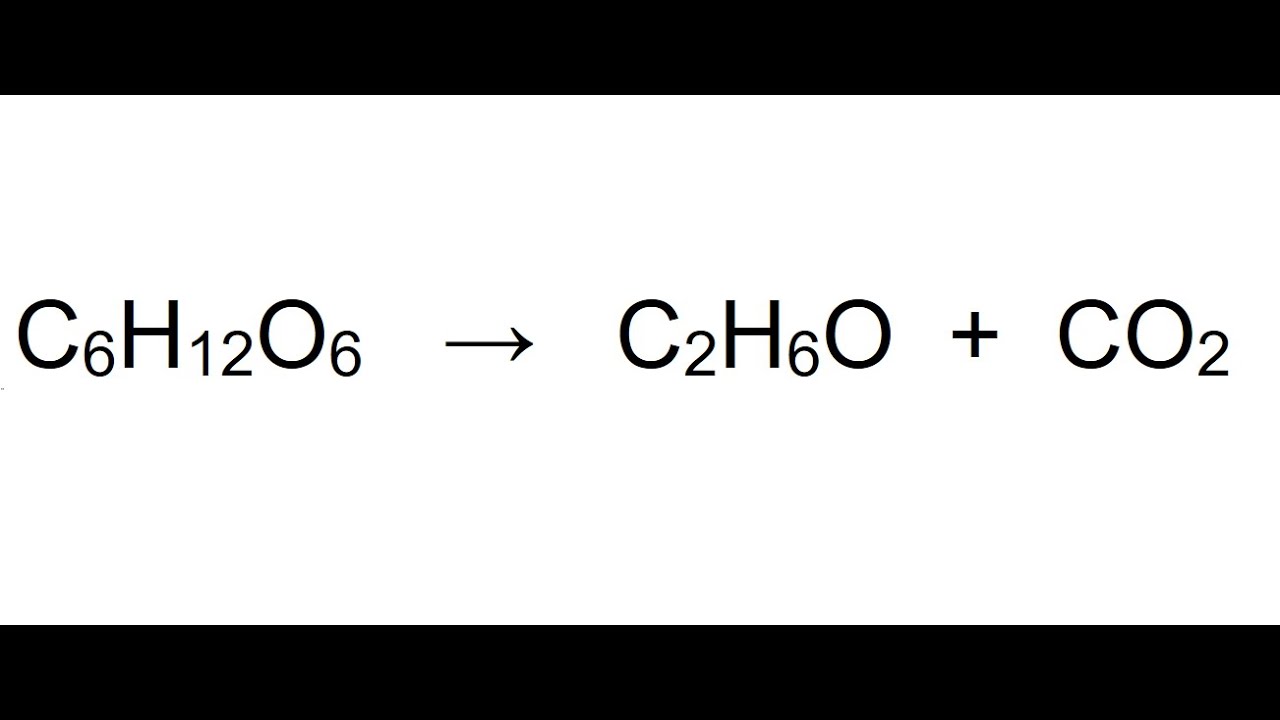Na aula de hoje nós vamos estudar sobre a entalpia padrão de Formação. A entalpia padrão de formação de uma substância pode ser definida como: o calor envolvido na formação de 1 mol de uma substância composta a partir de substâncias simples no estado padrão. Agora vamos relembrar o que são substâncias compostas e as substâncias simples: as substâncias compostas são aquelas formadas por mais de um elemento químico um exemplo é a água, a água formada por dois átomos do elemento hidrogênio e um átomo do elemento oxigênio já substâncias simples são formadas por apenas um elemento químico Esse é o caso, por exemplo, do oxigênio, o gás oxigênio, este gás é formado por dois átomos de um mesmo elemento químico que no caso é o elemento oxigênio.
Outro exemplo é o gás hidrogênio, esse gás é formado por dois átomos de um mesmo elemento químico que no caso é o elemento hidrogênio. Mas e o que é o estado padrão de uma substância? O estado padrão de uma substância nada mais é do que sua forma mais estável quando essa substância está sob pressão de 1 atm e temperatura de 25 graus celsius sendo que todas as substâncias simples na sua forma alotrópica mais estável estão no estado padrão e apresenta entalpia igual a zero.
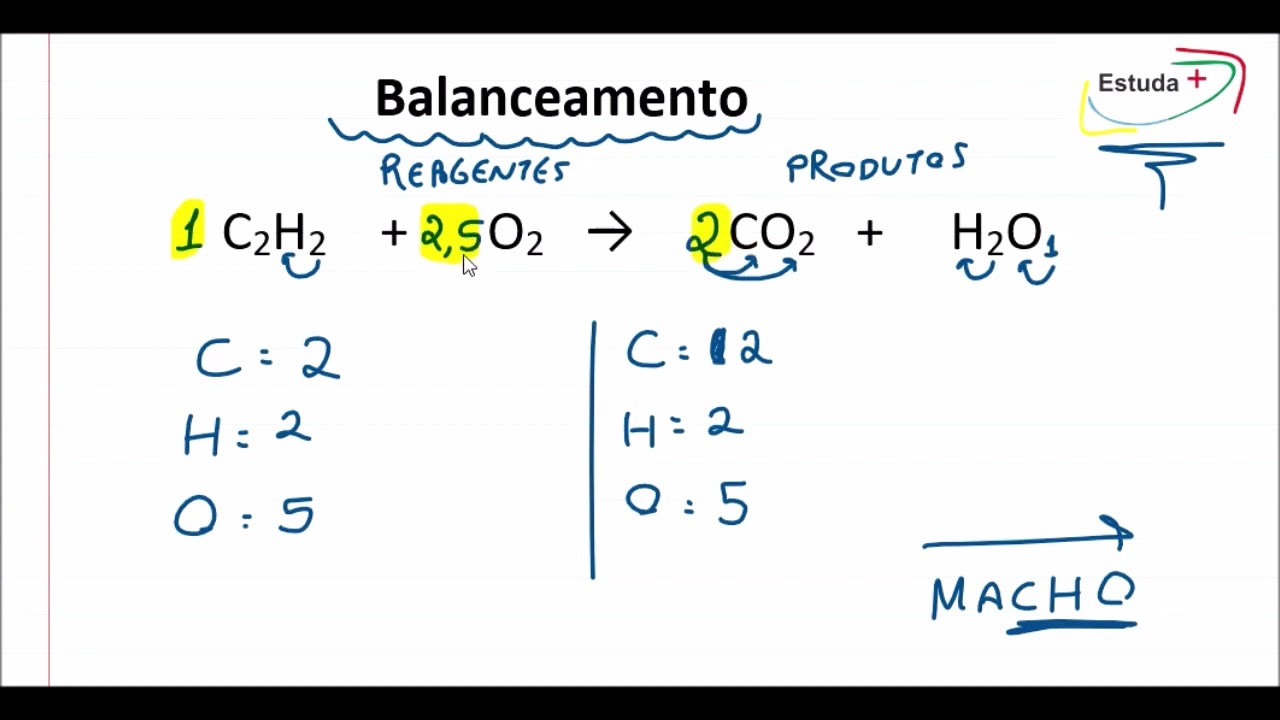
Você deve estar se perguntando Ok e daí ? Bem, Imagine que você esteja no laboratório de química e você faça reação de formação da água líquida a 1 atm e a 25 graus Celsius para isso você faz com que moléculas do gás oxigênio reajam com moléculas do gás hidrogênio e pra facilitar nós temos aqui a equação balanceada dessa reação. Observe que de fato foi realizada a reação de formação da água líquida já que a água é uma substância composta a reação foi efetuada a partir de seus elementos constituintes e a reação ainda foi realizada a 25 graus celsius e a 1 atm.
Com esse experimento você consegue então medir o calor envolvido nesta reação e você encontra então que o delta h de formação da água é de aproximadamente - 286 kJ/mol agora nós já conhecemos a entalpia padrão de formação da água líquida. Mas por que isso é tão importante? Bem, isso é importante pois existe uma equação que esta aqui é o lado que nos permite calcular o delta h de qualquer reação desde que a gente conheça a entalpia padrão de formação de cada um dos reagentes e de cada um dos produtos.
Agora pense comigo, existem muitas reações que tem como reagentes e produtos as mesmas substâncias como a água, gás carbônico, assim a gente não precisa ir para o laboratório para medir o calor envolvido em cada uma das milhares de reações possíveis basta conhecemos a entalpia padrão de Formação dessas substâncias mais comuns. Agora é só você voltar ao laboratório fazer as reações de formação das principais substâncias que nós utilizamos. Na verdade não precisa fazer isso, muitos químicos já fizeram esse trabalho para gente a gente tem várias tabelas aí com valores de entalpia padrão de formação de diversas substâncias.
Agora vamos realizar um exemplo para entendermos como aplicar a entalpia padrão de formação das substâncias no cálculo de delta h das reações. Suponha que você queira calcular o calor envolvido na reação de combustão do butano que no caso é esta aqui e para isto basta consultar-nos a tabela de entalpia de formação para encontrarmos a entalpia de formação de cada um dos compostos envolvidos nessa reação nós vamos encontrar então que a entalpia de formação do CO2 no estado gasoso = - 394 kJ/mol a entalpia de formação da água no estado gasoso = - 242 kJ/mol e a entalpia de formação do butano no estado gasoso = - 125 kJ/mol e para o oxigênio que é uma substância simples nem precisamos olhar nenhuma tabela pois já sabemos que seu valor é igual a zero com esses dados em mãos nós podemos então utilizar a seguinte equação para encontrar o delta h da reação: delta h = soma do delta h de formação dos produtos - a soma do deltaH de formação dos reagentes lembre-se de ficar atento aos coeficientes estequiométricos da equação assim Nós faremos cinco vezes - 242 + 4x - 394 que é a soma dos valores da entalpia dos produtos - a soma dos valores de entalpia dos reagentes E no caso é um vezes menos 125 + 3 e 6 x 0 resolvendo este cálculo nós encontraremos que entalpia de combustão de 1 mol de butano é igual a menos 2661 kJ/mol. Nas nas próximas aulas nós vamos disponibilizar algumas listas de exercícios sobre termoquímica para vocês baixarem que a gente vai resolver juntos.