E aí galerinha do me salva como é que vocês estão nessa aula nós vamos fazer uma introdução sobre pilhas E para isso a gente precisa entender um pouquinho como é que funciona o modelo teórico da pilha certo para isso a gente vai entender como é que funciona uma célula galvânica que é uma célula que existe lá dentro das pilhas e esse modelo teórico um dos modelos teóricos mais utilizados pra gente entender como é que funciona uma pilha na teoria é a pilha de Daniel ou Daniel como vocês quiserem de falar certo o que que a
gente precisa Lar num primeiro momento sobre célula galvânica que nada mais é do que a célula que tem lá dentro da nossa pilha a gente tem que lembrar que dentro de uma célula galvânica o que que acontece acontece uma reação química e essa reação química ela ocorre de forma espontânea essa reação química ela vai fazer com que ocorra ã a transformação de uma energia química proveniente dessa Reação Em uma energia elétrica que a gente chama de I lá na física que nada mais é do que uma corrente elétrica Então dentro de uma célula galvânica de
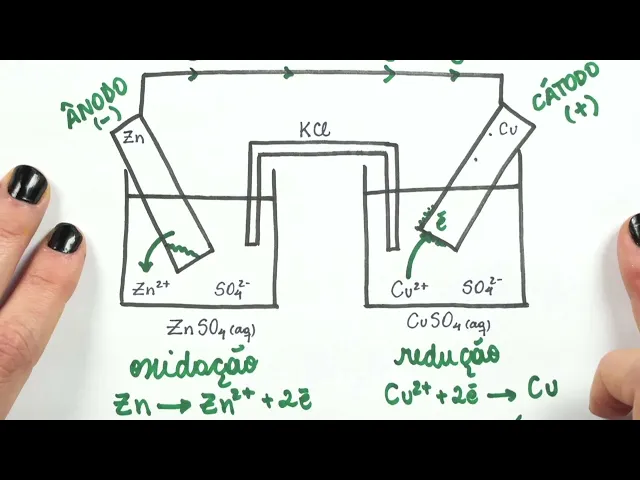
uma pilha nada mais ã a gente tem nada mais do que uma reação química ocorrendo de forma espontânea e essa reação química ela libera uma energia e essa energia vai fazer com que surja então uma corrente elétrica certo bom a gente tem aqui um esquema de como é que funciona uma pilha de Daniel certo e a pilha de Daniel ela é composta assim como qualquer pilha qualquer célula galvânica por dois eletrodos certo no caso da pilha de Daniel a gente tem um eletrodo de zinco e um eletrodo de cobre nós temos um fio por onde
a corrente elétrica vai passar certo nós temos também uma ponte Salina e a gente tem duas soluções contendo íons dissolvidos bom gente eu vou explicar agora cada partezinha da pilha certo que que acontece quando a gente tem dois eletrodos por exemplo de zinco e o de cobre e a gente conecta neles um fio o que que acontece acontece a reação química então que vai induzir a corrente elétrica qual é a reação química que ocorre nessa pilha aqui nessa pilha como o zinco ele tem mais chances de perder elétrons para o cobre do que o contrário
e a gente vai ver mais no fim da aula por quê o zinco então é quem vai liberar os elétrons para o cobre então Portanto o zinco ele tem que est afundado numa solução nesse caso de sulfato de zinco Então essa solução a gente tem ion zinco e a gente tem ion sulfato também e o zinco ele tá na sua forma metálica ou seja nox zero aqui e quando ele perde elétrons o zinco vai perder dois elétrons certo e aí esses elétrons vão passar pelo fio na direção então do eletrodo de cobra Então a gente
tem aqui uma passagem dos elétrons do zinco para o cobre Lembrando que cada zinco perde dois elétrons por isso a gente começa a ver cair na solução cada zinco zero que perder dois elétrons vai se transformar em zinco do mais a gente diz que eh esse processo de perda de elétrons é chamado de oxidação Portanto o que que acontece desse lado a gente tem o zinco zero né virando zinco 2 mais pois perdeu dois elétrons e os dois elétrons que ele perdeu que vão ir então para pro fio ali para gerar corrente elétrica sempre sempre
sempre no eletrodo aonde ocorre a oxidação nós vamos chamar esse eletrodo de ânodo E no caso da pilha dessa célula galvânica o ânodo é sempre o polo negativo e é sempre aonde vai ocorrer a oxidação bom Gente o que que acontece Então os elétrons foram perdidos pelo zinco e eles vão em direção ao outro eletrodo que a gente vai chamar nesse caso de cátodo que é o ã Polo positivo da minha pilha certo quando esses elétrons chegam aqui o cobre que está na sua forma metálica com nox zero ele não quer esses elétrons porém o
cobre do mais que tá em solução que a gente tem aqui uma solução de sulfato de cobre portanto a gente tem solução íons cobre dois mais íons sulfato dois menos esse cobre dois mais ele quer esses elétrons Então à medida que os elétrons vão chegando aqui nesse eletrodo certo então a gente tem elétrons aqui o cobre do mais que está em solução vem e se gruda na placa justamente para pegar esses elétrons E aí o cobre que era do mais quando ele recebe os elétrons a gente diz que o nome desse exesso é redução Afinal
está recebendo cargas negativas né e a reação que está acontecendo ali nada mais nada menos é do que cobre ions cobre ganhando os dois elétrons que vieram justamente do zinco né E se transformando em cobre zero cobre metálico certo e aí esses cobres dois mais eles vão virar cobre Z zero e eles vão começar a ficar aderidos aqui na placa é por isso que no cátodo a gente pode observar um aumento do eletrodo certo porque os ions cobre começam a se grudar aqui e virar cobre dois mais começam a fazer parte da placa então a
gente pode observar um aumento ali da massa da placa assim como eh no ânodo a gente pode observar que a placa o eletrodo ele pode corroer por que que ele pode corroer porque o zinco zero que estava na placa está caindo perdendo elétrons e está caindo na solução virando zinco dois mais então né basicamente no ânodo a gente sempre vai ter a oxidação e ele sempre vai ser o polo negativo na minha pilha E aí a oxidação nada mais é do que a perda de elétrons certo ã Além disso eh no cátodo vai ser aonde
ocorre a redução Lembrando que o ctodo vai ser o meu eletrodo meu Polo positivo e é aonde a gente tem ganho de elétrons certo eh a reação Global dessa minha pilha nada mais vai ser do que eu olhar o zinco né vou olhar nas semirreações a gente diz que essas duas são as semirreações nós utilizamos ela para elas para construir a reação Global a gente vai olhar tudo que tem nos reagentes das duas e reescrever né então no caso e eu tenho zinco mais cobre 2 mais mais dois elétrons certo formando então zinco 2 mais
mais dois elétrons mais o cobre zero e aí a gente pode aqui ó cancelar os elétrons que eles estão dos dois lados e o que sobra é a nossa reação Global portanto a nossa reação Global ela vai ser zinco zero né zinco metálico mais cobre do mais se transformando então em zinco do mais mais cobre zer cobre metálico tá pessoal mas e a ponte Salina para que que serve a ponte Salina a ponte Salina ela serve pra gente conseguir eh fechar o circuito e equilibrar as cargas se a gente for observar desse lado o que
que vai acontecer nessa solução a gente vai ver que ela vai começar a ficar com um excesso de cargas positivas Porque conforme o zinco vai perdendo elétron vai caindo em solução zinco do mais certo então desse lado esquerdo a gente viê um excesso de cargas positivas é por isso que a gente precisa que por exemplo deste eletrólito que é o cloreto de potássio a gente precisa ã que o cloro o ion cloreto na verdade seja ã depositado aqui o CL Men pra gente contrabalancear a as cargas positivas provenientes aí que vão estar em aumentando a
sua concentração por causa da oxidação do zinco certo do outro lado a gente vai observar que a gente vai ter um excesso de cargas negativas mas a que não é porque mais íons sulfatos foram liberados mas sim porque os íons positivos que são os cobre dois mais que estavam em solução eles começam a ficar aderidos na placa então eles começam a ser retirados eh da solução e aí a gente vai ficar com um excesso de cargas negativas portanto do eletrólito aqui do kcl quem vem para esse lado para contrabalancear o excesso de cargas negativas é
o potássio é o k mais que vai então fazer com que a tenha aí é um equilíbrio de cargas é para isso que serve a ponte Salina a ponte Salina geralmente ela é composta por um eletrólito forte que nada mais é do que um sal que se ioniza bastante certo e ela serve então né para fechar o circuito ela fecha o circuito E além disso ela as cargas é importante a gente observar que existem alguns modelos teóricos de pilha que ao invés de ponte Salina entre as duas soluções eles colocam uma membrana semipermeável que também
vai conseguir então ã fazer com que haja um equilíbrio entre as cargas então a gente pode tirar ponte Salina ou entre as soluções uma membrana semipermeável bom gente a além então dos eletrodos além da reação global e da ponte Salina a gente precisa entender também qual é a ddp Ou seja a diferença de potencial ou a fen a força eletromotriz dessa minha pilha E para isso a gente precisa olhar para os potenciais Vocês não precisam decorar potencial porque tanto o Enem quanto as provas de vestibular vão trazer estes valores para vocês geralmente o Enem traz
o potencial de redução certo e a gente pode descobrir pelo potencial de redução a gente pode descobrir o di oxidação porque é o mesmo valor com o sinal contrário Como assim quer dizer o potencial de redução do zinco é - 0,76 v o potencial de oxidação do zinco é mais 0,76 V bom sabendo né o potencial eh dos dois da das duas espécies envolvidas ali na reação de oxirredução do redox ali da minha pilha eu posso calcular a ddp dessa pilha ou a força eletromotriz que é a mesma coisa certo como é que eu calculo
isso bom se eu estou vendo os potencial de redução eu vou calcular com os de redução eu sempre vou pegar o potencial maior menos o potencial menor eu gosto de calcular assim certo portanto se a gente estiver calculando pelo potencial de redução quem é que é o maior aqui o maior é o potencial do cobre é por isso que é o cobre Quem sofre redução potencial de redução maior maior a chance do cobre sofrer redução é ele quem vai se reduzir certo então coloco aqui o potencial maior menos e vejam sempre bom P parênteses para
não errar o sinal menos o potenci de redução menor - 0,76 isso aqui né vai dar um potencial de 1,10 v e é assim que eu calculo o potencial ou a diferença de potencial da minha pilha eu posso calcular também pelo potencial de oxidação que lembrando é o mesmo valor só que com sinal contrário Então o potencial de oxidação do zinco já que o de redução é -07 o de oxidação é mais 0,76 v o potencial de oxidação do cobre por outro lado se o de redução é mais 0,34 o de oxidação é - 0,34
v e agora eu calculo da mesma forma a minha diferença de potencial vai ser o potencial maior menos o potencial menor lembrando se eu tô falando de oxidação eu uso os dois de oxidação eu não posso aqui colocar um de redução e um o outro de oxidação certo então aqui o maior é o + 0,76 e o menor é o menos 0,34 certo e aqui de novo meu potencial tem que dar igual né Afinal é a mesma pilha Lembrando que o resultado da ddp ou da F sempre tem que ser positivo pois a reação que
está ocorrendo ela é sempre espontânea então Se vocês fizerem o cálculo e encontrarem um sinal negativo aí é uma tensão vocês T que dar uma voltad lá e ver aonde vocês estão errando certo eu espero que essa aula ajude vocês a entender um pouquinho melhor a teoria de pilhas e até a próxima