[Música] Olá alunos seja bem-vindo a mais uma aula do curso de química e na aula de hoje nós vamos estudar as pilhas ou as células galvânicas fazendo uma breve retomada do que nós vimos na última aula nós começamos a estudar as reações de óxido redução ou reações redox que são aqueles processos que envolvem transferência de elétrons então a gente definiu alguns conceitos que seriam os vocabulários básicos para descrição dos processos eletroquímicos passando pelo nox que é o número de oxidação que aquele valor que a gente calcula utilizar uma tabela nós temos a oxidação e a
redução que são respectivamente os processos que simbolizam representam perda e ganho de elétrons e os dois últimos conceitos são os conceitos de agente oxidante redutor que são agentes que causam no caso do agente redutor a redução de alguém no agente oxidante causa a oxidação de alguém O que nós vamos fazer agora é retomar a partir do exemplo da fita do magnésio os conceitos mais importantes de um processo eletroquímico Lembrando que eu tenho uma equação química que aqui no caso já é a equação Global eu tenho os valores dos nox calculados para cada espécie E aí
eu faço a ligação entre os elementos que sofrem oxidação e redução nesse caso aqui o magnésio em verde sofreu oxidação oxigênio em laranja sofre redução e essa foi a estratégia utilizada para estudar processos de óxido de redução o Que Nós faremos na aula de hoje é encontrar uma forma experimental de organizar estes processos de forma que em havendo transferência de elétrons eu faço com que esse fluxo de elétrons passe por um fio condutor de forma que eu consigo obter energia elétrica então eu vou usar uma reação de óxido redução para produzir corrente elétrica ou em
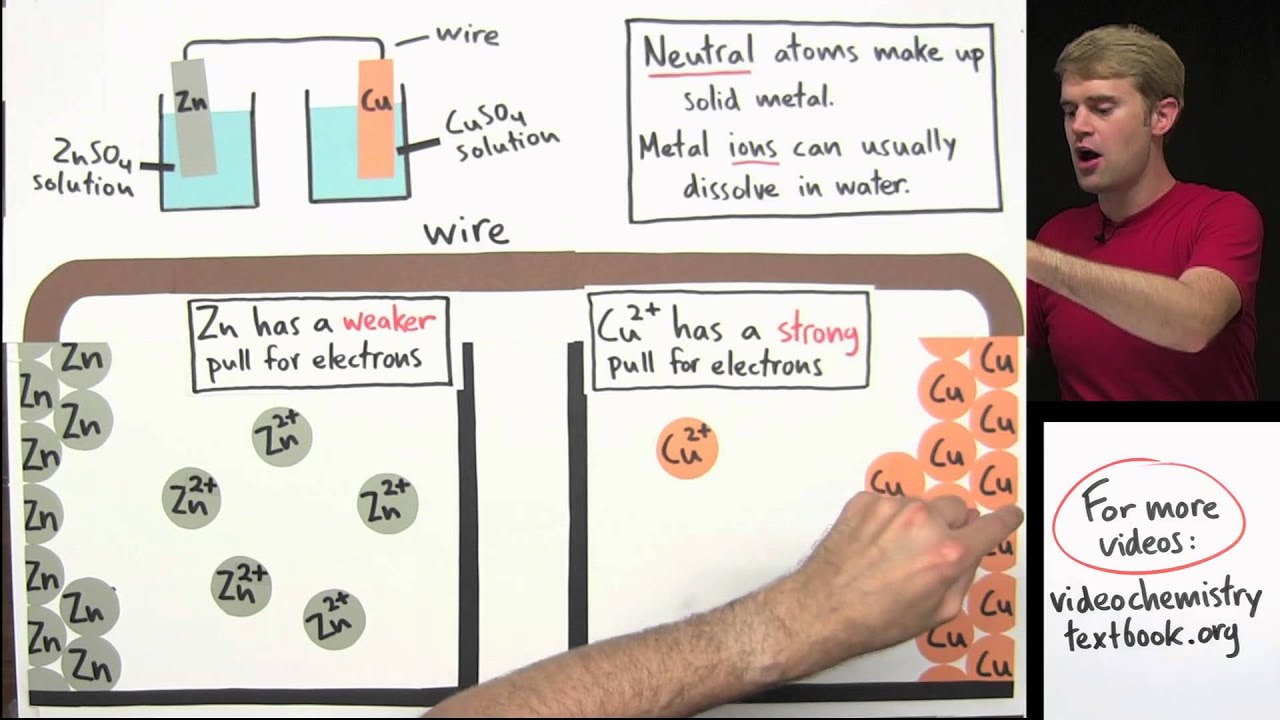
outras palavras eu vou criar uma pilha Então a gente vai ver hoje As convenções que são muito importantes nas pilhas ou nas células eletroquímicas e esse é o nosso foco conceitual da aula de hoje o foco conceitual são as pilhas Então a gente tem aqui nessa imagem um processo que acontece espontaneamente quando eu coloco uma placa de zinco metálico Então você tem uma placa que diz em comentário imersa numa solução de cobre dois mais e uns cobre dois mais nesse caso o sal que foi dissolvido em água é o sulfato de cobre o que acontece
com o tempo se você deixar isso aqui nesse estado por alguns minutos o que você vai perceber é um desbotamento da solução azulada Então veja que aqui o azul já é muito mais claro indicando que os íons cobre dois mais foram consumidos e você vai notar que na Barra acinzentada dos encometálico a formação de uma aglutinação de um outro sólido e na verdade é que é o cobre metálico que tem essa coloração é muito característica por exemplo dos fios de cobre ela não aparece aqui aparece num tom mais escuro por conta da interferência do azul
da solução de sulfato de cobre então é importante perceber que o zinco metálico reage com o cobre dois mais e eu formo cobre metálico e eu de alguma maneira devo produzir exemplo dois mais uma vez que eu tenho que combinar oxidação e redução Vamos tentar entender isso melhor o que acontece com o zinco metálico o que acontece com aquela barra de zinco metálico os encometálico ele se torna zinco dois mais ou seja os incumes metálico que está na barra ele durante este processo que nós vimos ele vai se converter a 52 mais e vai passar
a ficar em solução aquosa ele vai ficar dissolvido na água por isso que eu represento zinco dois mais a que de aquoso isso agora tá dissolvido na água há um aumento do nox o nox Aqui é zero o nox do zinco aqui é mais dois então este aumento do nox sugere que nesse caso zinco sofre oxidação veja que nesse caso é interessante porque a gente ouve falar que os metais sofrem oxidação o ferro sofre oxidação ou corrosão o que acontece na verdade é um desfazelamento você desmancha a estrutura reticular do sólido metálico e forma substâncias
que Ouçam sólidos que ficam em volta no caso da ferrugem ou nesse caso desse experimento um iam incolor que fica dissolvido na água a semi-reação que representa este processo de oxidação pode ser descrita dessa forma os zincos sólido forma zinco 2+ em solução aquosa mais dois elétrons então perceba de novo que não processo de oxidação a perda de elétrons então eu produzo um elétron que aparece aqui no produto e ele aparece aqui porque eu estou falando de uma semi reação então a vantagem da semi reação é tornar Evidente a participação dos elétrons na reação de
transferência de elétrons Então o que a gente tem que ver agora tá se eu já sei o que aconteceu com metálico o que acontece com os íons cobre dois mais que estavam dissolvidos em solução e que conferiram aquele aspecto azulado a solução na verdade no início o que você faz é eu pego uma quantidade do sulfato de cobre sólido então é um sal iônico e eu coloco ele na água e ele se dissolve na água ele não some do mesmo jeito que você dissolve açúcar na água sal de cozinha na água e isso não some
Se você pegar e jogar sal na água a água vai ficar salgada que é o indício de que o sal se dissolveu se ela não desapareceu o mesmo fato acontece com a dissolução do sulfato de cobre sólido que se dissolve na água então você vai ter nessa solução íons 2 mais cobre dois mais e um sulfato 2 menos este aqui de novo sugere que estes íons estão em solução Este é uma solução ou cobre dois mais confere aquela cor azulada que nós vimos no primeiro slide então aqui o que acontece é que durante o tempo
o cobre interagindo com a barra metálica o cobre mais interagindo com a barra metálica permite a formação de cobre metálico que vai se aderindo à própria barra então o cobre 2 mais se converteu em cobre zero o cobre dois mais aquoso que estava em solução se converte a cobre metálico que é aquele sólido que ficou aderido na placa de zinco então aqui eu tenho de dois mais para 0 avaliando o nox eu tenho uma redução do nox o que sugere que o cobre ganhou dois elétrons Portanto o cátion cobre dois mais ou o cátion cobre
2 sofreu redução posso de novo usar uma semi-reação para representar este processo e deixar evidente que neste caso da semi-reação de redução o cobre dois mais interagem com dois elétrons formando cobre metálico então eu de novo vejo como se dá a participação dos elétrons no processo porque eu estou lidando com uma semi reação o que acontece agora é que não há como ocorrer semi reações de forma isolada a gente já disse isso na última aula e se há um processo de transferência de elétrons nós temos que ter sempre a redução acompanhada da oxidação Então o
que ocorre aqui é um acoplamento uma reação global que vai ser obtida a partir da soma da semi reações então eu tenho a semi-reação do zinco o zinco metálico formas 52 + que é incolor com dois elétrons semi-reação de redução do cobre o cobre dois mais que é azulado interagem com dois elétrons formando cobre metálico e agora eu tenho a equação Global somando as duas equações de duas semi reações e aqui nós podemos já definir que os zinco 0 olhando equação Global vai de 0 para mais dois então ele se oxida Portanto ele é o
agente redutor nós temos agora o cobre 2 mais aqui no reagente que se converte a cobre zero o cobre sofre redução Portanto ele é o agente oxidante e esse círculos vermelhos que apareceram agora no nosso slide servem para de novo alertar que ao somar semi reações eu tenho que cancelar os elétrons porque todos os elétrons que serão produzidos na oxidação serão consumidos no processo de redução de forma que eles são intermediários que não precisam ser escritos na equação global bom até agora nós não percebemos muita diferença desta aula para aula anterior foi uma descrição de
um processo eletroquímico que ocorre agora com uma barra de metal e cátions em solução mas essa Sutil diferença é o que me permite agora falar das pilhas Então nós vamos fazer este processo acontecer num outro arranjo experimental eu vou ter dois Beckers eu vou ter duas placas e soluções com seus íons respectivos vou ter um fio ligando as placas metálicas e a ideia que eu tenho é fazer com que o fluxo de elétrons transite por este fio e eu vou ter aqui o que a gente chama de ponto Salina que vai fazer um balanço de
cargas entre os dois recipientes bom então vamos começar a desvendar o que é cada um dos itens que estão numerados aqui de um até seis vamos imaginar que o número um representa a solução de sulfato de cobre ela é azulada Então faz sentido representar este Backer aqui como sulfato de cobre então aqui no número 2 eu tenho a barra do Metal cobre então perceba que neste recipiente eu tenho a espécie reduzida cobre zero e a espécie oxidada cobre dois mais o que eu vou ter no outro recipiente que é este aqui é uma solução de
sulfato de zinco então aqui está dissolvidos em com dois mais e eu tenho uma barra de zinco sólido que é o número 4 então deste lado também eu tenho a espécie reduzida assim com metálico e a espécie oxidada assim com dois mais tem uma solução de sulfato de sódio preenchendo esse tubinho invertido que é a ponte Salina E como eu já Adiantei o número 6 é um fio condutor vamos verificar o que acontece quando eu Uno essas barras com fio condutor nós já verificamos que os incomentálico reage com cobre dois mais o que acontece agora
é que eu separei o cobre dois mais deste lado é esta solução a número um e a barra de zinco que é a número 4 está no outro recipiente ao conectar as barras metálicas com fio nós já sabemos o que vai acontecer o zinco vai sofrer oxidação o cobre vai sofrer redução mas por conta deste arranjo experimental eu vou conseguir fazer o trânsito dos elétrons passar por um fio e eu vou obter corrente elétrica Então vamos ver passo a passo o que vai acontecer os cinco metálico número 4 vai sofrer vai sofrer perdão oxidação Então
os zinco 0 vai passar cinco dois mais e esta solução vai conter cada vez mais cinco dois mais os 5 0 para espaçar a solução 5 2 mais o que acontece é que nesse processo de oxidação a perda de elétrons então a pergunta é para onde irão os elétrons os elétrons percorrem esta barra que conduz eletricidade e vai para o fio e na hora em que ela percorre esse frio ela chega na placa número 2 que é a placa de cobre metálico Então veja que agora eu estou neste outro recipiente e eu começo a ter
elétrons chegando na placa de cobre Então o que vai acontecer desse lado o cobre dois mais que está em solução vai ser reduzido a cobre zero a partir do momento em que eu tenho elétrons chegando nesta placa Então o que acontece aqui é que o organizei o processo eletroquímico de forma aqui os encometálicos se converte a Zinco dois mais e os elétrons que são liberados na oxidação percorrem este fio e chegam esta outra placa E aí nós temos que este recipiente será o Locus da redução então cobre dois mais passa a cobre zero uma vez
que agora eu tenho os elétrons chegando nesta barra com esta organização vai conseguir fazer eu consegui capturar uma corrente elétrica aqui então eu poderia ter por exemplo uma lâmpada aqui essa lâmpada se acenderia esse é o princípio Geral do funcionamento de uma pilha eu faço um processo eletroquímico ocorrer de uma forma organizada De forma que a transferência de elétrons gera uma corrente elétrica um detalhe muito interessante é perceber o seguinte elétron saem desse recipiente então aqui eu vou ter um acúmulo constante de cargas positivas elétrons chegam aqui neste recipiente Então como o passar do tempo
eu vou ter um acúmulo crescente aqui de cargas negativas eu preciso contrabalançar este acúmulo de cargas positivas e de cargas negativas o que entra em cena agora é a solução de sulfato de sódio que está nesse túmulo invertido em um que eu chamo de ponte Salina Então o que vai acontecer é se aqui há um excesso de carga positivas eu vou contra a balançar isso com a migração de cargas negativas quais são as substâncias que eu tenho Quais são os íons que eu tenho na minha solução da ponte Salina sulfato 2 - e sódio 2
mais então o que vai acontecer O sulfato 2 - que está dentro desse tubo vai progressivamente migrar para o Becker para o recipiente que vai ficando positivo porque os elétrons vão sendo perdidos então a carga aqui é contrabalançada o mesmo raciocínio só que de forma oposta é feita com este recipiente o que vai acontecer aqui eu tenho a chegada de elétrons e com o tempo a carga negativa vai se concentrando nesse recipiente como é que eu vou contra a balança a este efeito eu preciso promover a migração de espécies positivas o que eu tenho na
ponte Salina e uns na positivo Então o que vai acontecer aqui é que desta ponte Salina os íons demais vão migrar para o Becker da redução os íons sulfato vão migrar para o Becker da oxidação essa é uma descrição que vale a pena ver mais de uma vez porque com este slide nós guardamos os princípios fundamentais que mostram como um processo eletroquímico um processo de transferência de elétrons pode ser utilizado para produzir uma pilha Ou seja eu vou gerar corrente elétrica a partir de uma reação química que é espontânea uma outra representação dessa mesma pilha
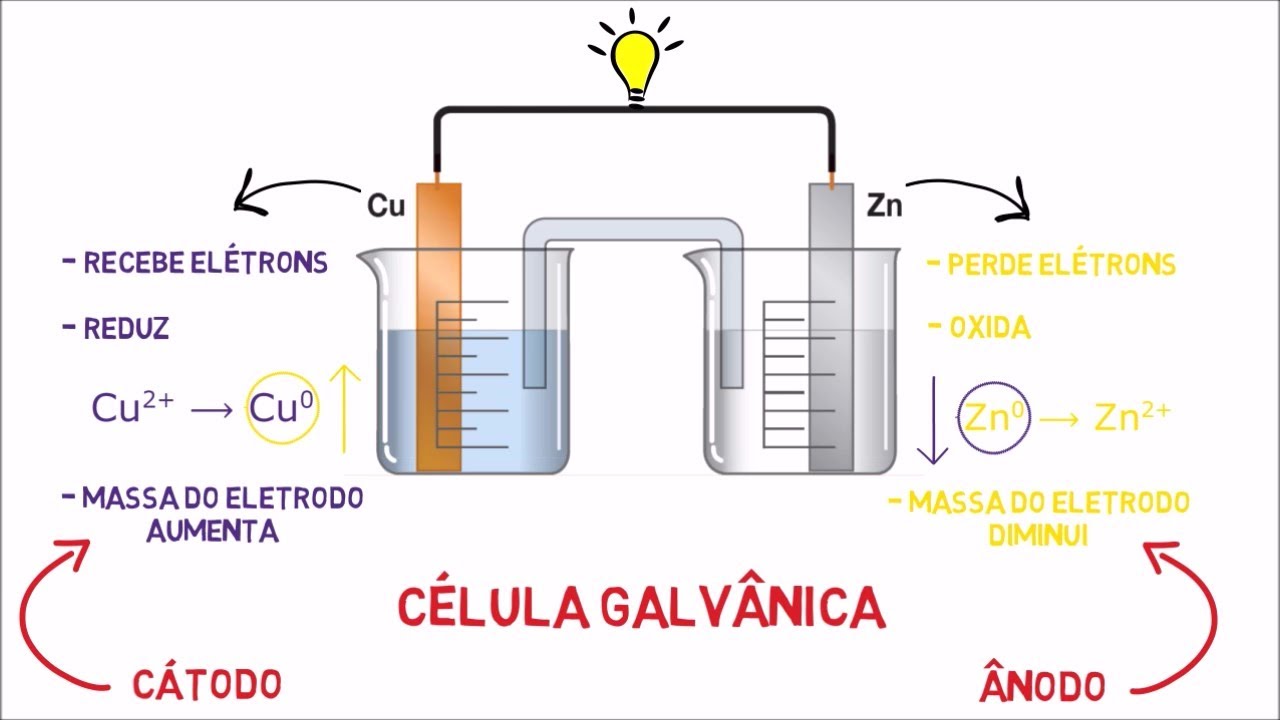
permite a gente agora chamar a atenção para os nomes que aqueles recipientes têm então nós temos aqui e aqui eu chamo a sua atenção que desta figura aqui o zinco está deste lado cobre do outro e essa é o inverso do slide anterior então vamos ver aqui com muita calma o zinco vai ser oxidado e os elétrons vão Então ser gerados aqui chegaram na barra de cobre que vai ser reduzida então o cobre dois mais é reduzido os zinco metálico é oxidado então a gente tem agora duas novas nomenclaturas que é o anodo e o
k todo o anodo é o local onde ocorre a oxidação então aqui o compartimento onde eu tenho zinco e Zinco dois mais é o anodo o cátodo é onde ocorre a redução então cobre com cobre dois mais é o local onde ocorre a então eu vou chamar este recipiente de cátodo então eu posso dizer que a pilha sempre tem um ano do e sempre tem um cátodo que são os polos da pilha e esses polos tem carga Então vamos pensar o seguinte os elétrons saem daqui e chegam até este ponto até este outro recipiente se
os elétrons saem daqui Este é o polo negativo então nós temos que o anodo é negativo onde ocorre a oxidação o cátodo que é onde os elétrons chegam então é uma atração os elétrons chegam aqui Este é o Polo positivo da pilha a gente chama de Cá tudo e sinaliza o local onde ocorre a redução veja aqui nesse caso nós temos uma ponte Salina que nada mais é do que uma barreira porosa Então os íons podem migrar de uma solução para outra para manter o balanço de cargas para terminar esta aula chama atenção para de
novo uma nova representação de todo esse sistema mas agora com duas diferenças que são muito interessantes de serem destacadas na medida em que o zinco vai se oxidando se a gente conseguir olhar microscópicamente o que ocorre nesse ponto da Barra átomos de zinco metálico são convertido a Zinco dois positivo e o zinco 2 positivo fica em solução dissolvido Então essa placa vai se corroendo se a gente olhar depois de algum tempo Olha que interessante essa imagem a barra tinha esta grossura ela se afina porque porque os encometálico que estava no ânodo ele sofreu um processo
de oxidação Então esta placa vai se desmanchando com o tempo e na hora que essa placa acabar a pilha para de funcionar nós temos o oposto acontecendo aqui no catodo os elétrons chegam aqui e ao chegar em perto da Barra metálica de cobre nós temos os íons cobre dois positivo que são reduzidos na superfície da Barra metálica Então você tem um aumento da massa de cobre zero aqui o que acontece é só você olhar o cato do de cobre que tinha essa espessura e ele sofram engrossamento uma vez que durante o funcionamento da pilha você
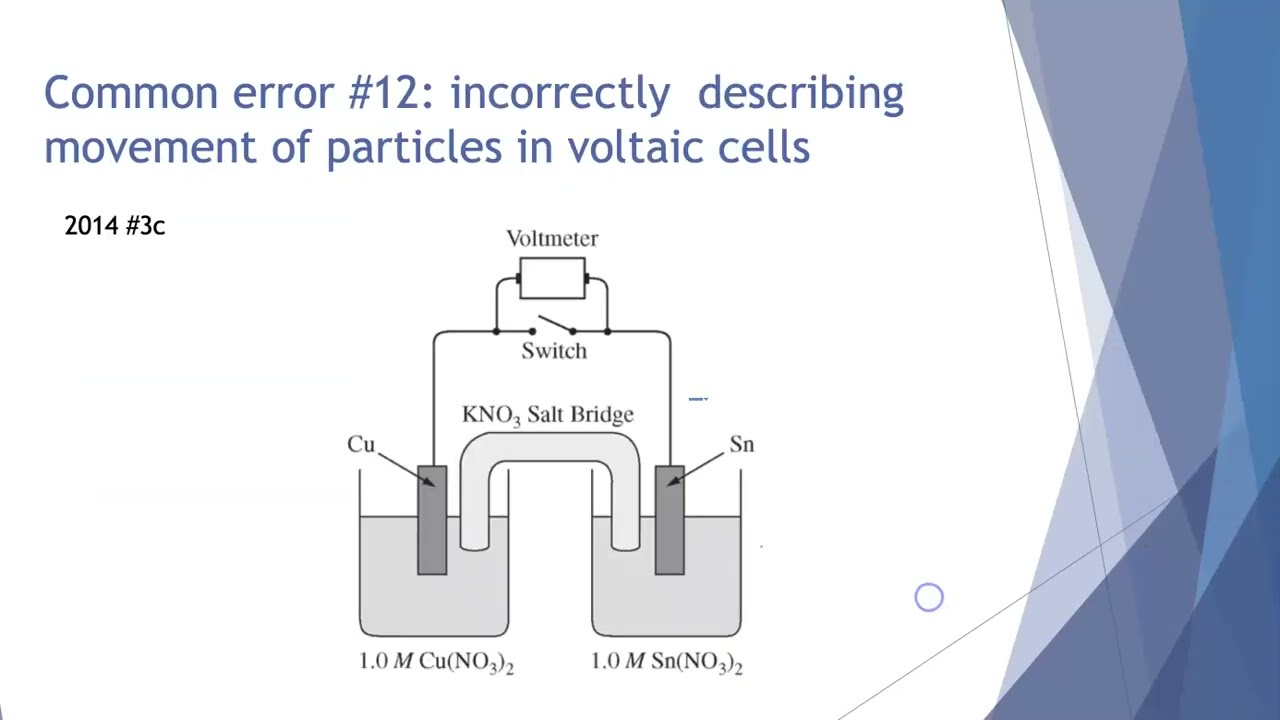
tem a deposição de cobre sobre a superfície do cobre metálico para terminar curiosamente é possível você medir quanto de corrente elétrica está passando por aqui Usando um voltímetro então eu tô medindo a diferença de potencial gerada pela pilha e essa certamente é uma informação importante Quando você vai comprar uma pilha e isso fica para aula que vem ou seja como eu consigo determinar a diferença de potencial entre a substâncias que eu selecionei para formar a minha pilha então variandos constituintes seja do anodo seja do catodo eu consigo produzir potenciais diferentes e aí eu consigo ter
pilhas para as mais diversas finalidades Então por hoje é só nos vemos na próxima aula [Música] [Música]