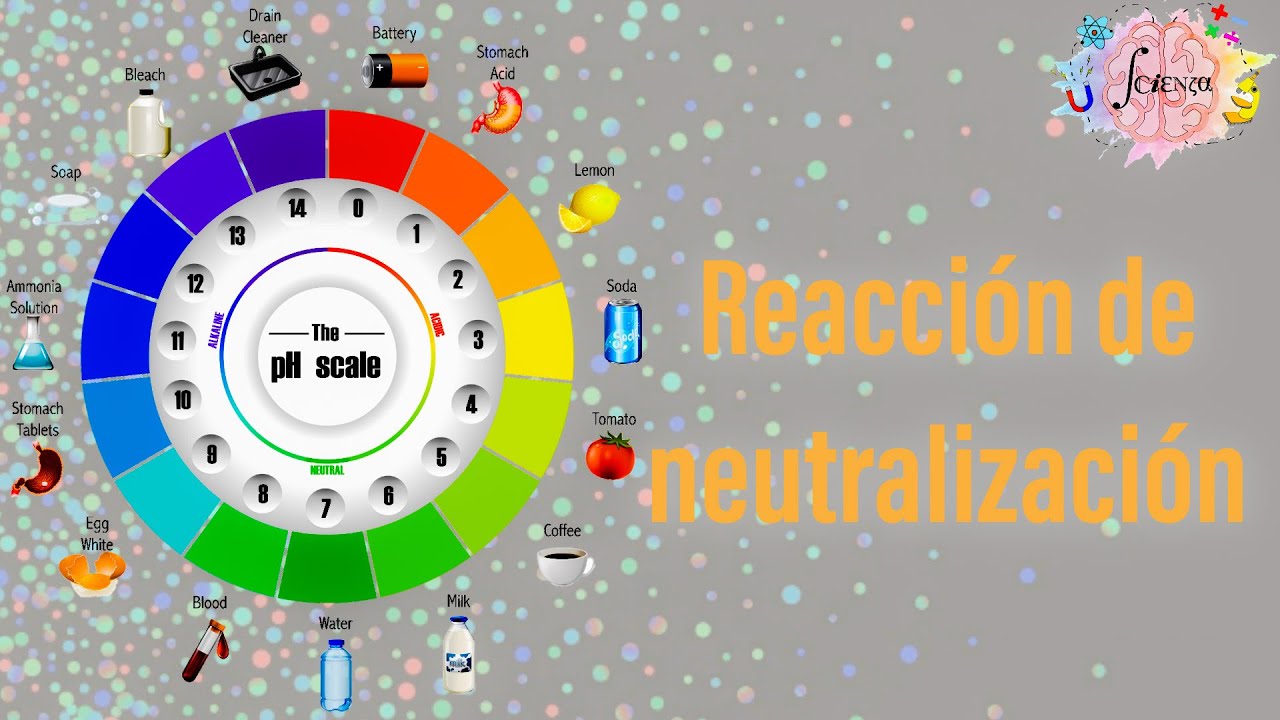
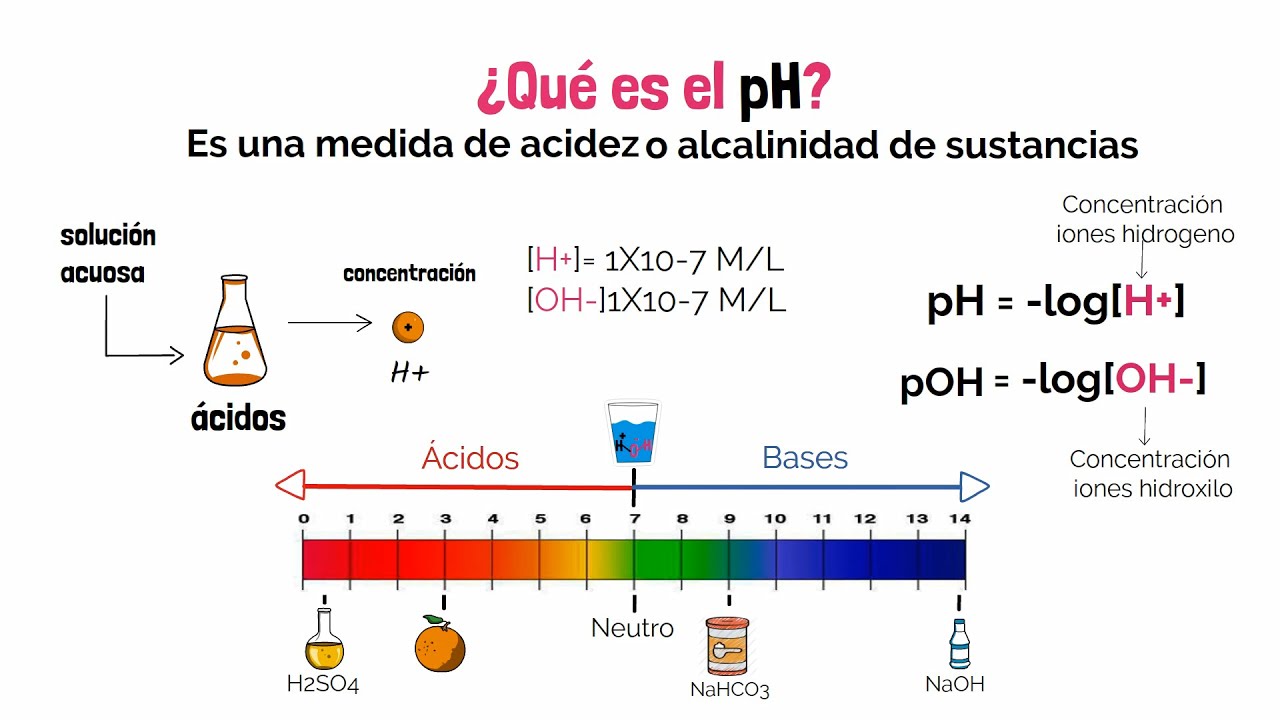
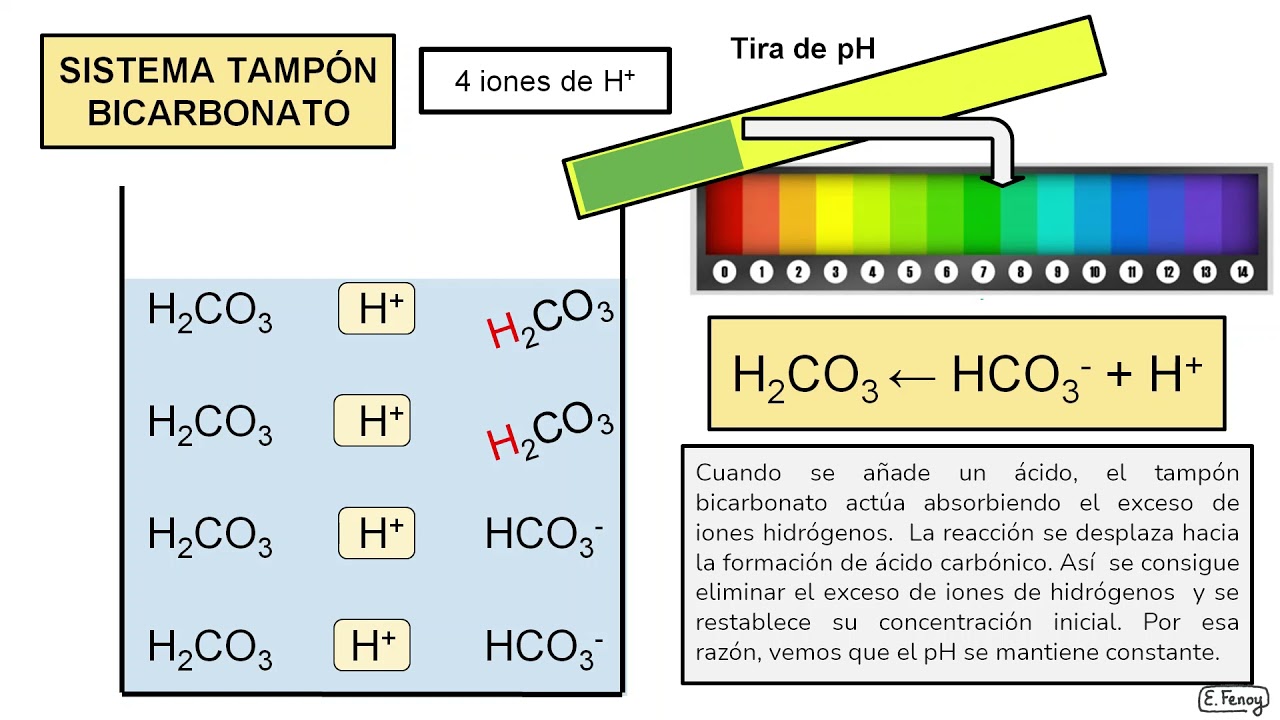
en este vídeo vamos a revisar a las soluciones amortiguadoras sabemos que cuando a una disolución acuosa se le añade una cantidad de ácido o de base su ph se va a ver alterado o modificado por ejemplo al agregar unas gotas de jugo de limón a un vaso con agua esta disolución va a disminuir su ph sin embargo existen ciertas disoluciones que impiden que el ph sufra algún cambio y éstas reciben el nombre de soluciones amortiguadoras este tipo de soluciones también se conocen como soluciones buffer o soluciones tampón y éstas las podemos definir como aquellas soluciones
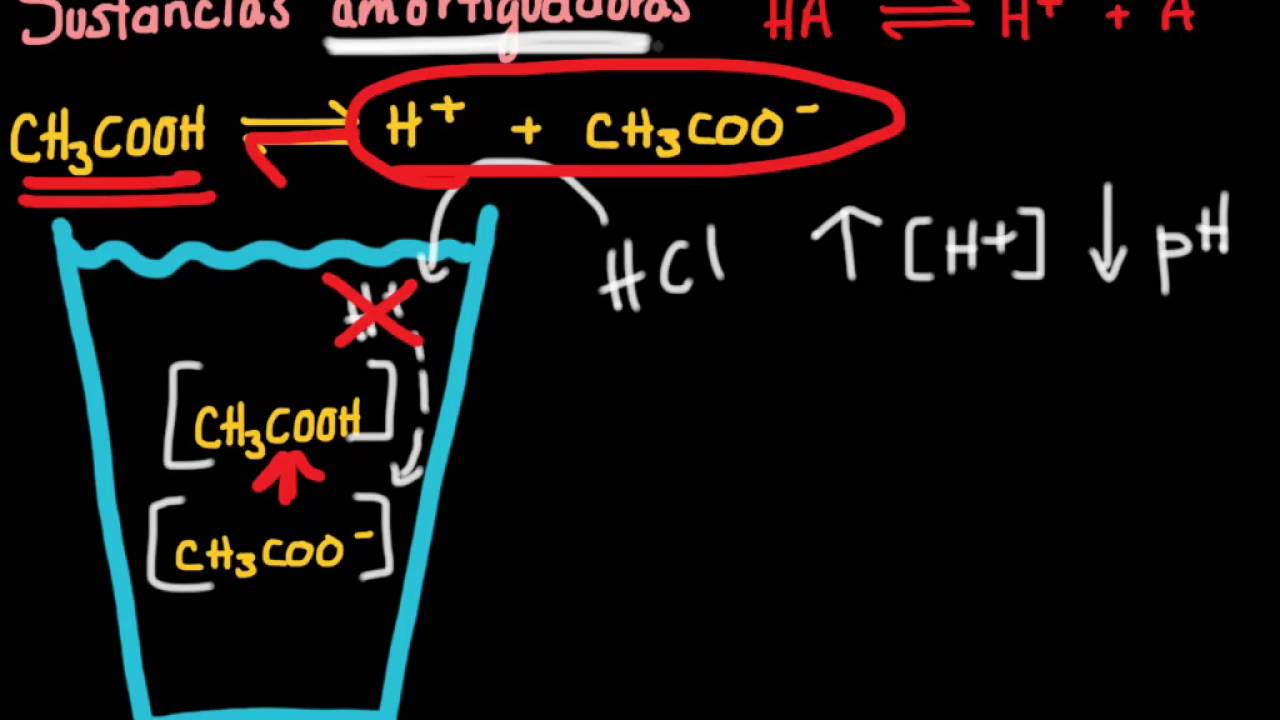
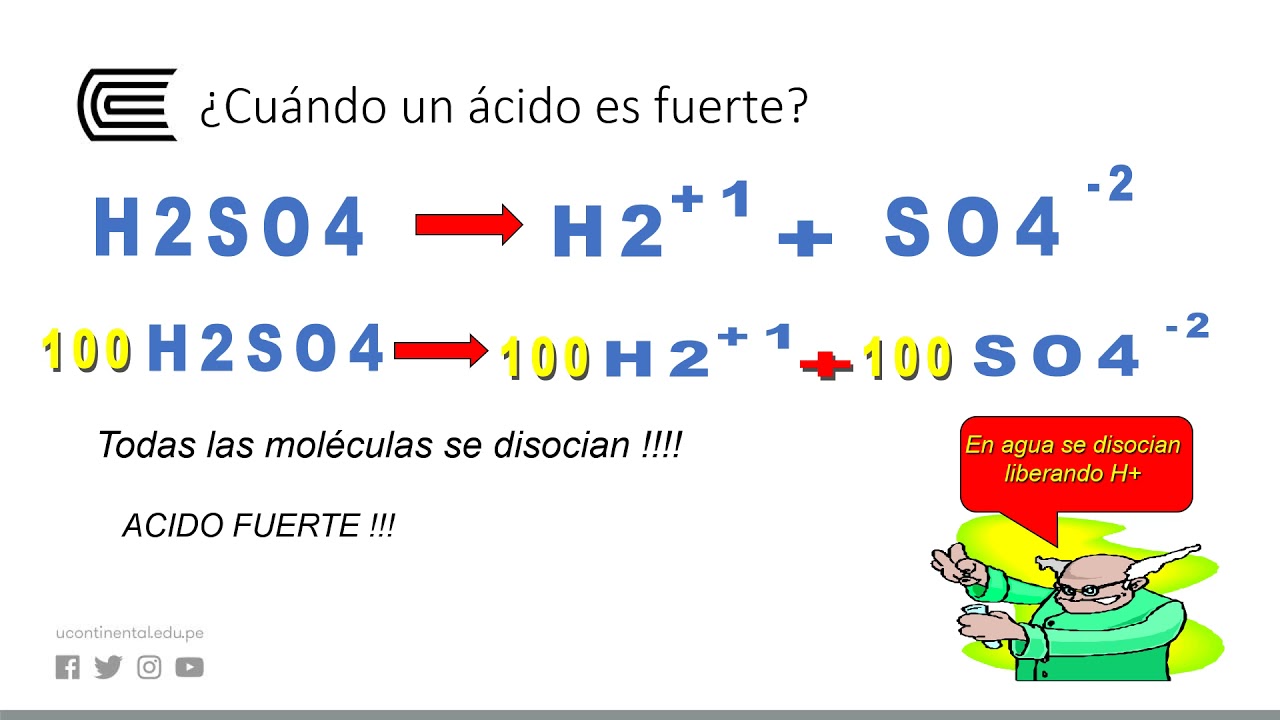
que son capaces de resistir cambios de ph cuando se agregan pequeñas cantidades de un ácido o de una base las soluciones buffer o tampón van a estar formadas por un ácido débil y su base conjugada en forma de sal por ejemplo el par conjugado formado por el ácido acético que es un ácido débil y su base conjugada en forma de sal que sería en este caso el acetato de sodio al observar este par conjugado te puedes dar cuenta que uno de los hidrógenos del ácido débil ha sido sustituido por un metal en este caso el
sodio y así de esta forma tenemos a la base conjugada del ácido en forma de sal o bien también pueden estar formados por una base débil y su ácido conjugado en forma de sal por ejemplo el par conjugado formado por amoniaco que es una base débil y su ácido conjugado en forma de sal que sería en este caso el cloruro de amonio estas disoluciones juegan un papel muy importante no solamente en los laboratorios sino también en la naturaleza ya que gran cantidad de sistemas biológicos requieren mantener un ph constante no olvides darle like a nuestro
vídeo si te ha gustado suscríbete a nuestro canal y síguenos en nuestras redes sociales [Música] i [Música]