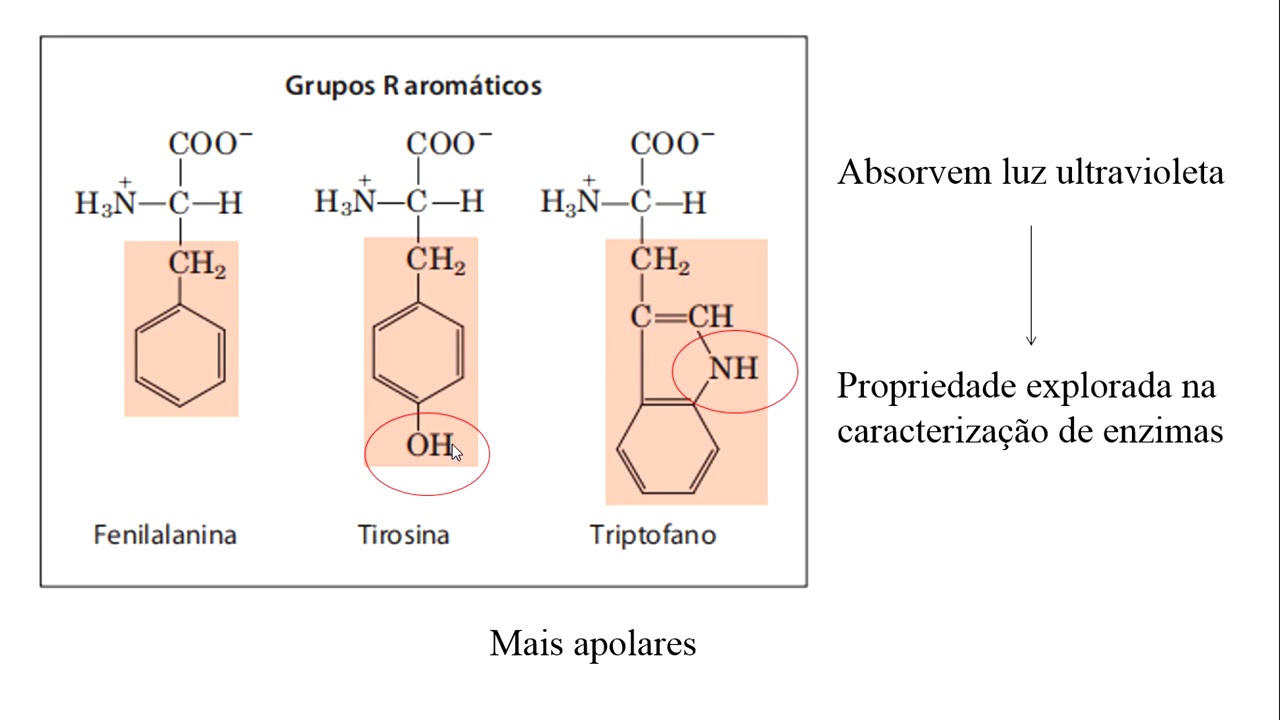
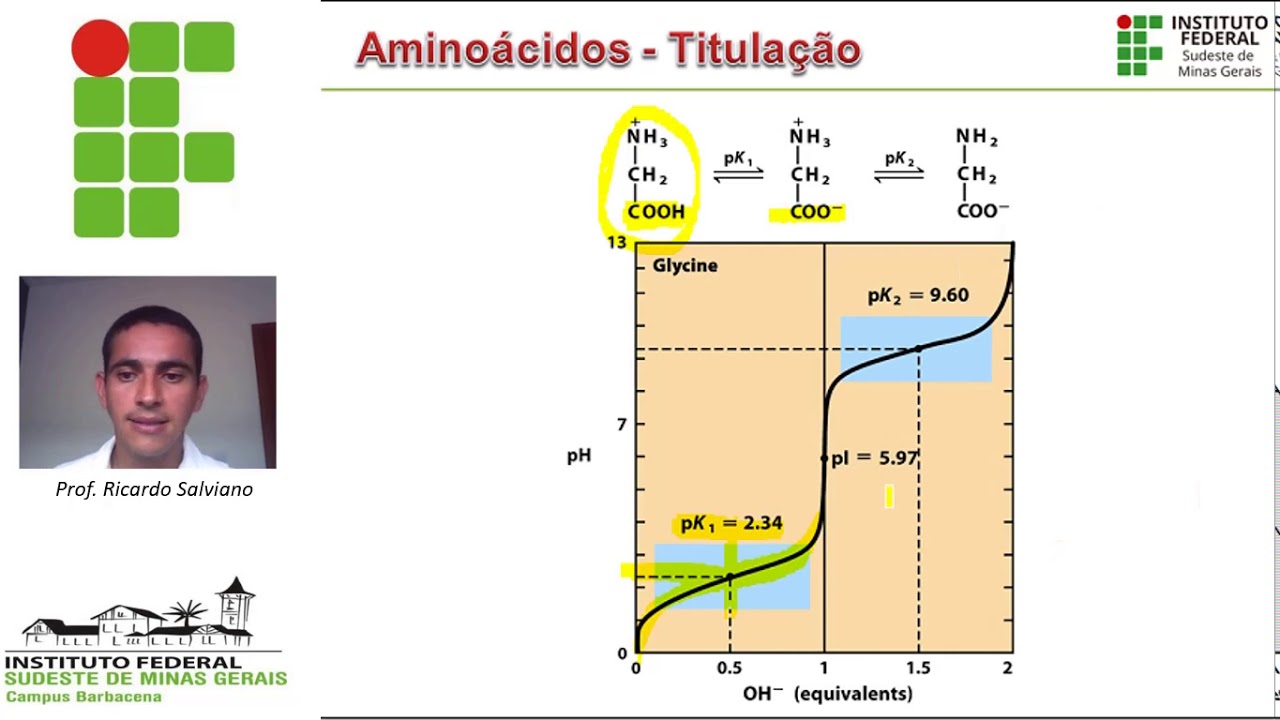
e a ch 005 um estudo diversificados bioquímica aminoácidos e proteínas os objetivos dessa aula são conhecer a estrutura geral dos 20 aminoácidos presentes nas proteínas estudar curvas de titulação para conhecer as propriedades dos aminoácidos conhecer os quatro níveis de organização das proteínas que são estrutura primária estruturas secundária terciária e quaternária o e finalmente estudar duas etapas de purificação de proteínas que é precipitação que sulfato de amônio e filtração em gel e geralmente você ouve na mídia ou teve algum tipo de informação nos ensino médio de que nos seus alimentos encontram-se proteínas estão por exemplo nesse bicho aqui para você tá muito claro evidente que ele é rico em proteínas no leite também o leite ele tem as proteínas do leite que nós utilizamos para nos alimentar assim como os grãos feijão grão-de-bico lentilha fava são grãos que contém proteínas o e as proteínas são constituídas de aminoácidos então daí você vê a relevância de se responder a seguinte pergunta o que são aminoácidos e proteínas e essa estrutura Geral de um aminoácido um aminoácido ele é um carbono Central que a gente vai chamar de carbono Alfa ligado à covalentemente a quatro grupos um hidrogênio um grupo que nós vamos chamar grupo carboxílico de ácido carboxílico um grupo Amino de Amina primária e um radical que diferencia os aminoácidos uns dos outros então se você quer diferencial aminoácido você vai ter que olhar os erres enquanto tudo esse resto está em preto e o carbono Central em azul vai ser igual e os aminoácidos são classificados em tipos existem apolares hidrofóbicos o que que é isso só me nossos que eles têm uma cadeia lateral R que não é solúvel em água o pouco solúvel em água Quem são eles glicina que tem hidrogênio a lâmina que de fato o menor aminoácido hidrofóbico embora glicina também seja considerado hidrofóbico né mas esse daqui você tem que ter um carbono então carbono realmente não tem nenhum interesse de ficar com uma água então ch3 Salinas pode ter que trocar de carbono leucina isoleucina metionina que tem dois ch21 enxofre uns H3 prolina você pode ver que a prolina ela tem aquela estrutura geral né o seu H esse aqui é o r mas olha que interessante o RG dela se fecha no n no Amino terminal e o que terminar acabou se ele fica aqui mas olha olha aqui um dois três carbonos isso hidrofóbico esse laço aqui se ciclo fenil-alanina tem um anel benzênico então metilbenzeno aqui que de fato é bem hidrofóbico eu tô falando que tem esse anel que nós chamamos de anel de indólico indol todos esses aminoácidos não são tão fáceis de dissolver em Água eles são hidrofóbicos que você imagina que uma solução aquosa eles vão tentar fugir da água dado esse nome em existem também os que são polares ou hidrofílicos substâncias polares são aquelas que se dissolvem em água tem afinidade pela água então os animais polares são divididos em três grupos polares sem carga significa isso a cadeia lateral R não tem nem carga positiva nem carga negativa mas é algo polar então por exemplo aqui cisteína tem esse h2s h&s agapo lar treonina o a hidroxila é polar hidroxila da Serena também é polar a treonina é fracamente Pular mas é polar claro que a gente tem uma quantidade de Apolar muito grande aqui é muito parecido porém a lâmina né mas isso aqui consegue uma polaridade ela Glutamina que é uma amido e as páginas que a outra é outra amido Veja a diferença entre asparagina Glutamina são as esses dois carbonos aqui na Glutamina é só um nas páginas polares sem carga Existem os polares como carga negativa que são chamados aminoácidos ácidos Quem são eles aspartato e glutamato cuja diferença basicamente muito parecido com que você viu nossa página e Glutamina o número de ch2 aqui na nossa batata tem um glutamato tem 12 né ele tem um braço mais longo né na cadeia lateral se o grupo carboxílico então são grupos que disputou não em água os aminoácidos polares com carga positiva aminoácidos básicos a questão eles lisina que tem quatro carbonos lineares e uma grupo Amino terminal é os causa minutos mais longos tem de cadeia mais longa arginina que tem essa em mina aqui no terminal e este Dina que tem que a gente chama de anel e me das óleo pode ver que todos eles têm essa carga Positiva em cima do nitrogênio bom Então significa que em água em condições específicas a carga dessa cadeia lateral é positiva em água em condições específicas a carga dessas cadeias laterais aqui dos polares com carga negativa é negativo então esses são os 20 aminoácidos conhecidos existem mais um chamado Selena sistemas a gente não vai detalhar esse daí tá são 21 aminoácidos que existem naturais mas a gente só vai falar desses 20 e se você pegar um béquer e colocar o homem nosso mais simples que tem glicina então talvez nessa estrutura você não consigo visualizar Vou retornar um slide Olha a glicina e esse aqui certo o rd ele é um h então ele está aqui de novo para você o grupo carbono Central né ele vai ter um hidrogênio ou R é uma dá um grupo carboxila e grupo Amino aí eu coloco isso num béquer e adiciona bastante ácido clorídrico quando eu coloco isso o ácido ele vai forçar por tô Nação dos grupos ionizáveis da glicina então eu vou ter protonação no grupo carboxila e classificá-los inico é o hidrogênio está aqui e protonação no grupo Amino então você vê carregar três está com a carga positiva porque eu tenho o hidrogênio protonado aqui e aí o PH dessa solução é muito baixa 0 e Se você começar adicionar quantidades pequenas de base você vai ver que tem um pulo de PH aqui no começo Mas a partir de um dado momento quantidades pequenas de base elas vão alterar muito pouco PH é isso porque atingisse um equilíbrio e esse equilíbrio nesse equilíbrio você tem desprotonação do grupo carboxílico então seu HD pro tornou o bebê ao seu a menos Mais h mais o que que é isso daqui nós Já estudamos é um tampão e pecar um é o PK desse tampão então quando o pH igual a pecar eu tenho um tampão a máxima capacidade tamponante como vimos na aula anterior o Messenger ainda tem grupo Amino protonado se eu continuar adicionando equivalência de base vai chegar uma hora que eu tenho um salto aqui a gente já fala desse ponto até aqui o PH ele resiste novamente a alteração já não pega mais básico isso se deve ao que se deve ao fato de que o meu grupo Amina ele está destronando então eu tenho esse equilíbrio aqui em pecadores então eu tenho aqui a máxima capacidade tamponante nesse segundo pecar um aminoácido Então ele pode ser um tampão pelo menos a glicina né em dois PH diferentes de k1 e K2 2. 34 9. 60 e o que que é esse ponto aqui ó e vamos calcular a carga elétrica total do aminoácido o primeiro a primeira espécie que a gente tinha aqui ele tem carga total mais um basta você ver se eu tenho um sinal de + no o segundo ele tem duas cargas mais um e menos um mas não da mina menos mundo as carboxílicos mais ou menos 10 e o segundo o terceiro desculpa Ele tem carga menos um porque eles pro tô no grupo amino que fica sem carga e só fica com carga negativa no grupo carboxílico e esse ponto aqui ele é chamado.
Isoelétrico e esse é um ponto especial exatamente onde a o número da soma das cargas do aminoácido é igual a serra então por isso que tem esse ponto aqui então eu sei que aqui eu tenho a formação dessa espécies entre os dois equilíbrios e de que uma forma de calcular o pontos elétricos e nos livros eles vão dizer que o p II metade de pk1 spk2 Ok vamos aplicar para ver se tá tudo certo então metade de 2. 34 mas 9. 60 da 5.
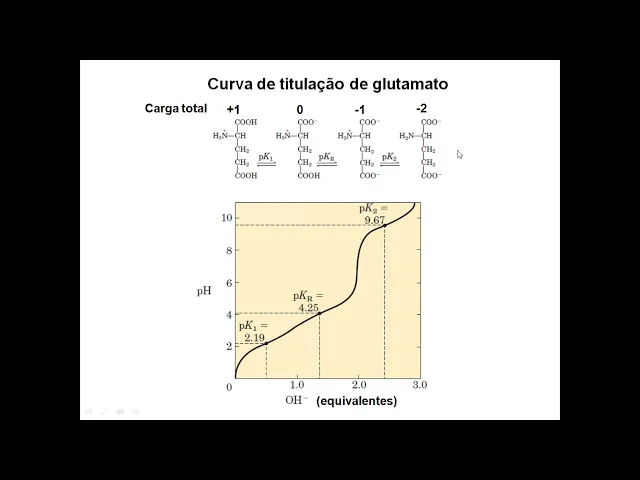
77 e bateu então a gente tá vendo que isso funciona pelo menos para glicina mas a glicina ela não é por exemplo um aminoácido ácido nenhum básico que contém uma cadeia lateral com carga se tem o lateral ele pode se protona desprotonar aí a pergunta é será que isso vale para mim no ácidos com carga Vamos fazer um teste aqui eu tô mostrando para você como eu titulação do glutamato que tem essa estrutura aqui o glutamato não pega mais as possível e ele terá um grupo carboxílico protonado dois e um grupo Amino à medida que eu subo PH fico vai acontecer vai ter o PK um que se deve a o grupo carboxílico não da cadeia lateral né mas da parte constante deles aqui da estrutura ele desprotona então aqui ó esse cara tá protonado e perdeu o próton e esse mantém Esse é o PK um bem Astro 2. 19 se eu continuar adicionando base vai chegar uma hora que eu vou ter a desprotonação do grupo ácido da cadeia lateral isso a gente chama pkr por causa do erre né É real radical resíduos da cadeia lateral radical da cadeia lateral se pro tornou aqui então tenho dois grupos as protonado um grupo Amino ainda protonado e lá não pega a básico que a gente ir aonde esse grupo sa - disputam eu vou ter desprotonação no grupo Amino E aí sim eu tenho somente duas cargas as curvas carboxílicos o grupo Amina está sem carga bom então essa Cruz titulação do glutamato e eu passei por equilíbrio para poder chegar nisso Então sempre que você precisar estudar essas coisas é bom Escrever à mão exatamente como tá aqui para você saber o que que tá acontecendo aí basta contar as cargas né aqui é 00 mais um mais um aqui é menos um mais 10 aqui é menos um com menos um mais um da -1 -1 -1 -2 ok é o ponto elétrico é o PH quando a carga zero pela fórmula né a gente é deveria chegar em três. 22 que é o Pein tabelado para o glutamato nós vamos aplicar bom acho que aqui não tá não tá não tô conseguindo fazer essa forma Então vamos fazer aqui no braço para mostrar para vocês aqui então vamos lá Se eu pegar 9,67 mas que é o pecado certo mas picão 2,19 19 e dividir por dois Esse é o pe Ah então você já desconfia que aquela forma P calma spk2 não está funcionando aí certo não dá para aplicar nesse caso Então qual que é a verdadeira forma não tem fórmula Camila cima se calcula simplesmente memorizando formas O PM né dominação se calcula assim porque você tem que seguir a definição a definição é o PH quando a carga zero então se eu quero calcular esse PH e ele tá no ponto médio de alguma coisa então é sempre assim desenha dissociação de um aminoácido identifique e a espécie de carga zero e tire uma média de pk1 e pecar é exatamente do PH do PK antes e depois da carga zero deixa fazer essa conta aqui para que você veja que essas coisas de fato funcionam Ok então tá aí a calculadora para nós calcularmos então a gente vai ter que somar pk1 2,19 mas pkr 4,25 e / 2 tá lá p e três.
22 então você vê aquela definição lá não é boa Siga essa desenha as estruturas de desprotonação pega a carga Zero Só não pecar antes Dessa espécie um pecado depois dividir por 2 a e na praça que você não precisa calcular nada disso porque todas essas coisas estão tabelados E então basta você ser vice do uso dessa tabela aqui então aqui você tem o nome do aminoácido peço desculpas mas essa tabela que está em inglês né mas a ser útil para você ver aqui o código de três letras abreviações então a menor mas pode ser abreviada por um código de três letras ou por um código de uma letra a massa molecular desses seus moléculas fica um pecador explicar R eo p i tá tudo também lado e aí você veio aqui que por exemplo piscina mas está em inglês abreviatura Green abreviatura internacional da em português você não coloca agrícola i. a. É com Y ou você usa G alanina ala ou a prolina p ou pro Vale naval leucina leucina e tá fácil na menina e o fenil-alanina fenil-alanina não posso como foi escrito inglesa eu não posso usar eu já usei Então vai ser F tirosina bom eu não vou usar ter porque esteja vai ser usado na treonina então tirosina pego Y vem depois de ter daqui triptofano Nossa é muito complicado porque eu esteja foi usado para tirosina o y foi usado para o te para treonina Wilson para tirosina o r vai ser usado para as menina que tá lá na frente então só sobrou usar uma letra não convencional então gente usou o w e por aí vai que você verá nos artigos científicos ou o código de três letras o código de uma letra e aí você tem lá pegar um pecadores pkr e você veio aqui os grupos carregados e se você quiser uma observação boa dessa tabela olha só que interessante olha APK em 222 alguma coisa 122 então mais ou menos isso daí o PK um de todos eles é mais ou menos na ordem de 2 PK 29.
6 10 9.