o Olá meu nome é Patrícia e esse é o segundo vídeo da série sobre estereoquímica nesse vídeo falaremos em maiores detalhes sobre os enantiômeros nós temos no vídeo passado que é diante o números são moléculas quirais que possuem uma relação objeto e imagem no espelho e não se sobrepõe perfeitamente ou seja são lágrimas diferentes Apesar de parecerem muito uma com outro vimos como exemplo o 2-bromobutano que por possuir um centro estereogênico o carbono que está marcado com asterisco vermelho é canal sendo quiral ele pode existir como um par de enantiômeros um é imagem do outro
no espelho mas são moléculas diferentes cada composto aquiral pode ter somente um ano de Homero Pois existe somente uma imagem sua no espelho e aqui nesse desenho em que temos o espelho no meio dos dois à noite ou menos as moléculas estão representadas uma de frente para outra mas também podemos desenhar aulas Uma de lado para outra dessa forma nós temos que a cadeia carbônica está no plano da tela e um dos enantiômeros possui uma cunha preenchida ligada ao Cromo indicando que o Bruno está para frente da tela mais próximo a você observador e quanto
o hidrogênio que está subentendido está para trás já o outro possui o centro estereogênico invertido em relação ao primeiro o Bruno está ligado através de uma coisa tracejada indicando que o Bruno está para trás da tela o mais distante de você observador com isso o hidrogênio que está subentendido deve ficar para frente e de qualquer forma desenhando um anti ombro de frente para o outro ou um de lado para o outro usual é que tenhamos duas ligações no plano no exemplo das moléculas desenhadas Uma de lado para outro nós temos a ligação com etílico a
metila no plano que só cadeia carbônica e duas ligações fora do plano sendo que um dos grupos fica para frente e o outro para trás do plano nesse exemplo bromo hidrogênio estão para frente ou para trás do plano dependendo do enantiômero de do qual estamos falando e observando agora os modelos moleculares um de frente para o outro conforme a imagem de uma de uma grande número no espelho nós temos que as mentiras estão para frente os bromus voltados para si acetilas lá para trás se virarmos jogando a cadeia carbônica para o plano igualzinho desenho lateral
nós temos uma noite o grupo grupo para trás e um com o bromo para frente igual a essa imagem que vemos então deles desenhados lado e para então que a cadeia carbônica está no plano tanto no modelo molecular quanto no desenho A etila está para o lado esquerdo a metila para o lado direito e o que varia Então dessa forma que está sendo colocado um modelo que está sendo desenhado é que uma noite obra tem o Bruno para trás e o hidrogênio para frente e o outro universo o outro ponto importante que devemos Celebrar aqui
e não te ombros apesar de serem parecidos um com outro são moléculas diferentes com configurações diferentes para transformar um enantiômero no outro precisamos fazer uma reação química ou seja deve envolver quebra de ligação a outra forma de desenhar enantiômeros é a chamada Projeção de Fischer nesse caso o carbono estereogênico é representado como um ponto de intersecção de duas linhas perpendiculares as linhas horizontais representam as ligações para frente do plano da terra e Oi Yasmim linhas verticais as ligações para trás do plano da tela ou para trás do plano do papel e geralmente a cadeia carbônica
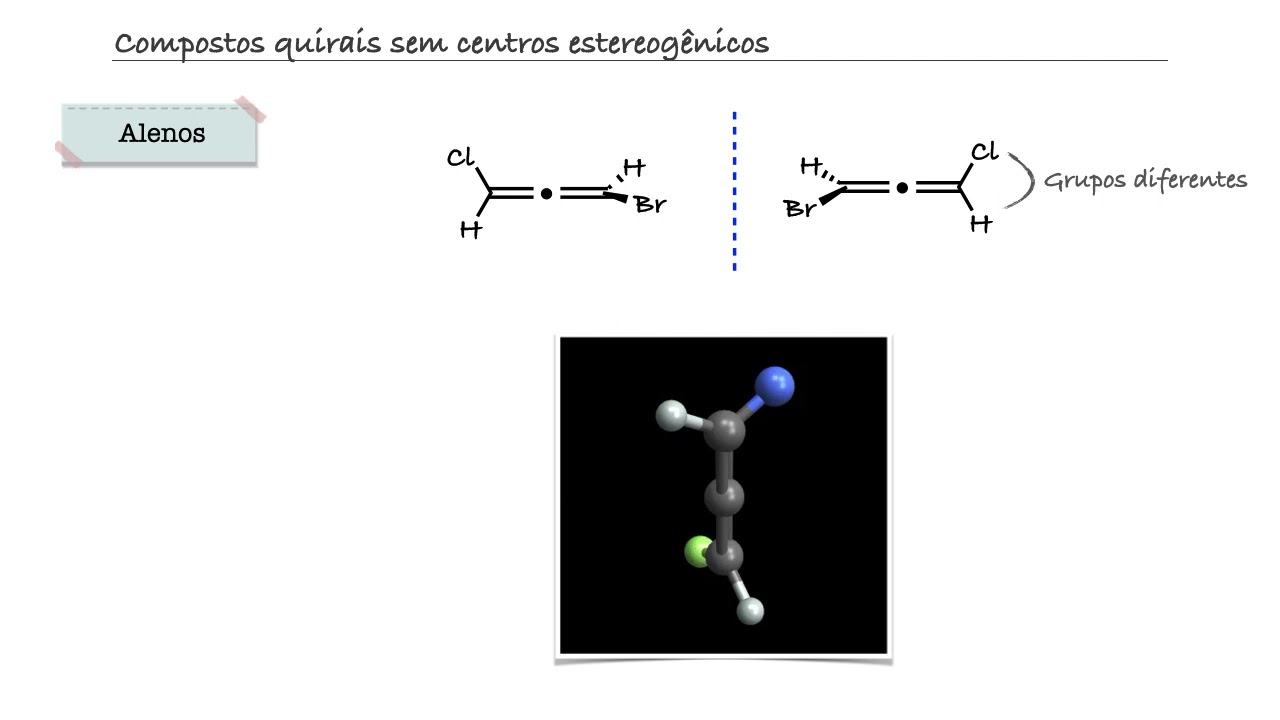
é desenhada verticalmente com o carbono de número um na nomenclatura o início da cadeia em termos de nomenclatura no topo e como fazer para passar da Fórmula em perspectiva aquela que acabamos de ver na outra tela para essa vejamos a estrutura em perspectiva primeiro e ela tem duas ligações no plano a ligação com o grupo nh2 que está representado em azul e a ligação com iodo que está representado em voz tem uma ligação para trás a do hidrogênio e uma ligação para frente a do cloro agora olhemos a estrutura 3D Então temos o mesmo cenário
ele H2 e o dono plano cloro para frente hidrogênio para trás é bem vamos agora imaginar as duas ligações ficando para frente e duas para trás dessa forma então agora o nh2 está para trás o hidrogênio está para trás e cloro e iodo estão para frente assim então cunhas preenchidas representando cloro e outro para frente com linhas tracejadas representando nh2 hidrogênio para trás então alguma diferença da primeira representação em 3D para essa na primeira nós tínhamos duas ligações do plano e duas fora do plano uma para frente ou para trás e agora nessa segunda representação
Nós temos duas ligações para trás e duas para frente nenhuma mais no plano é assim que devemos imaginar a molécula sendo movida para passarmos para a projeção de Fischer bom então nós temos que os grupos que estão para frente ficaram na horizontal na Projeção de Fischer são cloro iodo já os grupos que estão para trás ficaram na vertical na Projeção de Fischer são nh2 e hidrogênio falaremos mais das projeções de ficha no vídeo mais adiante nessa série mas sempre devemos lembrar como fazer para passar de uma fórmula em perspectiva ou de um modelo 3D para
Projeção de Fischer a nós falamos novamente dos enantiômeros uma mistura de enantiômeros em quantidades equimolares ou seja em quantidades iguais é conhecida como mistura racêmica ou racemato assim em uma mistura racêmica temos 50 por cento de um ano ante o metro e cinquenta por cento do outro quando se realiza no laboratório uma reação química que leva um composto que ir ao como produto e não se induz a preferência por um dos enantiômeros obtém-se uma mistura racêmica existem formas de induzir a produção majoritária ou até exclusiva de um dos enantiômeros e isso será discutido mais adiante
quando um dos enantiômeros está em maior quantidade do que o outro na mistura dizemos que existe um excesso enantiomérico ou e podemos calcular e diminuindo a porcentagem do componente o minoritário na mistura da porcentagem do componente majoritário com isso por exemplo se a cinquenta por cento de excesso enantiomérico de um dos enantiômeros significa que a setenta por cento setenta e cinco porcento de um ano de over e 25 por cento do outro dando um excesso de cinquenta por cento ou seja um dos enantiômeros está em cinquenta por cento a mais na mistura do que o
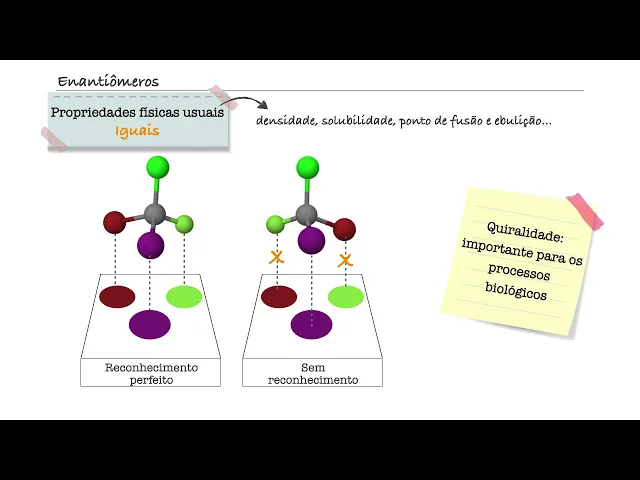
outro quando temos somente uma grande Homero Nossa produzidos uma reação por exemplo dizemos que o produto é enantiomericamente puro ou enantiopure um se falemos agora um pouco sobre as propriedades dos enantiômeros as propriedades usuais como densidade solubilidade ponto de fusão e ponto de ebulição são idênticas para ambos os enantiômeros o usa net ou menos tem diferença nas propriedades que dependem do arranjo espacial dos atos portanto os enantiômeros podem ser diferenciados por outra substância quiral ou seja podem ser diferenciados em um ambiente quiral um exemplo de ambiente geral são alguns receptores presentes no nosso organismo para
melhores visualizarmos podemos imaginar que esse retângulo um receptor canal com os sítios de ligação específicos indicados por esses círculos coloridos quando um dos enantiômeros de uma determinada molécula se aproxima reparem que ao reconhecimento perfeito se o mesmo receptor tentar se ligar ao outro enantiômero esse reconhecimento não ocorre mais pois o arranjo espacial de Siena de Homero é diferente a configuração é diferente é o primeiro nesse momento a essa diferenciação dá-se o nome de reconhecimento quiral e o receptor quiral interagem de uma maneira diferente com cada um dos enantiômeros de quiralidade é um elemento importante na
natureza e também exerce um papel fundamental em Ciência e Tecnologia uma grande variedade de processos biológicos é realizado através do reconhecimento perfeito de um substrato com base nisso funções metabólicas e respostas biológicas ocorrem Por que enzimas receptores celulares e outros sítios de ligação naturais reconhecem os substratos com stereo especificidade o ou seja reconhece especificamente um dos estereoisômeros possíveis para determinado composto a atividade biológica de substâncias quirais geralmente Depende de sua estereoquímica uma vez que um organismo vivo é um ambiente altamente grau no caso de moléculas com atividade biológica o efeito desejado está quase sempre presente
em um dos enantiômeros e o outro não de Homero ele ou ele não contribui com a atividade desejada ou pode levar a efeitos colaterais graves um exemplo clássico é o caso da talidomida uma droga que era utilizada por mulheres grávidas esse fármaco era administrado como uma mistura racêmica ou seja uma mistura de dois anos e causou uma formação de fetos pois um dos enantiômeros diminui os sintomas como enjoo Enquanto o outro causava teratogênese e e a talidomida possui o centro estereogênico que é que ir ao esse marcado com asterisco laranja existindo como esses dois enantiômeros
atualmente não se administra uma mistura de enantiômeros têm testá-los e geralmente utiliza-se somente um deles e esse controle é realizado por órgãos como Anvisa que Agência Nacional de Vigilância Sanitária aqui no Brasil ou também o FD e que o food and drug administration no caso dos Estados Unidos a outra propriedade que diferencia enantiômeros é a atividade óptica a atividade óptica é habilidade que uma substância quiral tem de desviar o plano da Luz clã nó polarizada em um equipamento chamado de polarímetro e o polarímetro possui uma fonte de luz e antes dessa luz passar pelo filtro
a luz derivada da lâmpada é como qualquer outra e o plano do vetor do campo elétrico pode assumir qualquer orientação no espaço ou seja ela não é polarizada ao passar pelo filtro a luz fica plano-polarizada o que significa a remoção das ondas exceto as ondas em que o vetor elétrico está em um plano determinado e essa luz agora plano-polarizada passa através do compartimento Contendo a substância a ser analisada em solução o solvente escolhido é geralmente água etanol o clorofórmio mas varia de acordo com a solubilidade da amostra se a substância que está lá dentro do
tubo dissolvida em solvente apropriado for opticamente ativa ela desvia o plano da luz e a direção EA magnitude do desvio são medidas por um analisador e leva ao que chamamos de rotação observada aquela que é observada no leitor do equipamento as moléculas aquirás são inativas ou seja elas não desviam plano da Luz plano-polarizada e já substâncias quirais podem ser ativas para isso a mostra deve conter um excesso de um dos enantiômeros porque os enantiômeros eles causam O desvio na mesma magnitude mas em direções Opostas por isso quando temos uma mistura racêmica no total não temos
desvio nenhum mas quando temos excesso de um dos enantiômeros esse desvio existir ar EA magnitude Claro está relacionada com quanto de sucesso temos de uma noite ombro em relação ao outro e o desvio dessa luz plano-polarizada pode ser positivo ou destrói Hero quando ocorre no sentido horário ou ainda negativo ou levogero quando o sentido do desvio for anti-horário E conforme comentado a rotação observada ou Alpha é o valor observado no aparelho para o desvio da Luz causado pelo mostra para a mesma substância ou mistura varia de acordo com o solvente utilizado a temperatura de medida
EA Concentração da amostra já a rotação específica ou Alpha entre colchetes é calculada a partir da observada através da forma onde se é a concentração da amostra em gramas por ml e l é o tamanho do caminho óptico em decímetros e a rotação específica é uma propriedade física da substância e junto com o valor do alto específicos são indicados a temperatura e o comprimento de onda utilizados na mistura na praça realizada medita e quando um dos enantiômeros está em maior quantidade na mistura a gente tem uma mostra ativa ou seja veremos o desvio da luz
plano-polarizada e teremos uma rotação observada E claro também uma específica caso um dos enantiômeros puros seja analisado haverá também um desvio uma das maneiras de sabermos o excesso enantiomérico na mostra é utilizar o alfa observado e o alvo específico como na forma fórmula mostrada onde o alfa observado O valor é dividido pelo alvo específico do composto puro e esse valor é multiplicado por cem assim saberemos a porcentagem de excesso enantiomérico na amostra nós vamos fazer alguns exemplos de cálculos utilizando o desvio da luz plano-polarizada para melhor entendermos quando o 03 g de colesterol é dissolvida
em 15 ml de clorofórmio e colocado em uma cela de polarímetro de 10 centímetros a rotação show observada lá no equipamento foi de -0,6 30 graus a 20 graus Qual é a rotação específica Ok vamos ao que sabemos a rotação específica é igual a rotação observada dividida pela concentração que deve ser dada em gramas por ml e pelo tamanho do caminho da óptico que é dado em de cílios a concentração é 03 G dividido por 15 ml se é o total de solução no tubo da nossa ou seja temos uma concentração de 0,02 gramas por
ml Essa é a unidade que devemos utilizar metros então podemos manter assim é o caminho óptico é 10 centímetros ou seja um decímetro porque ele deve ser colocado em decímetros na forma a rotação observada é de menos 0,632 colocando na forma temos a seguinte situação após calcular Podemos dizer que a rotação específica é - 31,5 assim 100 unidades mesmo podemos colocar a temperatura de análise junto ao símbolo da rotação específica assim podemos reportar esse dado em um relatório o artigo científico relatando também o solvente utilizado reparem que o sinal da rotação não muda o alfa
observado a negativo e o alvo específico também deve ser negativo Pois é para a mesma amostra Portanto o a direção do desvio da luz é a mesma e agora falemos do excesso enantiomérico nós vimos que ele é a porcentagem do enantiômero em maior quantidade menos o de menor quantidade somente se somente uma enantiômero assim como o colesterol está presente na mostra temos um excesso de 100porcento 100porcento menos zero por cento ou seja estacionando geométrico de 100 porcento Se tivermos uma mistura racêmica dos dois enantiômeros não observariamos nenhum desvio da Luz plano-polarizada e reparem que todos
os centros estereogênicos do colesterol natural quando olhamos o seu enantiômero estão invertido e as estruturas são imagens do espelho sendo assim um desvia a luz para uma direção e outro para outro e ela se anulam seres estão em mesma quantidade nesse cenário nós temos que as uma mistura racêmica temos 50 por cento de uns cinquenta por cento do outro ou seja o excesso enantiomérico é igual a zero se tivéssemos uma mistura de 85 porcento de um e quinze por cento de outro teremos um excesso net Américo então de setenta por cento e vejamos outro exemplo
de cobra e isso é uma mistura do colesterol natural e do seu enantiômero possui uma rotação específica de - 27° a 20 graus Celsius Qual o excesso enantiomérico dessa mistura e qual a porcentagem de colesterol natural na mistura sabemos que o excesso enantiomérico pode ser obtido dividindo o alvo observado da amostra pelo alvo específico do composto enantiopure nós sabemos o alvo específico do composto elantil furo do exemplo que acabamos de calcular é - 31,5 esse alvo específico ele foi obtido através da análise do colesterol natural puro então podemos usar esse valor junto com o valor
da rotação específica para a mistura entre o colesterol natural e seu enantiômero que é de -27% dado no problema e colocando na fórmula então nós temos o alvo observado na mistura que é menos 27 sobre - 31,5 que é o alfa do colesterol natural puro vezes sem isso nos dá um excepcionante Américo de oitenta e Seis por cento a b é a segunda a parte da pergunta quero saber a porcentagem total de colesterol natural na mistura se 85 porcento eu excesso do colesterol natural os outros 14 por cento são mistura racêmica ou seja 7 por
cento do colesterol natural e sete porcento do seu grande obra Então temos de colesterol natural os oitenta e Seis por cento do excesso mais sete no total de noventa e três por cento como a soma dos enantiômeros deve ser cem noventa e três por cento do colesterol natural 7 por cento do seu Mirante o número e o resultado está sentido Além disso Vimos que o excesso enantiomérico é a porcentagem do enantiômero em maior quantidade menos a do outro ou seja noventa e três por cento do colesterol natural que é o que está em maior porcentagem
menos sete porcento doutrinante ombro dá exatamente oitenta e Seis por cento que calculamos através da outra fórmula e tudo faz sentido Outro ponto importante que devemos observar é e nós tínhamos o alvo específico do colesterol natural puro que era de - 31,5 se quiséssemos saber o alvo específico do seu enantiômero puro nós precisaríamos somente inverter o sinal visto que cada enantiômero quando está puro desvia a luz com a mesma magnitude somente em direções Opostas se uma negativo o outro é positivo se falemos agora um pouco sobre configuração o arranjo espacial dos substituintes ao redor do
centro estereogênico é a sua configuração absoluta nem o sinal nem a magnitude da rotação nos falam sobre a configuração absoluta de uma substância por exemplo uma das estruturas mostradas é o 2-butanol EA outra ao menos 2-butanol mas assim sem informação adicional não se pode dizer que estrutura é qual o tanto os sinais positivos ou negativos ou ainda destrói gelo e levógiro são configurações relativas não se pode desenhar a estrutura somente baseado nessas informações para desenhar as estruturas Precisamos de mais informações essas informações vem da nomenclatura utiliza-se as letras R ou s maiúsculas e em Itálico
entre parêntesis antes do nome químico do composto e assim podemos saber de qual dos enantiômeros está falando as letras vem do latim rende recto ou seja direita ou indica o movimento horário enquanto S and sinister que o esquerda que indica o movimento anti-horário vejamos como observar a estrutura e determinar a configuração absoluta utilizando R ou s para nomear e observemos a molécula de um aminoácido tro o carbono Central possui quatro substituintes diferentes que estão destacados em laranja o grupo Amino 1 Rosa o hidrogênio em azul a metila ou em Preto a carboxila devemos numerar uma
ordem de prioridade de acordo com o número atômico do átomo que está diretamente ligado ao centro estereogênico átomos com números atômicos maiores possuem prioridade ou seja o número um será dado ao átomo com maior número todo observemos o átomo diretamente ligado em cada caso o hidrogênio e o nitrogênio e o carbono e outros carbono o átomo com maior número atômico é o nitrogênio ele recebe o número um e depois temos empate entre dois grupos que estão ligados pelo carbono a metila e a carboxila nesse caso olhamos os átomos na sequência a metila possui 13 hidrogênios
Oi e a carboxila possui dois oxigênio eo hidrogênio o oxigênio possui número atômico maior que o hidrogênio portanto a carboxila recebe era o número 2 E terá prioridade sobre a metila que receberá o número 3 e por último fica o hidrogênio com o número 4 quando existe uma hidrogênio Como substituinte ele sempre será o número quatro pois ele é um átomo com menor número atômico da Tabela Periódica agora para observar mos a molécula devemos girar e deixar o grupo de menor prioridade para trás do plano ou seja o mais distante de você observador Essa é
a regra sempre efeito assim a em todo o mundo e assim nós temos atribuição correta da configuração absoluta em todos os locais é uma dica para facilitar o giro e sem se perder é manter uma uma das ligações que estão no plano e gerar as outras três temos a mentira e a carboxila no plano vou manter a metila ela já tá desenhar podemos então copiar a molécula com a mentira no mesmo lugar as outras ligações sem substituir o hidrogênio deve ir para trás ou seja ele tem que tomar o lugar do mh2 bom então se
a gente fizer esse giro ficaria o hidrogênio no lugar do mh2 e agora o ele H2 deve ficar no lugar aonde estava carboxila continuando giro então ele fica no lugar onde está a carboxila ou estava carboxílico Ah tá e a carboxila agora deve ocupar o lugar que se que era do hidrogênio Então agora colocaremos ele ir lá no lugar aonde era o hidrogênio e terminamos o giro das três ligações é bem agora devemos desenhar uma certa que vai do número um passando pelo dois até o número 3 e se essa certa então que vai do
um passando pelos dois até o 3 possui sentido anti-horário e sendo assim a configuração absoluta desse carbono estereogênico é s.o.s. vai na frente do nome do composto essa é a a lâmina ou melhora é se a lâmina a r a lâmina é semelhante homem ou seja a sua imagem no espelho reparem que o nh2 e a carboxila mudaram de lugar e se traçarmos a seta agora e fica no sentido horário se acerta partindo do grupo de maior prioridade um passando pelo dois indo para o três com o grupo de menor prioridade para trás é bem
Então esse é noite o número é a r a lâmina com essa sistemática fica mais fácil de identificar a configuração absoluta e é possível também desenhar um composto corretamente a partir do nome nós vimos que quando um substituinte possui o mesmo átomo ligado ao carbono estereogênico devemos olhar para os próximos átomos ligados naquele grupo devemos ter cuidado quando os grupos substituintes possuem ligações duplas ou triplas nesses casos contamos como se os átomos estivessem ligados duas ou três vezes por ligações simples ou seja a carbonila é tratada como o carbono ligado a dois oxigênio explicação simples
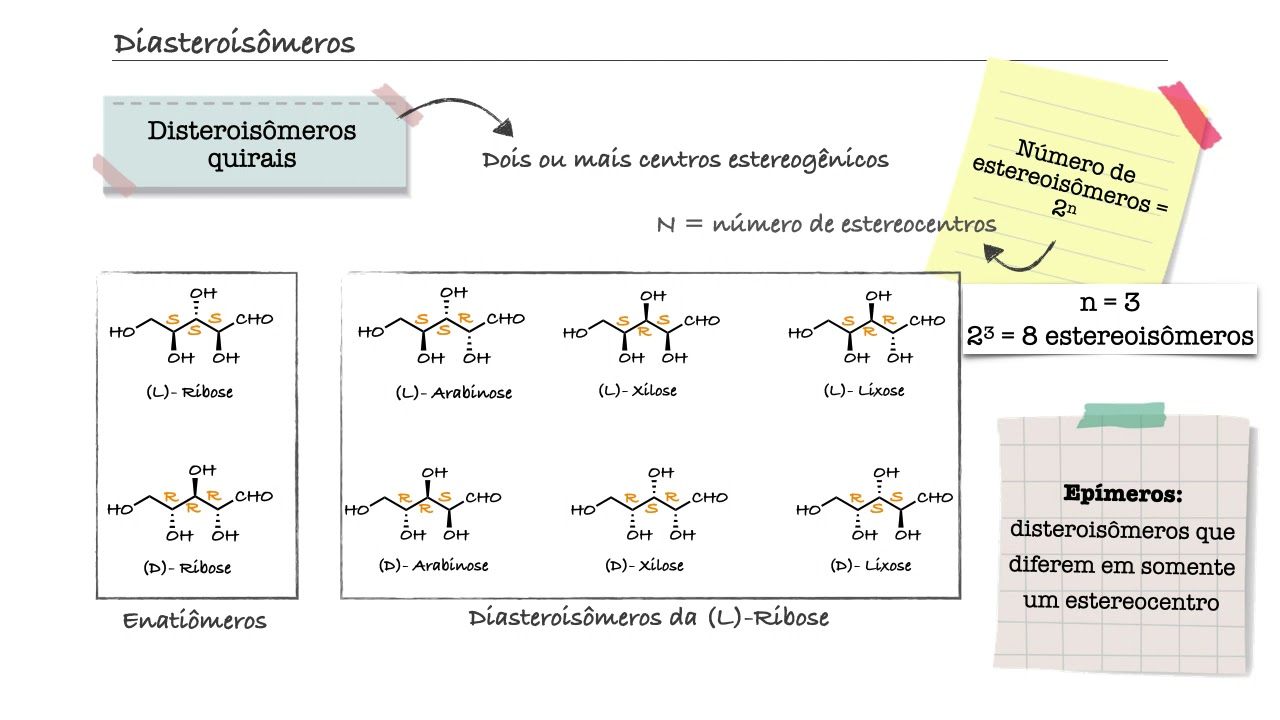
carbono dupla carbono é tratado similarmente como se um carbono estivesse ligado a dois outros carbonos por ligações simples isso vale para cada um dos atos dos átomos de carbono da dupla EA ligação tripla 3 sem triplas e por exemplo se comporta o devemos considerar como se cada carbono estivesse ligado a três outros carbonos por ligações simples vejamos um exemplo para ficar mais claro para exemplo claramente o grupo hidroxila é o número um de prioridade porque o oxigênio é o que tem o maior número atômico em que o meu quarto porque tem o menor número atômico
o problema é o empate entre o ch2oh e o cedo qual H é um dos ligados pelo átomo de carbono ao centro estereogênico tanto um grupo. O outro possui hidrogênio e oxigênio ligados a esse carbono como a gente vai fazer para o diferencial pé o aldeído possuir uma dupla ligação carbono-oxigênio contamos como o seu oxigênio estivesse ligado duas vezes por ligações simples no carbono dessa forma E no caso do ch2oh o carbono está ligado dois hidrogênios e um oxigênio somente o saldo é o seguinte o carbono desse grupo aldeído está ligado a dois oxigênio oxigênio
oxigênio eo hidrogênio oh e oh ch2oh o carbono Esse grupo está ligado a hidrogênio hidrogênio e oxigênio sendo assim na sequência das ligações o grupo aldeído por possuir dois oxigenios contra um oxigênio do grupo CO2 ch2oh ele tem prioridade Portanto ele será o 2 na prioridade já oh ch2oh para ficar com o número 3 assim a gente diz empata bem agora a gente tem que fazer tudo como a gente fez anteriormente temos que girar e verificar a configuração vamos fazer como a gente fez um exemplo anterior nesse caso como hidrogênio precisei para trás e ele
é uma das situações Clamam eu vou manter o ADR a outra ligação no plano e vou tirar as outras três ligações e bom então o hidrogênio vai para o lugar onde estava o aldeído é o aldeído vai para o lugar aonde estava o ch2oh Oi e o ch2oh vai pro lugar aonde estava o hidrogênio Pronto agora a gente coloca de novo os números de prioridade traça a seta do um passando pelo dois até o 3 e percebemos que nós temos aqui um sentido horário ou seja a configuração absoluta deve ser é o nome completo desse
composto é portanto r23 dehidroxi propanal em círculos também podem ser quirais e terena de Hórus eles podem ser tratados como cadeias abertas para atribuição da configuração absoluta é bom para facilitar os grupos de átomos envolvidos podem ser copiados como se estivesse uma cadeia aberta você vai o verificando a sequência e vai desenhando eles até um certo momento para cada lado tô aqui nós temos que o grupo M azul e grupo laranja e os grupos que pertenciam ao ciclo né então o cabo centro estereogênico ali tava ligado por um lado por não se H2 para o
outro também não Sega dois e depois fomos tendo diferença e fomos copiado assim podemos atribuir a correta configuração absoluta ao centro estereogênico dessa maneira para a molécula mostrada teremos esse desenho mostrado né EA dupla ligação ela tá sendo tratada como se o carbono da dupla estivesse ligado duas vezes ao outro carbono tá isso é importante bom então nós temos que dentre todos esses grupos ligados ao centro estereogênico nós temos Claro o hidrogênio é o de menor prioridade e todos os outros são grupos de carbono só que o grupo em laranja se a gente for seguindo
a ordem dos substituintes ele vai ter vantagem porque chega um ponto que ele está ligado a dois carbonos enquanto o grupo em azul por exemplo está ligado a dois hidrogênios e aí ele vai ter prioridade sobre o azul e o último dos grupos carboniladas com prioridade número 3 é a mente lá porque tem o carbono ligado a 13 hidrogênios agora Só nos resta fazer a seta do um passando pelo dois pegou três e atribuir a configuração absoluta R Já que é certa é no sentido horário e ainda falando de ciclos preciso chamar a atenção para
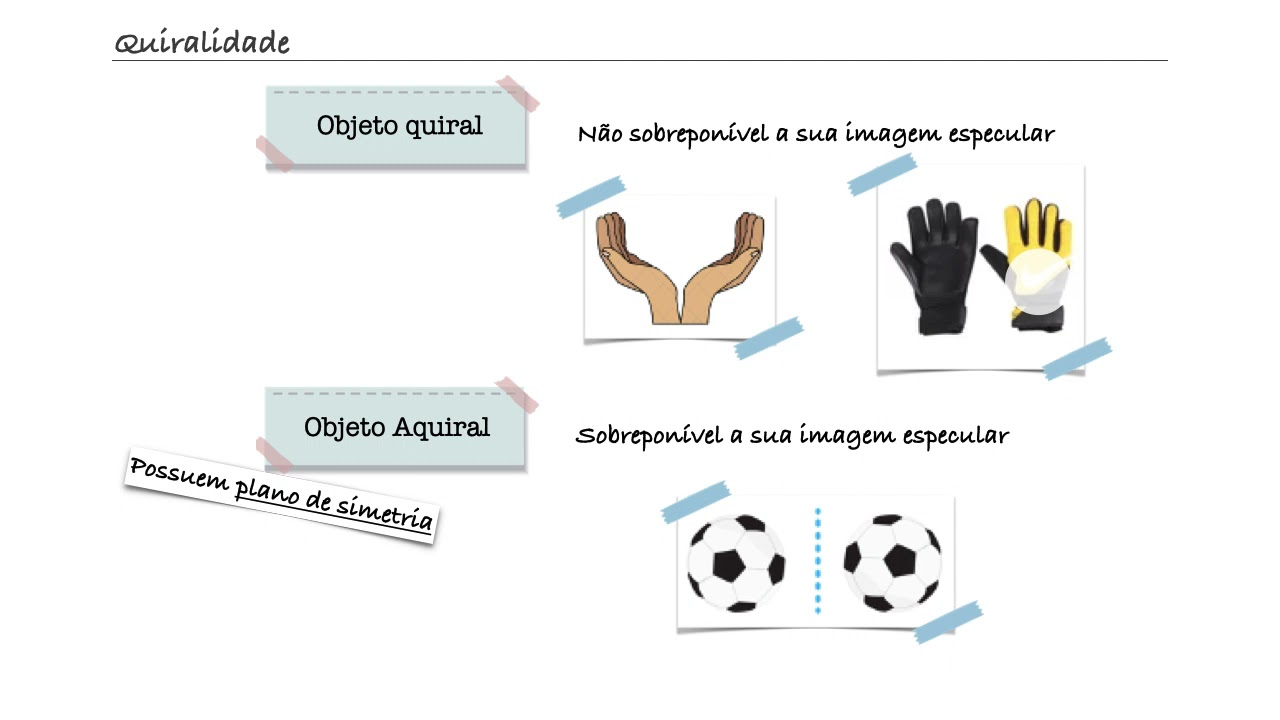
o ciclo hexano os monossubstituidos e dissubstituidos principalmente às vezes eles parecem ser quirais mas não são olhamos o ciclo hexanol desenhado assim com essa Cunha preenchida indicando que o a gastar para frente pode parecer que temos um centro de saúde e Nicole e que a molécula quiral Mas vamos desenhar o ciclo hexanol assim agora vamos traçar uma linha no meio do desenho pronto podemos ver que a molécula foi dividido em duas metades exatamente iguais ou seja temos um plano de simetria e sendo assim a molécula é aqui ao o mesmo ocorre para o metil-ciclo-hexano Vamos
colocar os hidrogênios da mochila novamente é possível traçar um plano de simetria e a molécula é aqui tal vejamos agora um exemplo do ciclo-hexano 14 de substituído como esse padrão de substituição possui uma simetria inerente se os grupos ligados não forem assimétricos haverá plano de simetria o exemplo 4 metil ciclo hexanol o plano de simetria existe como vocês podem observar e a molécula é a Kendall e vejamos agora um exemplo de um 12 de substituído nesse caso uma medida está para frente a outra está para trás e não há plano de simetria Já que as
duas metades não são iguais porque eu amo uma a metade tem leite lá para frente EA outra para trás sendo assim não temos planos de simetria e a molécula quiral e a configuração absoluta dos dois centros estereogênicos nesse caso R Claro se tivéssemos as duas mochilas para o mesmo lado a molécula teria plano de simetria mas não é assim que está no exemplo mesmo quando o padrão de substituição é mono ou até dissubstituído 14 se pelo menos um substituindo-os por assimétrico não haverá plano de simetria colhemos outro exemplo esse composto um composto 14 substituído ele
é quiral devido à presença de se substituir de que é assimétrico e esse substituinte possui o centro estereogênico Nesse caso a configuração desse centro é esse e esse centro confere qualidade a toda molécula e ele é o único centro sério gênico da molécula Pois o outro carbono aquele ligado a mochila possui dois substituintes iguais se percorrermos cada lado do ciclo aparecem os mesmos atos nos na mesma ordem mas como existe um centro estereogênico na molécula já é suficiente para deixar toda molécula quiral o outro exemplo de ciclo hexano substituído e quiral é esse ele é
trissubstituído ele também possui um grupo assim metro mesmo as Duas Medidas estando para o mesmo lado a presença desse substituinte contendo o centro estereogênico deixa a molécula quiral nessa molécula existem ainda dois outros centros estereogênicos aqui marcados justamente porque se percorrermos os dois lados do ciclo eles não vão ser iguais Então essas medidas esses carbonos cuidados essas medidas esses carbonos questão marcado também são Centros estereogênicos e portanto essa molécula também será geral bom então vamos marcar ela como que ela está e antes de encerrar esse vídeo falamos de como atribuir a correta configuração absoluta a
centros estereogênicos presentes em ciclos anos quando eles estão desenhados na forma em cadeira é mais fácil atribuir quando está na forma planar Então vamos ver uma dica para facilitar desenha estrutura planar ao lado de estrutura em cadeira o grupo que se encontra na ligação superior do centro estereogênico deve ser colocado para frente e o grupo da ligação inferior para trás bem Então temos o hidrogênio da ligação superior do centro estereogênico e o h na ligação inferior então o hidrogênio vai para frente e o olhar para trás agora faça uma seta do centro estereogênico até o
substituinte do ciclo pelo caminho mais curto então caminho mais curto e se a gente considerar o centro estereogênico como um vai ser esse indicado pela seta pois os substituintes estarão no carbono 3 replique isso no desenho Claro só pode número Ah tá E aí coloque o substituímos nesse caso o carbono número três ele possui um dos substituintes iguais são duas filas uma fica para frente ou para trás o plano Já que as ligações do ciclo estão no plano quando o ciclo está desenhado na forma planar mas ele não é um centro estereogênico é bem agora
é só você treinar espero que esse vídeo usa ajude a entender enxergar melhor os aspectos tridimensionais Bons estudos e até o próximo vídeo dessa série