Fala galera do me salva estamos começando mais uma aula do nosso módulo de ligações químicas e nessa aula a gente vai falar da última ligação química possível que é a ligação metálica bom eu gosto muito dessa definição de ligação metálica quem é que em primeiro lugar quem é que faz ligação metálica Como o próprio nome já diz né é uma ligação que ocorre entre metais então de novo a gente tem que lembrar que os metais eles são aqueles elementos que estão aqui ó mais abaixo e mais a esquerda na tabela né aqui a divisão entre
a metais que ficam para cá e os metais que ficam mais abaixo certo então tantos metais alcalinos alcalinos terrosos quantos de transição transição externa transição interna todos esses aí se eles se se ligarem uns aos outros ou com eles mesmos eles vão fazer ligaç do tipo metálicas certo e a definição aqui ó É bem interessante são C ordenados Lembrando que é aquele elemento que perdeu elétron que ficou positivo porque perder elétron perder carga negativa ficar Positivo né então CS ordenados espacialmente e esses CS eles ficam vibrando em torno de pontos definidos né então eles dão
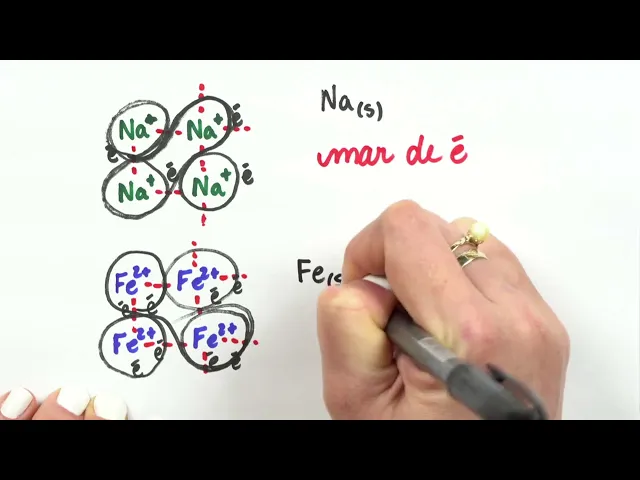
uma viadinha Mas eles estão cercados por elétrons semilivres e aqui muito interessante a gente observar né que esses elétrons semil H vão ser eh o que vai caracterizar a ligação metálica Principalmente quando a gente fala né que ocorre um mar ou uma nuvem de elétrons certo que é o principal característica aí da ligação metálica bom gente se vocês observarem né como é que isso ocorre então Afinal bom se eu pegar lá o sódio o sódio é um metal certo o sódio em geral ele perde um elétron para ficar estável e aqui então o que que
vai acontecer quando sódios se ligam entre si né ã cada sózinho cada átomo de sódio perde um elétron e esse elétron fica aqui ao redor certo então cada um ó representei aqui os quatro elétrons que cada um desses átomos perdeu mas é bom você saberem né que continua para cá um monte de sódio para baixo também enfim né todos perdendo um elétron formando seus c Por isso c ordenados ordenados Por quê Porque eles esse elétron que eles perderam fica girando em torno de todos esses átomos então todos os elétrons que foram perdidos aí ficam girando
em torno desses CS positivos e isso gera uma atração entre os né entre os sódios os CS de sódio certo então no fim das contas para cá continua que eu teria mais um sódio para cima eu também teria mais um sódio né no fim das contas esses elétrons girando ao redor eh dos CS de sódio dos ction do Metal fazem com que haja uma força de atração aqui entre esses ctions e isso é o que caracteriza a ligação metálica certo é uma ligação muito forte e é muito importante então vocês observarem que isso forma querendo
ou não uma rede de ction por isso que é ordenados espacialmente porque eles ficam aí eles vibram um pouquinho mas eles não saem do seu lugar porque essa nuvem esse mar de elétrons faz com que eles tenham uma força de atração que é o que a gente chama de ligação metálica Então isso é o que caracteriza né esse Giro dos elétrons aí perdidos por cada sódio é o que caracteriza o que a gente chama de mar de elétrons mar ou Nuvem de elétrons certo e a representação disso aqui seria o quê sódio metálico a gente
fala né sódio sólido é sódio metálico beleza a mesma coisa aconteceria com o ferro por exemplo né só para dar outro exemplo para vocês não precisa perder apenas um elétron o ferro em geral perde dois elétrons então cada átomo de Ferro perde dois elétrons ó esse perdeu dois esse perdeu dois aquele ali perdeu dois esse outro aqui de baixo perdeu dois e esses elétrons aí de cada ferro também ficam girando ao redor dos ction aí de Ferro como no sódio certo e isso de novo faz com que surja aí uma força de atração muito intensa
Entre esses ferros o que caracteriza aí uma ligação metálica de novo causada ali pelo mar de elétrons se eu fosse representar esse ferro aqui né Eu representaria por ferro sólido então vejam que as ligações metálicas elas ocorrem entre o metal ligando a átomos dele mesmo é muito importante a gente observar que a gente não encontra em geral metais na sua forma de substânci simples ou seja ligados a átomos só deles mesmos na natureza um dos únicos que a gente encontra assim na natureza é o ouro a u tá o ouro Sim a gente encontra ali
e na sua forma de substância simples então com ligações metálicas certo então as ligações metálicas pra gente obter por exemplo esse ferro a gente vai pegar lá um minério de ferro e diversas através de diversas reações químicas a gente consegue chegar no ferro puro digamos assim né que não é exatamente puro Mas enfim assim que a gente chega então quem é que faz ligação metálica esses metais que a gente obtém né através de processos industriais o ouro que é um dos metais que é encontrado assim na natureza Senão também a gente tem ligações metálicas entre
diferentes metais quando a gente tem as chamadas ligas metálicas então nas ligas metálicas é o único momento em que a gente vai ter metais diferentes se ligando através dessas ligações metálicas através da nuvem ou do mar de elétrons certo e quais são as características desses compostos bom gente os metais eles são encontrados na natureza Nas condições ambientes né de temperatura e pressão ambiente na no estado sólido tá exceto aqui o mercúrio que o Mercúrio é o único metal que a gente encontra no estado líquido Nas condições ambientes certo inclusive é um metal extremamente tóxico os
pontos de fusão e ebulição dos metais são bem altos certo um pouco menores do que os iônicos mas bem mais altos do que os compostos covalentes tá ã os metais eles conduzem eletricidade inclusive eles são ótimos Condutores a gente usa cobre por exemplo né fios de cobre para conduzir aí a eletricidade que chega até a nossa casa ã a dureza dos metais é de baixa a elevada Então depende o metal o sódio por exemplo tem uma dureza baixa e o ferro por exemplo tem uma dureza um pouco mais elevada um metal um pouco mais duro
Lembrando que dureza e tenacidade sempre características de das substâncias no estado sólido já a tenacidade dos metais é elevada O que que significa isso significa que eles deformam sem quebrar se a gente pegar por exemplo o ouro o ouro ele é bastante maleável ele é bastante tenaz a gente pode dobrar ele e deformar ele sem que ele quebre por isso que a tenacidade é elevada bom galera sobre metais eras isso e se alguém tá com alguma dúvida né Por que na aula de ligação covalente de compostos covalentes a gente não falou em ligação dativa é
porque Gente esse é um conceito que não é mais utilizado tá ele é um conceito ultrapassado então a gente não fala mais em ligação dativa por enquanto falamos só em ligação iônica metálica e covalente eras isso espero que tenha sido útil para vocês essa aula e até a próxima