E aí [Música] o Olá pessoal tudo bom hoje nós vamos falar um pouco sobre soluções dano em fazer as soluções aquosas soluções aquosas são aquelas então Preparadas utilizando a água como solvente vamos entender principalmente Quais os aspectos da molécula de água que permite com que boa parte dos compostos iônicos e moleculares possam ser dissolvidos neste solvente e antes de iniciar nós vamos definir o que é uma solução Lembrando que uma solução é uma mistura homogênea de duas ou mais substâncias então não necessariamente eu preciso ter uma substância dissolvida na água posso ter mais de uma
substância e essa soluções elas podem ser sólidas líquidas ou gasosas Mais especificamente Ao se tratar de soluções em que a água seja solvente nós vamos trabalhar aqui as definições em cima de soluções líquidas Benta composição de uma solução nós podemos definir habitaria mente a dois componentes uma solução é composta pelo solvente é insolvente é definido como sendo componente de maior quantidade o presente nessa mistura em um soluto ou solutos né seriam os componentes em menor quantidade presente nesta solução como eu falei essa classificação da composição ela é arbitrária Em alguns momentos nem algumas soluções dentro
da química que mesmo o solvente estando em menor quantidade em relação a massa ou o volume ele ainda continua sendo definido como solvente Mas nós vamos para todos os efeitos utilizar essa definição de composição então para preparar uma solução eu tenho um soluto em um solvente eles vão ser então soluto vai ser adicionado ao somente nós vamos agitar até que nós obtenhamos uma solução homogênea nesse ponto é importante que nós entendamos O que significa ser homogêneo numa solução quando nós dizemos que uma solução o gênio significa que qualquer porção igual dessa solução que eu pegue
Imagine que eu posso então a recortar essa solução vou tirar alíquotas de mesmo volume dessa solução vamos supor tortilha alíquota de 10 ml free quer dizer que essa solução é homogênea é dizer que para cada alíquota que eu tirar independentemente né mas obtendo o mesmo volume quantidade é do meu soluto vai ser exatamente a mesma ou seja suas propriedades e a sua composição não pode variar em função da Porção que o Perry se eu pegar uma porção maior vamos supor que eu pego aqui 20ml quantidade de soluto presente em 20 ml tem que ser proporcional
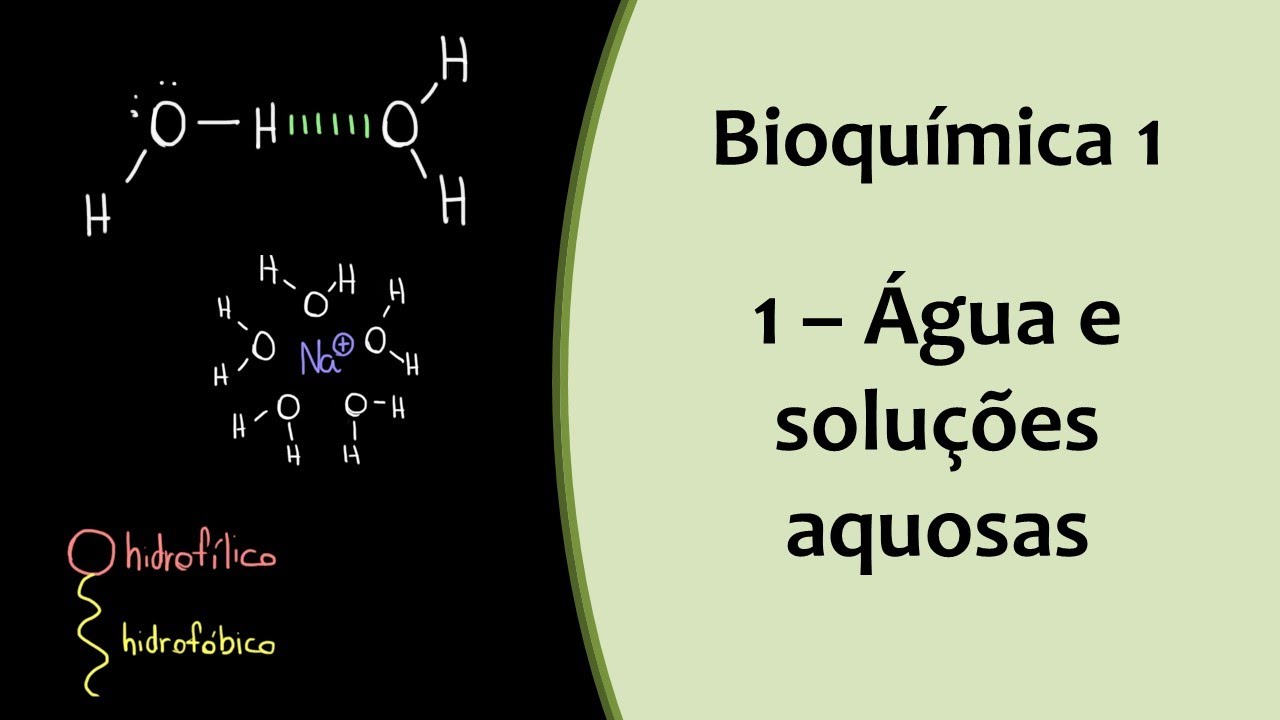
Então se aqui eu tinha Cinco partes para 10ml no caso de 20 é o dobro eu vou ter que ter 10 partes Isso significa que a minha solução ela é homogênea tá por isso que é muito importante no preparo de soluções homogenizar bem o sistema ou seja agitar bem o sistema para que nós consigamos obter esse resultado e não haja variações nas propriedades dessas soluções definido então soluções nós vamos então agora falar Mais especificamente das propriedades da água a água e tem essa estrutura uma estrutura angular nessa estrutura ela é composta pelo oxigênio um átomo
de oxigênio dois de hidrogênio apresenta essa estrutura angular a Aqui nós temos a eletronegatividade dos elementos envolvidos e ela é uma molécula é polar aí nós observamos aqui que alma densidade de carga espalhada pela molécula da água de forma a ter uma porção positiva né uma densidade de carga positiva aqui na região dos átomos de hidrogênio uma densidade de carga negativa aqui na região do átomo de oxigênio isso se deve exatamente a diferença de eletronegatividade entre o oxigênio eo hidrogênio o oxigênio por ser mais eletronegativo Acaba atraindo a nuvem de elétrons né envolvido nessa ligação
química e atrai esses elétrons envolvidos nessas ligações covalentes para se concentra então devido a carga do elétron se negativa concentra essa carga negativa na região do oxigênio deixando a deficiência de elétrons nos átomos de hidrogênio então aí nós temos a carga positiva isso forma é de Polo elevado na molécula de água são bem três propriedades que conferem a água habilidade de dissolver composto seja o único são moleculares nós temos o elevado momento de polar da água um elevado poder de dissociação que está relacionado principalmente à sua constante dielétrica a formação de ligações de hidrogênio em
aspectos específicos da estrutura de alguns compostos um o processo chamado de solvatação que nós vamos explicar mais adiante tanto de uns quanto de moléculas vamos entender então que quando nós promovemos a adição de um determinado solvente na água e ele se dissolve Nós estamos promovendo uma dissolução que significa integrar as partículas do som e as partes do soluto sejam eles íons ou moléculas nas moléculas do solvente neste caso a alho o que nós estamos promovendo aqui é um processo que nós definimos como solvólise essa dispersão ela é possível Devido as interações entre soluto e solvente
que provém daquelas interações intermoleculares se vê nos estudos de química geral que justamente vão auxiliar nesse processo apresentado algumas propriedades da água vamos entender agora de acordo com a natureza do composto como que se dá o processo de dissolução na água primeiramente nós vamos falar dos compostos iônicos os compostos iônicos né lembrando rapidamente são compostos formados por Íons de cargas Opostas que permanecem Unidos devido a uma interação eletrostática entre essa bom então nós temos aqui estes Rios Unidos né pela interação de atração entre essas cargas de distintas formando um retículo cristalino alguns compostos iônicos quando
colocados na presença de água eles são dissolvidos e essa dissolução nada mais é do que uma dissociação iônica que que é uma dissociação iônica é uma separação do rio na presença da água então a água vai ser responsável por separar desfazer esse retículo cristalino que e separar este Zinho isso se deve acontece devido a uma interação eletrostática entre união e um dipolo da água Como assim se nós olharmos a estrutura da água e nós temos uma densidade de carga negativa na região do oxigênio uma densidade de carga positiva nos hidrogênio e nós temos Íons de
cargas Opostas na solução a região negativa da molécula de água sua densidade negativa ela vai interagir 11 anos de carga positiva cargo Costa enquanto que essa região vai interagir né região de densidade de carga positiva vai interagir com os erros de carga negativa essa interação é forte o suficiente para alguns compostos iônicos permitir né as suas organização em Água Além disso nós temos que levar em consideração a elevada constante dielétrica da água o quê que isso interfere aumenta o poder de dissociação é a força que mantenha se diziam Unidos né é uma força elétrica dada
por esta equação em que nós temos aqui sem dizer a carga docinhos aqui a carga fundamental do elétron nós temos aqui a distância entre este Zeus e Aqui nós temos a constante dielétrica da água e o que nós observamos é que a força elétrica entre os rios é inversamente proporcional à constante de elétrico então uma constante dielétrica elevada garante para nós uma força de interação e precisemos mais fracas Daí vem a justificativa também porque que alguns compostos iônicos de sol homem na presença de água é importante dizer aqui que não é somente esse fator que
explica a solubilidade dos compostos em água há um balanço de energia entre vários processos físicos e químicos que devem ser considerados é energia de rede Cristalina energia de interação com o solvente não é um balanço energético aqui é um aspecto qualitativo para entender um pouco Aonde que a água a tua né quais são as propriedades o que atua nesse processo de torção é importante observar também que aliado é esse processo de dissociação iônica nós temos que mostrar um aspecto importante é a solvatação dos íons pelas moléculas de água ou seja Ao serem dissolvidos as moléculas
de água vão bombardear use Once de forma a Gerar em volta dele o que a gente chama de espera é de solvatação e nessa esfera de solvatação a gente forma um íon hidratado e não há como definir exatamente o número de moléculas de água que vão formais de uma hidratado isso vai variar da carga do íon do tamanho do hino e da intensidade de interação né a experimentos conseguem determinar para um compostos alguns o número exato essas essa espera de solvatação ela pode ser constituída por camadas ao longo da interação do Iam com as moléculas
de água o que se espera de solvatação o pai ela diminui a interação 12 anos né do salto do composto iônico que está dissolvido na água porque ela forma uma espécie de blindagem né E aumenta a dieta distância de interação entre terrível olha aqui força elétrica também é inversamente proporcional à distância entre você aumenta essa distância você tem uma força de atração entre eles menor então ao papel muito importante nesse aspecto a solvatação falando agora dos compostos moleculares a uma classe de compostos moleculares que na presença de água só tem um processo chamado de ionização
Ou seja a partir do momento que eles estão na presença de água eles formam íons em solução esse processo de formação de íons é um processo químico ou seja uma reação que envolve a ruptura EA formação de ligação covalente da onde que vem esse processo que nós observamos o exemplo aqui nós temos um ácido acético no ácido acético nós temos um hidrogênio ligado ao oxigênio o oxigênio apresenta uma grande a eletronegatividade um valor elevado da sua eletronegatividade e atrai os elétrons dessa ligação covalente para se deixando o átomo de hidrogênio com uma densidade de carga
por é suscetível a formar uma ligação convalente com qualquer outro composto que possa lhe proporcionar um par de elétrico e nesse caso a água apresenta dois pares de elétrons isolados E aí nós temos uma formação de uma ligação coordenada se rompe essa negação e o hidrogênio e passa por uma ligação coordenada com um dos pares de elétrons presentes na molécula de água com isso nós temos a formação de dois rios aqui em solução no caso do ácido acético nós podemos representá-lo ele dessa forma na presença então de água que tenha que os seus pares de
elétrons e esse hidrogênio e a forma o hidrogênio H3 animais e formam os seus acetato então é uma reação química formando íons esse processo ele pode acontecer integralmente nós temos compostos moleculares estão Lembrando que os compostos moleculares são formados por ligações entre a compartilhamento de elétrons mas esses compostos devido a diferença de eletronegatividade apresenta então densidades de carga em suas moléculas distintas por exemplo o ácido clorídrico é uma espécie molecular e quando na presença de água ocorre esse essa reação química eu e ele então forma e nenhum sidronio mas Eos cloreto e a sua ionização
ocorre 100% ou seja depois que nós colocamos uma certa quantidade de ácido clorídrico na água nós não temos mais essa estrutura passou-se a ter única e exclusivamente uns iam H3 ou mais e cloreto a esse aqui pode ser definido como sendo um eletrólito port e nós temos também ácidos são fracos e Nesse caso eles não ionizam tem por sempre a exemplo disso é o ácido acético Que Nós já mostramos aqui a reação que tem a sua porcentagem de ionização menor que um por cento e esse é um ácido orgânico maioria dos ácidos orgânicos apresentam a
sua propriedade nós temos os ácidos inorgânicos também Como por exemplo o Ácido cianídrico é um ácido fraco também sofre esse processo então com a água né Nós temos aqui essa reação que estabelece um estado de equilíbrio a forma 12 anos h3oh mais e essa propriedade de coordenação né de doação de formação de ligação coordenada não ocorre só para espécies ácidas ou básicas não ela pode ocorrer também na formação de compostos de coordenação são auxiliar a solubilização de alguns compostos através da formação de compostos de coordenação Então essa habilidade de doar o par de elétrons auxilia
neste processo de solubilização não somente de compostos molecular é importante dizer aqui que para esses compostos moleculares e formam íons em solução esses Rios também são solvatadas pelas moléculas de água então por exemplo esse contraiu um acetato cloreto também passam a ser rodeados aqui por moléculas de água e passa ser rodeado por moléculas de água 1 milhão H3 ou mais a uma relação também com as moléculas de água ao seu redor então processo de solvatação ele vai ocorrer indistintamente para o tipo de molécula ou ion que você tem em solução o ursinhos falamos os compostos
moleculares não ionizáveis que estão aqueles que estão dissolvidos em água mas que não liberam lente pulinho e a que se deve esse processo de dissolução se deve principalmente a diferença interações intermoleculares que são as interações de natureza eletrostática neste caso não ocorre nem o tipo nenhum processo químico essas interações intermoleculares elas são responsáveis pela solvatação dessa molécula quando nós falamos de interação intermolecular neste caso nós estamos falando principalmente das interações dipolo-dipolo que ocorrem entre moléculas de mesma polaridade que tem um momento de dipolo diferente de zero então moléculas polares e nós estamos falando das forças
de dispersão o que também é conhecido como as forças de London essas forças são interações mais fracas do que as interações dipolo-dipolo mas estão presentes em qualquer tipo de molécula seja ela polar ou apolar essas interações né apresentam energias de tintas entre a atração dessas moléculas que depende principalmente da distância a interação dipolo-dipolo Ela depende um e do Inverso da distância ao cubo enquanto que as interações de longo depende do Inverso da distância elevado a sexta ou seja a gente observa que que elas são muito mais fracas então a energia envolvida aqui ela é maior
do que a energia envolvida nessas forças de longo de qualquer forma que as energias não são tão elevadas mas garantem esse processo de solvatação além disso para algumas classes de compostos que apresentam na sua estrutura ligações do tipo o h n h e f h e o processo de dissolução desses compostos moleculares não ionizáveis se dá principalmente pela habilidade que a água tem de formar o que a gente chama de ligações de hidrogênio é uma interação intermolecular particular envolve uma energia superior a essas interações moleculares mais simples como dipolo-dipolo e forças de London mas só
ocorrem quando essa molécula apresenta na sua estrutura esse tipo de ligação como a gente pode ver aqui nesse exemplo de diferença alguns orgânicos né formando ligações de hidrogênio com a água o que acontece nessas ligações de hidrogênio nós temos um compartilhamento do hidrogênio que está presente na estrutura do meu soluto o que acontece é que o hidrogênio está ligado a este exato nos de eletronegatividade levado e Breno não né atrai esses elétrons envolvidos na ligação covalente para se deixando uma densidade de carga positiva no hidrogênio mas não a ponto de romper ainda essa ligação tem
dessa densidade positivas moléculas de água se aproximam e no caso do oxigênio que tem uma densidade negativa também exerce uma atração forte sobre esse hidrogênio já que ele apresenta essa densidade de carga positiva dessa forma ocorre basicamente um compartilhamento e do átomo de hidrogênio formando uma espécie de ponte até hoje não se usa mais o termo ponte de hidrogênio mas nós temos esse com esse compartilhamento do hidrogênio que vai ser atraído né pelo par de elétron isolado do oxigênio da molécula de água para vocês terem ideia a energia envolvida neste processo né nessas interações intermoleculares
é na ordem de dois quilojoules por mol já nas interações é nas ligações de hidrogênio a energia envolvida nesse processo de formação da ligação de hidrogênio é na ordem de 20 kilojoule o irmão então moléculas que apresentam os átomos de hidrogênio ligados a nitrogênio oxigênio e fluor são solubilizadas na presença de água Lógico que isso vai depender muito da sua estrutura mas havendo a essas características na sua estrutura vão ser colonizados principalmente devido à possibilidade de formação de ligações de hidrogênio nós estamos falando aqui da água como solvente mas ela pode ocorrer para qualquer molécula
e apresente por exemplo o hidrogênio ligados a um átomo eletronegativo são nitrogênio aqui na amônia o ácido fluorídrico e assim por dia é bom esse vídeo mostrou então algumas propriedades da água que não permite entender porque que alguns compostos iônicos e moleculares podem ser solubilizados em Água Além disso justificou o porquê que alguns meses formam íons em solução esses conceitos são importantes para que nós possamos avançar nos estudos de Equilibrio iónico Que bom se seguir