Hola Bienvenidos a este nuevo encuentro en este caso nos vamos a ocupar del metabolismo de los aminoácidos vamos a plantear como objetivos explicar el origen de los aminoácidos como producto de la proteólisis de las proteínas celulares y de las proteínas de la dieta vamos a describir las principales etapas del proceso digestivo de las proteínas y los mecanismos de absorción de los aminoácidos vamos a explicar los destinos metabólicos del nitrógeno de los aminoácidos y los destinos metabólicos de sus cadenas carbonadas resultantes vamos a describir las funciones centrales de las aminotransferasas y la glutamato de hidrogenasa en
el metabolismo de los aminoácidos vamos a describir los sistemas de transporte no tóxicos del amonio vamos a integrar el ciclo de glucosa lanina vamos a describir el ciclo glucano glutamato glutamina y su relación con el metabolismo de aminoácidos en hígado músculo esquelético sistema nervioso central intestino y riñón vamos a indicar los sustratos requeridos para la síntesis de urea y sus orígenes la ubicación subcelular de las enzimas que catalizan el proceso y los papeles de La regulación o lo estérica del nacetilutamato en La regulación de la vía vamos a integrar el destino de las cadenas carbonadas
derivadas del catabolismo de los aminoácidos al metabolismo intermedio dependiendo de las condiciones metabólicas analizadas y vamos a definir las funciones relacionadas vamos a reconocer ejemplos de los distintos productos especializados sintetizados a partir de los aminoácidos diariamente se produce en aproximadamente entre un 1 y 2% de recambio de todas las proteínas corporales el 75% de los aminoácidos resultantes pueden ser utilizados para formar nuevamente proteínas otra fuente importante de aminoácidos son los que provienen de las proteínas de la dieta analicemos entonces un poco el origen de estos aminoácidos el recambio de proteínas celulares es un proceso continuo
Existen dos vías principales de degradación de estas proteínas a través del protiosoma en donde aquellas proteínas ubicutilizadas son derivadas a esta estructura compleja que termina por degradarlas y a través de los procesos de autofagia en donde se forman autófagosomas continúan incluso orgánulos intracelulares que permiten luego de la fusión con los lisosomas degradar las proteínas diariamente se produce en aproximadamente entre un 1 y 2% de recambio de todas las proteínas corporales el 75% de los aminoácidos resultantes pueden ser utilizados para formar nuevamente proteínas otra fuente importante de aminoácidos son los que provienen de las proteínas de
la dieta la dieta es otra fuente importante de aminoácidos la digestión de proteínas comienza en el estómago tracción de la pepsina una enzima secretada como simógeno por las células principales y activada en presencia de ácido clorhídrico el ácido clorhídrico es producto de la secreción de las células parietales como consecuencia de la estimulación por gastrina por histamina y por acetilcolina que permiten la actividad de Añadir a carbónica y la traslocación de las bombas protón potasio a la luz a la perdón a la membrana luminal de la célula pariental una vez en intestino la secreción de un
juego pancreático rico en bicarbonato insimógeno producto de la estimulación porque les hizo quinina y secretina da comienzo a la degradación más importante de la proteína de la dieta la activación de estos simógenos requiere del estímulo por colecisto quirina sobre las células del epitelio de la mucosa intestinal de una enzima enteropetidasa encargada de la activación del tripsinógeno en tripsina a partir de la cual la propia tripsina actúa de manera catalítica sobre nuevas activaciones de tripsinógeno y la activación de los demás simógenos secretados por el páncreas el quemotripsinógeno equimotripsina la probe las tasas en las tasas y
la procarboxipetidasa en carbox y péptidasa la actividad de estas exoproteasas y endoproteasas son las que permiten entonces la degradación de la masa más importante de la proteína de la dieta en aminoácidos y oligopéptidos a nivel del ribete en cepillo se expresan endopeptidasas aminopetidasas y dipeptidasas que son las que permiten entonces completar el proceso digestivo de estas unidades de oligopéptidos logrando obtener como producto aminoácidos libres dipéptidos y trepéptidos que van a ser absorbidos a través de diferentes sistemas de transporte entre los principales los aminoácidos serán absorbidos a través de un cotransporte Pon sodio los dipéptidos y
tripéptidos a través de un cotransportes con protones en donde finalmente a nivel del enterocito la actividad de algunas diversidad así trepéptidasas permitirán obtener los aminoácidos libres que en el pasado esa circulación para formar parte del pool de aminoácidos que circulan el 75% de los alineados obtenidos por degradación de proteínas tisulares son reutilizados para reconstituir las proteínas celulares ese 25% de aminoácidos sumados a los aminosos obtenidos a partir de la absorción de las proteínas digeridas de la dieta pueden ser utilizados como veremos más adelante para la síntesis de productos especializados derivados de estos aminoácidos y Dado
que los aminoácidos no se almacena A diferencia de glucosa y de los ácidos grasos todo exceso de aminoácidos que no puede ser utilizado pasará un proceso catabólico en ese proceso de agradación de aminoácidos veremos como la molécula separa el nitrógeno del esqueleto carbonado siguiendo cada uno de ellos destinos metabólicos diferentes veremos como el nitrógeno finalmente es eliminado a través de la urea por la vía renal y el esqueleto y los sus esqueletos carbonados podrán ser utilizados para diferentes procesos celulares entre los que encontramos la síntesis de ácidos grasos procesos gluconeogénicos procesos cetogénicos ciclo de krebs
y síntesis de otras moléculas como puede ser el colesterol analicemos entonces en detalle Cómo es el proceso catabólico de los aminoácidos tanto en la eliminación del grupo amino como en el destino de la cadena carbonada el proceso de degradación de los aminoácidos implica la separación del grupo amino de sus cadenas carbonada la separación del grupo amino es un proceso que requiere de la actividad de una familia enzimas las aminotransferasas que realizan la distribución de grupos aminos entre aminoácidos y cetoácidos y la actividad de la glutamato es hidrogenasa para producir finalmente la deceminación del glutamato y
dar como producto amonio dado que la amonio es una molécula altamente tóxica se requieren de sistemas de transporte y eliminación no tóxico para finalmente permitir su eliminación a través de la urea por el otro lado el esqueleto carbonado resultante podrá ser metabolizado en diferentes destinos para la producción de glucosa para la producción de acetilcoa e integral del ciclo de krebs y procesos anacleróticos relacionados para la síntesis de cuerpos cetónicos en relación con los procesos de eliminación del grupo amino vamos a ver tres ítems para analizar por un lado hablaremos de las transaminaciones estas reacciones de
distribución de grupo amino por el otro lado hablaremos de la diseminación oxidativa catalizada por la glutamato deshidrogenasa para finalmente producir la desaminación y finalmente hablaremos del transporte no tóxico de amonio la transaminación es un proceso catalizado por una familia de enzimas denominadas aminotransferasas o transaminasas estas enzimas catalizan una reacción reversible entre un aminoácido y un cetoácido requieren fosfato de piridoxal como cofactor Y si bien participan de los procesos de eliminación del grupo amino en realidad su función principal es la distribución de grupo amino entre aminoácidos dado que siempre vamos a encontrar como parte de las
transaminaciones la dupla glutamato alfasetoglutarato conocemos algunos ejemplos de estas transaminasas la alanina minotranferasa que permite la eliminación del grupo amino de la alanina dando piruvato como producto laspartato aminotranferasa que realiza la eliminación del grupo amino de la espartato dando como resultado en oxal acetato y por ejemplo la fenera lanina transaminasa una enzima que elimina el grupo amino de la fenilalanina para formar fenil piruvato fíjense que en cada uno de estos tres ejemplos Hay una dupla que se mantiene constante esa dupla es el glutamato y el alfasetoglutarato que participa de todas las transaminaciones Esto es lo
que permite entonces reconocer que las transaminasas actúan como una red en donde el alfa se tolucarato y el glutamato funcionan como los nudos de esa red Y de esa manera dado que la constante de equilibrio de estas enzimas está cercado a uno pequeños variaciones en un lado de la reacción permiten volcar en sentido contrario la transaminación Y de esa manera llevar nitrógeno para aquellos aminoácidos que así lo requieran por otro lado dijimos que había reacciones en donde se eliminaba ciertamente el grupo amino La glutamato es hidrogenasa es la enzima responsable de este proceso una enzima
que encontramos a nivel mitocondrial y que también cataliza una reacción reversible en este caso el glutamato se desamina generando alfarato y amonio como producto pero la glutamato es hidrogenasa también tiene la capacidad de poder catalizar la aminación del alfabeto luterato para formar glutamato la glutamato es hidrogenasa es una enzima finamente regulada en donde altos niveles energéticos bajo la forma de gtp y nadache inhiben a la enzima Mientras que el adp como indicador de baja energía o la leucina estimulan digamos la reacción de desaminación este esta reacción catalizada por la glutamato de cirogenasa es un punto
anaplerótico que está plerotico del ciclo de krebs dado que permite la liberación del alfase tolutarato para la síntesis de glutamato y que el glutamato participe de otros procesos anabólicos o termina siendo el punto final del catabolismo de aminoácidos dado que las transaminaciones vía glutamato terminará eliminando el grupo amino como amonio disponiendo al fase glutarato a este ciclo de krebs nuestro tercer punto de análisis tiene que ver con el transporte no tóxico de amonio vamos a ver tres procesos Implicados En en este sentido el ciclo de la glucosa lanina el ciclo de la glutamina glutamato y
la síntesis de tal manera que existe una interrelación entre aquellos tejidos con alto metabolismo de aminoácidos el músculo esquelético el sistema nervioso central el riñón el intestino y el hígado que son los encargados de mantener este equilibrio en la formación y la utilización de amonio a través de la síntesis de alanina a través de la síntesis de glucosa y a través de la síntesis Brea el ciclo de la glucosa lanina o ciclo de la alanina es un ciclo en el que intervienen por un lado el músculo que en condiciones de actividad produce amonio como resultado
de la actividad de la enzima de nilato quinasa y la amp de amenaza este amonio a través de la glutamato deshidrogenasa forma glutamato junto con el catabolismo de los aminoácidos ramificados que se dan específicamente en el músculo esquelético y en condición de contracción El piruvato obtenido por la delegación de la glucosa se transamina con este glutamato para formar a la niña lalanina puesta en circulación es Entonces metabolizada por el hígado nuevamente a través de la alaninaminotranferasa generando por un lado piruvato o por vía gluconeogénica puede producir glucosa cerrando si las condiciones metabólicas lo permiten el
ciclo de la glucosa alanina y como consecuencia de la transaminación de la alanina se genera glutamato a nivel hepático que por acción de la glutamato es hidrogenasa produce amonio que será metabolizado como veremos posteriormente a través del ciclo de la urea el glutamato forma un ciclo con la glutamina a través de la aminación catalizada por la glutamina sin tetaza y a través de la desaminación de la glutamina por acción de la glutaminasa la glutamina sintetasa es una enzima altamente regulada dada la importancia que tiene la glutamina a nivel del metabolismo celular es precursor de la
síntesis de triptófano de cargamil fosfato de glucosamina disciplina es un dador de grupos aminos en muchos procesos Este metabólicos Y de esa manera la célula requiere un control estricto sobre la síntesis del nuevamente el ciclo glutamatoglutamina permite reconocer como los cinco principales tejidos relacionados con el metabolismo de aminoácidos se integran para poder permitir el transporte de amonio en forma no tóxica la glutamina es el aminoácido principal que encontramos en circulación como consecuencia de estos procesos analicemos entonces en particular la participación de cada uno de estos tejidos a nivel del músculo esquelético nuevamente como consecuencia de
la contracción muscular se produce amonio por actividad de la ampp de amenaza En consecuencia el músculo expresa glutamina sin tetaza que permite la formación de glutamina y su pasaje a circulación a nivel renal la actividad glutaminasa y glutamato de cirogenasa permite la obtención de amonio a partir de la glutamina y en segunda instancia a partir de glutamato este amonio es importante para La regulación que hace la célula renal del equilibrio ácido base por otro lado la integración del Alfa se tolutarato al ciclo de krebs permite que el riñón en condiciones de ayuno prolongado induzca las
enzimas gluconeogénicas y en consecuencia tenga capacidad de formación de glucosa a nivel del sistema nervioso central se establece un ciclo glutamato glutamina entre el astrocito y la neurona el glutamato es el neurotransmisor excitatorio más importante del sistema nervioso y ocupa aproximadamente el 80% de la neurotransmisión excitatoria Este glutamato es el resultado de la actividad glutaminasa presente en el neurona que disamina a la glutamina y que generen consecuencia amonio que es metabolizado por el astrocito el astrocito tiene la capacidad a través de la actividad glutamina sin detasa de poder equilibrar tanto el ingreso de amonio desde
circulación como el reciclaje del amonio producto de la actividad glutaminasa a nivel de la neurona de esa manera el astrocito es una célula fundamental para poder equilibrar los niveles de amonio a niveles del sistema nervioso central a nivel hepático vale la pena considerar algunas este características particulares metabólicas que encontramos entre los hepatocitos más cercanas a la zona periportal de los hepatocitos más cercanos a la zona centro de lobulillar vamos a encontrar que aquellos hepatocitos más periportales tienen una alta expresión de glutaminasa es decir la enzima que permite la desaminación de la glutamina y en consecuencia
producir amonio que va a poder ser metabolizado a través del ciclo de la urea mientras que a nivel de los hepatocitos más centros lobulillares lo que encontramos es una mayor actividad de glutaminas entretasa para poder metabolizar No solamente la moño que el propio hígado está produciendo sino también de todo aquel amonio que se escapa de los hepatocitos periportales y que digamos para evitar su circulación son metabolizados por estos hepatocitos centro-lobulillares de tal manera que minimiza los efectos tóxicos que pueden ocurrir como consecuencia de la presencia de amonio en sangre la mucosa intestinal también presenta actividad
glutaminasa y glutamina sin tetaza los enterocitos utilizan glutamina como combustible energético En consecuencia a través de la actividad glutaminasa glutamato deshidrogenasa integran alfasetoglutarato al ciclo de krebs con fines energéticos y dan como resultado la producción de amonio que pasa circulación para poder ser detoxificado a nivel hepático por el otro lado la microbiota intestinal es gran productora de amonio razón por la cual el digamos las células de la mucosa intestinal al expresar glutaminas de tasa permiten va aferrear un poco la cantidad de este amonio produciendo glutamina para poder ser digamos exportada circulación y exportando parte también
del tamaño producto de la actividad microbiana se estima que aproximadamente el 50% del amonio que diariamente se produce es de origen bacteriano en 1932 Hans crepes yin publican un trabajo en donde describen como la urea en el hígado se sintetiza a partir de amonio como un subproducto de la graduación de proteínas a través de un conjunto de reacciones cíclicas en donde la rutina es uno de los intermediarios más importantes de hecho el nombre original de esta vía metabólica fue el ciclo de la ornitina que posteriormente fue denominado ciclo de la urea vamos a analizar Entonces
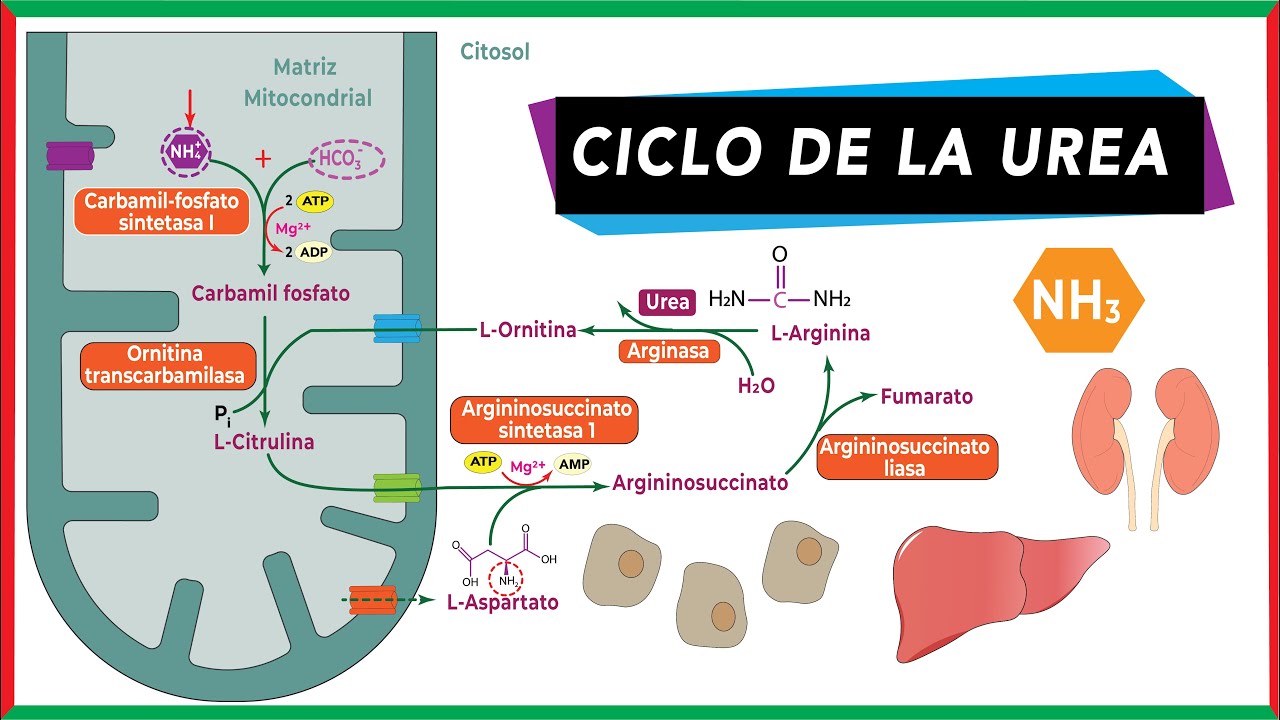
los aspectos más importantes del ciclo de la urea una vía metabólica mitocondrial y también citoplasmática el primer término vamos a remarcar el origen del amonio mitocondrial la glutamina y el glutamato se desaminan para producir amonio junto con el bicarbonato y en presencia de ATP catalizado por la caramil fosfato sintetasa 1 forman car mamífosfato el carbohil fosfato es sustrato del ciclo se condensa con una manejo de arritina para formar un intermediario llamado citrulina que se exporta al citoplasma otro punto rescatable de este ciclo es la incorporación del aminoácido aspartato que aporta un segundo nitrógeno a lo
que finalmente va a ser la molécula de la urea este apartato proviene de la reacción catalizada por laspartato aminotranferasa sobre el oxal acetato otro punto importante a tener en cuenta en este ciclo es la presencia de arginina como intermediario del ciclo de la urea la arginina por acción de la arginaza da finalmente urea como producto y vuelve a poner en el ciclo a la ornitina la misma hornitina que se utilizó para poder condensar con ese carnamífosfato para generar citrulina como primera intermediario del ciclo la expresión de arginasa a nivel citosólico es exclusiva en el hígado
razón por la cual el hepatocito es la única célula que tiene todas las enzimas necesarias para poder producir este ciclo metabólico existe expresión de arginaza en otros tejidos un arginaza y su enzima mitocondrial que también puede generar a partir de arginina urea pero no con los fines que estamos nosotros analizando es decir urea como producto de la detoxificación de amonio generada a partir de los procesos de desaminación de la glutamina y del glutamato desde el punto de vista energético podemos observar que el ciclo requiere de cuatro moléculas de ATP dos ATP en la primera reacción
catalizada por por la caramelo fosfatos intestasa uno y dos ATP finalmente dado que en la reacción catalizada por la arginina suctinato sin tasa este ATP genera amp y pirofosfato como productos otro punto para tener en consideración es La regulación del ciclo el ciclo de la urea regula su actividad principalmente a nivel de la carmamil fosfatosintetasa 1 que utiliza como modulador a lo estérico positivo una molécula formada a partir de acetilcoa y de glutamato el n acetil glutamato es el modulador a los térico de la caramil fosfatosintetasa 1 vale la pena tener en cuenta que el
ciclo en la urea es un ciclo metabólico que está continuamente funcionando como habíamos dicho al principio de la presentación los aminoácidos no se almacenan razón Por lo cual todo exceso de aminoácidos será catabolizado y en consecuencia habrá producción de amonio en distintas condiciones metabólicas postprandial como consecuencia de un potencial exceso de aminoácidos provenientes de la ingesta y en ayuno como consecuencia de la utilización de los aminoácidos por ejemplo con fines gluconeogénicos es decir que dependiendo de las condiciones metabólicas el ciclo por a acelerar o disminuir su tasa metabólica pero es continua la necesidad de poder
detoxificar el amonio generado como consecuencia de los procesos metabólicos a nivel de los tejidos y del propio hígado a través de este ciclo como podemos observar en este esquema existe una relación directa entre el ciclo de la urea y el ciclo de krebs ya que el aspartato sustrato del ciclo de la urea es producto de la transaminación del oxal acetato intermediario del ciclo de krebs y que el fumarato producto del arginino succinatoliasa puede ser reconvertido en malato Para volver a integrarse al ciclo de krebs habiendo analizado los procesos relacionados con la eliminación del grupo amino
nos queda ahora resolver qué es lo que sucede con las cadenas carbonadas de estos aminoácidos independientemente de la complejidad que podamos observar en el catabolismo de las cadenas carbonadas de cada uno de los aminoácidos este esquema nos muestra de manera clara el concepto de convergencia de vías metabólicas fíjense como distintos aminoácidos terminan degradándose a intermediarios comunes del metabolismo intermedio acetilcoa piruvato intermediarios del ciclo de krebs es decir independientemente de los pasos necesarios para catabolizar cada una de esas cadenas carbonadas Si nosotros reconocemos la consideración metabólica en la cual analizar este fenómeno podemos reconocer el destino
finalmente que van a tener esas cadenas carbonadas en este sentido fíjense como algunas cadenas carbonadas generan piruvato y en consecuencia tiene la capacidad de vía acetilcoa integrarse al ciclo de krebs con lo cual las cadenas carbonadas de esos aminoácidos puedan ser reconocidas como potenciales sustratos energéticos por el otro lado pensemos en aminoácidos cuyas cadenas carbonadas terminan generando acetilcoa que también podrán integrarse al ciclo de krebs y en consecuencia también podrán ser reconocidos como sustratos energéticos sin embargo también vale la pena considerar que dependiendo de las condiciones metabólicas por ejemplo en el hígado esos destinos metabólicos
van a poder ser modificados según se hable de situaciones de ayuno o situaciones postprandiales en este sentido podemos encontrar aminoácidos cuyas cadenas carbonadas terminarán siendo sustratos gluconeogénicos o aminoácidos cuyas cadenas carbonadas terminarán siendo sustratos cetogénicos más aún algunos aminoácidos podrán dar tanto precursores para la síntesis de cuerpos cetónicos como precursores para la síntesis de glucosa por ejemplo tenemos el triptófano que genera piruvato pero el mismo triptófano también genera acetilcoa es decir son aminoácidos que tienen capacidad mixta sus productos de degradación pueden ser utilizados tantos como sustratos gluconeogénicos como sus tratos cetogénicos es decir el destino
de las cadenas carbonadas se explica entendiendo la condición metabólica y el tejido en el cual se están considerando el músculo esquelético es el tejido principal para el catabolismo de los aminoácidos ramificados la valina la isoleucina y la leucina son metabolizados por ese tejido el tejido muscular y sus cadenas carbonadas pueden ser utilizadas con fines energéticos el hígado es el gran metabolizador de aminoácidos y sus cadenas carbonadas las derivará de acuerdo a condiciones metabólicas en condición de ayuno integrará las cadenas carbonadas al ciclo de krebs Y desde ahí a los procesos catapleróticos que pueden estar relacionados
llámese síntesis de ácidos grasos síntesis de colesterol o inclusive energía en condición de ayuno sus cadenas carbonadas podrán ser utilizados para la síntesis de glucosa o podrán ser utilizadas para la síntesis de cuerpos cetónicos volviendo a nuestro mapa conceptual hemos analizado como el recambio de proteínas celulares se establece entre los procesos de degradación y los procesos de reutilización de los aminoácidos para el mantenimiento de esas proteínas que las proteínas de la dieta son una fuente importante de aminoácidos sobre todo aquellos aminoácidos que son esenciales aminoácidos que van a digamos van a sumarse al pool de
ameninese aminoácidos necesarios para el mantenimiento de las proteínas celulares hemos analizado que Dado que los aminoácidos no se almacenan un porcentaje de esos aminoácidos no utilizados van a ser catabolizados en este sentido eliminaremos el nitrógeno a través de la urea y sus esqueletos carbonados serán utilizados para diferentes procesos dependiendo del tejido y la condición metabólica este analizada finalmente los aminoácidos además de ser las moléculas centrales o las unidades monométricas básicas para la síntesis de proteínas pueden cumplir con otras funciones celulares en este sentido hablemos un poco de Quiénes son estos productos especializados derivados de los
aminoácidos hay toda una variedad de moléculas que utilizan aminoácidos como precursores de síntesis más aún en muchos casos son los propios aminoácidos los que ejercen una actividad metabólica independientemente de formar parte de las proteínas así hablamos digamos hace un rato de El glutamato de la glutamina del aspartato este entre otros dentro de los productos especializados podemos encontrar las porfirinas los nucleótidos la creatina reclutatión todo un conjunto de moléculas obtenidas por descarboxilación de esos aminoácidos que son las aminas biógenas el óxido nítrico la melanina la niacina hormonas tiroideas henosis metionina fíjense la variedad de productos que
utilizan aminoácidos como precursores demos algunos ejemplos en particular para completar este ítem el emo requiere para su síntesis de glicina y sucsimilcoa un proceso que comienza en la mitocondria y que básicamente tiene como objetivo formar este anillo de tapirriólico que posteriormente por acción de la feria tarza unirá hierro para formar este grupo la metionina es un aminoácido muy central en el metabolismo celular participa de procesos de autofagia participa como sensor de nutrientes participa en la síntesis de proteínas es fundamental en el balance redox en el metabolismo de las poliaminas en elmetismo del ácido fólico y
en los procesos que tiene que ver con la metilación perdón de moléculas en este sentido es a través de la formación de la s adenosilmetionina que ocurren estos fenómenos de metilación de ADN de proteínas de lípidos de síntesis de otras moléculas y en el cual la metionina es fundamental la metionina un aminoácido que a través de su ciclo se encuentra integrando no solamente estos procesos que permiten metilar moléculas sino también la síntesis de cisteína la síntesis de glutatión como vamos a ver ahora y su relación estrecha con el metabolismo del ácido fólico que conduce también
a integrarlo a la síntesis de purinas a la síntesis de pirimidinas y finalmente a la síntesis de ADN la creatina la creatina la formamos a nivel de las células renal usando glicina y arginina que forman un intermediario o en idino acetato que el hepatocito metila utilizando ese de nación mitianina para formar finalmente la creatina esta creatina puesta en circulación es tomada por las células Diana uno de los sitios principales es el músculo esquelético para formar vía creativa una molécula de alta energía el glutatión el glutatión es un tripéptido formado por glutamato por cisteína y por
glicina lo reconocemos como un importante molécula que participa en los procesos antioxidantes celulares a través de su relación glutatión reducido glutatión oxidado permitiendo a través de la glutatión oxidasa reducir peróxidos y recomponer los niveles de glutatión reducidos por la glutatión reductasa en presencia de Nat pH por otro lado el glutatión participa de procesos de absorción de aminoácidos tanto a nivel de los enterocitos en la mucosa intestinal como también a nivel de las células de los túbulos renales en este sentido por acción de la enzima Gamma glutamil transpeptidasa a nivel de la membrana el aminoácido se
incorpora Sí al glutatión para formar un intermediario glutatión aminoácido que permite el ingreso de la aminoácido a la célula regenerando luego el glutatión en su forma reducida existen en las células un grupo de enzimas que son descarboxilasas de aminoácidos es decir producen la eliminación del grupo carboxilo dejando en consecuencia la cadena o el esqueleto carbonado con el grupo amino uno de los aminoácidos Versátiles que producen en consecuencia este grupo de moléculas terminadas a Minas biógenas es la tirosina la tirosina e vía tirosina hidroxilasa produce ldopa una molécula que puede tomar un camino metabólico hacia la
síntesis de melanina y un camino metabólico por la aminoácido de carboxilasa para formar dopamina como neurotransmisor que por una hidroxilasa puede formar noradrenalina como neurotransmisor y que por una n metil transferasa es decir por una enzima que permite la metilación sí de el grupo amino de la nueva adrenalina Perdón formar la adrenalina de esta manera la tirosina es precursora de dopanimia dopamina y noradrenalina como neurotransmisores centrales del sistema nervioso central de los pigmentos este derivados de la melanina y de la hormona adrenalina otros aminoácidos sí que son metabolizados a través de aminoácidos de carboxilasas triptófano
para la formación de serotonina del glutamato para la formación del gaba el ácido gama minobutírico el neurotransmisor inhibitorio central este más importante del sistema nervioso central de la histidina para formar la histamina un producto importante La regulación de la secreción del ácido clorhídrico un neurotransmisor también el sistema nervioso central un mediador de procesos inflamatorios entonces habiendo analizando un poco el contexto del catabolismo de aminoácidos pasemos a ver algunas ideas claves este para remarcar existe una continua degradación y síntesis de proteínas celulares se produce aproximadamente entre 1 y 2% de recambio de proteínas corporales diariamente aproximadamente
el 75% de los aminoácidos liberados por degradación de proteínas y reutilizan y Dado que los aminoácidos no se almacenan el resto se degrada rápidamente la fuente de aminoácidos intracelulares requiere de la actividad del protiosoma y de los procesos de autofagia Mientras que el aporte de aminoácidos de origen dietario implica la digestión de proteínas y la posterior absorción de los mismos la mayor parte de los esqueletos de carbono de los aminoácidos se convierte en intermediarios en fibólicos mientras que en los humanos el nitrógeno amínico se convierte en urea y se excreta por la orina el proceso
digestivo de las proteínas comienza por acción de la pepsina a nivel gástrico cataliza la hidrólisis de proteína generando algunos péptidos libres y aminoácidos importantes para el control de la secreción de gastrina y en consecuencia del ácido clorhídrico por parte de las células parietales la secreción de un jugo pancreático que contiene un conjunto de simógenos que a nivel del intestino una vez activados catalizan degradación de proteína generando aminoácidos libres y oligopéptidos la presencia de peptidasas y aminopeptidasas a nivel de ribete en cepillo completa la hidrólisis de los oligosacáridos produciendo aminoácidos libres dipéptidos y tripéptidos la absorción
de aminoácidos se realiza a través de varios sistemas de transporte para distintos grupos de aminoácidos por mecanismos de cotransporte con sodio a nivel de la membrana luminal e independientes de sodio en la membrana vaso lateral de los enterocitos la absorción de dipéptidos y tripéptidos se realiza por un mecanismo de cotransporte con protones los vertebrados superiores convierten el amonio en urea mientras que los peces lo excretan de manera directa y las aves y los reptiles lo convierten en ácido úrico la transaminación canaliza el nitrógeno de los aminoácidos hacia glutamato y permite la distribución de grupos aminos
entre ellos la glutamato deshidrogenasa ocupa una posición fundamental en el metabolismo del nitrógeno ya que participan de la desaminación de glutamato generando amonio y también puede catalizar la reacción de aminación del Alfa se tolutarato con formación de glutamato dada la toxicidad de amonio el organismo logra el transporte y la eliminación de amonio en forma no tóxica a través de la síntesis de glutamina la síntesis de la Lina y el ciclo de la urea en el hígado el intestino el músculo esquelético el sistema nervioso central en particular neurona antrocito y el riñón la expresión de las
enzimas glutaminas y tetasa que cataliza la síntesis de glutamina a partir de glutamato y amonio y o de la enzimaglutaminasa que cataliza la desaminación de glutamina a glutamato y amonio Establece en un ciclo glutamatoglutamina que permite el manejo intracelular y el transporte de amonio en forma no tóxica el músculo esquelético en actividad deriva piruvato en la síntesis de alanina para eliminar amonio producido por la actividad conjunta de la ninja toquinasa a MP de amenaza y del catabolismo de aminoácidos ramificados en el hígado el amonio producido por diseminación oxidativa del glutamato o desaminación de la glutamina
es junto a dióxido de carbono y aspartato sustratos necesarios para la síntesis de urea la forma principal de eliminación de nitrógeno derivado del metabolismo de los aminoácidos la síntesis durea en el hígado tiene lugar en parte en la matriz mitocondrial y en parte en el citosol los cambios de las concentraciones de enzima y La regulación en losteri de la carbamil fosfato sintetasa 1 morenacetil glutamato regulan la síntesis de urea a nivel hepático las cadenas carbonadas generadas a partir del catabolismo de aminoácidos se metabolizan dando como productos piruvato o acetilcoa y o intermediarios del ciclo de
krebs En consecuencia según la condición metabólica podrán ser sustratos gluconeogénicos o cetogénicos energéticos o para la síntesis de lípidos los aminoácidos Más allá de ser las unidades monoméricas para la formación de proteínas pueden participar de otras funciones celulares Como por ejemplo neurotransmisores precursores utilizados para la síntesis de hormonas precursores utilizados para la síntesis de neurotransmisores creatina coenzimas porfirinas glutatión óxido nítrico entre otros productos en fin hemos analizado un poco los aspectos principales sobre el metabolismo de aminoácidos básicamente el catabolismo de los aminoácidos nos vemos en un próximo encuentro hasta luego