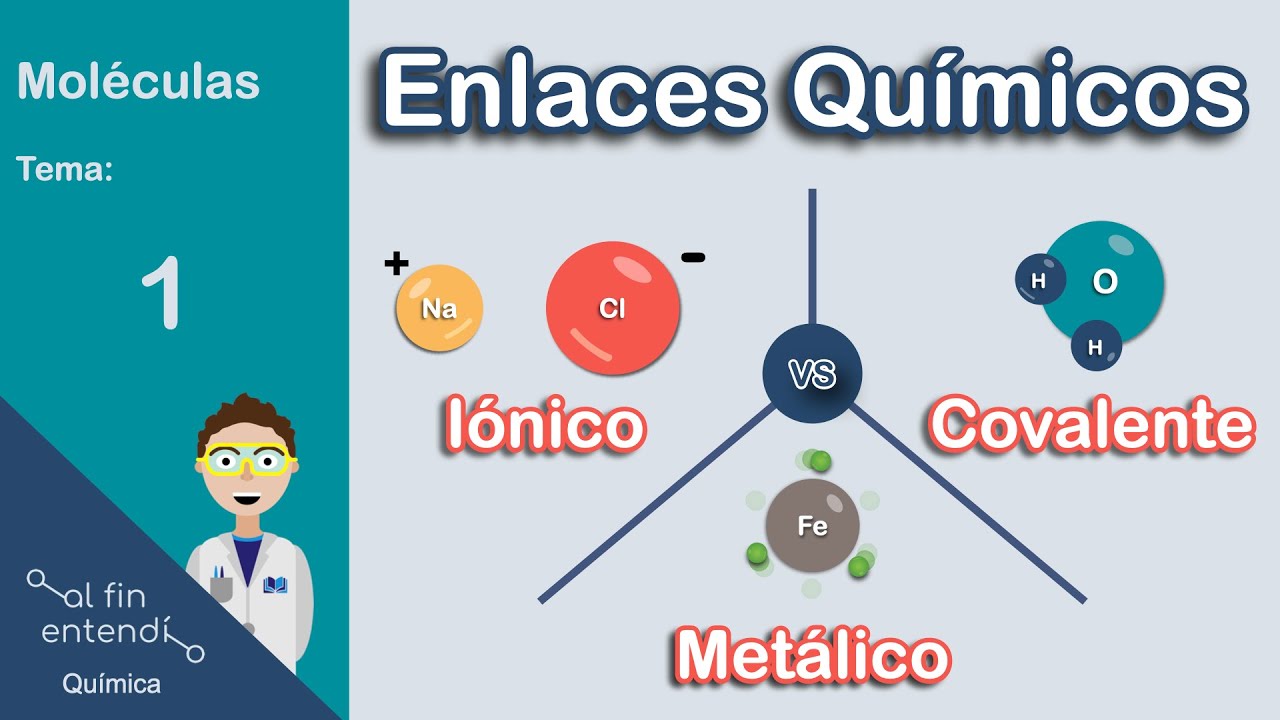
hola a todos hoy para acabar este quinto bloque de al fin entendí química vamos a entender cómo se puede relacionar una molécula con otra o sea vamos a aprender qué son y para qué sirven las interacciones químicas y para eso tenemos la trivia del día y animal puede permanecer sumergido en el agua el mayor tiempo posible una ballena un escarabajo acuático o un delfín [Música] [Aplausos] lo primero que tenemos que hacer es diferenciar entre un enlace químico y una interacción química como vimos en otro vídeo los enlaces son fuerzas de atracción intra moleculares o sea
unen átomos para formar moléculas ahora por el otro lado las interacciones químicas también son fuerzas de atracción pero son fuerzas inter moleculares es decir que gracias a ellas una molécula se puede sentir atraída por otra eso es todo el chiste habrá interacciones muy fuertes y otras más débiles pero en sí todas hacen lo mismo van a mantener a las moléculas muy unidas entre ellas oa veces también hasta los iones pero cualquiera que sea esta interacción son fuerzas electroestáticas entonces todas van a ocurrir de una manera similar todas ocurren cuando algo positivo se acerca a algo
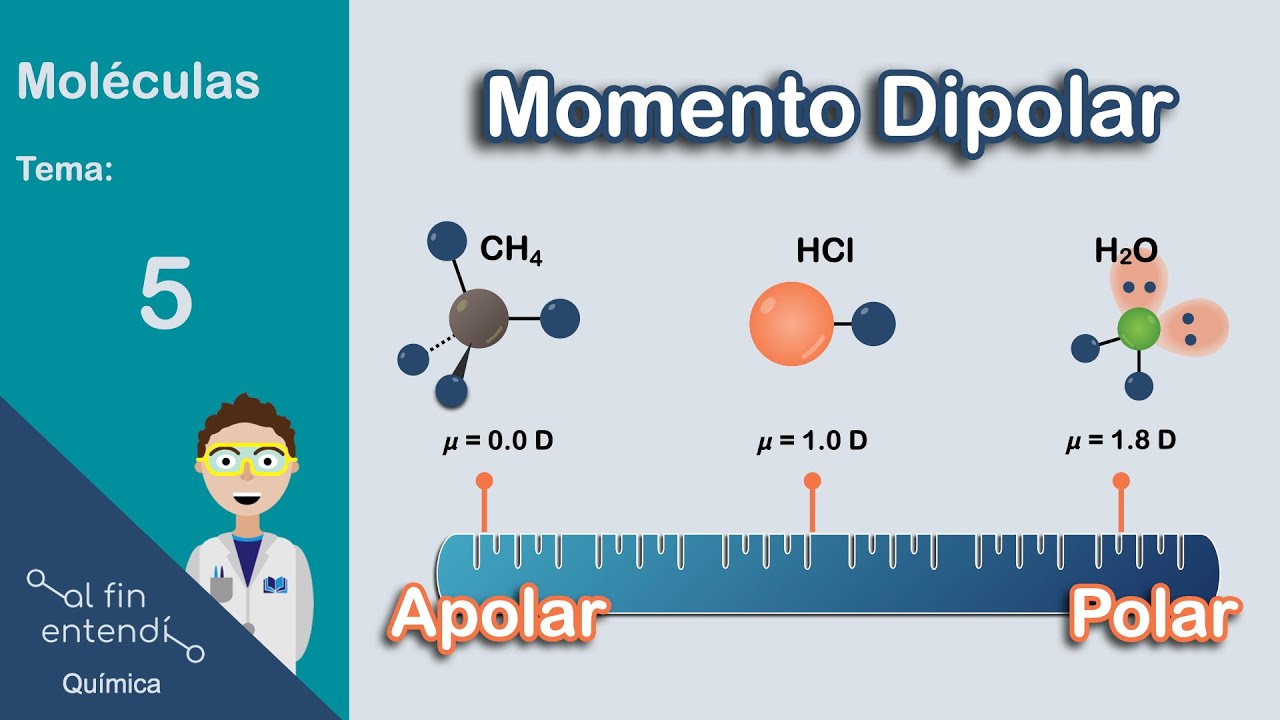
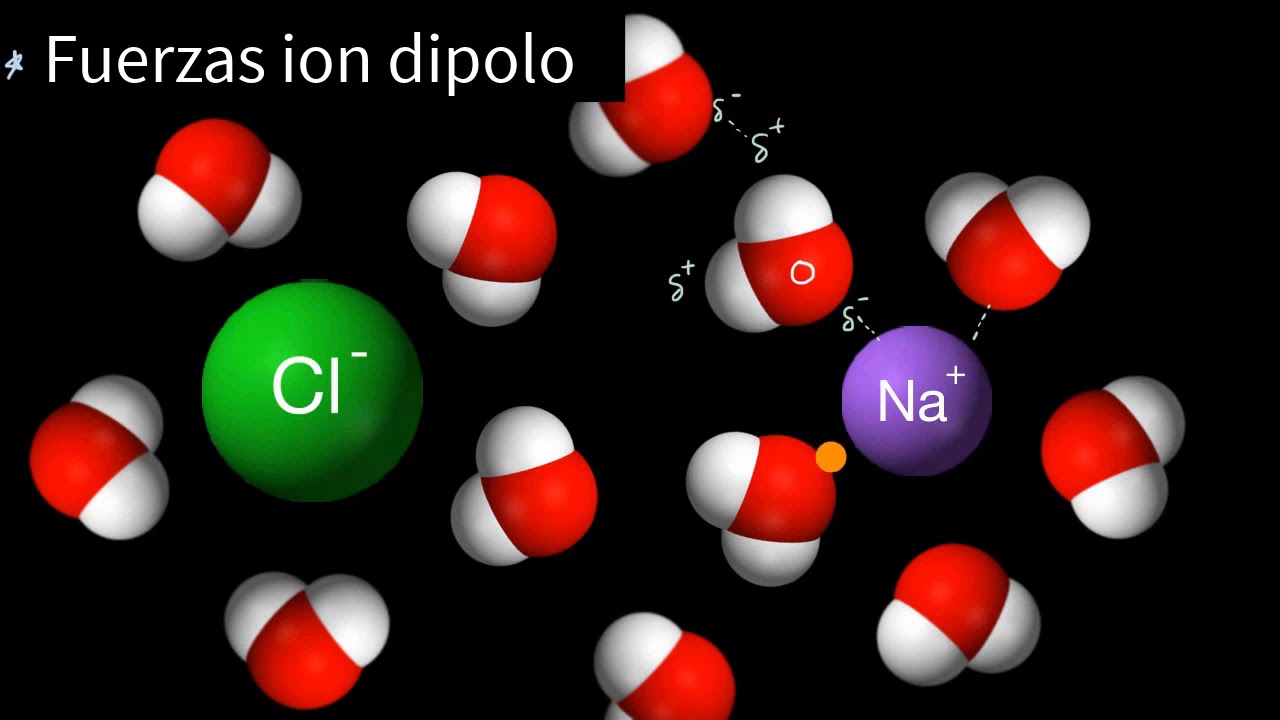
negativo ya sabemos que las cargas contrarias se atraen en realidad nuestro único trabajo aquí es aprender a diferenciar qué interacción se puede formar y para eso ya aprendimos que existen los iones las moléculas polares o sea las que tienen dipolos y las moléculas polares las que no tienen ninguna carga parcial acá arriba te dejo un link por si necesitas recordar un poco de esto pero en fin empecemos con la interacción jones de polvo esta interacción se forma entre unión osea un átomo con carga y una molécula polar esas que tienen un polo positivo y un
polo negativo como puede ser el agua o el amoniaco en sí la única condición es que si hablamos de un catión o sea unión positivo se le tiene que acercar el polo negativo de otra molécula y viceversa si tenemos una unión su carga negativa va a atraer los polos positivos esa es la interacción ión dipolo ahora las siguientes interacciones a veces les llaman fuerzas de van der waals en honor al científico que describió cómo ocurre todo esto pero son tres distintas la más fácil de ellas es la interacción dipolo dipolo si te fijas el nombre
nos dice todo dipolo dipolo se refiere a que una molécula polar se va a sentir atraída por otra molécula polar o sea una molécula de agua puede sentirse atraída por otra molécula de agua o una molécula de amoniaco o segunda con otra demoniaco o una molécula de agua puede sentir atracción por una molécula de amoniaco las interacciones no necesariamente ocurren entre moléculas iguales pueden ser diferentes y similar al caso anterior específicamente ocurre cuando el polo positivo de una molécula atrae al polo negativo de la otra de hecho existe una interacción dipolo dipolo tan común y
tan importante que tiene su nombre propio el puente de hidrógeno es algo así cuando un átomo de hidrógeno se une a uno de oxígeno de nitrógeno o de flúor el hidrógeno se queda con un dipolo muy positivo entonces cuando se con el otro extremo el dipolo negativo también es muy grande por lo tanto como estamos acercando un dipolo muy positivo a uno muy negativo la atracción es muy fuerte esa es la característica principal del puente de hidrógeno para separar moléculas que pueden formar puentes de hidrógeno es muy difícil por ejemplo no sé si conocerás la
molécula de adn esta es una molécula que mantiene todo nuestro material genético o sea la información que dice a nuestro cuerpo como debe de funcionar o como va a ser pero lo especial de esta molécula es que puede formar muchos puentes de hidrógeno entonces eso le otorga una estructura muy fuerte muy resistente eso es muy útil para poder pasar esta molécula de una generación a otra sin que se destruya pero en fin al final veremos un poco más sobre los puentes de hidrógeno por ahora veamos cómo se pueden atraer las moléculas que no tienen ni
nada positivo ni nada negativo las moléculas polares hay dos formas una de ellas es gracias a la interacción dipolo dipolo inducido que ocurre cuando una molécula polar se acerca a una no polar como los gases y atómicos o el dióxido de carbono o incluso los gases nobles que aunque son átomos solos también pueden formar esta misma interacción y ocurre más o menos así imaginemos la densidad electrónica del agua como es polar tiene su zona de baja densidad y una de alta densidad recuerda que la zona de alta densidad es donde están los electrones la mayoría
del tiempo y genera justamente el polo negativo ahora el león como es no polar tiene una nube electrónica muy equitativa digamos que la distribución de electrones es muy pareja entonces cuando el agua se acerca lo suficiente su alta densidad de electrónica o sea su polo negativo repele los electrones del neón y eso provoca que su nube electrónica se vaya deformando prácticamente es como si los electrones del agua empujaron a los electrones del neón ya sabemos que lo negativo aleja lo negativo y cuando la nube electrónica se deforma lo suficiente se puede formar un dipolo inducido
es igual a un dipolo permanente o un dipolo verdadero como el del agua solo que se necesitaba de esto que alguien empujara sus electrones y ahora que tiene un polo positivo y uno negativo el león ya puede sentir atracción por las moléculas polares es la interacción dipolo dipolo inducido y aunque se parezca mucho al caso anterior hay una diferencia importante y es la fuerza de atracción entre las moléculas por ejemplo la interacción fuente de hidrógeno es la más fuerte de todas es muy difícil romperlos después seguiría una interacción dipolo dipolo regular y la más débil
sería la interacción dipolo dipolo inducido hasta ahora la interacción más débil de todas son las fuerzas de dispersión o fuerzas del london vamos a representar las con un átomo de helio que tiene dos electrones así es más fácil de visualizar esta interacción y de animarla y bueno en sí ambos electrones están moviéndose todo el tiempo en su orbital pero no es un movimiento uniforme es algo totalmente aleatorio que no podemos predecir entonces en cierto momento puede llegar a ocurrir que ambos electrones se encuentren del mismo lado por así decirlo y eso provoca aunque sea por
un instante que se presente un dipolo a eso le llamamos justamente dipolo instantáneo y literalmente es instantáneo en un lo ves ya el otro ya no ese tipo lo va y viene rápidamente pero en ese momento que existe el dipolo instantáneo puede inducir dipolos en otras moléculas de esta manera incluso las moléculas polares pueden sentir una muy leve atracción entre ellas porque siempre habrá algunos dipolos instantáneos y dipolos inducidos esas son las fuerzas de dispersión de london al final de cuentas sea cual sea la interacción química la gran importancia de todas ellas es que van
a definir muchas de las propiedades físicas de las sustancias por ejemplo seguro habrás escuchado que la diferencia entre los tres estados de la materia es que tan cercanas están unas moléculas de otras en los gases las moléculas están muy alejadas unas de otras y se pueden mover mucho en los líquidos están relativamente cerca y tienen cierta movilidad sin embargo las moléculas de un sólido están muy juntas entre ellas y precisamente pueden estar muy juntas unas y otras gracias a las interacciones químicas entonces aquí podemos deducir en los sólidos existen muchas interacciones químicas en los líquidos
si hay interacciones pero no tantas y en los gases casi no hay interacciones químicas las moléculas están cada quien por su lado porque no sienten atracción otro ejemplo de la importancia de las interacciones es cuando disolvemos algo el proceso de disolución es simplemente agregar un sólido a un líquido y mover hasta que se generen nuevas interacciones químicas si imaginamos un sólido por ejemplo la sal el cloruro de sodio pensaríamos en muchos guiones juntos los iones positivos unidos a los negativos pero una vez que los metemos en un líquido por ejemplo el agua y empezamos a
mezclar y a provocar mucho movimiento las moléculas del agua pueden interaccionar con las del sólido en este caso con los iones y si se dan las condiciones apropiadas las moléculas de agua pueden llegar a romper las fuerzas que mantienen unidos a los iones y separarlos eso significa que se pudieron formar interacciones químicas entre los iones y las moléculas de agua que en este caso específico serían interacciones del tipo guión dipolo pero en resumen así sería cualquier proceso de disolución al inicio las partículas del sólido están muy juntas entre ellas por sus propias interacciones pero al
añadir un líquido y cambiar un poco las condiciones las partículas del sólido van a preferir formar interacciones con las moléculas de líquido llámese de un dipolo dipolo dipolo o las que sean pero en cualquier caso las partículas se dispersan por todo el líquido y eso hace que ya no las veamos después de agitar y un último ejemplo sería que las interacciones también afectan las propiedades físicas de los líquidos por ejemplo seguro habrás escuchado sobre la atención superficial del agua esa capacidad del agua para comportarse como una malla resistente que hasta algunos insectos se pueden parar
en el agua bueno justamente esa malla se produce porque las interacciones químicas entre las moléculas de agua son muy fuertes específicamente son puentes de hidrógeno que ya mencionamos los especiales que son por eso la tensión superficial es responsable de que un mosquito se pueda parar en el agua o la forma específica de las gotas de agua e incluso son responsables de definir la trivia de hoy el animal que puede permanecer más tiempo sumergido debajo del agua es el escarabajo acuático este animalito que nace en tierra firme tiene que nadar mucho tiempo para buscar comida pero
no aguanta la respiración como lo hacen las ballenas o los delfines en cambio este animal usa un mecanismo bastante interesante cuando se sumergen en el agua se forma una especie de capa como si llevara un traje espacial alrededor esta capa se forma porque la superficie del escarabajo está cubierta de muchísimos pelos cortos que están tan cercanos entre ellos que no rompen la atención superficial del agua lo útil aquí es que entre esta capa y el escarabajo hay aire suficiente para que exista un intercambio de gases por ejemplo el poco oxígeno que hay en el agua
puede atravesar esta barrera para que lo usen nuestro escarabajo o puede ser al revés el dióxido de carbono que desecha el escarabajo puede atravesar libremente así el escarabajo evita asfixiarse y de este modo este animal puede nadar toda su vida tranquilamente su cuerpo le permite prácticamente llevar un tanque de oxígeno inagotable no como el delfín olas que necesitan salir a la superficie a tomar más aire después de un par de horas muchas gracias con esto terminamos de entender a las moléculas con esto ya puede decir que aprendiste todas las bases de la química nos vemos
en los siguientes vídeos ahora si se viene lo bueno se cuidan y no olvides echarle un vistazo a nuestras redes sociales tenemos resúmenes más ejemplos de los ejercicios divulgación científica y mucho más [Música]