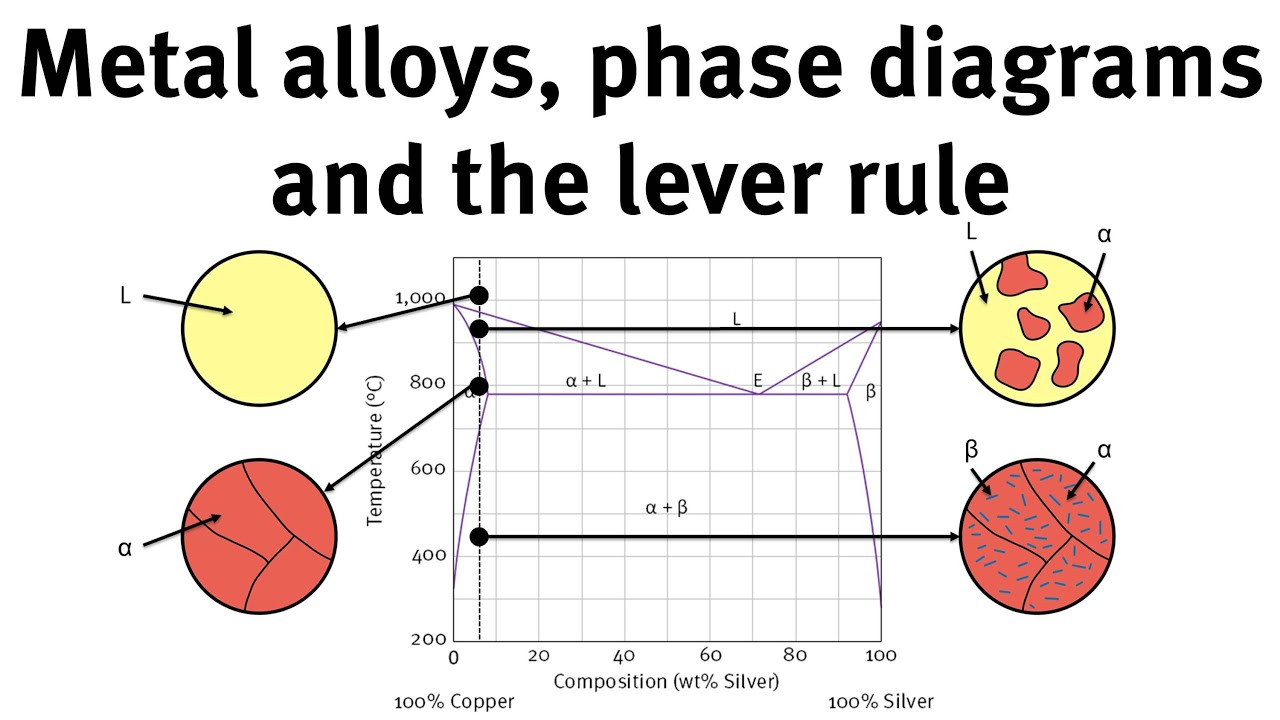
[Música] olá pessoal nesse vídeo nós vamos falar sobre diagramas de fases em soluções binárias vamos começar imaginando um recipiente conforme mostrado aqui nessa figura dotada de um êmbolo e símbolo é móvel e nós vamos assumir aqui que não existe qualquer tipo de atrito entre o embalo e as paredes do recipiente o êmbolo toca a superfície de um líquido que por um acaso é uma solução binária constituída pelos componentes a e b nós vamos assumir aqui que a concentração dessa solução é dada por 30% de a e 70% de bebê em base molar ou seja a
fração molar de até 30% ea fração de b é 70% nós vamos adotar aqui a convenção de que a fração molar dessa solução será dada pela letra z ou seja zé a afras um molar de a será igual a 0,3 zb a frança uma loja de bebê será igual a 0,7 nós vamos também acompanhar a temperatura desse sistema que será dada pela letra t e vamos assumir também que a pressão é constante vamos trazer então esse desenho aqui para a esquerda e construir um gráfico neste gráfico o eixo das ordenadas representa a temperatura eo eixo
das bicicletas representa a fração molar de a digamos que o nosso sistema esteja inicialmente a uma temperatura t e que a fração molar seja igual a zero nós estamos portanto no ponto mostrado aqui com she's not que nesse ponto o sistema constituído por uma única fase líquida e cuja composição nós conhecemos hoje a receber vamos então fornecer calor por esse sistema o que vai fazer com que sua temperatura aumente nós vamos parar então neste novo ponto veja pelo desenho que pouca coisa mudou nosso sistema continua sendo monofásico se nós aumentarmos a temperatura mais um pouco
nós vamos parar nesse novo ponto note pelo desenho da esquerda que desta vez há uma particularidade está começando a se formar uma fase vapor no nosso sistema dessa forma para que nós possamos disse completamente não basta nós identificarmos um único ponto no nosso diagrama nós precisamos de um ponto para representar a composição da fase líquida e outro ponto para representar a composição da fase vapor vamos marcá los então neste diagrama com um ponto azul representando a fase líquida e um ponto vermelho representando a fase vapor a temperatura correspondente ao momento em que começam a se
formar as primeiras bolhas de vapor é a chamada temperatura do ponto de bolha essa é a temperatura na qual a fase vapor começa a ser formada veja que nesse ponto a fase vapor possui uma fração molard a digamos y a maior do que a fração molar que nós tínhamos na solução original z isso é devido ao fato de que aqui no nosso exemplo a é mais volátil que b note também que nesse ponto a fase vapor acabou de começar a ser formada e portanto a sua massa é muito pequena por essa razão a concentração de
a e b na fase líquida que tem uma massa muito maior que aquela da fase vapor vai ser relativamente pouco alterada ou seja a fração molard a na fase líquida digamos x a vai ser essencialmente igual a zero se nós aumentarmos agora temperatura um pouco mais vamos parar no novo ponto mostrado com um x e pelo desenho da esquerda nós vemos que o mais líquido passou para fazer vapor veja que a fração de ano na fase líquida x a diminuiu em relação ao ponto anterior isso é esperado porque como componente é mais volátil ele está
saindo preferencialmente da fase líquida para fazer vapor e portanto a fase líquida vai ficar empobrecido de a da mesma forma a fração mullard anáfase vapor também diminui isso acontece porque apesar do componente a ser o mais volátil isso não significa que o bebê também não está migrando para fazer oa por havendo migração de b a fração molard a vai acabar diminuindo e nós podemos repetir esse experimento até nós chegamos a um ponto em que a fase líquida praticamente deixa de existir restam apenas algumas últimas gotas de líquido e imersas em uma atmosfera de vapor da
solução essas últimas gotas de líquidos são como olho já que elas estão imersas em uma atmosfera saturada na nossa solução por essa razão essa temperatura é conhecida como ponto de orvalho no ponto de orvalho a fase líquida está na iminência de deixar de existir por isso mesmo praticamente todo a e b estão na fase o vapor portanto z a fica sendo praticamente igual à y la aumentando a temperatura mais um pouco todo o restante de líquido irá valorizar e nós teremos novamente um sistema monofásico note que para realizar esse experimento nós fixamos um valor desenhar
e assim obtivemos este gráfico nós poderíamos ter começado esse experimento com uma solução por exemplo um pouco mais concentrada de a partindo por exemplo deste ponto se nós fizéssemos o mesmo raciocínio obteríamos novos pontos por exemplo esses aqui poderemos também ter feito esse experimento partir de uma solução muito menos concentrada em a como mostrado nesse ponto nós obteremos então novos pontos como por exemplo estes mostrados aqui um próximo passo seria tomar esses pontos e ligá los por meio de curvas removendo os pontos experimentais nós obteremos o diagrama de fases da nossa solução para a pressão
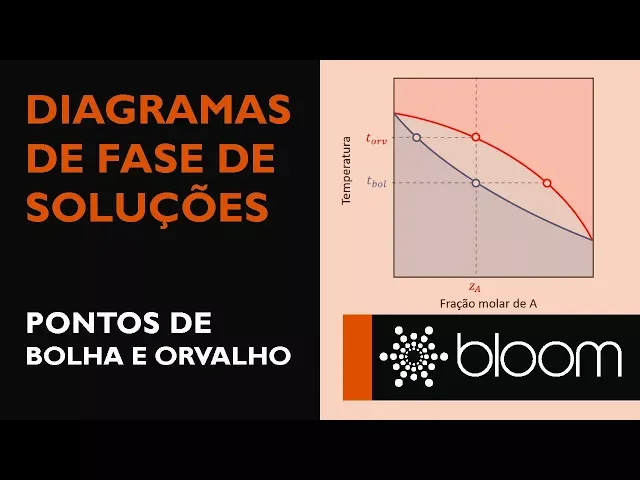
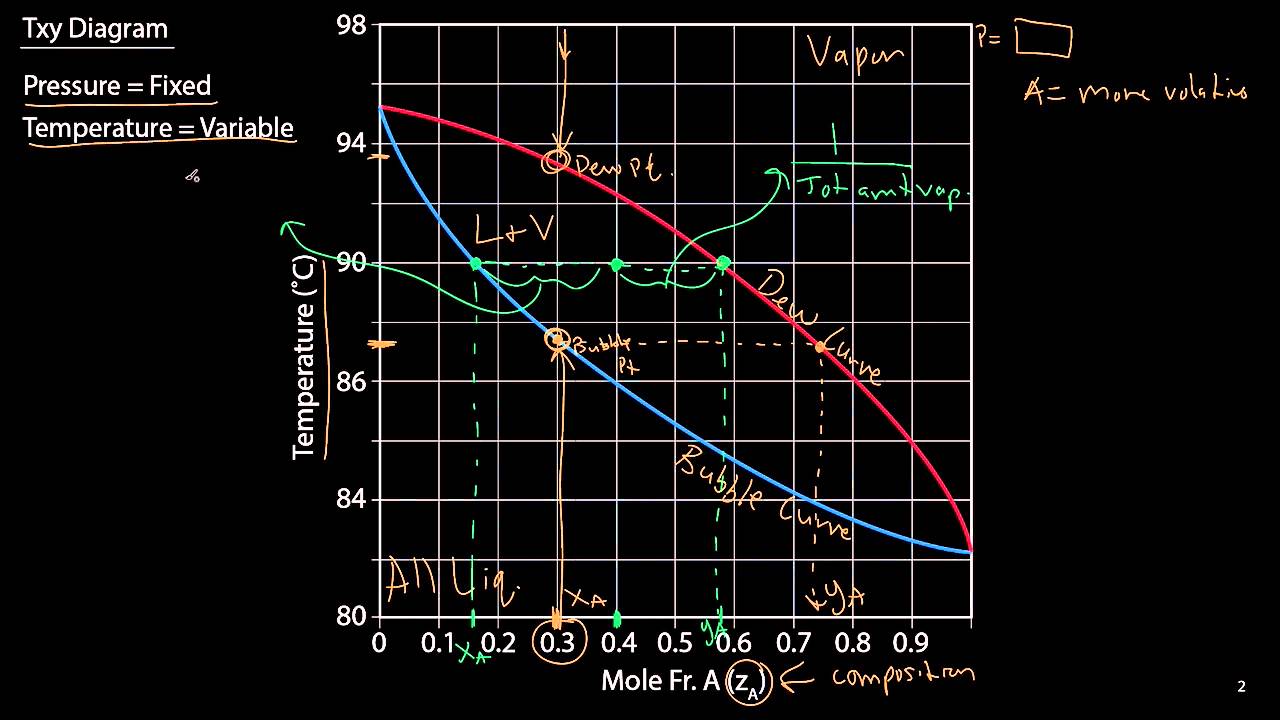
especificada vejo que o diagrama de vídeo gráfico em três regiões na região azul inferior em que as temperaturas são relativamente baixas nós temos essencialmente no sistema monofásico na fase líquida na região vermelha com temperaturas mais altas nós teremos também um sistema monofásico totalmente em fazer vapor na região intermediária nós teremos um sistema bifásico líquido vapor vamos agora nos lembrar do nosso experimento nós começamos fixando um certo valor z a para composição da nossa solução original esse valor é conhecido como fração molar global de ar e está aqui mostrado no gráfico como use a a intercessão
da reta vertical que passa por zh como a curva azul é o ponto em que começa a se formar a fase o vapor é portanto o ponto de bolha ea temperatura associada ele é a temperatura do ponto de bolha aqui mostrado como t ball dessa forma dar um sistema que faz com uma certa fração molar global de asia basta nós lemos a curva azul para encontrarmos o ponto de bolha ter bom a intercessão dessa reta com a curva vermelha é o ponto em que praticamente toda a fase líquida se vaporizou era o chamado ponto de
orvalho ou seja dada uma composição global para determinarmos a temperatura de orvalho basta ler mas no gráfico o valor correspondente a isso justifica o fato de essas curvas serem conhecidos comumente como curva dos pontos de bolha e curva dos pontos de orgulho se você gostou desse vídeo ou tiver alguma sugestão pode deixar nos comentários e não se esqueça também de curtir e compartilhar o nosso canal muito obrigado



![[ 40Hz ] GAMMA Binaural Beats, Ambient Study Music for Focus and Concentration](https://img.youtube.com/vi/Z8ANihFXlgU/maxresdefault.jpg)