Olá, pessoal. Tudo bem? Como vocês estão?
Então, nessa videoaula, eu vou discutir um pouco as questões sobre cromatografia, um pouco da técnica, falar da técnica de maneira geral, OK? E para que a gente possa dar continuidade aos nossos estudos em relação a técnicas analíticas, tá, pessoal? Então, eh, pessoal, a cromatografia é uma técnica analítica que pode ser utilizada tanto de tanto de maneira qualitativa quanto de maneira quantitativa.
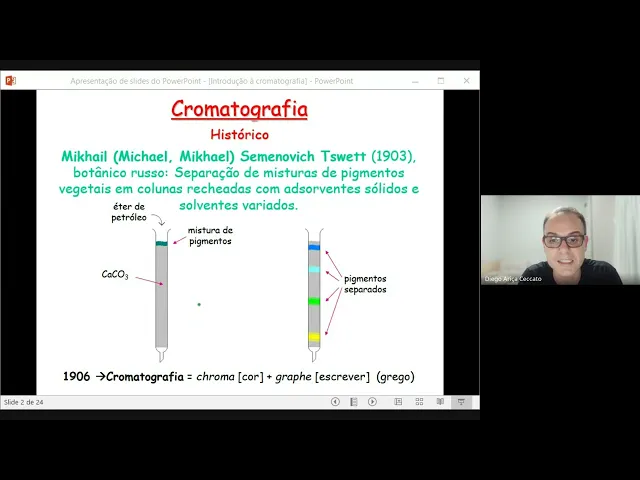
Ela foi pensada inicialmente, é uma técnica instrumental, né, claramente, e foi pensada num primeiro momento como uma técnica de separação de substâncias e não necessariamente como uma técnica de quantificação ou de identificação, mas com o evoluir da técnica, ela acabou se transformando também em técnicas de quantificação e identificação, mas no primeiro momento ela era uma técnica de separação. Então vamos dar uma olhada aqui como que a técnica se constituiu, né? Então nós tínhamos aqui eh o primeiro botânico, né, que estudou sobre a técnica, foi um botânico chamado Micael Semenovit.
E aí ele estudava pigmentos de plantas, né? E aí então ele precisava, ele tinha esse problema de pegar e fazer separação dos pigmentos de planta. Porque vocês sabem, né, pessoal, que, por exemplo, quando eu pego eh uma planta qualquer, né, eu tenho diversos pigmentos ali, né?
Então, eh, por exemplo, se a gente pega a uma planta hortelã, ela tem clorofila, que é o mais óbvio, que todo mundo imagina, mas ela também tem betacaroteno, ela tem outras substâncias chantaninas, ela tem outras substâncias ali que podem ser eh que estão presentes naquela planta. Então, já pensando em fazer uma extrapolação para nossa área, né, paraa área do biomédico, eh pode ser também ou de um químico, enfim, né? A técnica vale para qualquer área que vai utilizar a separação, mas eu posso, por exemplo, fazer uma separação de proteínas, né?
Então, posso ter uma amostra biológica ali com diversos eh diversos componentes, diversas proteínas diferentes ou diversas enzimas e eu precisar fazer uma separação dessas enzimas. Então, como que funciona a técnica, né? Ó, na técnica, pessoal, eu vou ter sempre aqui assim, né?
Eh, eh, uma cromatografia vem de estudo das cores, tá? Embora hoje a técnica não se resuma somente a isso, mas eu vou ter sempre eh uma parte aqui, ó, que eu chamo, não vou escrever, tá? Para não ficar rabiscando.
Vou vou colocar só como caneta temporária. Uma parte que eu chamo de fase estacionária, que é uma parte que vai ficar ali paradinha ali, né? Por isso o nome estacionária, tá?
Geralmente essa facea na cromatografia líquida, a gente vai ver daqui a pouco que existe cromatografia líquida e gasosa, ela fica nessa parte líquida, ela fica ali na cromatografia líquida, é um sólido eh ou um um líquido mais de alta densidade, que eu acho que um gel, correto? E aqui tá a amostra que eu quero separar de pigmentos. Então, imagine que eu tenho uma amostra de pigmentos aqui, eu quero separar os componentes dessa amostra, tá?
E aí, por fim, nós temos algo que a gente vai inserir nessa coluna cromatográfica, né, que é a fase móvel. Então, perceba, fase estacionária que vai ficar paradinha, geralmente um sólido ou um gel, um líquido bem viscoso, uma mistura, que é o que eu quero separar, e uma fase estacionária, que geralmente é líquida e vai passar pela minha amostra. Então, o que que esse Micael Semenovit fez?
Ele utilizou como fase estacionária. Aí esse essas especificidades vai variar de técnica para técnica, tá? de análise cromatográfica para análise cromatográfica, tô explicando especificamente o que o Semenovit utilizou.
Ele utilizou carbonato de cálcio como fase estacionária, mistura de pigmentos era a amostra dele que ele queria separar e o éter de petróleo, que é um solvente orgânico como fase móvel, tá? E aí ele simplesmente, né, inseriu aqui o éter de petróleo. Então a isso aqui é o momento um, não são duas colunas diferentes, tá?
É como se essa daqui fosse o momento um e essa daqui o momento dois, tá? Então, depois de um tempo, o que que aconteceu depois que ele colocou o éter de petróleo? O éter de petróleo, que foi a fase estacionária, foi arrastando os componentes da amostra, tá?
Foi arrastando ali, separando os componentes da amostra. Ó, se eu perguntar assim para vocês, qual foi a substância? Pense aí rapidamente um pouquinho.
Qual foi a substância? Pensa que o éter de petróleo, que é a fase imóvel, ele vai descer pela coluna. Então vai ser natural que eu vou colocar o de petróleo aqui, ó.
Ele vai descendo aqui pela coluna, arrastando com ele os componentes da amostra, ele vai sair aqui na parte de baixo da coluna, tá? Se eu perguntar assim para vocês, qual é a substância ou qual é o corante que tem mais afinidade pela fase móvel, pelo éter de petróleo? Que que vocês acham?
Pensando aí, vocês estão assistindo essa aula gravada, qual desses componentes aqui? Então, todos esses componentes aqui, ó, estava na minha amostra, que a princípio era só uma amostra verde, mas aí elas foram separadas. Qual desses componentes tem mais afinidade pela fase móvel?
É o amarelo, né, pessoal? Por que que ele tem mais afinidade pela fase fase imóvel? Porque ele é o primeiro que tá saindo da coluna.
Então, a nesse momento, a fase imóvel já saiu, né? Eu coloco a fase imóvel, ela se arrasta aqui pela coluna, né? Ela entra e sai.
Então, se eu tenho ali, ã, o amarelo saindo primeiro, ele é o que tem maior afinidade pela fase móvel. E quem tem menos afinidade pela fase móvel é o azul. Ele tá sofrendo aqui, tá aqui em cima ainda, ele quase não foi arrastado pela fase móvel, né?
Então, dessa forma, eu consigo fazer separações aqui de substância. Então, a partir da afinidade que eu tenho entre a fase imóvel, a minha substância e a fase estacionária, eu vou fazer essa separação. Eu posso fazer a pergunta de uma outra maneira.
Quem tem mais afinidade pela fase estacionária? Quem tem mais afinidade pela fase estacionária é o pigmento azul, porque ele tá ali no comecinho ainda, né? E aí depois quem tem menos afinidade pela fase estacionária, o amarelo, porque ele já tá saindo aqui ao final, tá?
Então, pessoal, eh dentro dessas eh a gente pode pensar já dentro dessas eh desse primeiro exemplo que a técnica de cromatografia ela é muito útil para fazer separações. como eu disse, então, se eu tenho um conjunto de enzimas que eu quero separar, eu posso então pensar numa fase estacionári um solvente que vai, por afinidades diferentes, vai arrastando essas enzimas, né, e vai separando-as ao longo da minha coluna cromatográfica. Posso pensar isso também para substâncias na área de toxicologia, né?
tiver uma amostra com substâncias tóxicas que eu quero analisar, que eu quero separar, enfim, as aplicações são diversas, né? Então, esse é um embrião da técnica de cromatografia. Foi assim que iniciou aí a técnica de cromatografia, tá?
pensando um pouco mais à frente, algumas definições, então, né, como eu já falei, né, que a cromatografia é um método físico químico de separação, identificação e quantificação. Então, começou como separação, depois foi ganhando eh outras eh outras vertentes, né? Essa separação, pessoal, depende da interação dos componentes da mistura com a fase imóvel e a fase estacionária.
Foi o que eu disse para vocês, né? Imagine vocês, deixa eu voltar aqui, ó. Se todos esses componentes aqui, se todos esses componentes da minha amostra tivesse a mesma afinidade com a fase imóvel, com a fase estacionária, que que ia acontecer?
Eles não iriam se separar, eles iriam todos sair de uma vez só, né? Então, eu tenho que ter eh essa separação, a a o quão bem-sucedido vai ser a minha separação, vai depender da afinidade dos meus componentes com a fase móvel e a fase estacionária, tá? E como que é essa afinidade?
Como que essa afinidade se dá entre fase móvel e fase estacionária? Pode ser por diferentes diferentes forças intermoleculares, né? Então, pode ser ali por diferentes tipos de ligações químicas que eu eventualmente ven a ter.
Pode ser ã por eh troca iônica, então diferenças de cargas que eu eventualmente possa ter ali eh durante uma eh uma separação, polaridade, tá? solubilidade e outros efeitos de afinidade. Então, vai depender.
Então, se eu tenho, por exemplo, eh, uma enzima que tem uma carga positiva, é normal, né, você, né, talvez alguns de vocês saibam, né, tenham visto na em bioquímica, que algumas enzimas eh a depender do pH do meio, vai ter carga positiva e outras vão ter carga negativa. Se eu tenho enzimas com uma enzima com carga positiva e a minha fase estacionário tem carga negativa, essa enzima vai ficar mais aderida à minha fase, porque ela vai se grudar a minha fase, né? Então são coisas que a gente eh esse tipo de interação que existe vai depender ali da eh das moléculas com as quais eu tô trabalhando, né?
Então, ó, eu peguei aqui um outro exemplo. Então, quase que em três tempos aqui uma separação, né? Então, eu tenho a minha fase estacionária, que é isso aqui em amarelo aqui, ó, que eu tô rabiscando de verde agora, né?
Ó. Então, essa é a minha fase estacionária. Aí eu tenho duas moléculas, eh, eh, bolinha vermelha e quadrado azul.
E aí eu passei aqui minha fase que eu tô chamando de soluto A e soluto B. Aí eu passei aqui, ó, essa seta tá indicando que eu estou inserindo a minha fase móvel. na minha coluna cromatográfica, tá?
E aí, perceba, o A bolinha vermelha sai primeiro que o B, quadradinho azul. Significa que o A tem mais afinidade pela fase móvel e o azul tem mais afinidade pela fase estacionária porque ele fica mais tempo retido. O A tem mais afinidade pela fase móvel porque ele sai primeiro, né?
Bolinha vermelha tem mais afinidade pela fase móvel. Quadradinho azul tem mais afinidade pela fase estacionária porque ele demora mais para sair, tá? Então eu tenho fase móvel, fase estacionária, corrida cromatográfica, que é esse processo todo, ou elição, tá?
Isso eu deixei escrito no próximo. Ah, não, ainda coloquei um slide anterior para exemplificar ainda mais isso. Ah, nesse slide.
Ah, então só voltar aqui porque daí a hora que eu se eu tiver colocado no no próximo slide eu nem comento. Então, ó, fase estacionária, aquela que fica parada, né, ali na minha coluna cromatográfica, que é a fase que vai ser responsável pela aderência dos componentes da minha fase, eh, da dos componentes da minha amostra, tá? fase móvel é aquela que vai tentar arrastar a minha amostra, tá?
Eh, os componentes da minha amostra, tá? Na cromatografia líquida, porque a gente vai ver também cromatografia gasosa, na cromatografia líquida, faz estacionária geralmente um sólido ou um gel, né? Um líquido bastante viscoso, faz imóvel líquida, porque a gente tá falando de cromatografia líquida, tá?
Esse processo todo a gente chama de ocorrida cromatográfica ou processo de eluição, OK? Então, se aparecer aí nos próximos slides, eu nem eu vou pular, não vou nem não vou nem falar, tá bom? Aqui eu dei outro exemplo, ó, agora já pensando num gráfico, né, pessoal?
Então, os aparelhos de eh cromatografia, eles têm ali detectores que eles vão conseguir detectar o momento em que alguma amostra tá saindo, algum componente está saindo ali do aparelho. Então, imaginem que vocês, olha o que eu que eu fiz aqui, eu preparei aqui, ó, esse essa essa figura é de um capítulo, é de um livro que eu gosto bastante, que é o Leninger, tá? Um livro de bioquímica, porque a cromatografia é uma técnica bastante utilizado em bioquímica, tá, pessoal?
Então eu peguei lá do Leninger essa essa essa figura aqui, tá? Então olha só, veja bem, eu tenho minha coluna cromatográfica aqui, ó, que a gente chama de coluna recheada, né? Recheada com quê?
Recheada com a fase móvel. Aí eu tenho aqui a minha amostra, ó, AB, uma amostra com dois componentes. Perceba que todas essas colunas aqui são as mesmas, é a mesma coluna.
Todas essas figuras aqui é faz referência à mesma coluna, mas em tempos diferentes, tá? Então, ó, tempo zero, tá aqui, ó, tempo zero, ó. E aqui um gráfico acompanhando de acordo com o que vai sair da minha coluna ali no detector.
Então, amostra, tá? Tá ali a amostra. E aí eu vou colocar aqui minha fase imóvel.
Fase imóvel vai percorrer toda a coluna e vai sair aqui, tá? Aí, pessoal, o equipamento ele vai detectar a minha fase móvel saindo, só que o equipamento tá zerado com a fase móvel. Então, é que nem a gente faz lá em espectro espectrofotometria, a gente zera ali com o branco, né, que em algumas análises são é água destilada, mas nem sempre pro equipamento desconsiderar aquela absorbância do branco.
Aqui é a mesma coisa. a gente zera o equipamento com a fase móvel para ele desconsiderar qualquer sinal referente à fase imóvel, né? Como como eu quando eu taro a balança, um becker para pesar alguma coisa na balança, a hora que eu colocar lá o beer lá em cima, ele vai desconsiderar aquela massa, tá?
Beleza? Então, tempo zero, hora que eu coloquei aqui a minha fase móvel, aí ó, a fase imóvel começou a descer aqui, ó, e foi arrastando com ela. Componente a AIB já separou um pouquinho, né?
Nesse momento já tem fase imóvel saindo aqui da minha amostra, tá? Da da da minha coluna. Aí, ó, tempo três já separou um pouquinho mais, mas ninguém saiu da coluna, só a fase imóvel.
Mas lembrem-se, fase imóvel tá zerada para não receber sinal, tá? Tempo três. Opa, já separou bem aqui, ó.
E o A saiu, ó, o componente A já saiu. E aí meu aparelho ele detecta que saiu, ó. Ele dá um sinal, tá?
fase B, depois sai o componente B ou outro sinal. Então, perceba aqui, isso aqui chama de, a gente chama de cromatograma, tá? Ou espectro.
Eh, eu prefiro chamar de cromatograma. Algumas pessoas chamam de espectro cromatográfico. Então, a gente consegue ver aqui, ó, a gente consegue ver aqui que tem duas substâncias presentes nessa amostra, tá?
A gente consegue saber também que a substância A tem mais afinidade pela fase móvel, porque ela é a primeira que sai. Mesmo sem olhar o desenho, ó, só olhando a figura, eu consigo perceber que o A é o primeiro que sai. Se o A é o primeiro que sai, né, ó, ele é o que tem mais afinidade pela fase móvel.
O B é o último que sai, então ele tem mais afinidade pela fase estacionária, tá? Bom, seguindo isso aqui, aquilo que eu falei que eu que eu pularia, né, que eu já falei para vocês. Olha esse cromatograma aí.
Agora, sem o desenho, só o cromatograma, ó. Só de bater o olho no cromatograma, eu consigo saber então que eu tenho três componentes, porque, ó, tenho três picos aqui, ó. O que que isso significa, ó?
Começou a leitura, começou a corrida cromatográfica, né? Ó, tudo esses pequenininhos aqui que tem aqui, ó, é tudo eh interferência, eh instabilidade do aparelho, né? Isso aqui não conta, tá?
Que é muito pequeno, não é porque tem uma amostra saindo aqui, tá bom? Mas aí, ó, primeiro num tempo próximo aqui de deve ser uns 7 minutos e meio aqui, ó, quase oito, sai minha primeira, meu primeiro componente da minha amostra, depois sai o meu segundo componente, depois o meu terceiro componente, tá? E aí, pessoal, o que que isso significa?
Só de olhar o gráfico, eu consigo entender que a minha amostra possui três componentes, tá? Componente A, componente B, componente C, porque eu tive três picos cromatográficos, tá? Qual desses picos, qual desses componentes saiu o primeiro?
Componente A. Logo, eu sei que ele é o que tem maior afinidade pela fase móvel. Qual componente saiu por último?
Componente C. Logo, eu sei que ele tem maior afinidade pela fase estacionária, tá? Muito bem.
Não é dif, é uma técnica super interessante, tá, pessoal? Eh, muito utilizada, tá? Então, como eu falei, né, área forense, área de toxicologia, área biológica, área bioquímica, ela tem uma utilização muito ampla nas áreas aí de análises eh de substâncias mais relacionadas a a ao corpo humano, a plantas, né, a seres vivos, na verdade, né, menos não tem tanta utilização eh quando eu penso em análise de compostos inorgânicos, tá?
E aí, pessoal, eu gosto dessa analogia aqui que não é minha, tá? Eh, não fui eu que criei essa analogia, eu simplesmente peguei, eh, encontrei na internet pesquisando algumas algumas coisas sobre cromografia, algumas imagens, né? Encontrei essa analogia que é o seguinte, né?
Quem vai sair primeiro e quem vai sair por último, vai depender muito de quem que é a minha fase imóvel, quem que é a minha fase estacionária. Não é uma regra, ah, a substância tal sempre sai primeiro. Depende de quem é minha fase imóvel e de quem é a minha fase estacionária.
Então, eu fiz essa analogia que é o seguinte, ó. Eu tenho os analitos, né, os componentes da minha amostra, eu tenho que é uma abelha e uma mosca, tá? são os componentes da minha amostra, uma abelha e uma mosca.
Aí, meus amores, a minha fase estacionária é uma flor e a minha fase imóvel é um vento. Então, imagine o vento passando, né? Imagine o vento passando aqui, né?
Nesse caminho aqui, ó. Imagine o vento como fazem imóvel passando nesse caminho aqui, tá? Então, ele o vento vai arrastar ali os componentes da minha amostra.
Quem são os componentes da minha amostra? abelha e mosca, tá? Então tá aqui.
E a mais fácil acionar é a flor, pessoal. No caso, né, o a o vento, que é minha fase móvel, ela ele tem a mesma afinidade pela abelha e pela mosca, né? Porque os dois ali são seres voadores, né?
Mas quem tem mais afinidade pela fase móvel, pela fase estacionária, perdão, pensa aí, né? Vocês estão assistindo essa aula gravada, não é ao vivo, né? Então pensa aí quem tem mais afinidade pela fase estacionária, a mosca ou a abelha?
Quem vai ficar retido há mais tempo nessa nessa corrida? Aquele que tem mais afinidade pela fase estacionária, já que pela fase móvel os dois são mais ou menos iguais. Então vamos colocar essa corrida para funcionar, ó.
Então percebe? A abelha tem mais afinidade pela pela flor e a mosca não, né? Então a mosca passa, né?
Ela sai primeiro da corrida, vamos dizer assim. Mas se a gente mudar a fase estacionária, olha só, mesma coisa, tá? A fase móvel vai ser aqui, ó, o vento passando aqui, que vai arrastar os componentes da minha amostra.
Os componentes da minha amostra, né? Os meus analitos é uma abelhinha, uma mosquinha. Só que agora minha fase estacionária é um lixo, tá?
Então pense aí. Quem tem mais afinidade pelo lixo? Isso mesmo.
Fase quem tem mais afinidade pelo lixo? A mosca, né? Então, a hora que eu colocar aqui, ó, a mosca fica retida e a abelha passa.
Então, se eu mudo os componentes da minha fase estacionária, da minha fase imóvel, eu mudo também, né? Quem sai primeiro, quem sai depois. Isso é um é um artifício que eu utilizo, né?
que eu que eu posso utilizar ali para tentar melhorar ali meus parâmetros analíticos no momento da minha análise, tá? Aqui já falei já. E aí nós temos, estou falando de cromatografia líquida, OK?
Estou falando de cromatografia líquida, porque depois também existe a cromatografia gasosa, tá? Mas estou falando nesse momento de cromatografia líquida. Existe também, pessoal, aí existe também quando a gente fala de cromatografia líquida, existe também eh os tipos de interação que eu tenho entre fase móvel, fase estacionária, tá?
Fase móvel, fase estacionária, eh, e o componente da minha amostra, né? Então eu coloquei aqui pra gente pra gente ver, pensar em alguns casos. Então a primeira coisa que eu tenho é a absorção.
Então é assim, é quando a minha o componente da minha amostra se absorve na superfície da face estacionária, tá pessoal? Absorver não é absorver ir para dentro, absorver ficar na superfície, tá? Opa, coloquei no lugar errado aqui.
Absorver ficar aqui na superfície. É quando os componentes da minha amostra absorvem a superfície da face estacionária. Aqueles que absorvem mais ficam mais retidos.
Aqueles que absorvem menos, tá? Passam mais facilmente pela fase estacionária, são levados pela fase móvel e saem primeiro da coluna, tá? Então, a gente tem aqui, né, ó, eu coloquei a diferença entre absorção, né, alguém comendo uma torta e a dissorção, a absorção é alguém tomando a torta na cara, né?
Então, eu tenho ali um um uma [Música] eh analitos ficando ali retidos na superfície da minha fase estacionada, tá bom? E quando é uma interação do tipo troca iônica, quando é uma interação do tipo troca iônica, pessoal, é quando eu tenho então na minha fase móvel ou na minha fase estacionária, uma certa carga e aí os componentes da minha amostra vão ter também cargas que vão ou fazer com que ele fique mais retiro na fase estacionária ou que passe mais facilmente pela fase estacionária. Então aqui, por exemplo, eu coloquei a minha fase estacionária, sendo aqui, ó, cargas negativas.
Os componentes da minha amostra que t carga positiva vão ficar mais facilmente retidos aí na minha fase eh estacionária, tá? Então, olha aqui, ó, esse exemplo que é o coloquei que é uma uma resina de troca iônica, tá? quando eu quero separar substâncias com cargas diferentes.
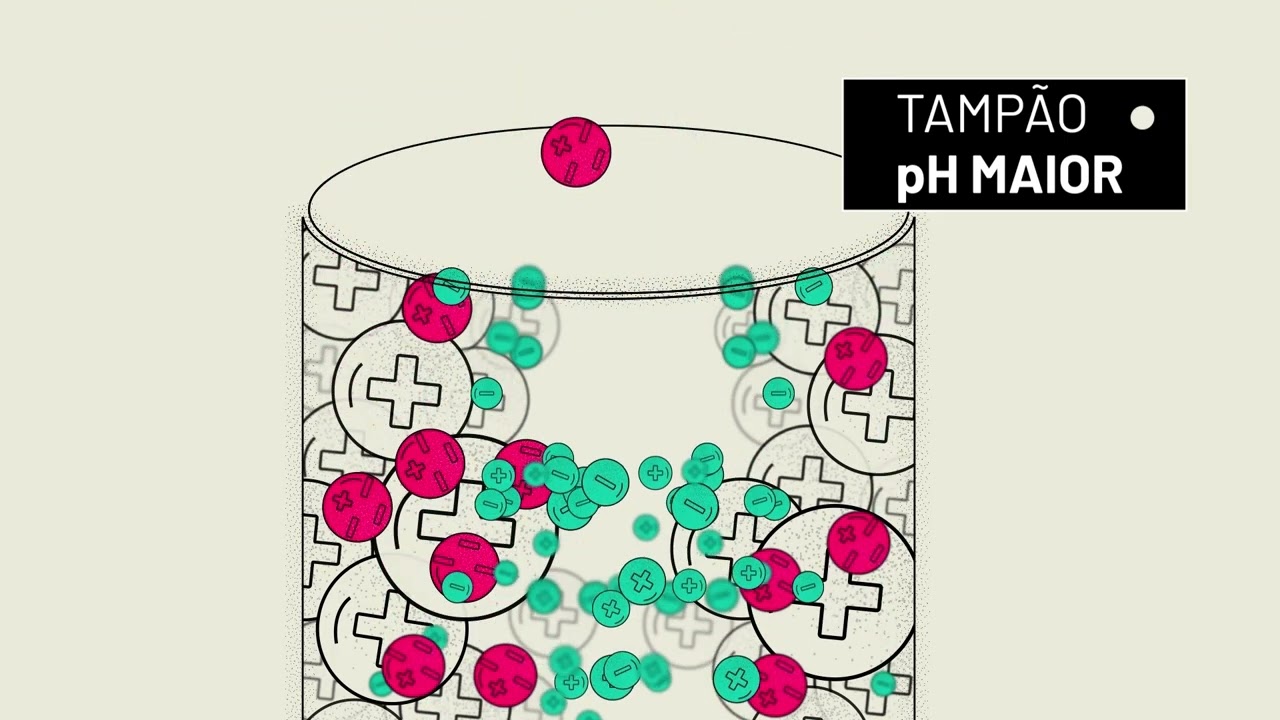
Então, ó, vamos analisar bem que essa figura é boa, tá? Melhor que a anterior. Então, eu tenho aqui, ó, na minha fase estacionária, são essas bolonas aqui, ó, todas com carga positiva, certo?
Isso aqui é a minha fase que é estacionária. Tudo aqui com carga positiva. Aí, ó, a minha amostra tem componentes com carga negativa, bolinha vermelha e componentes com carga positiva, bolinha preta.
E aí, então, ó, eu vou, tá aqui a minha amostra, eu vou passar aqui minha fase móvel por aqui, né? Vou passar minha fase móvel por aqui. Minha fase imóvel, nesse caso, é neutra.
Percebam, ó, como é a minha fase estacionária. Então, de novo, estamos falando por um tipo de interação que é por troca iônica. Como a minha fase estacionária é positiva, os componentes negativos da minha fase móvel vão se retendo, né?
Porque eu tenho uma interação de cargas opostas. E o que que vai chegando primeiro? O que que vai separando primeiro aqui na coluna, tá?
vai separando, vai saindo primeiro da coluna aqui a os componentes da minha motiva e os que têm carga negativa vão ficando vão vão se ficando retidos aqui na minha estacionária. Lógico, se o objetivo, se o objetivo é separar, depois eu preciso também achar um jeito de separar os componentes aqui que são negativos, de repente passar um outro solvente que tenha mais afinidades por eles para conseguir tirar eles da da fase estacionária. Mas eu já consegui fazer uma primeira separação aqui, tá?
Então de novo, né? Fase imóvel neutra, passando aqui, fase estacionária positiva, né? Fase imóvel neutra, componentes da minha amostra positivo e negativo.
O negativo vai se aderindo à superfície, né? Porque carga oposta se atraem e os componentes positivos vão saindo, tá bom? Aqui é algo parecido, né?
Pensando em proteínas, né, pessoal. Então eu tenho também aqui pensando em troca iônica, né? Então eu tenho proteí, eu tenho, por exemplo, quando eu penso lá em proteínas ou enzimas, a depender do pH, essas proteínas ou enzimas podem ser carregadas positivamente ou negativamente.
Então, que que eu pensei aqui, ó, nesse desenho aqui, que eu acho bem legal também, uma proteína carregada negativamente e outra proteína carregada positivamente, tá? E eu quero separar essas duas proteínas. Então, se eu quero separar essas duas proteínas, né, ó, a minha fase móvel, por exemplo, a minha fase móvel, ela pode ser uma minha fase estacionária, perdão, minha fase estacionária pode ser carregada positivamente, tá?
uma fase imóvel aqui que seja neutra, por exemplo. E aí, ó, a proteína que é carregada negativamente, ela se adere à superfície da minha fase estacionária, que é positiva. E aí eu separo a proteína que é carregada positivamente, tá?
Então, a proteína que é carregada negativa, se adere à fase estacionária e a que passa é a minha proteína que é carregada positivamente. Ah, Diego, beleza. Mas e aí, como que eu faço depois para tirar a proteína da minha fase negativa?
Para tirar a proteína da minha fase negativa, por a proteína negativa, eu posso ajustar o pH da minha solução, né? Trazer esse pH para cinco, né? PH5 pH ácido, vai ter cheio de H+ aqui na minha solução.
E aí essa proteína que é carregada negativamente vai sair com a a fase móvel que tem ali um pH5, né? Porque daí agora a o pH5 é um pH positivo, né? Porque ele tem H+.
Então perceba, primeiro eu tirei a proteína que era carregada positivamente, certo? Porque minha fase imóvel é positiva, a proteína que é negativa ficou retida na na fase estacionária. Depois eu separei a proteína que tem carga negativa, passando uma fase móvel aqui positiva para atrair essa negativa aqui, tá?
Acho que esse também é um é uma é uma boa figura que que mostra aí essas duas diferenças, tá? Por fim, eu tenho um processo de exclusão molecular. Já vou pular para um próximo slide que eu acho que fica mais esse slide eu acho que é o mais fácil de visualizar na processo de exclusão molecular.
É quando eu tenho ah substâncias de tamanhos muito distintos. Então aqui eu peguei, por exemplo, eh uma substância, né? Bolinha vermelha, uma substância grande, bolinha amarela, uma substância pequena.
Lógico, as duas são pequenas, mas comparativamente, né? Essa bolinha vermelha é umas quatro vezes maior, eh, é em torno de quatro vezes maior que a bolinha eh amarela, né? Então, vejam só vocês, quando eu tenho então e esse tipo de mistura, no qual eu tenho moléculas que têm tamanhos muito distintos, a gente faz por exclusão molecular.
Eu coloco uma fase estacionária que é porosa, né? Como essa fase estacionária é porosa, as substâncias que são menores vão entrando nos poros, ó, e vão ficando mais tempo retido na fase estacionária, porque elas vão entrando nesses poros. As substâncias que são maiores, elas vão, elas não entram no poro, então elas vão descendo, elas vão saindo aqui da minha coluna, tá?
Então elas saem primeiro, essas menores vão sair depois eventualmente, tá? Essa separação é muito feita com água e álcool, então etanol especificamente, quando eu quero fazer em processos biotecnológicos, separação entre etanol e água, obtensão de etanol 100% eh 100% anidro, né, sem nenhum tipo de de água, né? O etanol é uma substância consideravelmente uma molécula consideravelmente maior que a água, né?
Então a gente vai coloca os dois numa coluna desse tipo, né? E aí a água vai entrando nesses poros aqui, né? E o etanol vai passando por eles, saindo mais facilmente aqui ao final da coluna, tá bom?
Eh, bom, eu resolvi eh fazer isso em duas partes, né? Então, essa aqui, cromatografia líquida, né? E aí, no próximo vídeo, a gente vai ter ali explicações sobre cromatografia gasosa, OK?
Bom, pessoal, espero que vocês tenham entendido e até a próxima vez que eu gravar aqui uma aula para vocês, tá?
















![3. Substância Pura, Mistura e Alotropia [Química Geral]](https://img.youtube.com/vi/VVIUBoydb5Q/maxresdefault.jpg)
