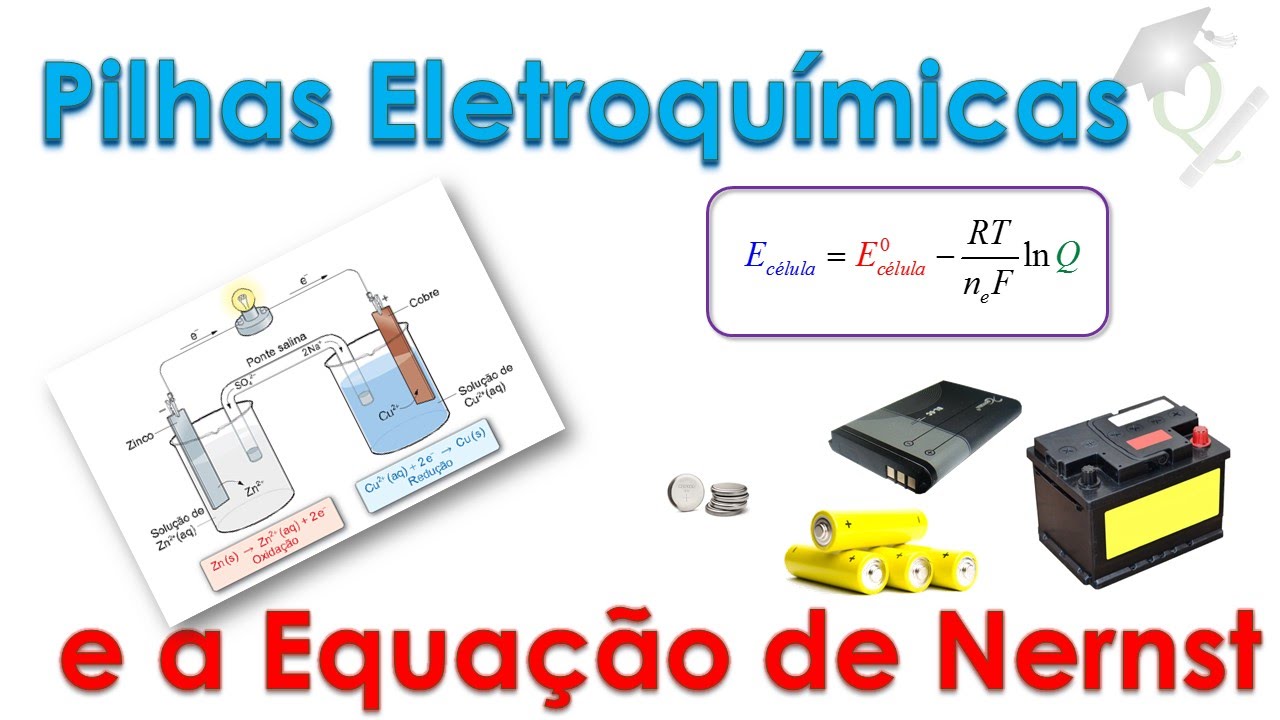
e agora a gente vai falar de algumas baterias que a gente utiliza baterias É como se você tivesse várias pilhas em série para que a gente vai ter várias Pires ou para você aumentar voltagem ou para você aumentar a carga Então essa primeira matéria que a gente tem aqui é uma bateria chamado de chumbo ácida corrigir aqui o nome a bateria chumbo-ácida é a bateria automotiva que utilizado no carro e nas mãos Então você vai ter a reação do cátodo É essa a reação do ano então isso aqui vai ser utilizado para produzir a corrente
Alerta e aqui vai ser o que demanda normalmente a maior quantidade de ácido sulfúrico produzido pela indústria aqui a gente já vai ter uma pilha mais comum que é a pilha alcalina aa pilha alcalina no capítulo ela vai funcionar com o dióxido de manganês reagir com água e no ando o Zico reagindo com os íons hidroxila então o nome é alcalino vem justamente dessas hidroxilas que tem aí é o que o meio é básico antes das pilhas alcalinas as filhas não mais elas geravam um gás como produto de reação separada e esse gás ele acaba
ficando entre os eletrodos fechando a corrente antes do esperado então por isso que a pilha normal ela dura menos do que uma pilha alcalina porque a pilha alcalina Não tem esse problema de formação de gás aqui é a bateria de lítio a bateria de lítio ela tem várias aplicações ela pode ser utilizado no computador calculadora pode ser utilizado em marca-passo nada mais é do que o lixo sendo carregado em um eletrodo e sendo descarregado no outro aqui no eletrodo catado o lixo ele vai estar um óxido de Cobalto e ele vai migrar para o eletrônico
que contém Carbon então isso aqui vai gerar esse potencial do leite a outra bateria que a gente tem chamada de célula combustível que quando você tem hidrogênio reage com oxigênio A corrente elétrica então no caso você vai ter a oxidação do hidrogênio e no ano do você vai ter a redução do oxigênio no final você tem água como produto essa aqui ela é uma matéria bem interessante porque ela não é poluente Você tem o hidrogênio e tem o oxigênio que não são poluentes e o produto de reação dela é a água que também não é
poluente se a gente for comparar a densidade de energia dessas baterias aqui tem a maior densidade de energia pão volume ou pô massa é a pia de ião-lítio tão como ela tem uma quantidade muito grande de carga pela massa dela permite que ela tenha um tamanho mais reduzido do que em relação às outras e ela dure mais também então é por isso que ela vai ser utilizado por exemplo marcapasso o que quando você tem um marca-passo Você vai precisar de uma bateria para alimentar esse marca-passo e você não pode ficar operando todo tempo a pessoa
para trocar a bateria tem que ser uma batalha é mas é aí que entra a bateria de lixo agora a gente vai começar a falar de eletrólise eletrólise são processos que você vai utilizar a energia elétrica para forçar uma reação química não espontânea tão a eletrólise ela pode classificar de duas formas a Electrolux né que é quando você tem um determinado o solo e você derrete ele para formar eletrólise e tem um eletrólise conhecida como a eletrólise em meio aquoso onde ela vai ocorrer com o somente utilizando água no caso da eletrólise ígnea Por exemplo
quando você pega o cloreto de sódio sal de cozinha você derrete ele e passa ele pela corrente elétrica Você vai formar no ano o cloro gasoso e no caso você forma o sódio metálico Então nesse caso os sinais são diferentes enquanto que na célula galvânica o ângulo é negativo e o caso da Positivo aqui vai ser o contrário o eletrodo cada e um vai migrar horas Sim O ano de positivo ele vai atrair os seus negativos se o k tudo é positivo ele vai atrair os íons positivos Então lembre-se sempre que os opostos se atraem
uma coisa que não muda Independente de ser célula galvânica ou célula eletrolítica é que no cacto você sempre vai ter o processo da redução isso não varia e no andando você vai ter o processo da oxidação a eletrólise em meio aquoso você vai ter já uma mistura de substâncias isso vai gerar uma competição para quem oxida e para quem Reluz no casa que a gente tem eletrólise da água você coloca aqui por exemplo o sulfato de sódio e o sofá de sódio ele só vai servir para conduzir corrente elétrica por dentro da água porque a
água sozinha ela não consegue conduzir nesse caso fato de sódio ele funciona só como condutor ele não participa o vídeo lado você vai gerar hidrogênio e do outro você vai gerar oxigênio foi aqui que foi comprovado que a fórmula da água contrariando o John Dalton era h2óó porque o volume de hidrogênio formado era o dobro do volume de oxigênio então foi comprovado aqui a hipótese de advogado professor se eu tiver uma eletrólise em meio aquoso como é que eu sei quem é que vai reduzir quem é que vai oxidar Se houver uma competição Já que
é uma mistura então aqui você tem uma tendência de descargo ela essa família uma tem tendência a perder os elétrons mais fortes do que os elementos da família dois a que por sua vez eles vão ter uma tendência mais forte a perder os Alex que elemento da família três lá que vão ter uma tendência maior do que o hidrogênio que têm uma tendência maior do que os outros metais já usamos os alimentos da família sete áreas têm uma tendência maior de descarregar que usa os anos não oxigenados que é maior do que a hidroxila que
é há muitos anos oxigenados colocar para você vai ter o processo de redução na redução a espécie está ganhando elétrico Então vai ser o processo contrário da descarga vai estar carregando então a tendência de reduzir ela vai aumentar na esquerda para a direita aqui enquanto que a tendência do ano um ano ele vai descarregar é uma tendência vai ser da direita para esquerda como é que funciona isso na prática se você tem o cloreto de sódio fundido o que é que vai acontecer você vai ter como único ou cátion o Enem a mais líquido porque
agora como você fugiu não tem como se dissolvem em água mas o CL menos líquido Então quando você fizer a operação de descarga o que é que vai acontecer o sódio ele vai ganhar um ela Eva formando sódio metálico Isso aqui vai ser no catodo o preto ele vai descarregar formando cl2 gasoso mais elétrico no ano se eu fizer um balanceamento você vai ter aqui no caso dois planetas para formar um cloro recebendo dois alertas Então como aqui é um eletrólise ígnea porque você tá partindo de um produto sólido você não tem competição então o
cátion carrega formando a sua forma reduzida e um ano ele vai descarregar formando uma forró que se dá já no caso quando a gente tem um a Célia acuso o que é que a gente vai ter a gente vai ter dois cátions Professor dois cátions Quem são a gente vai ter o n a mais aquoso e vai até o h mais da água nem pense que a água ela se alta ioniza ela vai produzir o enemax no caso dos Anjos Quem são os anos que a gente tem a gente vai ter o cloreto acuso e
vai ter a e a gente vai estar a competição entre dois cátions e dois anos quem é que vai ganhar vamos olhar aqui olha para o cátion quem é que tem a preferência de reduzir é o sódio que é da família um lá ou é o hidrogênio o h mais Então nesse caso como é da esquerda para direita a tendência é dor hidrônico então o hidrogênio vai reduzir E no caso do ano quem é que vai descarregar é o elemento cloro que é da família sete a ou é a hidroxila vai ser vai ser o
cloro Então quem são os produtos esperados no caso da redução do h mais vai ser o que 2 H + É só você olhar naquela tabela de oxirredução mas dois elétrons formando H2 gasoso é justamente eletrodo padrão de hidrogênio né a semi-reação dele e no caso o cloro descarrega você vai ter dois CL - a cor formando série 2 o gasoso mais dois Alex então respondendo à pergunta Quem são os produtos esterases você vai ter H2 gasoso você vai ter cloro Mas o que foi que sobrou lá dentro a gente tem que ter o que
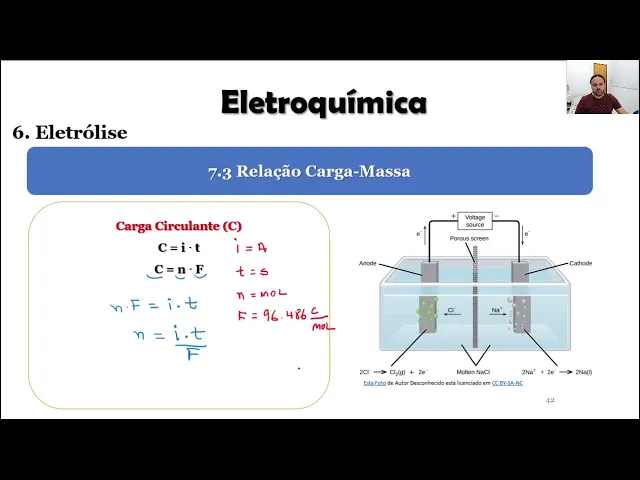
sobrou né sim o hidrogênio é gás e o cloro é gás eles vão sair de solução foi que sobrou dentro mas sobrar dentro hidróxido de sódio uma por isso que a solução ela fica básica beleza com relação a massa e a carga durante a eletrólise elas vão ter uma relação na física a gente sabe que a carga é a corrente mesmo tempo só que na Química a carga vai ser o número de mal vez a carga que o meu carrega que a constante fala de Então daqui a gente tira o que que se o número
de mols vezes a constando de farda é a carga então eles vão ser a corrente vezes o tempo então se eu pegar isso daqui O que é que o número de mol da de elétrons que vão participar de uma eletrólise ele vai ser a corrente vezes o tempo dividido pela constante farda vemos não voltando aqui ó vou molhar agora as unidades A corrente elétrica ela vai estar em ampere o tempo ele vai estar em segundos o n vai estar em mol e o HFA constante fardo né que vai ser o 96 1486 Colombi ou não
Beleza então vamos pegar um exercício aqui para ver uma amostra de 4,9 gramas de manganês foi produzido a partir de uma solução de nitrato de Magalhães em água quando a corrente de 350 mil amperes foi aplicada por treze, sete horas Qual o número de oxidação do manganês tão pelos lados aqui a gente tem a massa de manganês que foi produzido a gente tem a corrente que passou e o tempo então o que que a gente consegue saber e a gente pode determinar o número de mol de elétrons Então vamos fazer primeiro esse daqui determinando ou
número de mol de elétrons que a gente vai utilizar a equação número de maus é a corrente vezes o tempo dividido pela constante Faro Agora os detalhes um tempo ele tem que estar em segundo a gente vai ter que converter para segundo como é que eu converto você vai pegar 13,7 horas vez uma hora vale quantos segundos 3600 segundos então 3600 segundos equivale a uma hora se eu multiplicar isso aqui Cancela a hora com hora se aqui vai dar 49320 segundos agora a gente tem que converter também de que vamos converter de milho ampere para
perto 350 milho vale 10 a menos 3 é a mesma coisa você pode substituir cima aqui por 10 a menos 3 o pé fazendo essas contas da 0,350 até agora é só substituir não vai ficar corrente 0,350 vezes 49320 segundos dividido pela constante de Faraday 96 1486 isso aqui como é o número de mal vai dar em volta já vou colocar a unidade aqui para não ter problema eu já sabe que vai desses cancelamentos aqui se você duvidar você pode fazer não tem problema mas só para ganhar tempo quanto é que vai dar aqui na
minhas contas deu 0,179 mal de que molde Eletro beleza achamos o número de mal de Alex Professor como é que eu vou saber o número de oxidação do manganês Então nesse caso eu vou escrever uma equação genérica o manganês a gente não sabe o número de oxidação dele a gente vai colocar MN e animais sim eu li é completamente Ele disse que foi produzido o manganês você não tá falando nada a gente obtém que esse manganês é metálico com o número de oxidação igual a zero quantos elétrons tem que receber aqui ele vai receber n
elétrons Então quer dizer que um molde manganês reage com n mol de elétrons e esse n é justamente o estado de oxidação agora a gente pode fazer uma regra de três como a gente pode achar o número de mol de manganês que foi obtido aqui como dividindo a massa do manganês pela massa molar dele o número de modo manganês vai ser 4,9 G / 54,9 gramas por mol Então se a gente fizer essas contas vai dar 0,089 três Então essa quantidade aqui vai depender de que 0,1 em 79 Mall é justamente a quantidade de elétrons
que a gente viu que percorreu o circuito na le droit tá agora a gente só fazer a regra de três vai ficar esse vezes é esse e esse vezes você vai ficar 0,089 3M = 0,179 então ele vai ser igual 0,179 / 0,080 e 93 fazendo essas contas a gente vai encontrar que o n é aproximadamente dois Portanto o número de oxidação do manganês vai ser dois mais beleza vamos agora ver o tópico de corrosão corrosão e quando você tem o desgaste do material ela pode ser ocasionada por vários processos e um deles são reações
de oxirredução principalmente com o oxigênio da atmosfera então por exemplo aqui quando você tem o ferro o fim o que pode oxidar naturalmente pode ser tanto na presença de oxigênio atmosférico Quanto pode ser na presença de água água de ontem da própria umidade do ar ou da chuva então durante esse processo você vai ter uma reação de oxirredução onde o ano vai ser o ferro se convertendo em Ferro 2 e liberando dois elétrons e o meu caso o cátodo vai ser o oxigênio que vai reagir com água mais da água produzindo água e recebendo quatro
elétrons do fé Então é assim que você tem a formação da ferrugem professor e à corrosão a problema se séries você vê tem problemas que queda de internet por quê Porque a oxidação dos contatos do Fio na internet você tem oxidação de transformadores aqui em Quixadá é complicado a minha bicicleta Oxi dou certo oxidou até a corrente dela inclusive o cadeado e é um processo que a gente tem que evitar o desgaste de cima as portas para gente então Quais são os alguns métodos de proteção uma delas é chamado de ânodo de sacrifício e que
consiste assimétrico por exemplo aqui você tem o ferro então com ferro e vai oxidar Você tem o potencial de redução deles potencial vai ser de 0,44 volts negativo para evitar que ele na hora que ele tiver em contato com aqueles agentes que podem gerar oxidação dele você pega o fio condutor e conecta ele com um elemento que seja menos Nobre No caso Quem esse é lamento o magnésio no momento que você encostar o magnésio aqui o potencial de redução do magnésio vai ser de menos 2,43 volts ou seja ele tem mais facilidade de oxidar que
o ferro então no momento que o oxigênio e o h mais eles tentaram tirar os elétrons do ferro eo magnésio imediatamente vai repouso elétrons evitando assim que o ferro bom então esse aqui é o método do ano de sacrifício e o que é que vai acontecer com magnésio professor ele vai escorpião aí dentro até acabar no momento que ele acabar ele não consegue mais proteger o ferro Aí você coloca outra peça de magnésio segundo processo é chamado de galvanização a galvanização você consiste em você fazer o que você pode recobrir o metal com ou metal
que seja mais nova que ele ou metal que seja menos Nobre mas que quando ele oxide a camada fique impermeável ao ataque de novas espécies oxidantes nesse caso aqui a gente tá usando o cobre e você pegar um prego de ferro e mergulhar Nossa solução contendo cobre imediatamente ela vai ficar castanho que é a cor do cobre o cobre como é mais nobre ele tem mais dificuldade oxidar então consequentemente o que acontece ou prego ele vai resistir mais tempo o outro forma de você fazer isso é você colocar por exemplo cinco e você colocar o
zinco como cobertura o cinco quando oxidar ele vai formar o óxido de zinco O óxido de zinco diferente bloco de Ferro ele não fragmento e não esfarela ele faz uma camada de proteção chamar de camada de passivação ele adere na superfície do metal e impede que o oxigênio que entra em contato com o metal do interior tão ocorresse ele consegue proteger então com isso a gente encerra a nossa unidade eletroquímica um grande abraço a vocês e bons