Oi tudo bom amiguinhos Então vamos para aula complementar né aqui das proteínas e aminoácidos então não tivesse falar agora um pouco mais dessa parte molecular né das proteínas nos aminoácidos meus pedidos não se né e e ela requer um pouco mais de atenção essa aula é esse complemento na realidade então eu aconselho que se você não não pegou muito bem a parte básica que foi a anterior da mais uma assistida Nela né dá um presta bem atenção nos permos para você conseguir é pegar essa aula com qual se lhe dar certo se você não entendeu
os termos entre em contato com titio ele tá aqui para tirar suas dúvidas Neto alivia o WhatsApp segunda-feira um dia inteiro aqui horário de atendimento né então ainda hoje aí na aula você vai que o horário da aula que você pode pausar manda uma mensagem para mim vai tirando suas dúvidas mas eu aconselho que você Entenda bem a primeira parte para poder entrar nessa agora tá e não só isso você vai começar a perceber que na bioquímica as aulas são bom então a aula que vem posterior sempre depende da anterior tá então sempre estude tudo
que você já tem você já tem que tá estudando todo dia para poder entender os próximos contém outros Mas você vai perceber isso agora tá bom bom então a gente vai falar agora dessa da química aqui do primeiro mexer Falamos os alunos lá na frente vai evoluindo prazo proteínas né então a como eu tinha dito deu introduzidas em anterior né existe uma ocorrência de isômeros entre os aminoácidos né então os número é o seguinte pelo fato do aminoácido você essas quatro ligações aí nessas permite seus quatro componentes diferentes em volta dele né é ele faz
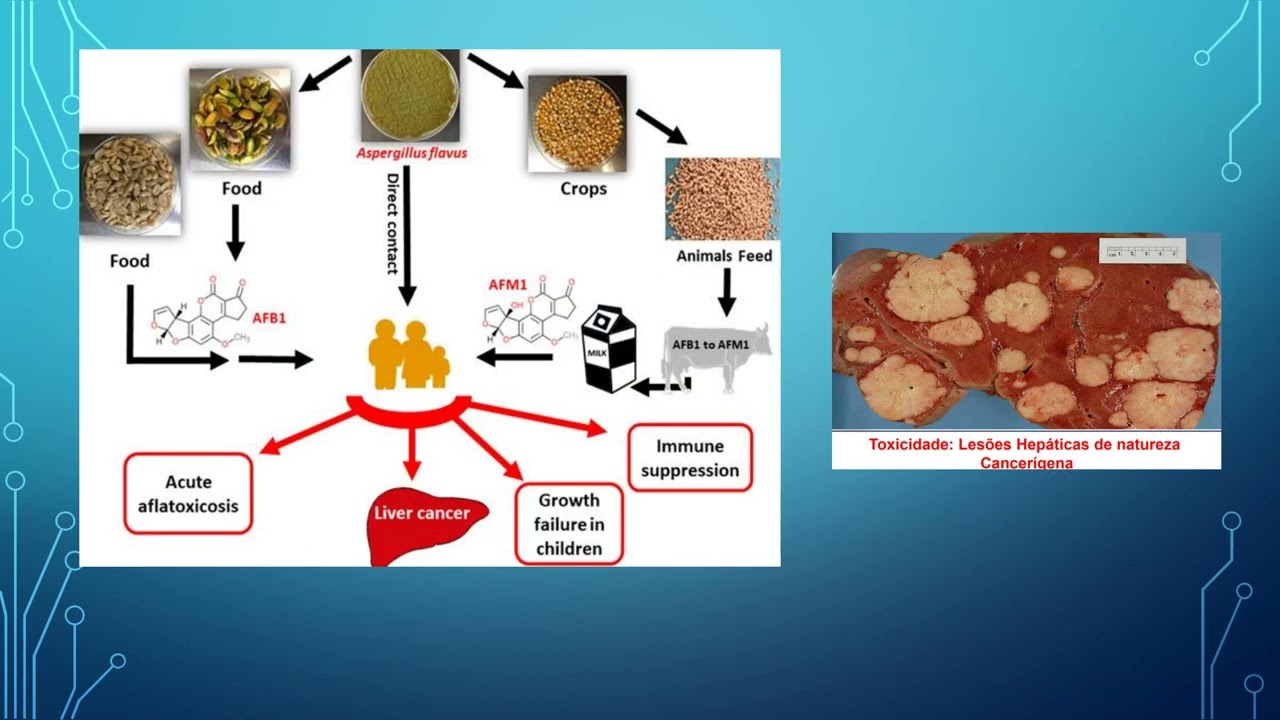
com que eu tenho um outro componente que como se fosse uma imagem especular não imagem refletida E esse aminoácido né só que para gente né não nos animais né a maior ocorrência real o dominou as uma posição Hélio mas como os senhores né sandália da saúde é importante entender quando você vê lá na receita do medicamento que aparecer isso aqui ó você pode ter certeza que você está na sua mão antibiótico né então isso é muito importante você pensa noção você beber na sua receita de aminoácidos você pode ter certeza que você tá cê tá
lidando com um antibiótico é porque esse Tipo de aminoácido só é presente antibióticos em bactérias então por isso que eu fiz só colocar tudo aqui a mais para utilizar né Principalmente ao pessoal da enfermagem né o pessoal aí da da área de medicina também né então você tem que saber quando você deu e você vê isso da Quina esse termino laço saiba que você está lidando com um antibiótico né e antibióticos são componentes você tem que tomar muito cuidado né porque você pode gerar no seu Paciente uma determinada resistência ali ele pode pegar uma super
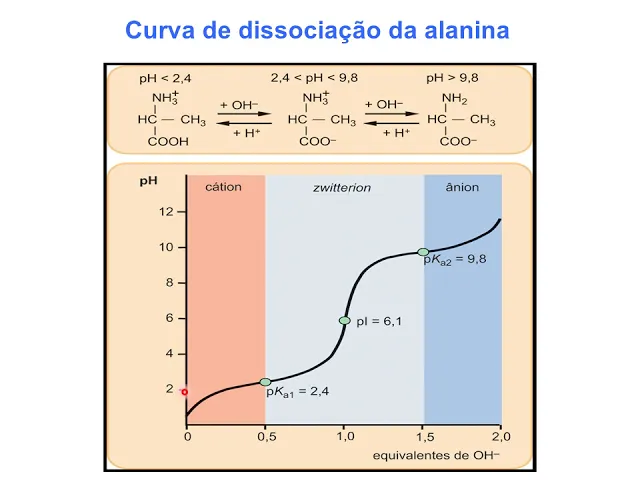
bactérias uma superbactéria e Babau né by Fábio vai-se embora e quem tiver perto dele também né sabe-se que existe uma teoria aí que o fim da Humanidade para ser através de superbactérias vai chegar uma hora que a gente vai selecionar tanto dele dos antibióticos que vai aparecer uma vez vai ter tecnologia para se livrar dela tão cedo tá bom então só para ver se aí frisado isso daí tá bom então vamos Relembrar um pouquinho essa estrutura e agora você vai entender um pouco melhor por que que eu coloquei na aula básica essa estrutura zwitteriônica né
que ela tem o cemitério Esse é o nome alemão né e se esse componente aqui positivo esse componente negativo né ele tem as duas polaridades de uma mesma molécula né eu coloquei isso daqui vocês estudaram já bastante aí sobre PH é sobre pecar né então vocês sabem que no PH fisiológico aqui acabou axila Ela já diz pro tornou Então pecado essa acabou axila aqui ela tá abaixo de 7.35 Com certeza né Enquanto aqui esse grupo aqui um um grupo A minha está protonado né significa que esse grupo aqueles ele não alcançou ainda o pecado ele
né então dentro de um PH de um um PH fisiológico o grupo Amino encontra-se protonado quando ele apresenta esse hidrogênio a mais aqui né então isso caracteriza um grupo carboxila como um grupo ácido Oi e um grupo Amino como um grupo base Porque e lembra lembrando vocês né que que o grupo a se daquele grupo que tem a capacidade de perder próprios para o meio né e o grupo basta de receber próprios então ele retém isso pronto até em PH básico né então é uma coisa muito interessante que você vai notar né é que não
solução a gente vai começar agora explicar isso daí é por isso que eu pus essa composição do interior única não é natural né você vai perceber que não existe a possibilidade um solução Pegadinha de prova em solução não existe a possibilidade de você encontrar um aminoácido na sua forma natural né você encontra às vezes ela é possível na sua forma cristalizada mas na sua forma em um solução é impossível a forma natural você vai ver isso daqui e vai ser agora o nos próximos slides exatamente para que você entenda isso daí tá bom Tá bom
então eu fiz aqui se vocês aí que estudaram né com certeza tô estudando Bastante né a essa parte de ácidos né que o assunto tem essa capacidade ácidos fracos é porque lembra um ácido forte e desprotona assim não é esporte de contato com um ali a água da atmosfera e já traz rebolando para fora e o seu hidrogênio porque a base desse ato a base conjugada dele não tem bastante afinidade pelo próprio né enquanto os ácidos fracos as bases Elas têm né Ela já tem uma afinidade maior ali pelo seu próprio né então é o
que acontece é que Essas bases à medida que o PH vai se levando então a concentração de hidrogênio by reduzindo no meio né então aqui ó você ver que eu tô jogando o hidroxila Então ela tá capturando os é que tá nessa solução aqui aí o PH vai subindo Só lembrando né o PH dois tem menos hidrogênio que o quatro porque eu dois eu tenho 0,01 olar de hidrogênios né o quatro eu tenho 0,0001 Olá e assim por diante sai por isso né Porque o PH é quando eu tenho minha concentração de 2 - molar
tomada na forma logarítmica na base 10 negativa então é por isso que eu contrário né então o que acontece é que os aminoácidos Se você olhar um aminoácido ele tem também então como a gente viu lá um grupo ácido no grupo básico né o grupo alcoxi né que é que dar e o grupo Amina o que dá o grupo aminoácido do nome dele né E esse componente sim solução de acordo com PH da solução opera igual ao máximo e nem tão o ácido fraco então militar em Solução e derretendo e de acordo com ph o
seu hidrogênio porque a base conjugada desse acho que eu tenho uma uma afinidade relativa nesse caso aqui a mina o apague aqui da mina que seria um nh2co grupo Amina né é ele tem uma afinidade muito muito muito mais alta pelo seu próprio ele não quer largar o próximo de jeito nenhum meu amigo só a cor não tem usar um PH que já encontra em condições alcalinas né um ponto aqui acaba boxe aqui ó tá bem noção no PH 2.4 Ela já tá no seu perca a lembra nós tivemos ficar na aula complementar de vocês
então é quando a isso é importante que é pergunta de prova né a equação de Henderson errar seu barra explica né E ela mostra que o pk a nossa que nesse PH aqui ó eu tenho PK até quando eu penso as condições as minhas concentrações de base conjugada do ácido e o o ácido conjugado a base estão em cinquenta por cento meio a meio então lembra lá na fração quando o Número de cima igual número de baixo ele é um né E aí o log na base 10 de um a zero então aí o pecar
é igual ao PH da solução então nesse ponto aqui Eu tenho 50 por cento da minha do meu ácido carboxílico do meu aminoácido ali eu tô cinquenta por cento sem o hidrogênio cinquenta por cento com o hidrogênio ele tá cinquenta por cento vamos falar a linguagem que eu que imitei eu acho que você já estudaram bastante eu já posso falar ela tá bom então eu tenho 50 por Cento desprotonado e eu tô com 50 por cento protonado como estou no pecar né quando eu é super opinar dopeka desse grupo com a box Lembrando que o
PK a ele é uma unidade de medida que é isso traída né não naturalmente mas eu preciso titular né então todos os esses grupos existe uma tabela que já foi feita né o isso é uma coisa estudada muitos anos né então um homem já tem uma tabela de todos esses pecados né Então olha só a medida Que eu vou adicionando mais hidrogênio eu vou cada vez mais passando desse sábado aqui para esse estado aqui nem provocada vez passando por esse estado aqui e aí olha só que interessante né então eu tô protonado aqui eu tô
eu tô Desculpa eu estou protonado aqui e eu também estou protonado aqui mas como ação de uma base né que eu tô numa carga positiva na medida que eu vou te pro tornando eu vou entrar numa carga e olha só se interessante uma coisa né Nesse momento nesse PH 2.4 né Eu tenho 50 por cento desse assim e cinquenta por cento né cinquenta por cento é desprotonado nesse ato de pecar mais se PH abaixo de 2.4 eu estou cada vez mais protonado estão cada vez que eu me distancio né do meu PH vamos lembrar né
Lembra daquela unidade da imunidade de um PH eu garanto que eu tenho quase cem porcento eu não tenho 100 porcento lembrando quê Por quê que eu não tenho Posso até fazer essa pergunta na prova Que tá acontecendo por cento nunca porque a constante de equilíbrio não muda nunca querido ela nunca muda eu nunca posso zerar esse valor aqui ele nunca vai ter zerado né porque tem condições reais eu não sei por cento da reação nem Tony nunca vai gerar mais abaixo eu garanto que eu tenho uma proporção extremamente elevada já dessa condição aqui do do
grupo carbox protonado né então eu tenho na quase quase cem porcento não é 100 Porcento tem um quase cem porcento dos meus aminoácidos eles vão estar numa condição de carga um olha só tem uma carga positiva não tenho mais nenhuma carga em nenhum outro ponto aqui eu tenho uma carga positiva aqui tá vendo então a medida que eu vou adicionando hidroxilico tirando prótons no meio o meu PH vai agora ser levando vai ser levando ele vai ser levando de tal forma agora até que vai chegar um ponto onde eu vou ter uma A grande maioria
ou até Quase que eu total dos aminoácidos eu já botei o meu grupo com a boca é totalmente desprotonado e eu vou ter o meu grupo Amino ainda aprontou nada porque eu já sou linda tá muito distante ainda do PK quando eu tenho 50 por cento e cinquenta por cento e eu estou abaixo de uma diferença de PH dois ainda do pecado dele então eu tenho nesse ponto aqui que é um intervalo entre os dois pecados aqui Ness eu sou mais se ficar com esse pecai dividir por dois Esse é o Ponto que sai com
distante entre o PK aqui do meu grupo Amino do ano ou da base né E aqui do meu carro adicionei aqui do do meu ácido eu estou indo e distante neste ponto é o ponto que probabilisticamente eu tenho uma concentração elevada de aminoácido com um grupo carbox desprotonado e o grupo Amino protonado hein Ah que legal eu tenho uma carga positiva e uma carga negativa Então eu tenho agora um aminoácido que tem uma carga Total 0 ele tem uma carga total agora zero né então o que que não tem que implica que isso daqui a
importante se meus amiguinhos né porque muitas vezes aí né você vai estar uma situação né o no hospital até mesmo no seu consultório né que você precisa fazer uma análise rápida de aminoácidos e de vida ou qualquer coisa do gênero ou mesmo tempo conhecimento se você for seguir uma linha Laboratorial né o que acontece é que os aminoácidos o possuir essa Capacidade de ter em cargas né eles são capazes de serem transportados num campo elétrico né esse campo elétrico geralmente é feito em soluções tampões que que vão amar estabilizar o PH da solução num determinado
PH específico né que faz com que eu tenho eu tenho lá um componente ali que permite o transporte de uma substância que tenha carga né então esses daí é feito no chá mais no chamados 10 de eletroforese eu vou Mostrar para vocês no finalzinho ali quando tiver falando de proteína não finalzinho já no final de tudo aqui que até agora a gente tá falando de cargas de só um aminoácido né a gente vai no final para você entender isso daqui que eu passar esse conteúdo a gente vai falar sobre a carga total de uma proteína
porque o quando você tem uma carga Total 0 né quando você tem aqui uma carga Total 0 o que que acontece quando eu coloco esse a Noah sido aqui Nunca o outro magnético ele não se movimenta nesse canto então se eu fizer um gel de eletroforese que eu tenho meu PH determinado né eu sei qual é o PH ali do meu da minha o meu campo eletroforético né vamos dizer que é desse eu quero isolar isso ali no astro aí eu jogo ele ali dentro do meu Pocinho vocês vão saber o que é esse daqui
a pouco do meu céu eletroforese e submeto uma carga né aqui sem carga positiva vão migrar no Sentido ali do ano aqueles que tem carga negativa vão migrar no sentido do cátion naquele gel e vão sair do gel uma hora ele vai sair do gel para carinho tampão né E aí você vai acontecer eu Rei extraindo agora aquele gel eu tenho certeza porque eu coloquei no PH 6.1 aquele que eu abrir o ácido vai sabe no meu céu porque ele não vai se movimentar Ah então você está aprendendo agora tá vai aprender o que é
o ponto isoelétrico que é isso que significa p i né que é o Ponto isoelétrico tem uma forma que a ciência tem e os profissionais da Saúde de Zola e aminoácidos para fazer análises dos pacientes né ou estudos biomédicos e o científicos biológicos né e sem muito importante para a ciência tá então agora a gente vai conhecer sobre porque no esse daqui é o genérico É então a gente tem que entender os outros também então só complementando então a medida que você agora começa a aumentar o PH da minha solução você está Extraindo os próprios
por causa da você tá acrescentando hidroxila Sally uma base forte está colocando ali em solução eu vou chegando no pecado meu ônibus e a que horas são que vai acontecer não vai chegar o ponto que ele vai agora desprotona ele vai perder aquele próton e agora ele se tornou aquela base né ele perdeu o próprio mas ele perdeu um PK já alcalino né então por isso que eu grupo Amina considerado uma base o carbox se né Então olha só eu já tô e pecar 9.8 e Eu não consegui chegar né a posição natural né do
meu que eu tô protonado aquietou produtor desprotonado aqui Então veja assim solução você não consegue chegar nunca a condição natural do seu aminoácido então é por isso que eu apresento a estrutura do interionica ali né justamente por causa deve é desse nesse dessa dessa situação aqui então a condição natural é só por aminoácidos está cristalizado em solução e você não vai conseguir Agora você Começa a entender a importância da água né então lá vou te permite existir um ambiente né sou o Uber uma solução né é importante para estrutura de todas essas moléculas biológicas né
Muito importante a água né Tá bom olha só agora aqui tá mostrando de uma forma mais química né então estudar aqui é uma linguagem bioquímica lembra que eu tô sempre falando para vocês desde a primeira aula sobre a flechinha né a pretinha está representando o que está acontecendo uma Reação química então estudar aqui esse tipo de reação química é uma reação de dissociação né então eu tô Ah desculpa é uma ração de análise né Eu estou dissociando estou eu tô Diz pro tonando perdendo esse próprio aqui do meu grupo Car boxe e amei um movimento
nesse sentido eu vou também de fazer uma outra reação de análise né onde eu perco mais 1 e 2 sendo aqui para solução né e é no quando o meu grupo a mim está destronando né então aqui com a Minha forma indo elétrica por quê que ela é isoelétrica porque ela tem uma carga Total 0 a carga Total dela é zero porque eu tenho uma carga positiva e uma carga negativa uma carta positiva com a carta negativa fica uma carga Total 0 né aqui só tem uma carga positiva Então esse esse grupo aqui né que
saiem PK chamado clicar muito que quando eu estou apaixonada nesse ponto eu estou abaixo do pecado do grupo caboxe porque o pecado ele está no ambiente ácido né Nesse ponto aqui eu o meu aminoácidos tem carga residual um nesse ponto aqui eu tenho uma carga reduzir 10 porque eu estou implicar um e o pecado dois o que garante que ama probabilisticamente que o meu aminoácido está o máximo de concentração possível com essas duas condições aqui a minha caboxe protou nada meu grupo é desculpa a minha caboxe desprotonada e o meu Amino protona à medida que
então que eu vou aumentando vou promover numa reação De análise aqui perdendo o meu hidrogênio aqui né sociano pro tonando é do meu desculpa perdão eles pro tornando aqui do meu grupo Amino perdendo esse esse hidrogênio aqui eu vou contornando eu vou perdendo esse grupo aqui e aí eu vou chegando a uma condição do meu aminoácido agora tem uma carga residual um negativo né então não vai ter uma carga residual um negativo mas que eu amei o meu BH não vai e não amiguinha ciumenta' cada vez mais O meu PH eu vou desprotonar esse hidrogênio
aqui e eu vou então tem uma carga cedo ao menos dois então eu nunca vou conseguir tá por tornando aqui e aqui desprotonado então você nunca atingir né a condição do amigo não acho a produção natural isso que eu tô te mostrando né e Inclusive tem uma fórmula Zinha muito simples aqui é só somar o PK um mais você K2 se divide por dois eu tenho untei agora é uma coisa pergunta de prova prestem muita atenção o que é o Pe cara Eu repito isso várias vezes né mas chega no dia da prova carai rap
é um PH repita amigo é um p a pagar você vai repetir 10 milhões de vez vai com 40 da prova é um PH da solução quando o meu aminoácido que está dissolvido encontra-se na forma isoelétrica Então tem que é o PI é o PH meu condenado meu filhinho mas um monte de gente baixar na prova é o PH da solução é o valor do PH da solução isso é o PI é o valor do PH da solução quando O meu aminoapp tem uma carga residual zero Ela É zero eu a somatória entre todas as
cargas dá uma carga residual tu meu aminoácido zero e isso acontece em condição fisiológica aqui daí uma alguma parte desses aminoácidos vem condição fisiológica mas olha lá embaixo ali monoamino né o Uno carboxílico né então isso é uma condição para os aminoácidos que são [Música] monoamino monocarboxílico né Porque que O titio tá falando isso daqui para vocês né como vocês estudar tem gente até que já sabe desenhar até né todos os aminoácidos aqui é emocionante isso né Você sabe tudo já sabe todas as siglas eu nem precisava tá falando isso que você já sabe dentro
de tudo né então vamos lembrar que existem aminoácidos que o grupo erre também é carregado ou Who ácido não é um grupo aqui então por isso esses que tem carga negativa são chamados de grupos polares cargas Negativas ou grupos ácidos né e eu tenho aqueles grupos vasilicos porque eu tenho uma carga positiva está pro todo é um PH fisiológico né então isso aqui em PH fisiológico né Então meus grupos erres né eles encontram-se com cargas Ou seja eu preciso ter uma outra fórmula um outro cálculo para eu poder alcançar o ponto isoelétrico desses aminoácidos é
o ponto isoelétrico PH da solução onde o aminoácido tem carga residual zero ou seja ele encontra-se na sua forma isso Elétrica é o PH da solução não adianta pelo ainda mais de 50 anos a prova do do pessoal terra na prova é impressionante né eu é legal Depois eu mostro em todo mundo dá risada né até os que erraram Bom enfim é né Então Significa o quê então Neco é os meus aminoácidos que tem esse grupo R né um a possibilidade de protonar ou desprotonar significa que eu não posso levar em consideração a mesma forma
daqueles Mundo Animal monocarboxílicos Né neste caso aqui eles são monoamine micos mas dicarboxílicos né eu tenho uma acabou se lá no meu grupo R Então à medida que o meu pé tava subindo né É óbvio que no ambiente ácido eu vou desprotonar o grupo ácido mas eu vou desprotona também outro grupo astro e daqui a pouco eu vou mostrar um ter uma tabelinha né é muito importante Importante perceber que o pecado esses dois indivíduos aqui esses dois pecados aqui ó eles são muito próximos aqui Desculpa esses dois pecados aqui ó prendam esses dois pecados aqui
ó eles são muito próximos certo é deixa eu ver uma coisa que isso é esses pecados aqui são muito próximos então esses esses pecados aqui então são aqueles que você vai verificar qual é o ponto isoelétrico de um aminoácido porque amiguinho que tem que ser com esses dois aqui porque nesta condição aqui no intervalo entre esses dois é quando eu tenho minha carga residual olha só aqui tem a carga Residual um positivo Olá neste caso aqui eu tenho a minha casa residual zero então entre esses dois pecar he's a garantia deste grupo aqui porque nesse
outro aqui meu amigo eu tenho carga residual já menos um porque olha eu tenho uma positivo aqui e eu tenho duas vendas ativas eu tenho menos um à medida que eu me desloco para cá eu vou aumentando o número agora de cargas tentativas eu tenho menos dois subir imagens para tornar esse cara eu Vou ter menos três certo então neste caso dos mundo não amigos e carboxílicos mono a mim Vinde carboxílico a fórmula para o cálculo da data do PPI né do PH da solução onde o meu aminoácidos encontra-se na forma isoelétrica é um pegar
um mais um pkr E aí e o meu amigo grupo R né meu camarada radical né aqui o grupo R né lembra que ele pode ser chamado de grupo R ou cadeia lateral né e assim por diante né Tem vários rapidinhos isso daqui isso não pertence aqueles aquelas funções que dão o nome do aminoácido Amino Ácido é o grupo R certo então eu tenho aqui a somatória do pkr mas vou pegar aonde / 2 eu vou ter o Pein que é o PH da solução quando eu encontro a forma isso elétrica ou a carga residual
do meu aminoácido é fizeram certo então agora a gente vai ver aqui né e a dissociação de um aminoácido carboxílico né d-amino monocarboxílico e Meu amigo ele não eu não vou nem perder tempo e aqui olhando aquela hora namorado que tio vai mostrar porque precisa tem paciência com você né E é assim que você vai entender olha só aqui carga Total 2 né aí a medida que vai subindo É lógico que é o ácido que vai desprotonar né meu amigo então diz pro tornou carga residual Total mas com menos zera 1001 mais ou menos vê-lo
carga residual Total um né A medida que eu vou subindo agora eu vou desprotonar Né aqui um dos grupos amigos mais uma vez esses pecados aqui eles são muito próximos eles são bem próximos Então quando você quiser e do Pein mede um dia menino carboxílico UFPI sempre vai estar lá numa posição mais básica enquanto quando você fizer de um monoamino dicarboxílico como pe é próximo dos carboxilas os dois eu voltei UNP em uma solução ácida Lembrando que ele tem na sua cadeia lateral carregada é tanto esse quando o de carboxílico né É um PH fisiológico
isso tem uma importância muito grande amigo e você vai saber daqui a pouquinho essa importância né então como esse daqui eu já tô no meu ponto isoelétrico já numa condição uma região mais básica né então eu vou fazer o que eu vou eu estou entre um intervalo do pecadores aqui e eu estou destronando lá o meu grupo Amino aqui ó tá vendo e quando eu estou destronando entre o intervalo de quando eu já tô tornei aqui o meu grupo Amino Da cadeia lateral do grupo R policial pegar Ah é Então a fórmula para eu saber
quem é esse carro aqui então eu dar tanto probabilisticamente que a distância de PH mais longa dessa aí mais longa dessa eu tenho quase que sem por cento Total desse grupo aqui né então o meu ponto isoelétrico para antes de do desses indivíduos aqui está entre esses dois foi para o pecado dois que é o pecad desprotonar quando disputou no meu grupo Amino lembrou a nunca estou Tornando no ambiente básico e o meu grupo é rico e também uma minuto parece que eu tô dando do grupo baixo então comeu Pein vai ser o ph alcalino
feia eu a solução quando eu encontro a forma isso elétrica do Meio aminoácido tão e posso dizer então miopia aqui ele está em um ambiente alcalino né enquanto usado o grupo o carbox eu estou em um ambiente ácido né entenderam é facinho não é difícil é só você rever sua mente vezes que você vai entender né eu sei Que tem muita gente aqui já entendeu não é difícil Tá bom tô te pedindo tá brincando com você tô deixando você apavorada para ver se você estuda tá bom Não deixe para o dia da prova que você
não se está com problemas né Tá bom então aqui tem uma tabelinha né dos aminoácidos aqui né Tá vendo aí você vem aqui uma tabelinha aqui dos aminoácidos o Pein desses aminoácidos né então se você for lá naqueles grupos né ali ó a tirosina ali né que tem tem uma Mina lá se olha depois lá na composição você pode bater o olho aqui direito e já falar meu amigo olha só eu nem vou olhar o aminoácido eu vou fazer a bolinha aqui tu já vai lá olhar retinho tá com a garganta Bad né olha lá
esse aqui é pertence ao grupo básico esse pertence ao passo esse potencial básica hipertensão básico Esse é o ácido Esse é o ácido e sal assumo meu amigo né eu acabei de explicar que o p II né instalar como entre dois grupos a Meninos né ele vai estar em um ambiente básico Então pode conferir lá tirosina pertence ao uso os grupos de aminoácidos é de carga positiva é a minha cisteína ali também né ali a minha visinale também né aliás menina também quantos grupos Zap puxa aspartato e glutamato né a Speed não pode bater o
olho lá que ele tá pertencendo as grupos ali ácidos ali né porque né meu grupo é ele já tá me formando né então você pode ter certeza ali que isso já tá ainda tem Certeza que o seu grupo é muito forma quem é o indivíduo né Tá bom então galera Então vamos continuar tenho certeza que todo mundo já entendeu isso daí não tá difícil né pelo amor de Deus não está difícil tá bom Valeu então bom então agora o seguinte vamos falar sobre o pe de uma proteína né porque amiguinho igual quem estiver dentro de
um pronto socorro em um hospital no laboratório você vai ver esse equipamento né e muitas vezes você vai Ser tudo lá dentro só seu médico enfermeiro auxiliar técnico biomédico você vai ser tudo então você tem que ter um pouquinho de noção você vai ver se vai mais para frente né Então olha só o p i de uma proteína é um calculável cara não adianta você querer tomar o pedido de um play-doh outro peido aquele cara eu perdi um não adianta você querer fazer isso porque um altera o outro altera o outro vai ser em calculável
a única forma de você verificar o pedido De uma proteína é você colocar ela aqui dentro desse Pocinho Oi e o céu né O gel é tipo uma gelatina que você tem pão líquido para fazer ela certo então que líquido que você vai para o você vai por líquidos com ph as variáveis aqui né Então na hora que você ligar cargas positivas os as proteínas que tem uma carga total é negativa vão me dar no sentido aqui positivo e as que têm negativa vão cair fora aqui e as outras como chegar em um PH que
é o Ponto isoelétrico dela ela para ali ela para de se movimentar Então você deixa o aparelho ligado por um determinado tempo né e pronto aí depois você pega ali Purifica o céu você vai ter certeza que a única proteína que ficou ali foi a proteína que você colocou o PH desejável bom né isso daqui é muito feito nos próximos procedimentos chamados de 1 e tem blocking né a forma de você identificar a presença de determinadas proteínas e depois você tem até como Quantificar elas de forma relativa né você vai comparar ela com uma outra
loja tem mais do que aqui nesse outro Pocinho né O que você coloca uma de coco agora aqui depois nela né cê vai fazer o procedimento esse tipo gruda na proteína né E aí você tira uma foto ali dela com uma luz fluorescente né E você vai ver que um tá mais brilhante do que o outro é você fala Olha tá vendo esse tem mais que o outro você não diz a quantidade exata Mas você pode fazer uma análise Relativa olha essa a proteína que eu botei nesse ponto Sininho aqui tem mais do que essa
ficou na bota o anticorpo que tá ligado a uma substância brilhante e essa que brilha mais do que essa a Deus é uma chamada análise relativa então não tem como você calcular o pi de uma proteína É incalculável né mas você pode zoar essa proteína quando ela chega em um campo elétrico Aonde a capa residual total da minha proteína fica zero né aquelas radicais disputando os Plantamos defrontando para o cano cortando os até que no total fica zero e ela não tem mais a capacidade de ser deslocada em um campo elétrico ela precisa ter carga
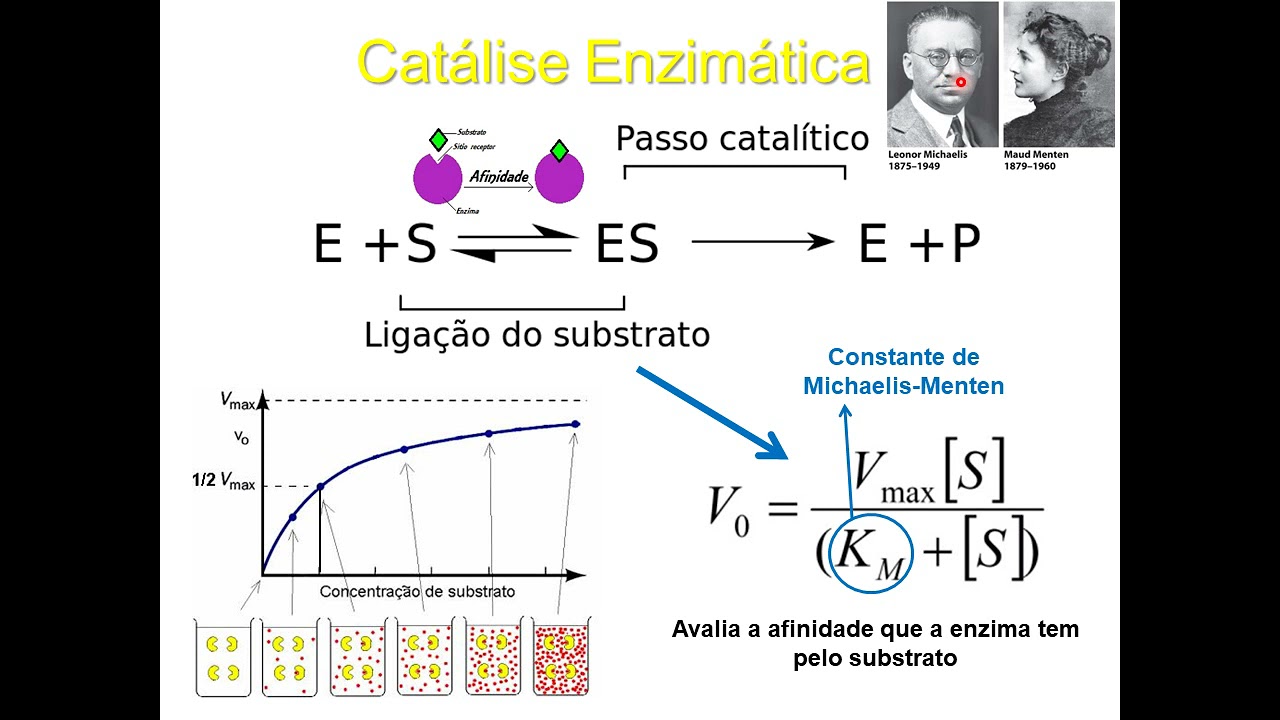
para se deslocar no campo elétrico tanto ela quanto um aminoácido né certo então aqui agora a gente vai começar agora aumentar o tamanho das coisas né E já vão partir agora para analisar com mais detalhes essas estruturas tridimensionais que as proteínas fazem Lembrando que ela é a União de vários aminoácidos Ah entendeu agora um pouquinho mais da química do aminoácido agora a gente vai entender um pouquinho mais a da proteína né e meu amigo o que que determina a função de uma proteína se tu não sabe meu irmão você está com um problema muito sério
né muito sério meu amigo o que determina é a estrutura tridimensional dessa proteína Eu já falei isso um milhão de beijos e é óbvio que titio vai cobrar de alguma forma Isso na prova né então a estrutura tridimensional de uma proteína é o que determina a função dela Então nada mais do que natural a gente entender um pouco mais de como que se forma nessa estrutura tridimensional de uma proteína sítio tá aqui não fica assustado que tio faz aquele papel de professor né tá no sangue foram muitos tá dando aula para Ensino Fundamental e Médio
né então eu tento fazer você escutar de qualquer jeito que no dia da Prova estudar no dia da prova um dia anterior tu não vai passar irmão não vai e mão irmã Ore ore bastante mas estude depois tá entendendo todos os dias estamos lá e não eu coloquei isso daqui né para gente se relembrar né que a proteína ela pode ser analisada né De acordo com a sua estrutura primária que a sequência né estrutura secundária então tocou nesses desenhos que nós vamos ver várias imagens disso aqui agora daqui para Frente para você entender como a
literatura Pode mostrar uma proteína para mostrar assim ela pode mostrar assim ela para mostrar assim é de várias formas né então a gente vai agora analisar parte por parte aqui a estrutura primária primeiro depois a gente vai analisar secundária separadamente né alfa-hélice e a folha Beta pregueada depois a gente vai entender a estrutura terciária que entendendo isso daqui a terciária Quaternária fica muito fácil né Só lembrando uma coisa já Ai meu Deus Eu repito 1 milhão de vezes e metade da sala sempre erra essa pergunta sim determina a estrutura terciária e quaternária da proteína e
todo e bota na prova não errou é a sequência de aminoácidos que determina determina tudo aqui amiguinho é a estrutura primária né então vamos começar essa análise aí né antes disso a gente precisa entender uma coisa E quando se forma uma ligação peptídica que eu perco uma molécula de água né e eu fumo essa unidade peptídica que é extremamente importante para a formação da estrutura secundária sem ela não cola estrutura secundária e já imagina o resto né Então essa unidade peptídica né que tem a ligação a ligação que pedir de ter só isso aqui a
unidade pedir que é o seu duplo em H É esse aqui é a unidade que pedir dica certo aí todo mundo ela também o meu Deus né ela ocorre um Evento de chamado de ressonância então o que que acontece este eletromaq que tá fazendo aqui uma ligação covalente aqui com esse oxigênio ele fica girando lá então você já me buscar nos dizendo capa para dizer ele fica segurando os dois mas eu tenho dois elétrons que estão fazendo isso não se esse danadinho escapar um e esse elétron garante esses dois presos certo e o que que
acontece momentaneamente né A eletronegatividade ali do nitrogênio e do oxigênio aqui elas não são tão distantes assim não tem que faz isso aqui faz com que momentaneamente o meu nitrogênio consiga né esse elétron acaba se sentindo atraído ele dá uma tardizinha uma paradinha no oxigênio que a nossa do nitrogênio oxigênio não é um pirilampo esse elétron aqui né então quê que acontece amiguinho quando ele vem pressa posição que vai ensinar um truque para você ó pega duas canetas agora e Pega uma caneta né e coloca entre o seu dedo lá aquele que faz um gesto
feio e o do lado né taça entre os dois uma caneta você Gira né segurando essa planeta seus punhos viram tem uma rotação né seus punhos conseguem ter uma rotação se encaixa entre o dedo que faz a coisa feia né entre o dedo faz a coisa feia e o da direita aí o das seda duas canetas tenta girar o punho seja não consegue girar o Bruno né você não consegue porque quando você tem essas duas aqui Ligações você não permite com que isso Rode para lá e para cá porque isso aqui tá fazendo assim isso
aqui tá fazendo assim essas duas conexões aqui paralelas não deixa ter rotação aqui certo isso faz com que a unidade peptídica se torna uma estrutura rígida ela fica que nem uma uma folha de papel ela é riso dela não roda eu só vou bater rotações somente nas ligações onde eu tenho o meu carbono quiral meu carbono Alfa então isso consegue rodar aqui assim estou Aqui consegue rodar aqui assim ou em volta aqui mas isso aqui não gira esse cara não vira e dois ele passa um presente para baixo e não roda esse aqui não roda
e subiram estrutura se vida é exatamente isso daí que faz com que os formatos esse cordão de aminoácidos consegue ter né ele não consegue adquirir qualquer forma qualquer formado por que essas estruturas rígidas e diminuem a rotação que você tem ali entre os átomos e não Deixa eles formar em qualquer figura não eles formam figuras limitadas né Então as figuras limitadas se eles vão fazer é o que vão caracterizar nem as estruturas secundárias e terciárias porque é lógico que eu dependo a terciária depende da minha secundária para ter o fubá tão dela depois a cara
dela né E a unidade peptide que é o que vai limitar a minha proteína né o meu Desculpa o meu pedido né A minha proteína já em e vamos falar alguma coisa grande né Acima de 10 10 cada alto Sabe o que eu tô falando né Então tá bom então uma coisa assassina sedex 10 tá daltons né eu vou limitar essa esse portão Assim eu vou dar só em duas formas Hoje vai ter aquele formato helicoidal da Alfa hélice ou ele vai ter aqueles tirado transando um Pocinho por baixo formando a folha Beta pregueada É
lógico que Existem forças e vão estabilizar essas estruturas ligações que vão estabilizar essa estruturas né mas do que vai Limitar ter somente esses dois tipos não tem como ter outro formato é a unidade peptídica Então é isso daqui essa estrutura rígida que limita com que os cordões de peptídeos só consigam formar o Fairy se ou formar foi a Beta pregueada E aí a gente depois vai entender como é que essas estruturas interagem entre elas faltam formatam t e ao final de uma proteína sérica bom então pessoal então agora a gente vai falar das estruturas primárias
né Então aqui é eu não vou estar cobrando isso daqui nesses anos dessas essas essas estrutura esses anos Philips se isso não interessa isso daqui para vocês né É agora nós temos um algo em comum medicina enfermagem nutrição aí depois da nutrição segue um caminho no terceiro a aula complementar a enfermagem não tem mesmo porque a carga horária são diferentes da Medicina também né e a medicina seja um caminho e aí depois da aula complementar nessas e terceira né As turmas e medicina são cobrados esses esses eventos aqui porque segue no sentido para dar suporte
a futuras disciplinas que eles vão ter né então não não interessa agora nesse momento para enfermagem mas o resto todo mundo é incomum aqui tá bom então não fiquem assustados nutrição medicina para mim não fique é a terceira cumprimentar é uma coisa feita para e vocês inclusive Então não é igual a complementar a terceira nutrição e Medicina não são iguais tá então mas isso aqui é importante que eu vou falar agora certo então é quando você analisa uma estrutura primária né Você sempre tem que analisar ela você isso daqui são as siglas né dos meus
dos meus é aminoácido eles recebem letras aqui né então quando você coloca essas você descreve as siglas dos seus aminoácidos então toda no exemplo aqui a Acabei de cá né então a Cadê não é igual a de cá amiguinho são diferentes o que neste Caso aqui o grupo Amino está em ar e nesse caso está em b e biologicamente isso são estruturas diferentes porque proteína se ligam a e as proteínas em atividades biológicos e isso faz uma diferença muito grande principalmente em um medicamento ou em um hormônio ou quando você tá caracterizando alguma coisa e
você vai enviar um relatório lá para o cara ai meu Deus põe honesto carro aí qualquer uma entendeu Você causar um problema Muito sério mas você tem que entender que um grupo Amino sempre é descrito na posição esquerda e o grupo carboxi sempre na posição direita o que estabiliza o estrutura né O que garante a estabilidade de uma estrutura primária amigo é a ligação peptídica e a ligação peptídica é uma ligação muito muito forte amigo não é tão fácil romper essa ligação aqui diferente da estabilizam as estruturas secundárias terciárias e quaternárias que a gente Um
pouco então é importante vocês entenderem aqui que jamais você pode descrever em qualquer posição né a linha de descrição dos aminoácidos da estrutura primária 70 e sempre colocar na sua esquerda o que saco um grupo Amino terminal e o que está com carboxiterminal do lado direito certo tudo bem então vamos entender que isso é muito diferente de isso daqui tá bom então vamos falar agora da estrutura secundária vamos começar pela pelas Alfa Service né Então as alfas hélices amigos são estruturas ele cuidar Então esse meu peptídeo ele como você desvira se sobre um eixo daí
eu tenho eu tenho um mês tô aqui e corta paralelamente aqui bom né as minhas essa estrutura né na cidade perpendicular aí eu posso traçar uma estrutura perpendicular para esse meu eixo né então meu essa minha essa minha é esse nessa estrutura helicoidal ela podem tô em torno de um eixo então isso daqui é uma alfa-hélice certo então Vamos entender alguma coisa muito muito muito muito importante e isso é pegadinha de prova preste bem atenção que um que faz a Pontes de hidrogênio da desculpa o que dá a estabilidade da minha alfas eles são as
pontes de hidrogênio que ocorrem entre o oxigênio da cara do grupo certo né agora e da carbonila né que não é mais carboxila né porque agora é um dupla ser aqui e o meu hidrogênio aqui e o meu hidrogênio que está conectado ao meu O hidrogênio nesse do grupo menino aqui então esses dois vão fazer Pontes de hidrogênio e essas Pontes de hidrogênio era só com pés em paralelamente ao eixo imaginário que existe no centro dessa minha alfa-hélice então presta atenção que os grupos erres eles não participam não participam da formação da minha alfa-hélice Opá
Pera aí que eu tenho que dizer uma coisa que alguém pode ler no livro lacinho mentiu para mim então deixa eu te dizer uma coisa os grupos é Né esses grupos aqui que estão voltados para o ambiente externo como se tivesse de uma forma imaginária ligado rapper pedido é perpendicularmente aqui aos meus ao meu eixo imaginário né esse o pênis eles eles podem alguns casos interferir no formato da minha da minha alfa-hélice né Por exemplo eu tenho cadeias longas aqui de vizinhos que têm Carlos aqui na sua extremidade que se estiverem muito próximas aqui elas
podem fazer esses grupos LC expelirem e não Consegui permitir a estabilidade aqui da minha alfa-hélice seu variar o PH isso pode acontecer né então e eu tenho por exemplo grupos grupos prolina lembra que a prolina ela tem um grupinho e não Amino a linha naquela conexão ali então a prolina não faz não consegue fazer Pontes de hidrogênio Então indirectamente nem tão indiretamente ali eu posso estar interferindo ali né os dois grupos R né na minha estrutura Mas eles na Em geral ali quase cem porcento ali não participa né ele não pensa participação direta de dar
estabilidade ele pode interferir na estrutura mas ele não vai estabilidade para estrutura Trindade sua habilidade para as estruturas secundárias são as pontes de hidrogênio ocorrem entre as cartolinas e os grupos e hinos aqui serve para essa ponte de hidrogênio aqui que vai vai dar estabilidade para mim estrutura no caso da alfa-hélice ela ocorre paralelamente Ao eixo certo e eu tenho uma volta de 3,6 aminoácidos né Então é eu tenho marcado 3,6 anoas essa estrutura mais abundantes que tem estruturas nem lembra que a gente falou do colágeno que ela é mais despedida por causa daquela sequência
né que ela tem lá né glicina prolina e hidroxiprolina né lembra disso daí é Essa é mais uma forma mais genérica eu tenho a minha alfa-hélice em 3,6 aminoácidos né isso pode acontecer de Ser variável em algumas determinadas situações né de atividade proteica daquelas que das globulares são dinâmicas lembra a gente falou sobre sua aula passada né então uma média de na maioria numa estrutura mais estável tem uma volta de 3,6 aminoácidos acaba 3,6 aminoácidos eu tenho uma volta na minha alfa-hélice né e isso é muito importante o Presta atenção então os grupos erres estão
voltados então se eu pensasse assim como se fosse uma vareta né seria Uma vareta de espinhos e os espinhos são os grupos é isso é muito importante porque é o grupo R que vai dar estabilização estabilidade para as estruturas terciárias né e eles ficam voltados para o ambiente externo da minha Alpha é a forma perpendicular ao eixo imaginário certo então isso é muito importante para estabilização da estrutura terciária e quaternária também das minhas proteínas essa foi que a entrar terciária e Quaternária é uma coisa muito próxima é quase a mesma coisa só tem uma pequena
diferença a gente vai falar sobre isso daqui a pouquinho tá bom então agora a gente vai falar sobre as estruturas secundárias né Ah desculpa sobre as estruturas secundária folha Beta pregueada Então se a gente falou sobre a estrutura secundária Alpha é esse agora a gente vai falar sobre a folha Beta pregueada meu amigo tá fácil já me ver aqui né Eu não fumo estrutura ele Cuidado formam estrutura mais vendida mas olha se você olhar isso daqui ó você vai entender Por que que é folha pregueada né a uma coisa interessante a para ver se é
porque Rafa e dentro né então é porque se foi a ordem com que e cobertos então a alfa-hélice foi descoberta primeiro do que a folha Beta pregueada né então ela é saber que ela tem um formatinho se você olhar uma folha é meio que assim né agora existe uma diferença sakineh tão a o que dá Estabilidade para folha Beta pregueada que a estrutura secundária é a mesma coisa né então é a ponte de 12 e do oxigênio da carbonila e o do grupo do hidrogênio do grupo menino aqui certo então essa estrutura aqui que vai
um conjunto delas aqui que vai estar da estabilidade Veja uma coisa que é importante entender uma ponte de hidrogênio em si que é uma o a força e tá tendo exercido ali pergunta de prova é a força eletrostática então que dá Esse estabilidade as e qual é a força que dá estabilidade para uma estrutura secundária a força a força eletrostática Qual é o tipo de interação é a ponte de 12 anos certo então essa interação se a ponte de hidrogênio né entre essas essas forças aqui mas é suave é mais forte né tirando a cor
Valentina Então ela é mais EA iônica né que são as ligações ela é a mais forte que tem dessas interações mais fracas porque é aqui quase sentiu Núcleo do hidrogénio consiga chegar o mais próximo possível da nuvem de elétrons do meu oxigênio nem Tony seja bem pertinho mesmo assim ela é fraca e tá Professor você é fraca como é que ela vai estabilizar Que estrutura é porque meu amigo tenta quebrar um palito de dente é bom fácil agora pega uma caixinha junta tudo no bolinho e tenta quebrar quero ver se é macho né você a
surpreendeu aí para poder quebrar o negócio né você não É porque a união faz a força né então o conjunto de todas as pontes de hidrogênio presente cima alcoeres ou numa folha Beta pregueada é o que dá a estrutura a estabilidade da estrutura então é o conjunto de todas as fontes que vai dar estabilidade daquela estrutura certo então só que aqui então uma diferença Então as minhas grupos R é muito importante também não participa da estabilidade da minha folha Beta pregueada a grupo web não participa na Estabilidade de nenhuma estrutura secundária né ele vai e
neste caso a mesma coisa estamos voltados não posso falar para fora mas para cima e para baixo o seu pensar ela aqui no eixo paralelo aqui né A minha o meu esse aqui é paralela Então essas linhas grupo Services são perpendiculares a esse meu eixo falar paralelo a minha estrutura da minha folha Beta pregueada né então eixo paralela me estrutura e os meus grupos Eles estão virtualmente em uma formação perpendicular essa estrutura certo então está perpendicular ao eixo que corre paralelamente a minha estrutura da minha folha Beta pregueada esses grupos é esses são voltados para
fora isso é muito importante porque é isso daqui que vai dar a estabilidade para a formação da estrutura terciária que dá aquela carona tridimensional a minha proteína certo então tá muito fácil então só uma coisinha aqui né é esses essas fitas Aqui nessa essas peptídeos que estão as estruturas elas correm sentidos antiparalelo Mas eles podem correr também em sentidos Paralelos é lógico né amigão que existe aqui podes formal pra ela está E aí volta ou para informação uma alça e volta né então aqui também forma alguma coisa para Não alguma coisa que tem outras estruturas
e vem para cá quando eu mostrar para vocês uma estrutura mais complexa né Vocês vão conseguir visualizar isso daqui essas Folhas Beta se formando tá então no final das contas amiguinho aquele meu Aquele e-mail é é a minha unidade peptídica que é rígida e ele pede votações ela vai na realidade só deixar no estrutura mais linear ou vai deixar um estrutura helicoidal né então quando elas se encontram dias antes paralelas o paralelas acaba a formação essa pomada essas Pontes de hidrogênio isso vai acontecendo amiguinho o trânsito funcionalmente Então vai Acontecer na medida que a a
tradução vai acontecendo né lembra com mecanismo ribossomo Renato mensageiro transportador blablablá daquele mecanismos estão com outras funcionalmente Isso aqui vai rolando e tem um auxílio já de duas proteínas que eu citei antes e aquela Platina e as proteínas de choque térmico hsp70 né Então tá bom então agora vamos lá nalisada né com mais detalhes nas nossas duas terciários né Então veja bem eu já Falei na aula anterior o que vai determinar você falou Eu Tô analisando estrutura terciária eu estou analisando uma estrutura aonde ela tem formato tridimensional que ela vai de um ponto né de
um ponto ali Amino né até o meu ponto carbox eu preciso saber o cego aqui tá aqui ó tá Escondidinho Olha lá atrás ali o meu grupo é o o hiato desculpa aqui o meu grupo Amino ou o meu grupo Amina o meu grupo carbox esse aqui não dá para poder saber quem é Quem Mas é uma unidade só com uma extremidade Amino uma extremidade para box aqui a mesma coisa aqui a mesma coisa O quê que eu botei isso para vocês então é meu globina é aquela estrutura que auxilia no transporte do sangue ali
no plasma né participam muito em animais ali principalmente maminhas né E para poder fazer reserva de oxigênio quando tá no me profundidade né é cerveja que ela é formada só de estruturas de Alpha zero né já que a com cavalinho na que Que é uma que uma um componente vegetal que tem uma alta afinidade para o carboidrato com Cavalinho é usada para fazer um e para fazer a estrutura de aparelhos de análise de purificação né de carboidratos ali e outros componentes também colunas e Purificação né que a com cavalinha ar né você vê que ele
é feita só de folha Beta pregueada e aqui eu fiz a lisozima né que aquela lembra eu falei já na primeira aula que ela tá Presente ali na lágrima do olho é que é um componente é bactericida Ela também tem uma grande presente ali na clara do ovo né também tem visor Zinho ali na cara do ovo Ela já tem a folha Beta pregueada e Alfa hélice para você entender que as proteínas elas podem ter um tipo de estrutura secundária só né ou ela também pode ser mista ela pode ter dois tipos de estruturas secundárias
o que importa aqui amiguinho e lembrar que aqui lembra É como se fosse uma vareta Com espinhos os lucros é resultados para fora e na folha Beta pregueada os grupos vivem voltados para si e para baixo porque como é que vai funcionar agora então esses grupos erres ali né ele tem na extremidade deles ali na cisteína seu tenho um grupo sulfeto Essa é a interação mais forte que ocorre nas estruturas especiais essa ligação aqui só é cumprida né com quando você aplica uma quantidade de energia muito alta ou por um aquecimento ferver o Produto lá
né ou você colocar ali mulher e a NET de que ela vai ali no Comper lá essas essas Pontes aqui ligações né seu você vai colocar ácidos muito fortes aqui e aí você vai poder conseguir quebrar ela é uma ligação muito forte Inclusive essa ligação aqui amigo que é da cisteína que é muito presente nas proteínas que está no cabelo é inimiga nº 1 o cacheadinhos mesmo Sim porque que essa mulherada odeia o cacheado adora queimar Essa ligação aqui bota até mercaptoetanol que aquele negócio pede para ficar com cabelo liso durante o período mais prolongado
Meninas Não façam e o caracolzinho é tão lindo né tá que é uma música na para ele então para você lembrar que as stelenas está presente ali nas pontes né de desculpa ela está presente ali naquelas proteínas né kikas né de Alpha piratinhas nos cabelos ali né E ali Justamente que é você passa Chapinha né depois você passa o mercado de etanol para sei lá e aí você compra essas Pontes de sulfeto mexer no seu cabelo lisinho aí durante o período prolongado né Agora você tem que ter ações mais fracas aqui a isso aqui é
uma ligação covalente viu Colega ela é forte é a única covalente que acontece entre essas estruturas terciárias que são as pontes de sulfeto de sulfeto né sim ocorre quando eu tenho aminoácido cisteína E eu tenho as pontes de hidrogênio né Você já sabe já viu tá falando um monte sobre essas fontes de 2 aninhos ela entre essas interações fracas EA maior que tem né porque ela ela permite com que o núcleo do hidrogênio se aproximar o máximo possível da nuvem de oxigênio ali né e eu tenho ali para mim as pontes Salinas quando eu tenho
aminoácidos carregados negativamente positivamente ele se atraem né isso aqui interfere muito nos dobramentos mais internos ali Da estrutura esse povo aqui geralmente fica mais voltado para fora ali da proteína né e sente essa daqui é a força né a interação mais forte de todas né que ela é hidrofóbica né eu não vou cobrar tanto isso daqui mas a força que interfere aqui eu posso até cobrar eu mando é um vai está aqui vai para a terceira aula complementar né eu vou falar um pouco mais sobre isso daqui mas essa força aqui é chamada a força
um tópica Né a entropia lembra que a gente falou ali na segunda aula sobre a água né que quando eu tenho dois componentes que são gorduras ele se ligam entre eles porque o diminuo a quantidade de partículas de água que estão organizados então quando eu vou de um estado mais organizado por menos organizado isso daí se chama intropia né Então essa é a força entrópica e essa daqui a mais importante de todas porque meu amigo olhe lá tabelinha de classificação de acordo com A polaridade dos nossos aminoácidos amiguinhos nove deles né são é são apolares
são hidrofóbicos né então o que que acontece se a pro e os 20 né eu tenho quase que a na metade deles são hidrofóbicos né eu tenho uma grande porcentagem deles hidrofóbicos então isso exerce uma força muito grande na estrutura tridimensional final da minha proteína e a chamada estrutura na ativa da minha proteína Então essa interação faz com que esses Aminoácidos se voltam para o interior da minha proteína né eu ia acrescentar um slide a mais aqui sobre os domínios potentes Mas isso fica mais aí para o pessoal da turma da Medicina e da nutrição
para poder entender isso daí quando você vai fazer desnaturação proteica que alguns dos Senhores é vou ter que realizar esse exame porque você tem que desnaturar proteínas para correr ela no chão né ou também se a virem a linha Laboratorial é os enfermeiros Casos caso Sigam a linha você já tem uma base muito grande não vou entrar em detalhes né ver depois a ganhar no conhecimento à medida que vocês vão entrando na área da ciência É muito raro você ver um enfermeiro que liga para essa linha né Mas a gente dá a base aqui para
todo mundo tá bom então agora aqui a gente vai falar da estrutura quaternária calma meu amigo não tomou um susto né eu não vou ficar procurando aqui tá cada pontinha né mas Que você já tem um monte delas aqui né é um CD que essa é uma estrutura quaternária eu tenho a união de várias estruturas várias estruturas terciárias aqui né eu tô colocando mais uma vez aqui para você entender que elas podem ser de uma estrutura secundária apenas podem ser Também estás né Mas o que importa ó tá vendo cada. Cada extremidade a mim no
carboxi amina com a boca e olhando por cima olha só se legal concentra ninguém ficou olhando para ela Olha se não consegue perceber isso tá lá no fundo isso aqui tá mais em cima olha que eu tá vendo não consegue visualizar isso daqui é um canal transmembrânico eu tô olhando ele por cima ou então lá dentro então se eu tiver dentro da célula eu tô olhando lá fora dela Olha aqui nós estamos aqui dentro eu tiver do lado de fora ou lá dentro da célula Tá vendo isso é um canal transmembrânico provavelmente todos esses aminoácidos
nós vamos ver Que ser um canal de potássio é todos esses aminoácidos que estão voltados para essa região do canal aqui ó eles são são que são hidrossolúveis né porque o potássio ele é hidrossolúvel e esse povo que tá aqui ó esses aminoácidos que estão por aqui eles são lipossolúveis e o que faz com que o canal fiquem colado na membrana né legal esse daí né você já tá vendo ela estruturalmente funcionando né Essa aqui é a toxina diftérica na que idade teria né Então olha só que legal Você tem não só uma estrutura quaternária
mas você tem uma proteína conjugada é um grupo prostético ali dentro ó tá vendo Ah que legal né então para você ir visualizando você vê que eu vou mudando aqui porque quando você pegar a literatura é bom que você bate o olho você sabe o que que você tá vendo ali né então gente eu não vou ficar reprisando tudo isso aqui para você que a gente já falou na anterior né então é a mesma Coisa amiguinho a quaternário que que sabe lisa ela são as pontes de sulfeto as pontes de hidrogênio as pontes Salinas e
as interações hidrofóbicas só que a diferença entre a estrutura quaternária é e a terciária é que na terciária essas interações acontecem dentro de uma mesma cadeia peptídica enquanto na quaternária é ocorre entre cadeias Diferentes né muito simples não tem diferença Rua agora vamos lá então o que que vai determinar essa estrutura Tridimensional final aqui da quaternário não amigo a sequência de aminoácidos não é as estrutura terciária é a sequência de aminoácidos que determina a estrutura quaternária final amiguinho porque se eu mudar somente um aminoácido aqui pode ser que todo mundo pode ser que tudo fique
diferente certo então isso é muito importante saber disso daí se eu mudaram aminoácido aqui então isso fica para todos né a gente eu queria colocar Alguma coisa aqui sobre alguma doença então eu já vou incluir aqui para vocês né anemia falciforme né Se eu mudar somente um um aminoácido Zinho da minha estrutura é da minha estrutura terciária ali de uma das Comunidades ali da mesma o bobina a minha hemoglobina ela vai e tira aquela formato arredondado para ter um formato de foice é por isso que se chama anemia falciforme Porque ela fica com formato de
uma foice então que determina e eu vou perguntar na prova a Estrutura quaternária ou apreciar é a sequência de aminoácidos porque se eu mudar Só um só um hemoglobina ela deixa de ter o formato arredondado passa a ter um formato de foice destruindo o urso ali o as hemoglobinas a membrana e matando as hemoglobinas fazendo com que ela não tem a capacidade de transporte do oxigênio né E aí o indivíduo venha a óbito né então por isso que eu pego firme isso daqui que você entender se eu mudar um somente uma minoar então nós Falamos
aqui entre Essa é a outra aula falando sobre dois casos de doenças né a gente falou aqui sobre eu ia falciforme Se eu mudar um por isso que é ser complementar mais para o pessoal aí né na saúde aí né a pessoa mais na enfermagem medicina nutrição essa aqui depois tem umas outras mais complementares aí pessoal da nutrição é porque eu vou eu sinto muito gente mas a nutrição e a medicina Isso é uma disciplina quase fica sem essa vocês não Vão para frente né então aqui eu tô colocando a gente falou sobre qual outro
né a gente falou sobre o caso normal consumo da vitamina C que eu não consigo produzir aqueles aminoácidos modificados né e eu produzir um Colágeno é menos estável E aí eu tenho aquela doença chamada escorbuto né onde você começa a aprender a apresentar principalmente nas crianças né que têm problemas de ensino tradicionais aqueles bairros muito pobres né então elas têm sangramentos na Gengiva sangramento nos o e as mucosas né tem ossos frágeis né então ela vai ter raquitismo outras coisas com gato favorece né o rappi dismo né Lembrando que eu tenho também colágeno ali na
matriz óssea em Então é eu recebi eu faço o envelhecimento do formato de alguns órgãos ali né pulmão uns e outros então isso é um problema muito sério esse é o chamado escuro um puto né e agora a gente falou aqui porque a gente está comentando sobre a Estrutura das proteínas então ausência de um só um sou gente então tirar um aminoácido a minha Globo hemoglobina pede aquele formato dela e passa a ter um formato né de foice o que faz com que o indivíduo tem anemia falciforme tá bom Por fim então a gente vai
falar aqui sobre a desnaturação das proteínas Então as proteínas elas podem ser desnaturadas e elas precisam ser desnaturados como você vai fazer algum certo tipo de análise nela Se você tem vários componentes vídeos Natura então quê que é desnaturar uma proteína pegadinha de prova não é com peso ligações do aminoácido é fazer simplesmente com a proteína perca a estrutura tridimensional atingindo uma forma linear voltando para uma forma linear né que você conhece na estrutura primária então você pode inserir ureia né a ureia ela vai a linha age ali interromper naquelas Pontes de hidrogênio ali né
uma esse um agente Redutor né você tem a temperatura né Lembrando que as moléculas estão vibrando a medida que elas vão Então tem para toda a visão de Brasil um grande Vamos que vamos mais e aí elas não conseguem mais sustentar as ligações né e HG Extremo sou muito básico ou muito alcalino não é meu amigo lembra você começa a interferir no que não é primeiro você primeiramente de que você interfere nas extremidades a mim um boxe né Mas o mais importante é que Você tem aqueles as pontes Salinas né que tem dos radicais é
esse são carregados positivamente né os básicos e o negativamente os astros né Você desfaz essas ligações fazendo criado proteína começa a se abrir Eu tenho um detergente centro o detergente ele interfere na principal ali interação a mais forte ali que a mais interna da proteína que são as ligações e interações hidrofóbicas né é o repetir temperatura aqui é só para ficar tudo bonitinho igualzinho né e eu Tenho aqui os solventes orgânicos também que vão interferir na constante de elétrica ali do ambiente e aí também né interferem em tudo porque Lembrando que é a água que
faz porque tudo isso aconteça né então quando eu tenho um solvente orgânico eu interfiro na constante de Elétrica Ltda h Olá Tudo começa assim ter mudar né agora é muito importante entender que uma proteína que é desnaturada' ela tem já as características físico-químicas ela Volta renaturação normal dela depois essa estrutura é o chamado estrutura o estado nativo da minha proteína entretanto algumas não conseguem fazer isso quando porque quando você promove uma desnaturação principalmente por aquecimento né você torna essa proteína solúvel O que impede com que ela retorna para o estado nativo dela então os exemplos
aqui Albumina do ovo então amiguinho cito fritar um ovo nunca mais ele vai ficar aquela Claro molinha é Impossível EA caseína do leite né porque quando você faz isso daqui que você 40 anos e até se lá o leite né que você interfere na estrutura tridimensional da caseína você permite com que ela se torne alvo de bactérias é uma fazer o processo lá de fermentação ali é dentro de agendamento ali do leite e aí vai fazer o queijo coalhado um a Daiane Cruzeiro tá ficando com fome então tá bom então gente então é só linha
complementar e espero que vocês Tenham gostado ela é um pouco mais tensa né mas você precisa dar que vai cair na prova entendeu vai cair bastante para vocês Tá bom então estuda e que tu não quer ser mal titio só é um é muitos anos de educador ensino médio tá na feia tem que ficar cobrando tem que tá em cima de gente não sou eu não sou eu foi feito juro para vocês foi feito um uma estatística Ali há dois anos atrás a bioquímica EA disciplina que mais reprova na UFAM Mas não sou eu é
Juntando a média Entre todos os professores é porque gente ela é tudo novo né são coisas você vai ter que contextualizar se vai ter que gra o que você não consegue fazer isso no dia da prova aqui ó titio botou só dois conteúdos a próxima prova já é muito gorda a outra nem se fala então que tu ta ta tu ta fazendo você primeiro gatinha aumentar né para depois você começar a correr entendeu tem que ir na manha então agora para você sentir a fé Da próxima vai ser pior ainda então adquira o hábito né
tá lá lembra que tu falou né lê antes da aula e depois da aula depois na prova estudar pelo menos quatro dias seguidos Antes pelo menos cara pelo menos quatro dias não deixe o dia da próprio Não deixe para aula para você vai em tomar um suco com seu amigo ficou no semestre passado tá bom valeu gente tudo de bom aí para vocês estudem por favor





![[AQUECIMENTO 6/7] Refluxo, azia e hérnia de hiato! Hemorroidas! Não tem como fugir](https://img.youtube.com/vi/gB0j9vysqZw/maxresdefault.jpg)