dando continuidade ao estudo da tabela O que que você precisa saber sobre propriedades periódicas primeiro galera é que as propriedades periódicas existem três que super caem na sua prova né quais são essas propriedades as propriedades periódicas que mais caem são raio atômico energia de ionização e eletronegatividade sem as propriedades periódicas o que que é isso as propriedades periódicas são propriedades que vão alterar vão variar com o decorrer da tabela então a gente precisa olhar a tabela precisa saber identificar onde os elementos químicos estão E aí a gente consegue saber diferenciar né quais são essas propriedades
para onde aumenta para onde diminui e por aí vai como que elas caem nas provas né galera eh ele geralmente cita Qual é o tipo de propriedade e vai perguntar qual é o que tem maior raio maior energia de ionização alguma coisa assim ou uma característica muito importante daquele elemento Tipo o fluo que é muito eletronegativo né mais paraa frente entendendo essas propriedades periódicas a gente vai conseguir entender eh sobre a forma das ligações químicas também né que são as próximas aulas aí que a gente vai ver então presta atenção porque é muito importante esse
estudo aqui Essas são as principais propriedades periódicas que a gente vai ver E aí a gente começa com o raio atômico o raio atômico A gente trabalha com tamanho do átomo para ficar mais fácil de você entender né mas o raio atômico é a distância do núcleo até a última camada da eletrosfera né E aí a gente consegue identificar mais ou menos o tamanho desse átomo o bom mesmo é focar o elemento químico tem um raio grande tem um rio pequeno então a gente pensa ele é grandão ou ele é pequenininho pensa em tamanho que
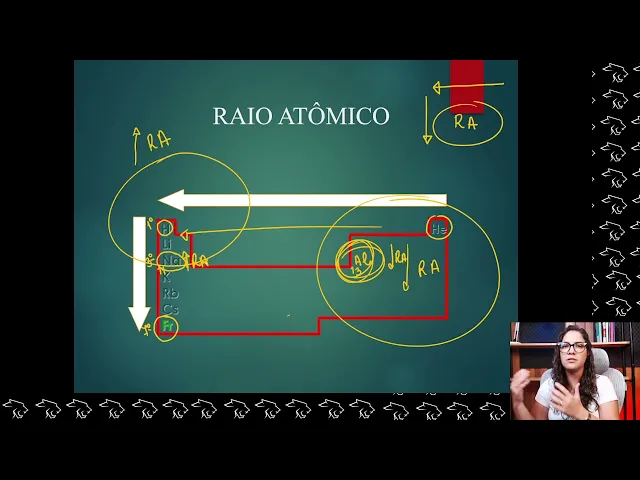
fica mais fácil o que que você tem que saber galera quando a gente olha uma tabela a gente vai analisar todos os elementos químicos então eu vou te dar um exemplo aqui tá bom eu tenho o hidrogênio tá aqui eu tenho o sódio e eu tenho o frâncio tá vendo eles estão no mesmo grupo beleza Qual que é a diferença é que o hidrogênio tá no primeiro período então ele tem uma camada o sódio ele tá no terceiro período então ele tem três camadas e o francio tá no sétimo período então ele tem sete camadas
pensando de uma maneira básica que Qual é o que tem o maior raio o que tem mais camadas as camadas sempre vão aumentar de cima PR baixo os elementos químicos que estão mais abaixo da Tabela Periódica eles têm sempre mais maior tamanho então eles vão ter sempre o maior raio atômico Beleza então raio sempre vai crescer de cima para baixo essa é a primeira coisa que você tem que saber Beleza agora eu tenho hidrogênio e eu tenho o héo Os dois têm uma camada só aí aqui a gente tem que já analisar de outra forma
como assim eu tenho o átomo o átomo é dividido com núcleo e eletrosfera não é núcleo tenho prótons e nêutrons eletrosfera eu tenho elétrons o núcleo eu tenho carga positiva na eletrosfera eu tenho carga negativa essas cargas Opostas se atraem certo galera Como que eu vou analisar aqui quem tem maior ou menor raio pelo número de prótons quanto mais prótons o átomo tem no núcleo mais carga positiva ele tem se ele tem mais carga positiva nesse núcleo ele também tem mais carga negativa na eletrosfera mas quanto mais carga positiva ele tem no núcleo mais atraídos
esses elétrons vão ficar então se eles ficam mais atraídos o o tamanho dele vai reduzir então ele vai ter um menor raio se a ordem é crescente da esquerda para direita de número atômico Quem tá na direita da Tabela Periódica tem um menor raio atômico e quem tá na esquerda da Tabela Periódica tem o maior raio atômico quanto maior é o número atômico menor é o seu raio como que cresce então o raio da direita paraa esquerda beleza galera Essas setinhas são extremamente importantes para você assim tem que gravar mesmo então você vai pegar vai
resumir vai quando essa aula acabar você vai ter um resumo raio cresce de baixo para cima da esquerda pra direita e perdão da direita pra esquerda e você precisa cara cola no seu quarto igual Cola assim ó cola no teto para quando você for dormir você ficar lembrando é melhor tô falando então quanto maior o raio atômico né Eh quanto maior é o número atômico menor o seu raio vou te dar outro exemplo aqui pra gente passar já ó eu tenho o sódio que tá aqui aí depois teria o magnésio e aqui eu tenho o
alumínio o alumínio tem o número atômico 13 e o sódio tem o número atômico 11 quem tem mais prótons no núcleo o alumínio não é então se o alumínio tem mais prótons no núcleo ele atrai mais os elétrons para perto de si então entre o alumínio e o sódio como eles estão no mesmo período né Por o alumínio aqui ele ter mais número de próton no seu núcleo ele tem um menor raio atômico e o sódio tem um maior raio atômico beleza tudo bem a prova geralmente vai te perguntar alguma coisa assim ou eu quero
a ordem crescente ordem crescente é do menor pro maior o sódio tem um o alumínio tem um menor raio atômico e depois vem o sódio ou decrescente do maior pro menor e por aí vai é muito tranquilo Beleza agora energia de ionização ou potencial de ionização a energia de ionização é energia necessária para que se retire um elétron de um átomo né de um átomo que vai est isolado no estado gasoso Então eu tenho um átomo aqui tranquilo tá neutro tá bem Aí do nada do nada assim tiram Um elétron dele aí você pensa se
Tiraram um elétron dele ó eu tô aqui tô com minha aliança Eu vou tirar a minha aliança Eu gasto uma energia não gasto para tirar minha aliança é a mesma coisa o átomo tá aqui com o seu elétron eu gasto energia para tirar esse elétron a energia de ionização é essa energia necessária só que a gente pensa sempre né como que eu gasto muita energia com um átomo grandão ou com um átomo pequenininho ó eu tenho um átomo desse tamanho e eu tenho um átomo desse tamanho galera qual que eu gasto muita energia para tirar
o elétron dali esse aqui ó que o elétron Tá super afastado do núcleo não né quando o átomo é muito grande eu dou um Peteleco e eu tiro esse elétron tá ali agora se o átomo tá pequenininho igual a esse aqui que eu fiz ó cara como é que eu tiro esse elétro eu tem que gastar muita energia né imagina que o meu dedo tá tá gordinho aqui eu gasto muita energia para tirar esse anel daqui né que esse é elétron Então se o raio é pequeno eu gasto muita energia para tirar esse elétron se
o raio é grandão eu gasto pouca energia para tirar esse elétron Então como que a gente vê sei como que o raio cresce a energia de ioniza ação cresce ao contrário né o raio não cresce para baixo então a energia ela tá lá em cima porque lá em cima o raio é pequeno o raio não cresce pra esquerda então a energia ela é grandona lá pra direita porque o raio é pequeno beleza aí a setinha você pode botar em cima ou embaixo tá a que vai lá para pro pro lado dos gases noves né e
o Hélio é o elemento de maior energia de ionização da Tabela Periódica isso já caiu na discursiva da werd e né essa parte aqui sempre cai em questão básica né objetiva de qualquer V pular aí beleza então a energia de ionização cresce contrário do raio e aí a gente vai seguir aqui pra próxima falando ainda de energia de ionização a gente tem que pensar no seguinte né parâmetro aqui eu tenho um átomo neutro tá ele tem a mesma quantidade de prótons e de elétrons aí o que que acontece eu tiro um elétron dali dele aí
eu tenho mais próton e menos elétrons na eletrosfera o que que vai acontecer galera se eu tiro um elétron ali do meu do meu átomo cara tendo mais próton e menos elétron o raio vai diminuir Então a primeira energia de ionização eu gasto um tanto Beleza agora que eu redu o tamanho do raio né do tamanho do átomo galera a segunda energia de ionização eu vou gastar uma energia ainda maior quanto mais mais elétrons eu tiro maiores vão ficando essas energias de ionização né então Ó eu eu gasto aqui ó no magnésio 7,6 V eletron
volts né para tirar o primeiro elétron só que eu já reduzi o tamanho desse átomo não já aí eu vou gastar agora 14,9 de energia galera para tirar o terceiro elétron olha quanto que eu tenho que gastar 79,7 é muito maior não é então quanto mais elétrons eu tiro maiores vão ficando essas energias de ionização Então a primeira energia de ionização ela é sempre a menor de todas né a segunda vai ser menor que o quê que a terceira mas ela a segunda energia Ela é maior do que a primeira e por aí vai né
vou tirando o elétron quanto mais elétron eu tiro maiores são essas energias de ionização agora coisa importante aqui caiu na prova da werge já né aqui a gente consegue ver ó que daqui para cá ó ocorreu uma Mud ança de energia muito grande né a gente fala aí que é um salto energético então a gente consegue enxergar aqui que da aqui de 14 para 79 é muito alto né então você consegue achar onde que esse elemento tá na tabela periódica né as duas primeiras energias foram tranquilas de tirar pra terceira já é muito mais difícil
então esse cara esse elétron já tá numa camada mais interna então aqui eu tenho dois elétrons na camada de valência como que a gente enxerga também a gente vai enxergar na forma de gráfico eu tenho aqui o gráfico esse é um gráfico de questão da werge mesmo uma questão discursiva E aí você tá vendo que a energia tá aumentando certo bonitinho só que eu tenho um salto energético a mesma coisa do exemplo anterior Como assim daqui do sexto pro sétimo né da sexta paraa sétima energia de ionização o salto foi muito grande ó tá vendo
quando a gente tem esse salto muito grande né a gente consegue enxergar essa mudança né esse cara aqui ó o sétimo elétron ele tá numa camada mais interna então o que que a gente consegue enxergar aqui que até o sexto elétron Eles estão numa camada né então eu tenho seis elétrons na camada de valência quando tem esse salto muito grande aí esse elétron que já tá lá em cima ele tá na camada mais interna e aí a gente consegue enxergar aqui ó Quantos elétrons eu tenho na camada de valência nesse caso aqui eu tenho seis
elétrons na camada de valência então ele tá na família Sea no grupo 16 já no exemplo anterior Eu tenho um salto energético da segunda paraa terceira né da segunda para terceira energia de ionização Então esse cara aqui vai ter dois elétrons na camada de valência então ele tá no grupo dois ou na família doa beleza show isso é muito legal e muito importante agora a gente vai pra eletronegatividade a eletronegatividade é a tendência que o átomo que um átomo tem em atrair elétrons como que é galera o átomo tá sozinho tranquilo Aí do nada do
nada ele puxa um elétron Tranquilão sem fazer força como que é a eletronegatividade na tabela periódica galera a eletronegatividade eh a gente tem que saber isso porque já caiu noem e sempre cai em qualquer vestibular né Eh a eletronegatividade tem um elemento específico na tabela periódica que é o mais eletronegativo né que é o fluor o fluor é um elemento químico mais reativo por que que ele é o mais reativo da tabela Porque ele é o mais eletronegativo então a eletronegatividade sempre vai apontar para ele beleza então se eu tenho o meu átomo de fluor
na tabela periódica eu vou apontar sempre para ele a professor gases nobres galera por que que a gente chama os gases de Nobres porque eles são inertes eles não gostam de reagir com ninguém então a gente não trabalha com eletronegatividade aqui com eles por quê Porque eles não são eletronegativos eles não gostam de atrair elétrons mas o fluor atrai e é por isso que o fluor ele consegue se ligar com os gases nobes mesmo com eles não querendo porque eles estão com aquiteto completo mas o fluor é tão eletronegativo consegue fazer isso então o que
que você tem que saber daqui galera eletronegatividade a tendência que o átomo tem atrair elétrons e qual o elemento que mais atrai o flor então na tabela a gente sempre vai fazer esse apontamento para ele beleza foi tá aqui ó bonitinho pode jogar a setinha para cá também não tem problema fechando no flor tá E aí passou sem querer mas já pode chegar aqui afinidade eletrônica ou eletroafinidade a elro afinidade é a energia liberada quando o átomo ele captura Um elétron Então olha só presta atenção capturou um elétron agora aqui ó capturou um elétron não
foi maior o barulho da segunda quando a gente trabalha com afinidade eletrônica a gente tem que lembrar da eletronegatividade por quê Porque se um elemento não é muito eletronegativo ele nem vai querer capturar esse elétron então ele não libera muita energia pro meio Agora pensa no fluo ele é extremamente eletronegativo então quando ele faz a captura desse elétron para ficar com a carga negativa aqui ele vai liberar muita energia para você ter noção em laboratório de química orgânica a gente quase nunca faz experimento com fluor por quê Porque ele é tão eletronegativo que quando ele
faz essa captura do elétron ele libera tanta energia que ele explode o recipiente onde tá ocorrendo aquela reação entende então se o elemento é muito eletronegativo nessa captura do elétron ocorre muita liberação de energia então ele tem uma afinidade eletrônica muito grande esse energia liberada é sempre chamada de eletroafinidade tudo bem e aí vai ser a mesma coisa que a eletronegatividade os gases nobres não não participam e vai sempre apontar pro fluor né o fluor é um elemento que mais vai liberar energia na captura do elétron tudo bem beleza e a eletropositividade ou o caráter
metálico é a tendência que o átomo tem ficar positivo como que ele fica positivo doando elétrons tá então eletropositividade é a tendência do átomo do ar elétrons ali e aí galera como que a gente Analisa aqui se o elemento né mais eletronegativo é o fluor que tá na direita da Tabela Periódica os elementos mais eletropositivos que querem perder os elétrons eles estão pra esquerda da tabela né então como que a gente Analisa isso se cresce de baixo para cima e da esquerda paraa direita apontando pro flour aí ele eletronegatividade a eletropositividade vai ser ao contrário
vai ser para baixo e pra esquerda né tendo o frâncio aqui como elemento mais eletropositivo por quê Porque ele tem um raio muito grande Ele só tem um elétron na última camada os metais né eles TM esses elétrons nas últimas camadas Eles não gostam dele por quê Porque eles querem chegar no octeto né eles querem ficar com o octeto completo Então imagina os elementos do grupo um com um elétron só na camada de valência eles não querem de jeito nenhum né então aqui eles querem doar de qualquer jeito esses elétrons metais são muito eletropositivos pensa
eletropositivo tá ficando positivo Então tá doando Eletro pro meio eletropositividade cresce junto com raio Beleza então o elemento que tem maior raio atômico ó é o frâncio e ele também é mais eletropositivo tudo bem aqui a gente finaliza a nossa aula de propriedades periódicas faz agora o seu resumo bota satinha pra direita pra esquerda cola lá no seu teto né Eu espero que você tenha gostado aqui fica agora com a próxima aula fica com Quiz também pelo amor de Deus faz esse Quiz aí para você ver que você tá mandando bem e até breve tchau
tchau