clases particulares en Ávila por Miguel Fernández collado Hola a todos y bienvenidos al Canal futuros sobresalientes hoy vamos a ver la asignatura de física y química y por cierto si no estás suscrito suscríbete que es gratuito también puedes unirte al canal O apoyarme en patreon y si necesitas clases particulares puedes echar un vistazo a nuestra web que te la dejo en la descripción el tema de hoy es muy sencillo vamos a ver el enlace iónico pon atención que empezamos y empezaremos resolviendo la pregunta que es un enlace iónico un enlace iónico se establece cuando se
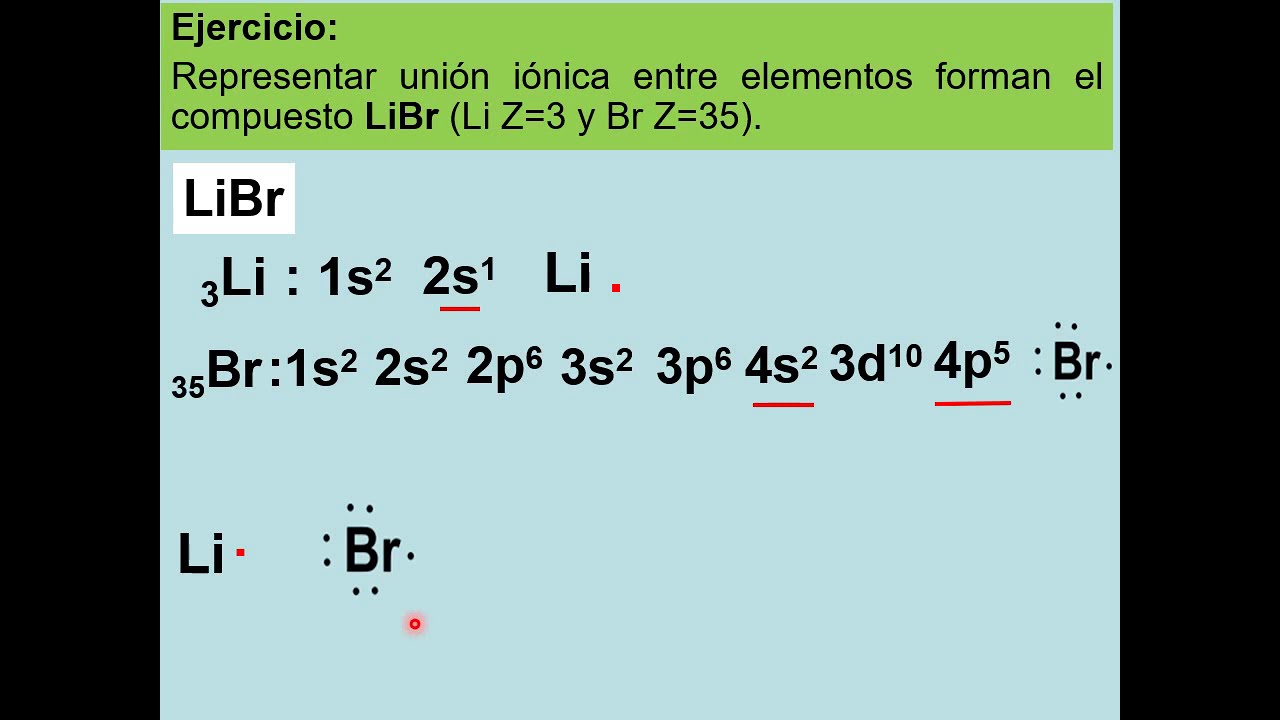
combinan un metal y un no metal ambos alcanzan la configuración de gas noble formando iones estos de aquí son los gases nobles el enlace iónico resulta de las fuerzas de atracción entre aniones y cationes los iones se combinan en la proporción adecuada para que el compuesto resultante sea neutro observa lo que sucede a los átomos de sodio y cloro el átomo de sodio cede su electrón de valencia y se convierte en el catión con una carga eléctrica positiva es decir ha perdido un electrón de esta manera si nos fijamos en su configuración electrónica podemos decir
que el sodio partiendo desde el Neón es 3s1 por cierto si tenéis que repasar las configuraciones electrónicas os dejo un vídeo aquí y en la descripción para que le echéis un ojo al perder un electrón la configuración electrónica del catión del sodio tiene la misma configuración que la del neón pasemos ahora a ver la del cloro el cloro Por su parte gana un electrón y se convierte en un anión con una carga eléctrica negativa es decir ha ganado un electrón si nos fijamos en la configuración electrónica del cloro partimos del Neón y es 3s2 3p5
ahora al ganar un electrón partimos también del Neón y sería 3s2 pero en este caso sumamos 1 al 5 3 B 6 si nos fijamos se cumple la regla del octeto 2 + 6 son 8 electrones Esto hace que tenga la misma configuración que el gas noble argón por lo tanto el átomo de sodio cede su electrón de valencia al cloro Y ambos completan así la configuración de gas noble y como los dos iones tienen carga del mismo valor y de distinto signo cada átomo de sodio se combina con uno de cloro formando el compuesto
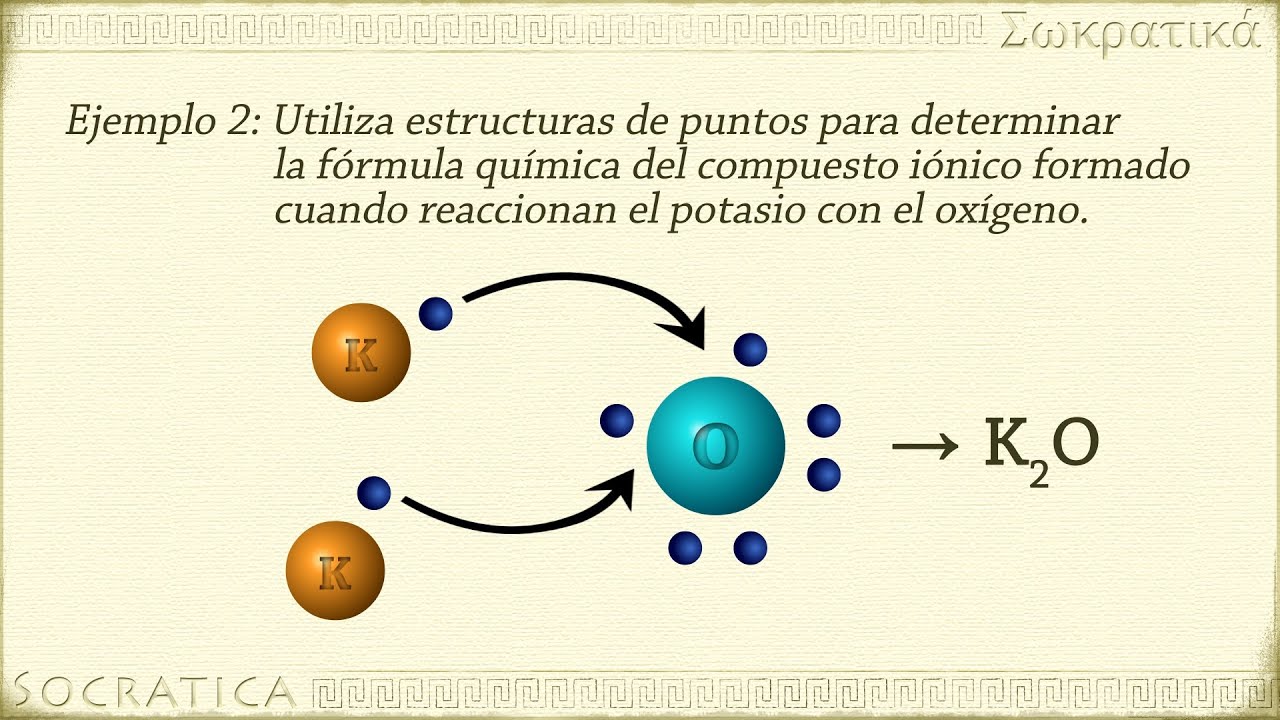
NaCl cloruro de sodio ahora vamos a ver qué pasa si se combinan átomos de sodio y oxígeno ocurre lo siguiente el átomo de sodio cede su electrón de valencia y se convierte en el catión es decir en el ion con una carga eléctrica positiva ha perdido un electrón vamos a ver la configuración electrónica la configuración de electrónica del sodio parte desde el Neón y sería 3s1 al perder un electrón el catión del sodio tiene la misma configuración que el Neón es decir que un gas Noble pasemos a ver ahora la del oxígeno el átomo de
oxígeno gana dos electrones y se convierte en el anión con dos cargas eléctricas negativas es decir gana dos electrones si nos fijamos en la configuración electrónica el oxígeno parte del helio y a esto le debemos Añadir dos s2 2 p4 pero al ganar dos electrones el anión del oxígeno parte del helio y hay que sumarle dos electrones por lo tanto sería 2s22 p6 de esta manera al tener 8 electrones la configuración electrónica de la Unión de este oxígeno sería Exactamente La misma que la del neón de esta forma nos encontraríamos antena2 o es decir el
óxido de sodio Oye Miguel Pero por qué el oxígeno gana dos electrones en vez de uno vamos a verlo cada átomo de oxígeno necesita captar 2 electrones por eso se tiene que combinar con dos átomos de sodio que ceden un electrón cada uno en los compuestos iónicos los iones se organizan en una red cristalina del tamaño de la muestra el enlace iónico no forma moléculas la fórmula del compuesto iónico indica la proporción en que se combinan los átomos expresada con los números más sencillos pasemos a ver las propiedades de los compuestos iónicos son consecuencia de
estar formados por muchos iones positivos y negativos organizados en una red cristalina vemos aquí un ejemplo también podemos ver el cloruro de sodio o el óxido de sodio determinando que la forma de la red cristalina depende de que haya el mismo número de aniones y cationes o no los haya a temperatura ambiente son sólidos cristalinos y su temperatura de fusión es elevada además un golpe sobre el cristal iónico hace que los iones se desplacen y los iones del mismo tipo se repelen por lo tanto podemos determinar que son duros y frágiles algunos como el cloruro
de sodio se disuelven en agua Aquí podemos ver la sal sin disolver y posteriormente la sal disuelta varias moléculas de agua con orientación adecuada pueden rodear un ion positivo negativo y llevarlo de la red cristalina al líquido poco a poco el cristal se va disolviendo Y por último tenemos que señalar que en estado sólido los iones ocupan posiciones fijas en el cristal por lo tanto no conducen la corriente eléctrica en estado sólido sin embargo cuando los iones se pueden mover conducen la corriente esto ocurre cuando están fundidos o cuando están disueltos en agua y hasta
aquí el tema de hoy Espero que te haya gustado tanto como a mí ya sabes que puedes unirte al canal O apoyarme en patreon y si necesitas clases particulares echa un vistazo a nuestra web que te la dejo en la descripción aquí te dejo una lista de reproducción para probar física y química sin dudar y suscríbete y sígueme en mis redes sociales nos vemos mañana chao chao bacalao [Música]








![💫 ¿Qué es enlace químico? Tipos de enlace: Iónico, Covalente, Metálico💫 [Fácil y Rápido] | QUÍMICA |](https://img.youtube.com/vi/9Oljha_Syv8/maxresdefault.jpg)