los compuestos inorgánicos son aquellos que se forman por la combinación de un elemento metal calcio sodio hierro etcétera con un elemento no metal cloro oxígeno carbono etcétera el enlace iónico es el tipo principal de enlace en los compuestos inorgánicos una atracción eléctrica entre el guión del metal cargado positivamente más y el ion del no metal con carga negativa menos esta interacción es de gran fortaleza y explica muchas de las propiedades de los compuestos inorgánicos tales como poseer puntos de ebullición y fusión altos por otro lado los compuestos inorgánicos también pueden resultar de la combinación de
dos elementos no metales que comparten un par de electrones formando el llamado enlace con valente un ejemplo de ello es el agua h2o la principal diferencia entre los compuestos orgánicos e inorgánicos es que los organismos siempre contienen el elemento carbono mientras que la mayoría de los compuestos inorgánicos no lo tienen otra característica principal de los compuestos inorgánicos es que no presentan enlaces carbono hidrógeno tradicionalmente se ha dicho que los compuestos inorgánicos son propios de las rocas y los minerales sin embargo varios compuestos inorgánicos son sintetizados por los seres vivos pudiéndose citar como ejemplos el ácido
clorhídrico sintetizado en el estómago y el dióxido de carbono co2 un producto del metabolismo corporal ejemplos de compuestos inorgánicos son el agua el dióxido de carbono la sal de mesa o el ácido clorhídrico propiedades de los compuestos inorgánicos a pesar de la gran diversidad de los compuestos inorgánicos la mayoría de ellos comparten un conjunto de propiedades comunes pudiéndose citar las siguientes enlace iónico los elementos químicos de los compuestos inorgánicos están unidos mediante un enlace iónico que consiste en una atracción eléctrica entre partículas con cargas eléctricas opuestas es decir con carga positiva y negativa conductores eléctricos
los compuestos inorgánicos en solución acuosa son buenos conductores de la electricidad debido a que se disocian en millones al disolverse en agua los iones son partículas cargadas eléctricamente y por lo tanto son buenas conductoras de la electricidad puntos de fusión y ebullición los compuestos inorgánicos tienen puntos de fusión y ebullición altos esto es debido a que para cambiar de estado físico se deben romper los enlaces iónicos de alto contenido energético por lo que es necesario un suministro de energía elevado solubilidad en agua los compuestos inorgánicos son generalmente solubles en agua las moléculas de agua son
dipolos eléctricos es decir poseen una carga eléctrica positiva y una negativa en sus extremos por lo que pueden interactuar eléctricamente con los iones partículas con carga eléctrica el agua interactúa con los iones utilizando estos polos lo cual favorece la solubilidad de los compuestos inorgánicos estado o fases sólidos los compuestos inorgánicos suelen ser sólidos debido a los enlaces iónicos que existen entre los elementos químicos que lo forman una consecuencia de esto es que las interacciones eléctricas termina organizando los iones en redes cristalinas y por ende en sólidos cristalinos dureza de los cristales los cristales de los
compuestos inorgánicos presentan una gran dureza por los enlaces iónicos que están presentes en ellos no obstante al ser deformados se produce el acercamiento de elementos con la misma carga eléctrica lo cual puede originar fuerzas de repulsión capaces de romper la estructura cristalina baja volatilidad los compuestos inorgánicos suelen ser poco volátiles y no combustibles la explicación es que estos compuestos no suelen experimentar evaporación a temperatura ambiente y están formados además por elementos químicos que no arden fácilmente clasificación tipos de compuestos inorgánicos los tipos de los compuestos inorgánicos suelen establecerse con base al número de elementos químicos
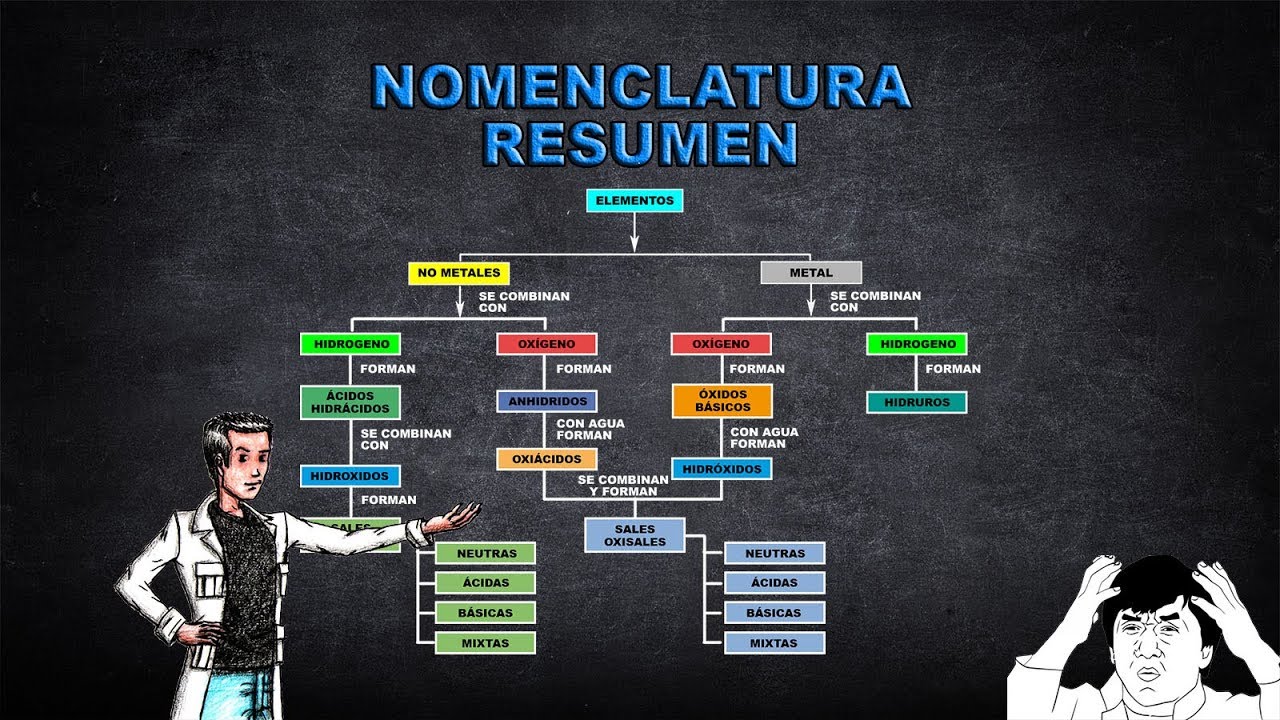
diferentes presentes en ellos siguiendo este criterio los compuestos inorgánicos se clasifican en binarios ternarios y cuaternarios compuestos inorgánicos binarios son compuestos formados por la unión de dos elementos químicos diferentes entre ellos están óxidos peróxidos hidruros hidr ácidos hidróxidos y las sales binarias óxidos se forman por la combinación del oxígeno o2 con otro elemento químico se clasifican en óxido básico y óxidos ácidos sin embargo existen otros óxidos muy característicos entre los cuales sobresalen por ejemplo los peróxidos inorgánicos óxidos básicos se forman por la combinación de un elemento metal con el oxígeno estos compuestos originan hidróxidos por
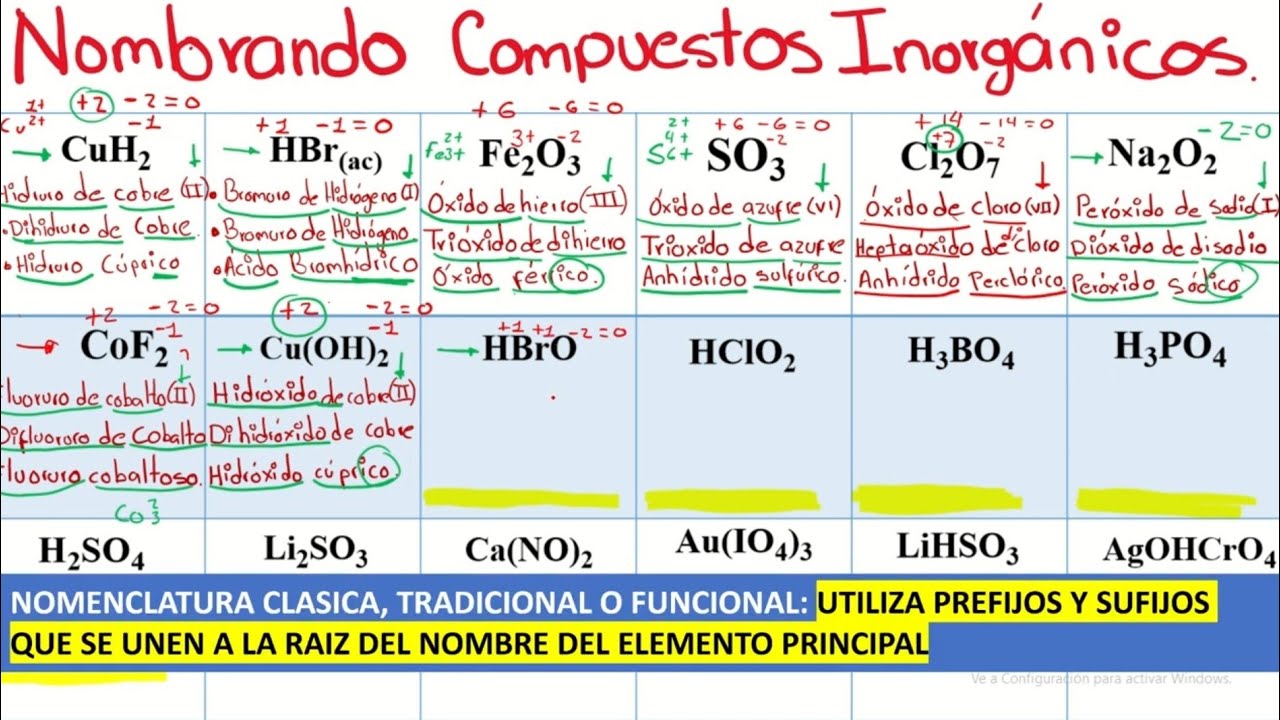
ejemplo el óxido férrico óxidos ácidos se forman por la unión de un elemento no metal con el oxígeno se caracterizan por originar ácidos por ejemplo el óxido crómico pero óxidos inorgánicos tienen en su estructura un enlace de oxígeno oxígeno que puede combinarse con el hidrógeno para originar el agua oxigenada o puede combinarse con un metal por ejemplo el peróxido de sodio y duros pueden ser hidruros metálicos e hidruros no metálicos hidruros metálicos se forman por la unión de hidrógeno con valencia o estado de oxidación -1 con un metal por ejemplo hidruro de potasio y duros
no metálicos compuestos químicos originados por la combinación del hidrógeno con valencia + 1 con un elemento no metal utilizando su menor valencia son gaseosos y al disolverse en el agua originan ácidos por ejemplo cloruro de hidrógeno ácidos hidra si dos resultan de la combinación generalmente en fase gaseosa del hidrógeno con un elemento no metal por ejemplo ácido yo hídrico sales binarias se forman por la unión de un elemento metal con carga positiva y un elemento no metal cargado negativamente por lo que establece entre ellos un enlace iónico por ejemplo cloruro de calcio compuestos inorgánicos ternarios
están presente en ellos tres elementos químicos diferentes formando parte de este grupo luz hidróxidos los óxidos y la sal stern arias hidróxidos se originan por la reacción de un óxido básico con el agua presentando grupos hidroxilo sse por ejemplo el hidróxido cálcico ox ácidos se forman por la reacción de un óxido ácido con el agua estos ácidos presentan oxígeno por ejemplo el ácido nítrico sal stern arias resultan de la reacción de neutralización de un box ácido con un hidróxido formándose las alternaria y el agua por ejemplo el carbonato de sodio compuestos inorgánicos cuaternarios entre ellos
se encuentran las sales ácidas y las sales básicas sales ácidas se forman por la sustitución parcial de los átomos de hidrógeno de un óxido por un metal por ejemplo el bi sulfato de sodio sales básicas se originan en reacciones en las cuales no se sustituyen totalmente los grupos hidroxilo dos por uno metal por ejemplo hidroxi cloruro de calcio ejemplos de compuestos inorgánicos óxido de aluminio oxidoc lorica hidróxido de potasio y del óxido férrico y duro de litio ácido clorhídrico ácido sulfúrico peróxido de litio cloruro de sodio cloruro cálcico bicarbonato de sodio permanganato de potasio agua
dióxido de carbono amoniaco ya hemos terminado con los compuestos inorgánicos espero que haya sorprendido si te ha gustado dale a like y suscríbete también puedes visitar live.com y buscar lo que necesites hasta pronto y ten un buen día




![What are organic compounds? [Classification, characteristics and examples]🧬](https://img.youtube.com/vi/aHQzxYeCS7E/maxresdefault.jpg)

![Chemistry course from 0 ✅ [COMPLETED AND RE-EDITED]](https://img.youtube.com/vi/2jyxYUQXKBQ/maxresdefault.jpg)