o Olá sou fã desse lado direito engenharia física negativa nela eu vou ser o teu rosto nesta série de vídeos sobre física e química espero que goste Vamos agora falar da energia dos electrões dos Autos à luz pode ser tentada com partículas de energia chamados funções energia de cada faltam é proporcional à frequência de Selos fórmula energia é igual a h constante de Planck vezes é frequência espectro eletromagnético é constituído pelo conjunto das radiações eletromagnéticas ordenadas por energia a zonas do espectro deve saber se são as seguintes está chegando tá x ultra-violeta luz visível infravermelhos
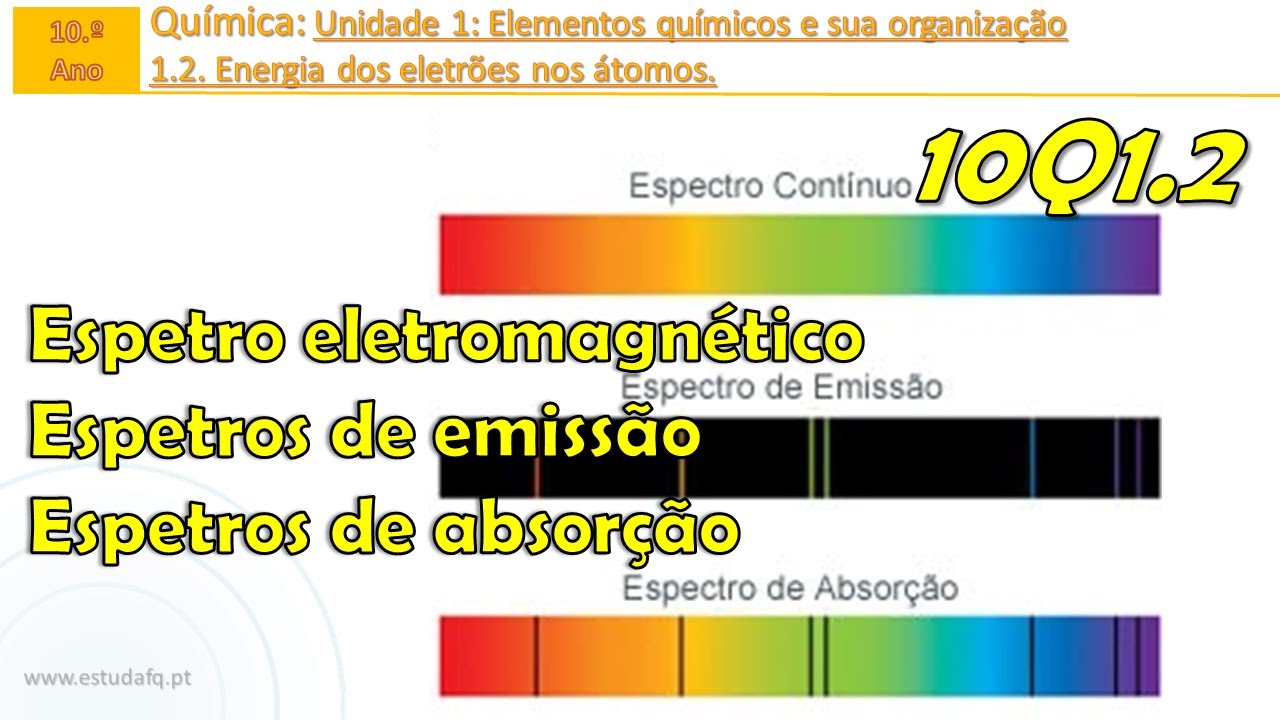
micro ondas e ondas de rádio aspecto resulta da decomposição da luz e pode ser de dois tipos de emissão resulta da composição pelos na função resulta da absorção de luz entre os vários aspectos que existem saco o diminuição continuam no junto cultivo de cores é visível emissões continuous iscas conjunto ricas coloridas bem definidas no fundo negro a situação discontinuous riscas conjunto riscas negras bem definidas no fundo colorido e o elemento químico identificável através do seu espectro atômico porque os espectros de absorção e emissão de cada elemento químico são característicos deste dado um fiz não assim
do mesmo momento que as riscas coloridas no espectro de emissão coincidem entre si frequência com as riscas negras dos respectivos espectros de absorção nele Bohr físico dinamarquês de renome duas ideias fundamentais do cidadão primeira regra existem níveis de energia bem definidos segunda regra ocorrem transmissões de electrões entre os diferentes níveis quer para absorção quer permissão de energia em quantidades bem definidas segundo este modelo atômico de Bohr os elétrons movimentam-se através órbitas circulares de raio bem definido a volta do quanto mais longe do núcleo se encontra um electrão menor energia necessária para remover o do lado
hoje em dia sabe-se que as órbitas em cozido transformou em não são bem diferentes e daí o nome no eletrônico o lado apenas são permitidos carros valores de energia de um elétron ou seja a energia do elétron no lado estar foi utilizada a energia de lado nível é ser negativa e quando não forem mais negativa Serasa a energia será anulada a resposta do nível de futebol infinito conhecimento elétron Deixa de estar sob a influência do núcleo exemplos classificou ionizado o estado mais estável de um átomo no estado fundamental responda ao nível como não energia é
nível 1 nos restantes níveis 2 3 até aqui energia maior correspondem a estados agitados nada que ela se sente aqui quando o elétron passa de um nível de energia inferior tiveram superior a sorte de energia no processo e é isso chama-se agitação sala de rir quando Letra faz o trajeto contrário liberta energia e chama-se desse Estação e o inicialmente o modelo atômico de Bohr foi proposto para o átomo de hidrogênio sofrendo uma visitação o átomo de hidrogênio emite radiação e apresentou o espectro de emissão discutido neste Preto às riscas visíveis correspondem a três séries espectrais
cujo não é o nome dos cientistas que descobriram ser de Lima transições eletrônicas níveis sobre os fera é igual a um estendi missão de luz ultravioleta estas transições implicam maior energia série do Walmart transições eletrônicas níveis superiores para = 2 emitindo luz visível e ultravioleta série de paixão transições eletrônicas níveis superiores para n = 3 e mente de luz infravermelha estas tradições aplicam menor energia e a variação de energia que existe na transição entre diferença de 20 energia calcula-se Fazenda diferença entre energias do nível final e Inicial desta forma positiva sabemos que o atlas horrível
energia ou agitação uma negativa sabemos que libra tu/emitiu energia ou de situação sem energia absorvida for suficiente para o adquirir até o nível n infinito então ocorre realização de uma conferência e voltam transforma-se em iam e o elétron ganha energia cinética para eletrão ir por um nível de energia superior a energia que é fornecida o átomo tem que ser inferior a energia de ionização e tem que ser exatamente igual à variação de energia envolvida numa transição existe uma técnica chamada espectroscopia atômica que através da interação entre a radiação eletromagnética EA matéria torna-se possível detectar um
elemento uma acho que os aplicações que são por exemplo a identificação de elementos químicos nas E aí na determinação de quantidades vestigiais em química forense é um Vila atômico de Bohr funcionava assim por cento para o átomo de hidrogênio tem apenas um elétron mas tem limitações para anos tem mais do que um electrão pode eletrônicos uma vez que nesse aqui não existe não só a atração entre elétrons e núcleos que diminui a energia dos electrões mas também é repulsão entre os electrões que aumenta a energia dos atrás atualmente sabemos que apenas podemos saber a localização
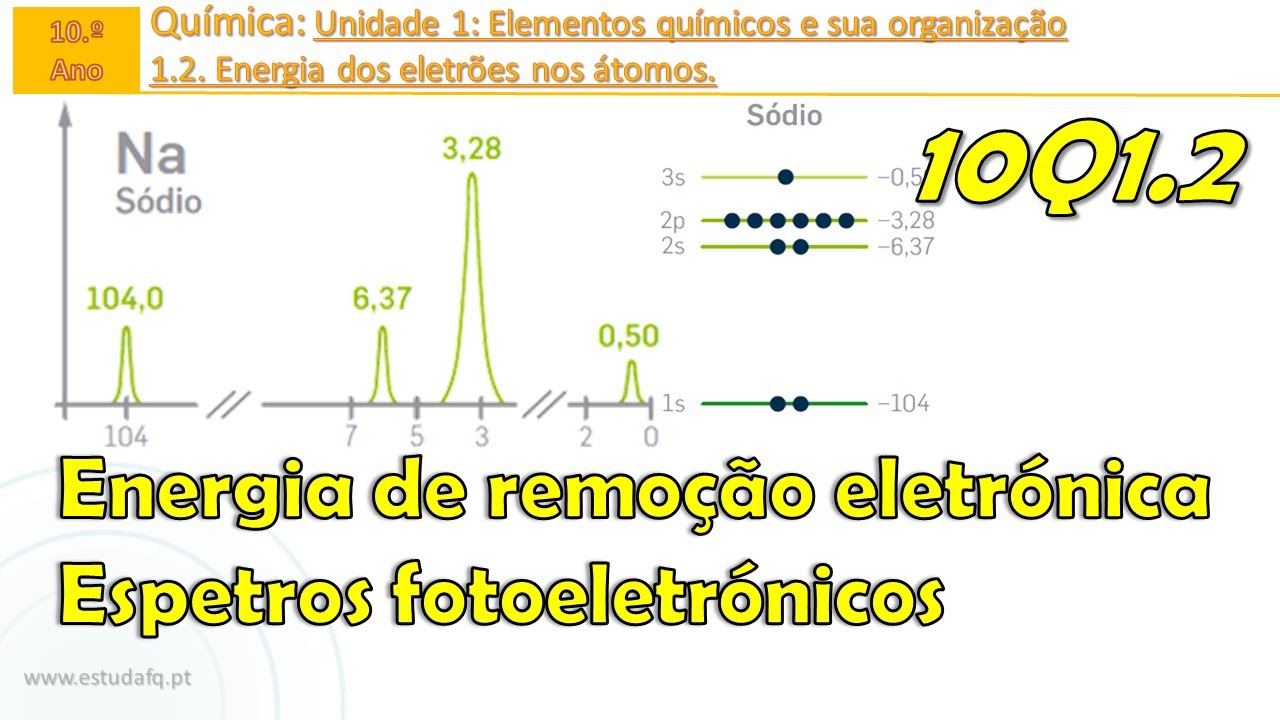
dos electrões em termos de probabilidade tinha sentir surgiu atualmente Aceito o modelo quântico do átomo modelo da eletrônica a nuvem eletrônica representação de disposição e densidade dos elétrons em redor do núcleo e as donas com maior densidade mais perto do mundo respondem uma melhor parafusado encontrar letras existe a técnica estas chamadas espectroscopia fotoeletrônica pés e consiste na determinação da energia necessária para remover um elétron de um energia de remoção energia de remoção vai ser maior junto ao núcleo e o menor mais longe duplo ó é através desta técnica obtenção gráfico número relativo de electrões em
função da sua energia de redução da análise gráfica tiras que os valores das energias de redução forem de ordem de grandeza muito diferentes então correspondem a níveis de energia diferentes se as ordens de grandeza forem próximas Então significa que o nível de energia se encontra dividida em subníveis altura dos Picos é proporcional ao número de elétrons existentes em cada nível ou subnível de energia a partir desta análise é possível concluir que átomos de elementos diferentes têm eletrões com diferentes valores de energia e com os elétrons dos átomos sua vez ocupam diferentes níveis e subníveis de
energia estacionamos orbital a zona À Volta do núcleo Onde existe maior probabilidade de encontrar o elétron quanto maior for o nível de energia maior a quantidade de energia e maior a distância entre o elétron eo núcleo o subnível de energia varia com a forma de orbital aqui é importante saber Skill orbital do tipo é se tem forma esférica as três orbitais do TP tem fórmula o ar as cinco orbitais do tipo de tem formas diversas orbitais degenerados são aquelas que pertencem ao mesmo subnível e por isso tem a mesma energia exemplo 2 s21 e os
pin inglês para rotação é o sentido de rotação dos eletrões cada Orbital que tem no máximo capacidade para 2 electrões de seguinte opostos a configuração eletrônica é a forma como os elétrons distribuídos orbitais no que toca a este conceito É preciso conhecer estes três princípios princípios da construção os elétrons ocupam os subníveis por ordem crescente de energia dos orbitais de um mesmo nível de energia possuem a mesma energia a sequência de crescimento é 1s 2s 2p 3S 3P 3D 3D Verifica o princípio de exclusão de Pauli cada orbital tem no máximo 2 electrões com seres
opostos regra de primeiro distribuição eletrônica porque é habitual para ficar aqui o mesmo semente só depois distribuem seletrans consumir nossos esta regra é bem exemplificada pelos diagramas de caixas aqui tens uma tabela com os dados mais relevantes dos orbitais Até outro a energia E aí e como exemplo prático temos a escrita da configuração eletrônica do lixo símbolo químico SC número atômico 16 s16 como tenho 16 electrões posso escrever da seguinte forma com s 2 2s 2 2p 6 3S 2 3P quatro os elétrons no último nível de energia chama-se electrões de Valência e esse nível
chama-se nível de Valência chama-se serve do átomo ao conjunto do núcleo e todos os electrões interiores ou seja não são de Valença E é isto até já E aí