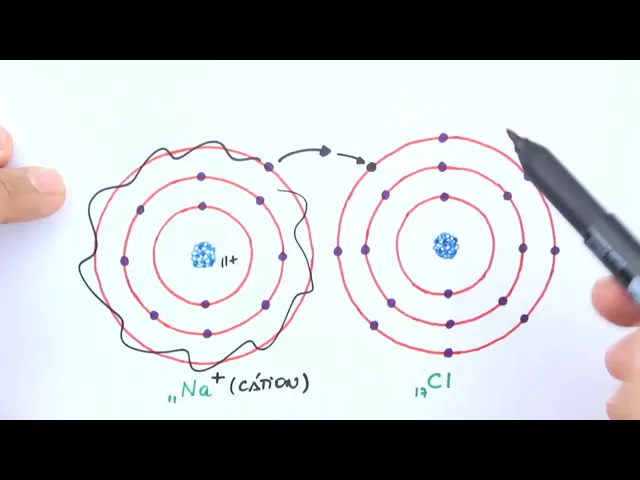
E aí galera do me salva tudo beleza estamos aí mais uma aula de química falando ainda de ligações interatômicas focando um pouquinho agora nas ligações iônicas T ligação iônica como o nome tá dizendo é a ligação que ocorre entre ions então aqui o segredo é se ligar o nome ligação iônica vai acontecer entre ions Tá mas esa aí vamos lembrar um pouquinho o que são ions como eles se formam bom não quia mus cânico olha ali ó simples assim a gente D uma revisada rápido agora olha lá pensando em cloreto de sódio NSL ok nós
temos ali o sódio que tem 11 elétrons número atômico dele é 11 então ele tem 11 elétrons ao todo esses 11 elétrons estão divididos organizados em níveis dois elétrons no primeiro nível tá aqui olha lá dois elétrons no primeiro nível oito elétrons no segundo somando 10 e um elétron no terceiro nível eletrônico beleza até aí tranquilo né no caso do cloro número atômico 17 isso quer dizer que ele também tem três níveis eletrônicos dois elétrons no primeiro nível oito elétrons no segundo nível formando 10 certo e para fechar o 17 de novo o que falta
no terceiro nível nesse caso sete elétrons como o sódio é um metal tem do grupo um apenas um elétron no nível de Valência a tendência dele para se estabilizar é perder este elétron Ok então a gente vai perder esse elétron aqui para que ele fique com os oito do nível anterior este nível Deixa de existir ele não existe mais e este elétron aqui pipoca daqui ele salta para outro lugar neste caso o sódio vai ficar apenas com os 10 elétrons aqui se ele tem 11 prótons número atômico dele é 11 se ele tem 11 prótons
11 cargas positivas e agora tem só 10 cargas negativas logo ele passa uma espécie positiva por isso esse maizinho aqui em cima ó simbolizando que ele agora passa a ser um átomo não mais neutro mas sim um átomo eletricamente carregado chamado de íon I positivos chamamos de C Ok então só para lembrar ali ó ion positivo nós chamamos de c e o que que acontece com cloro bom o sódio não perde esse elétron sozinho do nada ele precisa justamente de um outro átomo mais eletron negativo do que ele neste caso o cloro que é um
ametal lá do grupo 17 coincidentemente certo lá do grupo 17 e o que vai acontecer aqui ó este átomo para ficar estável falta um elétron então a tendência dele é ganhar elétrons de outros átomos neste caso há um átomo de cloro se aproximado um átomo de sódio este elétron aqui que pipoca daqui para cá então este elétron passa agora a ser um elétron do cloro ah mas os elétrons são diferentes tudo igual tudo a mesma coisa não tem elétron diferente não os elétrons o número de elétrons e o número de prótons faz com que os
átomos sejam diferentes mas a partícula elétron em si é a mesma para todos os átomos OK assim como a partícula próton partícula nutron é a mesma para todos os átomos certo Então olha lá agora o cloro continua tendo 17 cargas positivas no núcleo 17 prótons mas elétrons ao redor ele tinha 17 agora tem 18 então ele tem uma carga negativa a mais do que cargas positivas o que faz com que ele torne-se um anion ok bota lá o nomezinho lá anion anion é um átomo negativamente carregado ou seja ele ganhou um elétron de outro átomo
e por isso ele agora está estável e passa a ter essa carga negativa certo então isso aqui é a formação do ion quando dois ions se aproximam ocorre uma ligação iônica Então olha ali ó nós temos aqui uma carga positiva e uma carga negativa um ction e um ânion certo este ction e esse ânion como eles têm cargas Opostas a tendência deles é se atrair à medida que ele se atraem nós temos esse aglomerado de átomos sempre intercalando positivos e negativos ao qual nós chamamos de retículo cristalino certo então a gente não usa a palavra
molécula aqui ok é uma estrutura Cristalina é um cristal uma estrutura cristalina e isso apresenta-se de várias formas geométricas diferentes à medida que eles vão se organizando positivos negativos positivos negativos eles vão se atraindo para essa diferença de carga eletrostática e vão formando estruturas vão se intercalando sempre no mesmo intervalo nos mesmos tamanhos na mesma ordem formando estruturas cúbicas estruturas que mais ortogonais estruturas monoc clínicas estruturas hexagonais e assim por diante certo aí de acordo com o tipo de cristal com tipo de substância química e os átomos tamanhos dos átomos que estão intercalados aqui nós
temos uma ligação iônica acontecendo Ok fórmula iônica para poder entender melhor o que acontece o que acontece a gente costuma representar aqui ok a fórmula iônica docomposto ou seja de que maneira eu vou saber quantos átomos de sódio e quantos átomos de oxigênio são necessários para interagir entre si tá legal então pensa assim ó sódio vai precisar da ajuda tela periódica sempre a tabelinha Periódica do ladinho aqui tá bom e pensa assim ó o átomo de sódio ele apresenta um elétron na camada de valência vou botar um pontinho aqui que representa S Um elétron tá
legal então o sódio representa um elétron de Valência o que interessa na ligação química em si são os elétrons da última camada ou seja desse nível de Valência porque são as primeiras camadas os primeiros níveis que o outro átomo vai entrar em contato então o último nível mais energético e nesse caso mais interessante paraa ligação química e já o oxigênio se encontra lá no grupo 16 isso quer dizer que ele tem seis elétrons de Valência olha não é coincidência não cara isso aqui não é truque Não é magia não isso isso aqui é Pura ciência
sódio grupo um um elétron de Valência oxigênio grupo 16 seis elétrons de Valência Então vamos botar lá ó oxigênio tá aqui o oxigênio tem que ter seis elétrons como é que eu disponibilizo como é que eu disponho esses seis elétrons ao redor imagina aqui que nós temos quatro setores Ok E tu vai dividir 1 2 3 4 5 6 Ok é fácil de entender isso aqui é mais fácil de organizar dessa forma Por quê a gente faz assim ó sempre que os el fem pareados eles não costumam fazer ligações diretamente com outros átomos quem está
desempar quem está desemparelhado é que vai fazer isso então o oxigênio para ficar estável precisa fazer duas ligações ou seja mais dois elétrons se ele tem seis para chegar a oito e fechar octeto precisa de mais dois elétrons Fechou então o que nós vamos fazer aqui nós vamos representar o elétron do sódio sendo transferido para o oxigênio lembra oxigênio mais eletronegativo vai ter a tendência a atrair o elétron do sódio pra sua nuvem eletrônica Ok então ele vai ganhar esse elétron a palavra transferência aparece muito pra gente transferência de elétrons porque na realidade é isso
aqui aqui ó que caracteriza uma ligação iônica é a transferência entre os elétrons de um átomo para outro ok então essa palavra aqui é bastante importante transferência transferido Um elétron aqui nós tínhamos seis agora temos sete ainda não tem oito elétrons aqui não temos o número de elétrons suficiente para estabilizar então o oxigênio vai se aproximar de outro átomo de sódio para pegar elétron de outro átomo a gente representa do elétron com essa setinha aqui tá na real na real o ideal seria usar uma semeta certo a gente não usa muito isso livros de Ensino
Médio raramente tocam nesse assunto mas o correto é representar um elétron usando uma semeta OK depois nos próximos exemplos eu vou usar C7 então para você dar uma olhadinha tá legal neste caso que que nós vemos que para estabilizar um átomo de oxig para ter dois elétrons são necessários dois átomos de sódio cedendo elétrons então a fórmula iônica fica na2 o este dois aqui nós chamamos de atomicidade atomicidade o que é atomicidade é o número de átomos sempre referente ao cara da esquerda então sempre referente ao átomo à esquerda dele então tem dois sódios e
um oxigênio o un não precisa representar que eu não tô colocando ele aqui então o do aqui tá representando a quantidade de átomos de sódio então na2 dois sódios na2 o1 Ok dois átomos de sódio para um átomo de oxigênio certo tranquilo Olha só vamos seguir essa lógica e usar mais alguns exemplos para entender bem o que eu tô falando tá bom mais um exemplinho aqui cálcio dois elétrons oxigênio vimos antes 1 2 3 4 5 6 a medida que o cálcio passar um elétron ficou com sete passou o segundo elétron ficou com oito então
um átomo de cálcio é suficiente para estabilizar um de oxigênio Fechou então tá bom Até a próxima tchau tchau formando aqui ó ca certo até a próxima galera