Ahora sí ahí estamos entonces empezó ahí la grabación Entonces lo hacemos de vuelta esta pequeña introducción en la que decíamos que de lo que vamos a hablar son de cuatro conceptos entre los que están relacionados entre sí pero que son distintos la osmolaridad el proceso de ósmosis la presión osmótica y la tonicidad vamos a hacer un recorrido por esos cuatro conceptos Y por supuesto se relacionan pero cada uno toma características que los distintos entonces Os molaría es el primero el más sencillo decíamos es una forma de expresar la concentración en la cual indica o nos
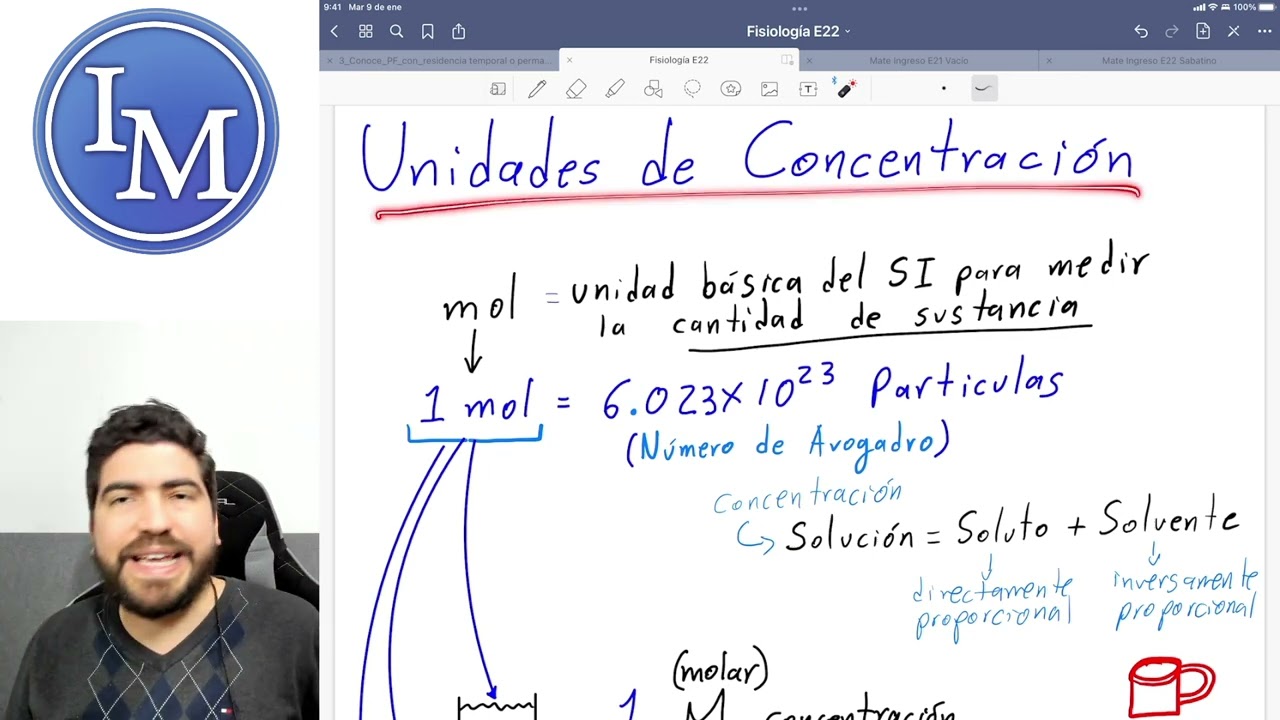
indica el número de partículas que están presentes en una solución esto nosotros ya lo vimos en varias oportunidades a lo largo de diferentes seminarios en diferentes temas desde el primer año digamos hasta Esta parte y sabemos que bueno para esto deberíamos poder definir si es unos moles que un número de abogados de partículas y hacer la distinción en tres muy y Osi se acuerdan Cuál es la diferencia entre mol y small alguien se acuerda Yo calculo que se deben acordar Pero bueno lo vamos a repasar no sé si es que no me escuchan o no
se acuerdan o se cortó la La comunicación porque no tengo imagen de ninguno de ustedes yo no entendí bien profe no escuché le pregunto qué pregunta bien y recuerdan la diferencia entre mol y osmol puede ser que el mall sea de una sustancia en específica y los moldes sea de partículas independientemente de que de que sustancia sea exactamente exactamente pero Es importante de talle y otro detalle más que tiene que ver con que las moléculas las moléculas a veces se pueden dividir en varias partículas Sí entonces hay moléculas que tienen vamos a poner por ejemplo
esta forma y cuando se mezclan con agua o sea cuando están en solución siguen teniendo esa forma entonces Cada molécula da una partícula remoléculas que son como si fueran un Pequeño rompecabezas Sí con esta forma porque están formadas por más de un átomo Entonces cuando se mezclan con agua es decir cuando se disuelvan cuando están en una solución liberan más de una partícula sí Acá tengo una molécula y acá fijo teniendo una molécula acá tengo una molécula y acá también sigo teniendo esa misma molécula Esta molécula que han pensado en estado sólido cuando se mezcla
con agua sigue siendo la misma molécula solamente que ahora se dividió en dos partículas Sí entonces esa distinción es importante para diferenciar lo que es un mol de lo que es un osmol por eso nosotros cuando hablamos de moles hablamos siempre de la misma sustancia porque tiene que tratarse siempre de la misma molécula pero cuando hablamos de dos moles podemos mezclar Diferentes partículas Entonces estamos con la diferencia entre mol y osmol Sí profe definida profe cuál sería o sea como que hablando así qué concepto podría decir si tengo que hablar la diferencia como que una
es de es que no me perdí Perdón bueno no hay problema no hay ningún problema La diferencia es que el mall esto por definición No es cierto el mall es la cantidad de sustancia que tiene un Número de avogadro de moléculas y en los mol es la cantidad de sustancia que tiene un número de avogadro de partículas en algunos casos Esto es lo mismo como por ejemplo en este caso Ah vamos a suponer que estamos hablando de una sustancia Como por ejemplo podría ser la glucosa Sí entonces Cada molécula libera una partícula porque la glucosa
es una sustancia que no se divida no se disocia no solución No libera varias partículas Entonces Cada molécula libera una partícula por lo tanto en un molde y glucosa hay unos mol de glucosa el caso Este es de El que tenemos más abajo podría ser el caso por ejemplo del Cloruro de sodio la cloruro de sodio es una molécula que está formada por dos átomos el sodio y el cloruro Entonces esta molécula en solución se parte digamos se divide es una sustancia iónica que libera dos iones dos partículas cargadas Por un lado por otro lado
el sodio sigue siendo cloruro de sodio pero esta molécula liberó dos partículas por lo tanto un mol de cloruro de sodio equivale a dos moles de cloruro de sodio Olivera dos dos moles de cloruro de sodio sí diferencia entre mol y osmol es el número es la cantidad de sustancias que contiene un número de abogado de moléculas eso es lo que no también lo podemos definir como el peso Molecular gramos el número de ovarios se acuerdan que número es un número que no existe exactamente o sea es un montón a ver Esto es para repasar
No es cierto un poquito estas formas de expresar la concentración que involucra en este número abogado que es una constante un mol cantidad de sustancia que tiene un número de abogado de moléculas unos cantidad de sustancias que tiene un Número de partículas un equivalente cantidad sustancia que tiene un número de avogadro de cargas intercambiadas se usa para sustancias electrolíticas es todo un capítulo que ahora no vamos a desarrollar pero si es importante hacer esta distinción entre mol y quedó claro en esto sí es importante identificar Entonces qué en los monos los moles o la Concentración
osmolar o la osmolaridad entonces a nosotros nos sirve para conocer la cantidad final digamos de partículas liberadas en una solución entonces podemos decir que unos mol o que los molaridad estima el número de partículas presentes en una solución en realidad lo más estricto sería decir que los molaridad está determinada por la cantidad de partículas que están presentes en un litro de solución Sí hay que recordar que estas Tres formas de expresar la concentración que son las molaridad las molaridad de la normalidad siempre están referidas a un litro se acuerdan que decíamos cantidad sobre volumen bueno
acá el volumen siempre es un litro empírica en cambio podría ser en un litro o en un decilitro sí estamos hasta acá con osmolaridad sí Entonces como Dijeron por ahí alguien Dijo agregó de manera muy atinada que a nosotros nos sirva para medir partículas o para sumar o para conocer la cantidad total de partículas independientes Mentes su naturaleza Entonces vamos a suponer que yo meto esto que tengo acá en el pizarrón en un frasco que era un molde de glucosa y un molde sodio lo mezclo con agua lo meto en un litro de agua voy
a tener un litro de agua con un molde de glucosa y un mol de cloruro De sodio pero cuántos moles voy a tener en ese litro entonces entendió esto os molaridad es una forma de expresar la concentración que estima el número de partículas presentes en una solución específicamente en un litro de solución hasta ahí estamos se pueden Obviamente que justamente la utilidad que tienes que se pueden sumar sustancias de diferente naturaleza No no nos importa que en este caso hasta ahora qué tipo de sustancias para la osmolaridad Sí o sea se llama osmolaridad si no
es casualidad estas tres primeras letras con las que empieza la palabra No es cierto o sea algún parentesco con la ósmosis va a tener Entonces vamos al segundo concepto que dijimos recién es el de osmosis Entonces pasamos al segundo punto que es hay varias cosas que podemos decir La gnosis es el flujo de agua disolvente o del soluto es un proceso activo o pasivo es un proceso espontáneo bien entonces yo hay dos cosas que sabemos que se trata del flujo neto de agua pasivo es un proceso espontáneo entonces para que un proceso pasivo tiene que
haber primero una diferencia tiene que haber una diferente Nosotros sabemos que las cosas el calor se Transmite del cuerpo de mayor temperatura al de menor temperatura que las sustancias se transportan de donde están más concentrados hacia donde están menos concentradas que el aire va desde donde la presión es mayor hacia donde la presión es menor lo mismo flujo de un líquido cualquiera bueno acá también tiene que haber algo que va de más A menos bueno Cuál es ese parámetro que se modifica en este caso bueno nosotros Tenemos que distinguir lo que sucede con el agua
pura de lo que sucede con el agua cuando está mezclada con un soluto o cuando disolvemos mal Bueno no es cierto vamos a suponer que nosotros tenemos dos compartimientos el agua pura va a tener un determinado una un determinado contenido energético o hay un parámetro que podemos llamar que se llama actividad La actividad del agua no sé si lo tienen así en la bibliografía actual pero tres solamente hablamos de actividad lo que tiene que ver con el contenido energético de este espacio de este compartimiento la actividad del agua es máxima cuando el agua está en
estado puro sí O sea que cuando nosotros metemos un soluto en un espacio en un compartimento donde hay agua lo que hacemos Es disminuir la Actividad disminuir el potencial químico se entiende eso sí Entonces qué va a hacer el agua va a ir de donde está en mayor actividad hacen de manera activa recordar eso Entonces que la actividad de la voz Es máxima cuando está en estado puro la presencia de soluto siempre reduce la actividad entonces el proceso de ósmosis es el flujo neto De agua espontáneo o pasivo a favor de un gradiente químico donde
la actividad es mayor hacia donde la donde la actividad es menor nosotros lo decimos esto al revés y es una forma apropiada me parece expresar lo que es que es el flujo neto de agua que se produce en forma espontánea entre dos compartimentos que están separados por una membrana semipermeable desde el lugar donde la concentración es Menor hace el lugar donde la concentración es mayor la concentración del soluto No es cierto se entiende esto sí sí profe sí sí Entonces estamos hablando del flujo espontáneo de agua entre dos soluciones que están separadas por una membrana
semipermeable Por qué se produce este flujo espontáneo del agua porque la presencia de partículas en uno de los compartimentos modifica ciertas Propiedades del agua modifica las lo que se conoce como propiedades coligativas hay varias propiedades cualitativas una de esas es la actividad del agua pero otra es el punto de ebullición el punto de congelación y la presión de vapor todas estas características que se conocen como propiedades cualitativas son modificadas por la presencia de soluto cuanto mayor es la presencia de soluto mayor es ese cambio en estas propiedades cualitativas por ejemplo La presencia de soluto en
un en un compartimiento en un recipiente con agua hace que nosotros tengamos que agregarle más calor para que el agua se evapore nosotros vamos a suponer que estamos hirviendo agua en una olla y empieza a empieza a empieza el proceso de ebullición Qué pasa si nosotros le agregamos sal de repente le haremos una cantidad de sal eso lo podemos ver en la práctica cotidiana qué pasa con eso Disminuye esa ebullición No eso lo hemos visto todos alguna vez o no sí Bueno ese es el aumento del punto butroscópico y lo que hicimos fue agregarle sal
agregarle partículas entonces modificamos Esas propiedades cualitativas Entonces el concepto que está por debajo Es que la presencia de solutos modifica algunas de las propiedades del agua que son estas Propiedades cualitativas presión de vapor y la actividad donde hay mayor cantidad de partículas la actividad del agua es menor por eso el agua se desplaza desde el compartimiento donde está puro hacia el compartimiento que tiene presencia de partículas hasta acá estamos Sí sí está claro entonces que es el proceso de ósmosis ahora fíjense que para hablar de ósmosis nosotros estamos Involucrando en el concepto mismo una membrana
en particular que no es cualquier membrana es una membrana impermeable Qué características tienen esta membrana semipermeable pero impide el paso de cualquier soluto bueno eso es una definición para ósmosis que es de relevancia bueno ahora Qué pasa acá Bueno nosotros a esto a este proceso Lo podríamos cuantificar porque nosotros decimos bueno acá tenemos agua pura acá ponemos un soluto cualquiera entonces la presencia del soluto modifica la actividad del agua el agua se va a desplazar va a haber un proceso de ósmosis Perfecto entonces qué va a pasar el volumen de este compartimiento va disminuyendo el
volumen de este va a aumentar en la misma proporción sí estamos hasta ahí sí Que yo le sigo agregando soluto ese proceso va a ser aún mayor entonces diferentes cantidades de soluto generan diferentes flujos de de agua entonces Cómo podemos medir Esto bueno una forma sería intentando evitar este proceso pasamos de vuelta al momento cero nosotros tenemos agua pura y los dos compartimientos en el compartimiento de este lado agregamos soluto El agua va a ir de este lado Vamos a ponerle Perfecto entonces y va a haber un desplazamiento de agua o ver una reducción de
volumendera y un aumento del volumen de B ahora si yo acá le aplico una presión para impedir ese proceso aplica una presión para impedir ese proceso no va a haber flujo de agua pero yo voy a tener un índice de la fuerza que hay que hacer para evitar ese Proceso Entonces eso es la presión osmótica la presión que hay que realizar para evitar ese flujo neto de agua sí esa sería la presión osmótica que me preguntaba Paola profe podrías volver a repetir por favor partimos de esta situación en la cual tenemos dos compartimientos con agua
pura agua pura separado por una membrana semipernable Agregamos soluto Entonces como vimos el agua se va a desplazar desde el compartimento donde están estado puros hace el compartimiento de soluto O sea si hay un desplazamiento de Agua que va a pasar con el volumen de a va a disminuir sí pierdo el volumen vamos con esto sí pierdo uno va a aumentar ese mismo volumen que pierde B Perdón que pierde a velo lo va A ganar Sí ahora si yo aplico en este compartimiento de te pongo un émbolo una tapa de que ustedes quieran unas zapatillas
no sé y evito el aumento de volumen es una presión que yo estoy aplicando en ese compartimiento Sí esa es la presión osmótica la presión necesaria para evitar el flujo neto de agua Y qué genera esa presión no no esto si yo lo quiero medir en un Laboratorio nosotros yo me pongo en una mesada compartimiento Cómo hago para saber para tener un índice de la magnitud del proceso porque yo el proceso lo puedo ver pero cómo para medirlo como para medir esa este proceso bueno aplicando una atracción para editarlo tengo que aplicar Una atmósfera uno
como cinco atmósferas dos atmósferas Sí entonces tengo forma De medirlo profe Pero puede ser que la presión osmótica no sea algo propio de una solución sin necesidad de que haya una barrera entremedio Bueno sí pero para que eso podemos llegar a esa conclusión al final después ver todos los los otros ingredientes podemos decir más cosas de las reaccionesmótica por supuesto O sea que la ósmosis se puede medir con la presión osmó La presión osmótica sirve para medir ese proceso justamente para medir el proceso un curso o para poder predecir cómo va a ser cómo sería
la magnitud de este proceso Sí gracias Un ejemplo Acá tengo no sé dos coma cinco Y este tiene un valor de atrás unos Entonces yo ya sé en qué sentido Va a ir el agua pero esto es una forma la presión osmótica Digamos para que se entienda De dónde sale esto de que Bueno hablamos de este proceso en términos de presión No es cierto una presión ahí que hay que aplicar para para evitar este proceso pero otra otra manera de estimar esa presión es calculándolo nosotros esto también lo podemos calcular y cómo lo podemos calcular
Bueno hay una pequeña formulita Sí entonces ahí vamos a la fórmula de Presión osmótica sí vamos a ir al tercer puntito que íbamos a hablar Que es la presión osmótica y ahora vamos a terminar de caracterizar este concepto pero ya nos habían entonces cómo la podemos calcular Bueno a través de la fórmula que dice que recorte por n por y Acá hay unas algunas cositas que hay que tener en cuenta sí las vamos a calcular r es la constante general de los gases Que el cero coma cero ochenta y dos litros por atmósfera sobre mol
por grados Kelvin es una constante la constante general de los datos ya la conocemos a la constante final de los gases de varios procesos nosotros lo hemos visto en la ecuación de la ecuación del Nerf en bueno en diferentes procesos sí está ahí profe Sí disculpe Es necesario que sepamos el numerito Tampoco se tienen que acordar la unidad pero fíjense que estamos hablando de volumen presión Mall y temperatura presión por volumen por temperatura se acuerdan de esta relación recorrió sobre qué cuando vimos en el trabajo cuando hablamos de la ley de matriota Y de dónde
viene lo de la constante general de los vacas bueno es acá lo tenemos volumen presión temperatura volumen presenta temperatura Cómo se relacionan estas tres variables para los gases los cuento para que lo recuerden como para que la encontremos algún sentido Pero la pregunta que podríamos hacer es que tiene que ver la constante general de los gases acá no sé a veces llama la atención y qué hace acá la constante con este proceso alguien se le ocurre algo Bueno no sé qué es que No hay emociones o o se cortó la la conversación porque no escucho
nada No veo nada me escucho a mí misma me da mucha impresión es como que yo misma y Pero bueno me están escuchando Sí sí se escucha el trabajo lo habíamos estudiado pero personalmente no no lo recuerdo bien a las ilusiones que digamos Están digamos el comportamiento de algunos solutos que están muy diluidos o idealmente diluidos por ilusión infinita se estima que ese comportamiento de esos solutos en solución es similar al comportamiento de los vasos sin fin de esto listo no le importa a nadie se pueden olvidar Qué es la temperatura media en grados la
temperatura es constante listo eso es siempre así la Temperatura obviamente imagínense que va a modificar la presión acabamos de decirnos cierto que esto tiene que ver con Cómo afecta la presencia de partículas ciertas propiedades del agua la actividad el contenido de energía etcétera imagínense que [Música] aumenta la temperatura en un compartimiento determinado va a aumentar las cosas o sea va a afectar el proceso Y por supuesto Lo que pasa que esto tampoco va a ser un problema para nosotros Porque nuestros compartimientos están a la misma temperatura el intracelular y el extra celular mantienen la misma
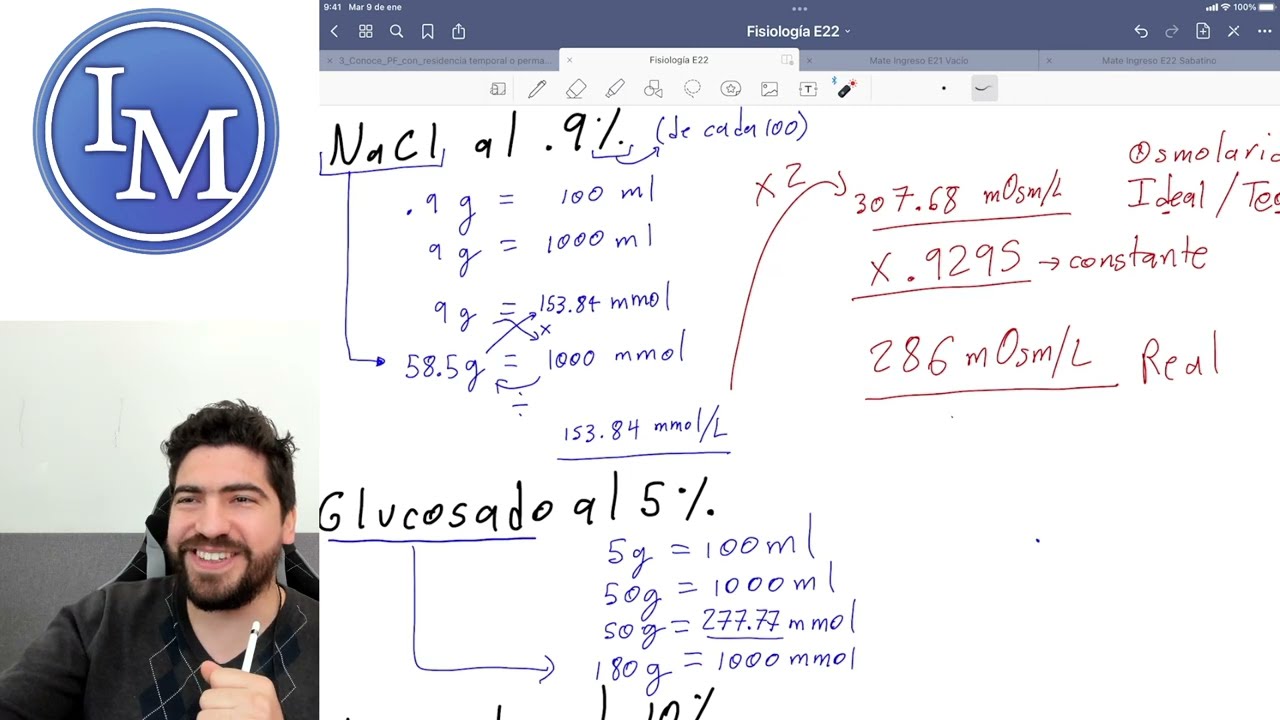
temperatura Entonces no va a ser una variable que nos va a interesar para lo que nosotros queremos medir para mis parámetros que nosotros queremos medir Entonces estos dos es como que no le damos mucha importancia Por ese motivo sí Entonces sí nos vamos A quedar con este pedacito de la fórmula que es m por y porfi y Sí sería lindo que lo recuerden entonces tanto que los judíos al final estamos hablando de moralidad y no desmoralidad Bueno sí por qué porque los multiplicamos por este factor que es el factor y o factor de Van Gogh
cuando nosotros multiplicamos las moralidad por el factor debajo lo que tenemos como resultado finales de la Osmolaridad Por qué Porque y nos indica el número de partículas que libera Cada molécula Entonces como dijimos antes se acuerdan cuando teníamos el cuadradito y los dos cuadraditos abajo acá una molécula liberada una partícula Entonces el Y en este caso cuánto valdría uno molaridad y osmolaridad tienen el mismo valor directamente hablamos de osmonería en este caso una molécula libera dos Partículas acá el Y cuánto sería dos dos cuando nosotros multiplicamos la molería por este factor ya directamente el resultado
que tenemos es la osmolaridad sí Entonces estamos viendo Cuál es la relación que tenía las modalidades del concepto inicial que empezamos a hablar con este proceso fíjense la importancia que tiene ahora no es lo mismo y el otro factor que está acá es el coeficiente osmótico es un circulito con una raya es la letra Suficiente osmótico que es un factor de corrección si ustedes se fijan este coeficiente osmótico es siempre un valor cercano a uno parecido a uno o sea que en realidad si nosotros multiplicamos este valor por un valor eso parecido a uno no
va a modificar mucho el resultado final vamos a Modificar un poco lo va a corregir Por qué está dado este coeficiente Bueno por lo que decíamos antes nosotros tenemos partículas Moléculas en solución que liberan partículas un montón de partículas y nosotros pensamos que por dar un ejemplo un mol de cloruro de sodio o sea 6,023 por Dios la veintitrés moléculas de cloruro de sodio son dos moles de cloruro de sodio o sea dos veces ese número dos veces un número de abogado Esto es así pero imagínense que en esa masa de De moléculas y después
de partículas que tenemos en solución por alguna van a interactuar entre sí y se van a funcionar y ya no se van a volver a unir van a funcionar como si fueran una sola partícula en vez de dos eso qué significa que el número real de partículas que están presentes en una solución porque nosotros estamos hablando de partículas individuales el número real puede ser un Poquito inferior porque quizás algunas partículas que se asocian o interactúan de alguna forma entre sí y que en vez de funcionar como dos partículas funcionan como una eso se modifica con
la concentración Cuanto más concentrado sea un sistema Esto va a ser mayor Cuanto más diluido el sea el sistema eso se va a acercar más a uno no a las concentraciones digamos que se usan en la práctica y ni hablar las Concentraciones fisiológicas ese número es próximo uno por ejemplo para el cloruro de sodio no me acuerdo cuánto creo que cero noventa y cinco noventa y siete una cosa si es bien próximo entonces simplemente lo que hace este coeficiente osmótico es estimar el número real de partículas que hay en una solución si nosotros no tenemos
en cuenta el coeficientes músico Estamos estimando la concentración osmótica teórica si agregamos el coeficiente osmótico estimamos la concentración osmótica real Sí profe Yo tengo una duda de eso sí digamos Cómo cómo sé cuándo usar cada ecuación cuando uso no la ecuación es esta la que habría que usar siempre esta Sí pero esa no sería la real Y sí Y si es teórica en realidad que le tengo que sacar el coeficiente osmótico Es para explicar hacemos esta difícil esta diferenciación para explicar la presencia del coeficientes si nosotros hacemos el cálculo con y sin el coeficiente osmótico
los números van a ser muy parecidos Por ejemplo si hablamos de vamos vamos a suponer esto yo tengo pero 15 moles de cloruro de sodio 0 15 moles de cloruro de sodio en un litro de agua Esa sería la concentración molar lo multiplico por y que en el caso del Cloruro de sodio es 2 Cuál sería la concentración osmolar en este caso 0,30 exactamente esto Solo puedo expresar en los moles por litro como sería este caso o lo puedo expresar lo que es de mayor uso de la cuestión de practicidad nada más Emilio esto sería
la concentración osmótica Teórica vamos a calcular la concentración nosmótica real Sí sería cero quince por dos por cero noventa y cinco alguien lo puede hacer por favor O sea sería calcular sería multiplicar 300 Por 0.95 yo no tengo a mano son concentraciones bastante parecidas pero esta diferencia estima el número real de partículas Sí sí claro profe Yo tengo una duda Sí ese Coeficiente osmótico va a depender del soluto porque yo tenía la idea de que era según la solución O sea pensé que si la solución estaba muy concentrada le va a impedir al soluto disociarse
ponele para el cloruro de sodio va a ser ese número fijo sí okay Bueno gracias Bueno lo que nosotros vamos a hacer a partir de ahora una vez que nosotros identificamos eso A diferencia en realidad después para facilitar el análisis y lo que yo voy a hacer después Porque no lo quiero enloquecer para hacer algunas cuestiones prácticas de resolución sí lo vamos a manejar con la concentración osmótica teórica Sí pero sepamos esta diferencia entre la concentración osmótica teórico la concentración esmótica real la concentración involucra el coeficiente osmótico incluye el coeficiente osmótico y estima El número
real de partículas se entiende la diferencia Sí ahora queremos no un momento hablando Entonces de qué es la presión osmótica porque hay que terminar de definir nosotros ya vimos Cómo se puede medir vimos Cómo se puede calcular Entonces ahora debemos poder decir que o para qué nos sirve conocer este parámetro sí bien y Qué diferencia hay entre ustedes Fíjense que presión osmótica es una cosa que se calcula a través de esa fórmularidad era otra no pero sin embargo la presión osmótica incluye los modelos O sea que una cosa que esta persona es música depende de
los molaridad Pero no es lo mismo Cuál es la diferencia nosotros podemos medir los molaridad de cualquier solución como yo puedo medir Los moralidad del agua que tengo acá del Marco que me estoy tomando de una botella con la cola de un frasco de solución fisiológica cualquier cosa cada uno tiene pero cuando nosotros hablamos de personas modificadas ya estamos hablando de un parámetro que no sirve para comparar una cosa con otra Sí nosotros cuando hablamos de este proceso de ósmosis anterior vimos que había dos Compartimentos un compartimiento a con agua pura y un compartimiento de
con una solución sí queríamos cuantificar el proceso y podemos medir y calcular la presión osmótica entonces la presión osmótica va a ser o va a representar la capacidad de una solución de absorber agua sí cuanto mayor presión osmótica mayor tendencia absorber agua vamos a verlo con ejemplos Si yo les digo por ejemplo ustedes que ya vienen estudiando del área es una solución que tiene una concentración osmolar de 300 mililitros por litro eso es mi concentración osmolar Sí usted qué dirían de estas soluciones isosmótica hiperosmótica o hiposmótica s porque tiene la misma concentración que el plasma
están comparándolo con respecto a algún Otro compartimento me explico o sea decimos esto es un músico con respecto al plasma Bueno yo pongo acá otro compartimento que tiene 400 por litro Esto va a ser hipognóstico sí Y si yo acá tengo otro compartimento que tiene los moles por litro Esto va a salir pero ustedes lo relacionaron y con inmediatamente con las molaridad plasmática y está muy bien pero lo que hoy es esto que esta presión osmótica Nos indica o nos sirve a nosotros para saber cómo es esa capacidad sobre el agua con respecto a otro
compartimento nosotros era un término que es medio que cayó de sufre creo que no lo tienen en la bibliografía pero hablábamos en ese sentido de ósmosidad para distinguir esta característica de los molaridad y de la tonicidad entonces la presión osmótica es la el parámetro que a nosotros nos indica Cuál es la capacidad o la tendencia absorber agua que tiene una solución y nos permite clasificar justamente a esta solución en isosmótica hiperosmótica y cosmótica porque lo comparamos con respecto a otro compartimiento sí que va a tener su propia osmolaridad se entiende la diferencia sí Entonces vamos
a poner dos compartimientos acá tenemos una concentración osmolar Determinada y acá tengamos una concentración osmolar supongamos el doble estas dos veces más concentradas que entonces acá voy a tener una presión osmótica mayor acá Sí este compartimiento B va a ser hiper óptico con respecto a este compartimiento a sí Y si nosotros medimos el con respecto al B cómo va a ser el a con respecto sí Entonces hasta acá estamos hablamos de configuración osmolar a los de ósmosis ahora hablamos de presión osmótica y aquí en este punto estamos hablando de dos motricidad si nosotros acá siempre
tenemos de por medio una nombre más semipermeable ya con estos valores podemos predecir el cambio de volumen Sí porque la membrana semipermeable no No permite El Paso absoluto permite solamente el paso de solvente eso con esto podemos y bueno Y acá tengo una presión osmótica mayor que acá el agua para dónde hay idea hacia B entonces Sí sí Bueno hasta acá todo bien hasta acá si quedáramos acá estaría fenomenal Hola profe Sí una pregunta cómo definimos osmoticidad Bueno en realidad son más que hablar se lo exento digamos este concepto un Poco para diferenciar esto estas
características de la osmolaridad y de la tonicidad pero es un parámetro que está dado por la presión osmótica que es la capacidad de absorber agua que tiene absoluta tener presente que acá nosotros estamos Cuál es la diferencia con las molaridad y acá estamos comparando un compartimento con otro para saber si va a haber flujo de agua para poder predecir si va a haber flujo de agua por Eso yo les digo nosotros veíamos esa ese esta solución Donde había 300 moles por litro de algo bueno eso es una concentración osmolar pero usted porque ustedes por qué
dirían que estos hiperosmóticos isosmótico hoy pero estos músculos y porque lo estoy comparando con algo usted lo compararon con los mareas plasmática que es válida con respecto solamente indica una forma de expresión Solamente indica una concentración pero la presión osmótica ya nos está indicando la capacidad de absorber agua por ceder agua que tiene una solución se entiende la diferencia Sí sí clarísimo Bueno hasta acá digamos vendríamos bien pero qué pasa Nosotros sabemos ya a esta altura que estos molaridad en nuestros compartimentos es uno de los de las Variables fisiologías que se regulan y hay un
montón de sistemas que están digamos que que se encargan de esto no es cierto varios sistemas hay un mecanismo capaz de pensar los molaridad plasmática y desencadenar una serie de eventos y hay modificaciones de modalidad O sea que fue muy alto O sea que fue muy bajo ya saben esta altura también que sos molaridad plasmática bueno está determinada por todos los solutos que están presentes en el plasma Pero que entre ellos uno de los más importantes Cuál es exactamente Bueno no es el único pero es un electrolito importante dentro de las moralidad plasmática ahora sabemos
por otro lado que el resto de los compartimientos por ejemplo Ahí estamos hablando cuando hablamos de plasmática de que cumplimiento estamos hablando acompañamiento extracelular Sí exactamente pero el compartimento Intracelular tiene que ser igual Sí más allá que o parecida lo más parecido posible en realidad del espacio intracelular bueno predominen otros electrolitos por ejemplo quién predomina el espacio de intracelular entre los cationes a eso no predominan el sodio el potasio pero también hay proteínas etcétera dos compartimientos distintos osmolaridades similares compuestas diferentes diferentes solutos no Y esto se tiene que mantener más o menos estable para que
no haya Qué cosa justamente cambios importantes o significativos en el volumen de los compartimentos porque esto mantiene estos dos compartimientos ajustadas dentro de ciertos valores entre 280 y 320 ni los moles por litro mantienen entonces cierto volumen si hubiera un desequilibrio entre las osmolaridades de los dos compartimientos intra Y extracelular qué pasaría habría Modificación de las presiones ópticas Entonces el agua podría ir de un compartimiento a otro entonces bueno por eso estamos viendo este tema ahora entonces qué pasa hablemos de esto de los de las moralidad de los compartimentos más bien el intro celular Esto
hace que las expresiones son góticas sean similares invadimos que la presión osmótica no es lo mismo que las molerías pero que Depende de los sí sí entonces sí esto se va a modificar esto se va a modificar y si se modifica la capacidad de absorber agua de una solución puede haber un pasaje neto de agua de un compartimiento por eso la voz monerida de diferentes compartimentos se regula y debe mantenerse dentro de ciertos parámetros bien eso ustedes ya lo saben ahora nosotros hablamos de osmolaridad Vamos a ver qué sucede en ciertas situaciones si yo tomo
una célula como el famoso glóbulo rojo que le hacemos de todo Pobrecito en en este capítulo Cuál es la osmolaridad del glóbulo rojo que hay en el interior de un glóbulo rojo trescientos el glóbulo rojo representa los moralidad de que compartimiento intracelular Exactamente lo que pasa con los glóbulos rojos en soluciones de diferentes concentraciones es un fenómeno más o menos fácil de medir entonces lo que estamos evaluando en realidad es esta interacción entre dos espacios el intracelular y el Entonces tenemos el glóbulo rojo Como representante del compartimiento intracelular y vamos a ver qué sucede resulta
que acá yo tengo dos soluciones dos Acá una que tiene cloruro de sodio 300 mililitros por litro cada una que tiene glicerol 300 mililitros por litro calculo la presión osmótica el reporte es reporte si tiene la misma osmolaridad la misma concentración osmótica teórica o real vamos a suponer que es la misma concentración real la presión osmótica va a ser igual los dos van a tener la Misma operación osmótica si yo comparo uno con otro Sí la misma presión osmótica cómo son estas dos soluciones entre sí yo comparo una con la otra y quedan flotando felices
un rato después con el tiempo se hizo terminando los lijando pero yo pongo glóbulos rojos acá y se rompen todos se produce una hemólisis que la mayoría de los glóbulos rojos Por qué sucede esto Si las dos soluciones eran esos por la permeabilidad de la membrana y por la naturaleza del glicerol bien exactamente todos tienen razón en lo que están diciendo Entonces hasta acá hasta este hasta antes de hacer este experimento veníamos hablando de membranas impermeables pero las membranas biológicas no son semipermeables entonces o tenemos un problema la presión osmótica No nos des un parámetro
suficiente para predecir cómo va a ser el flujo de agua porque las membranas biológicas no son membranas semipermeables dejan pasar solutos algunos sí otros no otros a veces otros depende porque tienen permeabilidad De qué tipo selectiva entonces Bueno ahí aparece esto que dice este concepto de solutos osmóticamente activos y soluto no osmóticamente activo que tiene que ver Con él Entonces hasta ahí estamos hablando de antes de introducir este esta este problema impermeables ahora sabemos que la membranas biológicas no son semipermeables Entonces vamos a ver algunos ejemplos que me parece que van a ser suficientes para
comprender ciertas diferencias Bueno vamos a seguir usando el ejemplo De los glóbulos rojos que de paso me parece que es el que han visto alguna vez en seminario laboratorio Sí así que les va a sonar Aunque podríamos usar dos compartimientos por cualquiera Entonces vamos a usar soluciones distintas en este caso van a estar compuestas por glicerol en diferentes concentraciones acá vamos a tener una concentración de 300 millas moles por litro Acá una de 400 miles por litro y a cada una de 200 mililitros por litro sí bien entonces yo lo que voy a hacer es
suspender glóbulos rojos en soluciones de glicerol con estas concentraciones O sea que yo voy a comparar esta osmolaridad que va a determinar una que son los modificada con respecto a la osmolaridad del comportamiento intracelular que va a ser de 300 Micromoles por litro Sí eso quiero remarcar que siempre nosotros cuando hablamos de esta presión osmótica la tenemos que comparar con un compartimiento con que se con quien vamos a poner en contacto esta solución que estamos estudiando entonces medimos la presión osmótica y sabemos la presión osmótica está determinada en el espacio intracelular donde tenemos una concentración
osmótica una concentración Osmolar de 300 moles por litro Entonces cómo es esta la de 300 millones por litro con respecto al glóbulo rojo es ISO osmótica sí cuando nosotros hablamos de tendencia a absorber agua que tienen un compartimento cuando se compara con otro asumiendo estar como Si estuvieran separados por una membrana semiper pero dejemos ese elemento por ahora aparte Esto Cómo va Esto va a ser ISO osmótica esta cómo va a ser hiperosmótica y esto cómo va a ser hiposmóticos tipo osmótica entonces metemos los glóbulos rojos en estas tres soluciones glóbulos rojos con unos movimientos
ahora Qué pasa esta membrana no es una membrana semipermeable y estamos frente a una sustancia que es el glicerol que Vemos que por sus características es capaz de atravesar la membrana Entonces qué hacemos porque hasta ahora todo lo que definimos lo definimos para membranas semipermeables hasta acá estaba todavía pero ahora es diferente está en alta concentración en el espacio extracelular pero el espacio intracelular está en Baja concentración Porque estos trescientos como dijimos antes con el resultado de un montón de Un conjunto de muchos productos pero no de glicerol sí Entonces el glicerol va a ingresar
a la célula por diferencia de concentración de donde estamos concentrados hacia donde está menos concentrado va a desaparecer del espacio extracelular para ingresar a la célula hasta acá me siguen sí cuándo hasta cuándo hasta alcanzar el equilibrio va a entrar a la célula por qué puede entrar a la célula porque tiene un coeficiente de reflexión Bajo Bueno eso es la conclusión nosotros la explicación que uno debe un coeficiente de reflexión bajo puedo decir Bueno entonces esto sustancia puede pasar las membranas por qué puede trabajar la membrana la naturaleza lipídica porque la membrana también es está
formada por lípidos Bueno ahí va No es cierto entonces recordar eso la estructura de la membrana que es que tiene una Una un núcleo empírico una matriz idílica muy importante y por ser de carácter lipídico es de carácter apolar todo lo apolar es soluble medios apolares el glicerol es apolar por lo tanto va a poder atravesar la membrana hasta cuando hasta alcanzar el equilibrio a los dos lados 250 acá Esto va a pasar exactamente lo mismo afuera 200 adentro 200 y acá Exactamente lo mismo afuera 100 adentro otros Entonces qué pasa en el glóbulo rojo
se cargó de solutos al cargarse solutos aumenta su presión es valor absoluto porque entró acá tenemos una mularidad final de 450 acá de 500 y acá de 400 Entonces qué va a pasar con en este caso el agua va a ir de dónde Hacia dónde es del led al glóbulo rojo y acá En este segundo caso también sí adentro Y en este último caso donde afuera quedó cien y otro 400 también en todos los casos el glicerol fue capaz de ingresar a la célula y aumentar los mueblerías finales por lo tanto en el primer caso
siguiendo las soluciones y sos música es como desde el punto de vista de la tonicidad y botánica En el segundo caso era ahí perosmótica teníamos pero cómo es desde el punto de vista de la tonicidad y botánico y en el tercer caso hipotónico también entonces varias conclusiones la presión osmótica determinar la capacidad absorber agua que tiene una solución si nosotros consideramos que está separada de otro compartimento por una membrana Semipermeable en el caso hipotético de que fuera separada por una membrana semipermeable esto nos permite a nosotros clasificar a las soluciones en isosmóticas y ferosmóticas y
sos músicas y ferogmáticas ecosmóticos ahora eso es un parámetro dado únicamente por la concentración osmótica efectiva y considerando el caso hipotético que la membrana se trata de una membrana Impermeable de ahí hablamos hasta ahí hablamos de dos motricidad no quiero meterles un término nuevo problemas hasta ahí de personas mórticas Ahora hasta ahí dijimos que estábamos hablando Siempre de casos hipotéticos donde intervenían compartimientos estaban separados por una membrana nosotros como dijimos antes si calculamos la presión osmótica para saber qué pasa cuando se pone en Contacto con una membrana biológica no nos alcanza para predecir el flujo
neto de agua porque las membranas biológicas no son semipermeables sí Entonces qué es la tonicidad es la capacidad que tiene una solución de inducir cambios de volumen en el compartimiento con quien se ponen en contacto generalmente se compartimiento del que hablamos es el intracelular Sí entonces lo que nosotros podríamos decir también sería válido Sería que la tonicidad es la capacidad de una solución de Modificar el volumen celular sí Sí sí bien entonces solutos osmóticamente activos y solutos no osmóticamente activos fíjense lo que pasó acá tenemos un soluto Como dijo Iván con un coeficiente de reflexión
bajo sí que es capaz de atravesar la membrana celular ya dijimos Por qué O sea Reflexión bajo significa que el soluto se refleja poco o sea atraviesa Perfecto entonces coeficiente de reflexión bajo ya sabemos que se trata de un soluto no osmóticamente activo fíjense que solutos que son no osmóticamente activos siempre dan soluciones hipotónicas siempre dan soluciones hipotónicas independientemente de su concentración Repito solutos no osmóticamente activos no osmóticamente activos aquellos que Tienen coeficiente de reflexión bajo que atraviesan la membrana libremente siempre dan soluciones hipotónicas independientemente de su concentración como Lo acabamos de ver sí Acá
está igual concentrado glóbulo rojo que estaba más concentrado siempre Dios el mismo flujo de agua en el mismo sentido siempre soluciones hipotónicas solutos no osmóticamente activos son Solomóticamente activo siempre va a inducir Un aumento del volumen celular que puede poner en riesgo la vitalidad celular entiende Sí profe el fenómeno sería similar al cual pusiéramos agua pura O sea que es como si el soluto no estuviera a estos fines entonces Cómo si nosotros ponemos glóbulos rojos en agua pura qué va a pasar El agua afuera no tiene soluto se produce el pasaje de agua desde el
agua pura hacia el hacia el glóbulo rojo exactamente entonces aumentar su volumen hasta que llega un punto en que puede lesionarse la membrana mezcla de glóbulos rojos con con agua destilada los glóbulos rojos se rompen todos escapa de hemoglobina y quedan todos los Glóbulos rojos de movilizados qué tendríamos que hacer para evitar esto tendríamos que agregar solutos al agua exactamente pero un soluto que no atravieso la membrana o sea son solutos que sí sea osmóticamente activo y ahora vamos a ver un ejemplo de esos Entonces tenemos los y ahora lo que vamos a analizar es
el Otro viejo y querido regreso Entonces vamos a estar concentraciones similares al caso anterior el primer caso de sodio en el segundo caso 400 moles por litro y en el último 200 mil creo que sodio Sí entonces calculamos la presión asmática y la clasificamos de acuerdo a su a este valor Cómo podríamos decir que es el primer caso Cómo es esta solución con respecto al compartimiento intracelular y sus motivos en el segundo caso Y en el tercer caso ponemos los glóbulos rojos y vamos a ver qué pasa acá sabemos que entonces el glóbulo de sodio
tiene un coeficiente de reflexión más cercano a uno esto nos está indicando que no atraviesa la membrana celular por lo tanto se queda donde está eh No hay transporte de glóbulos rojos sodio hacia el interior del lóbulo Entonces en este caso tenemos estos Trescientos que están ahí afuera y los 300 que corresponden al interior del glóbulo rojo no va a haber un cambio del volumen celular porque hoy no va a haber flujo neto de agua entonces si no hay flujo de método de agua y no hay cambio cerebral cómo es esa solución con respecto a
la tonicidad vamos a ver acá acá tenemos 300 en el interior del glóbulo rojo y 422 sodio del lado externo acá va a haber flujo de Agua neto sí o no sí De dónde Hacia dónde hacia fuera de glóbulo rojo O sea que el tamaño del glóbulo rojo se va a achicar Sí porque pierde agua entonces cómo es esta solución desde el punto de vista de la tonicidad y vamos al último caso tenemos 200 del lado externo de la membrana del interior qué va a pasar acá va a ingresar va a ingresar agua qué va
a pasar con el volumen del Glóbulo rojo Entonces cómo va a ser esta solución desde el punto de vista de la tonicidad solutos que sí son osmóticamente archivos solutos osmóticamente activos tienen un coeficiente de reflexión alto no atraviesan la membrana celular y el efecto sobre el volumen del compartimiento con el que se ponen en contacto dependen directamente de su concentración fíjense que siempre conseguimos Y posmótica hipotónica sí entonces un soluto activo con estas características que acabamos de decir es un soluto que es capaz de retener agua en el compartimiento donde está pero el flujo neto
final va a depender de su concentración digo esto porque uno escucha a veces lo siguiente no bueno Qué es un soluto que que mantiene el volumen Es cierto pero faltan las otras dos es un soluto que puede hacer que el doble rojo sea achique de volumen es un soluto que esfuerzo Bueno si todos son ciertas la diferencia es esta No es cierto de los que son osmóticamente activos y los que no son osmóticamente activos los solutos no ostitamente activos siempre dan soluciones hipotónicas siempre independientemente de su concentración los solutos osmóticamente activos van a dar soluciones
que pueden ser isotónicas Hipotónicas o hipertónicas dependiendo de cuál sea su concentración sí Y son solutos que por supuesto en las cantidades apropiadas son capaces de mantener el volumen celular como son isotónicas se entiende la diferencia y la similitud con las cosas o sea repasamos un poquito nosotros hablamos entonces de esto se entendió esto último sí entonces hablamos de osmolaridad Osmolaridad es una forma de expresar la concentración hablamos de ósmosis Recuerden que cuando hablamos de domos y estamos definiendo un proceso en el cual está implicado una membrana impermeable hablamos de presión osmótico cuando hablamos de
presión osmótica También estamos asumiendo que hay una membrana impermeable hipotética la presión osmótica nos sirve a nosotros para clasificar a las solucionesmóticas y cosmóticas o hiposmóticas cuando Nosotros queremos aplicar esto a nuestros compartimientos que involucran membranas biológicas del concepto que nosotros nos resulta interés es la tonicidad Qué es la tonicidad es la capacidad de una solución de Modificar el volumen del compartimiento con quien se pone en contacto podríamos decir si la queremos hacer un poquito corta la capacidad de una solución de Modificar el volumen celular Sí hay un montón de ejemplos ustedes fíjense que Acá
los solutos osmóticamente activos actúan como si la membrana fuera semipermeable no se entiendan Sí sí sí Bueno Esas son las cosas que más o menos a mí me gustaría haberles podido transmitir digamos más o menos que eso es lo que uno espera Porque sí porque nosotros después en la en la clínica usamos esa soluciones hay soluciones y hay soluciones isotónicas hay soluciones hipertónicas Hipotónicas y cada una tiene subjetividad nosotros tenemos más o menos que poder predecir qué es lo que va a pasar con el volumen celular eso es la solución fisiológica le llamamos solución fisiológica
porque está compuesta por un solutomóticamente activo a una concentración de 300 O sea que hizo tónica bueno dejo espacio para preguntas Tienen alguna duda quieren que hagamos algún ejercicio se entendió esto más o Menos Sí profe yo entendí todo el resto profe Yo quiero saber si esto se relaciona con el sistema multiplicador de contracorriente Sí por supuesto estos fenómenos o sea esto nosotros lo podemos aplicar nosotros hablamos acá general de flujo de agua entre dos grandes compartimientos Bueno tengo diez minutitos más Porque si no me quedo encerrada hasta el lunes en la facultad y este
quisiera poder regresar a mi hogar qué preguntas estaban haciendo Cómo se relaciona con el sistema multiplicador de contracorriente este entonces decíamos que estamos hablando de este proceso entre dos grandes componentes no menos de osmosis se producen por supuesto flujos netos de Agua que van y vienen en diferentes sectores en el territorio capilar bueno es para integrarlo No es cierto también con otro con otros fenómenos podríamos hablar de hongos y de equilibrio de las leyes de las leyes que gobiernan las fuerzas de filtración y de absorción Cómo este proceso en el territorio capilar dependiendo de Qué
territorio capilar estemos hablando porque ocurren algunas cosas por ejemplo a lo largo siempre un proceso de filtración Concretamente responder lo que vos decís con respecto al sistema multiplicador de contracorrientes Sí por supuesto que se producen estos fenómenos porque porque hay cambios en la permeabilidad de los de la membrana de los diferentes segmentos del túbulo con respecto al agua y el soluto Sí claro bueno Tienen alguna otra pregunta profe y con respecto a si el líquido es Hiperosmolar o hipertonicidad que es mejor hablar en el sistema contracorriente multiplicador de contracorriente de ahí pero osmolaridad y pertenecía
por ejemplo en la descendente de No a mí me parece que mientras vos tengas claro digamos mientras vos tengas claro cómo son las características de la membrana con respecto al agua que a los solutos en ese segmento me parece no había no había problema en hablar de en Términos de osmolaridad De hecho está escrito así el proceso Ah bueno gracias bueno alguna otra pregunta profe Cómo puedo seguir Me escuchas Sí sí te escucho en cuanto a la ganancia o pérdidas en el deck del diagrama de Darwin o no sí está relacionado No es cierto eso
está relacionado Lo que pasa que bueno tiene que ver con esto por ejemplo voy a explicarlo para ti voy a intentar explicarlo rápido y ahí ya cierro porque de verdad me van a estar encerrado [Música] Bueno hay un ejemplo lindo para para hablar por ejemplo una solución hipotónica como la glucosa la solución de glucosas lipotónica porque la glucosa ingresa a las células por diferentes mecanismos para hacer utilizada como Sustrato energético No es cierto no ingresa a las células como el gliferol que atraviesa directamente la membrana pero sí ingresa a través de diferentes mecanismos transporte específicos
que son modificados donde situaciones específicas algunos de ellos dependen de la presencia de la insulina para que para entrar Dependiendo el tejido No es cierto pero bueno para entrar a la suele ser metabólica entonces la glucosa ingresa a la célula es un líquido Hipotónico por lo tanto sí Entonces vamos a suponer que nosotros tenemos compartimientos intracelular vamos a un volumen estimado 36 litros 12 litros en extracelular 24 litros del intracelular con una osmolaridad en ambos de 300 moles por litro por supuesto acá los volúmenes menor los cuales van a ser menor acá el volumen es
mayor los moles totales van a ser mayor o sea la misma distribución No es cierto para que las relaciones Y nosotros infundimos un litro de dextrosa en cinco por ciento esa ese litro de agua se va a distribuir de la misma manera se va a repartir como están distribuidos entonces un tercio va a quedar en el intracelular perdón dos tercios en el intracelular o sea 333 mililitros van a quedar en el extra celular 666 más o menos va a quedar confinado el intro celular Se van a diluir ambos compartimentos Sí en la misma proporción porque
acá va a haber un pasaje primero de agua del compartimiento extra primero va a aumentar el volumen del comportamiento intracelular va a disminuir los molerías pero después de eso va a ser que ingrese en el intracelular Por supuesto que esto tiene que ver con el tipo de soluto que se trate productos móticamente activo o no y Cómo Se distribuye en los comportamientos recuerden entonces que un soluto que no es osmóticamente activo que son todos aquellos que son capaces de ingresar a la célula se van a comportar como si fuera agua pura y el agua se
va a distribuir como se distribuye naturalmente los compartimientos sí bueno profe gracias Bueno chicos y chicas mucha suerte Espero que les haya servido un poco al menos ahora medio que tengo que terminar la reunión Lamentablemente Pero bueno Cualquier cosa yo les dejo acá mi correo electrónico bueno me alegro que les haya gustado Ya les dejo nosotros lo tienen pero les dejo acá mi correo electrónico porque le quedó alguna duda me escriben y bueno yo Generalmente contesto cada vez tanto me queda uno sin contestar pero hago lo posible por contestar siempre Gracias profe