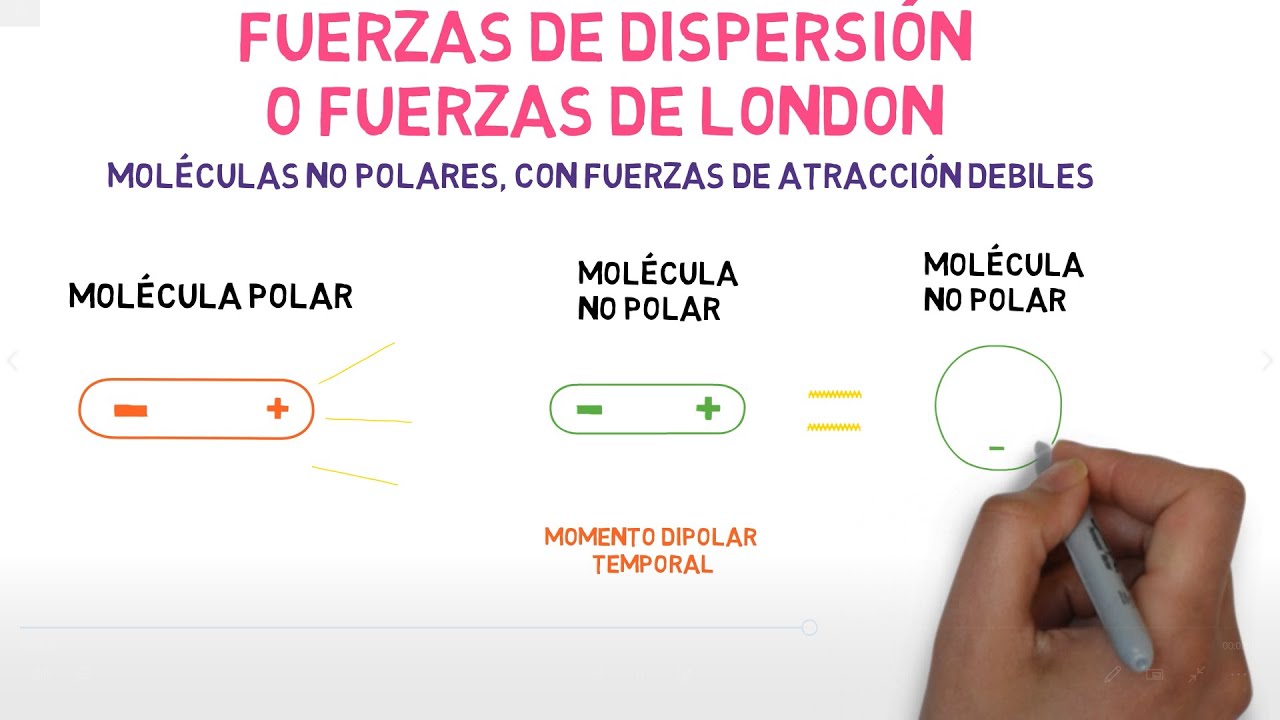
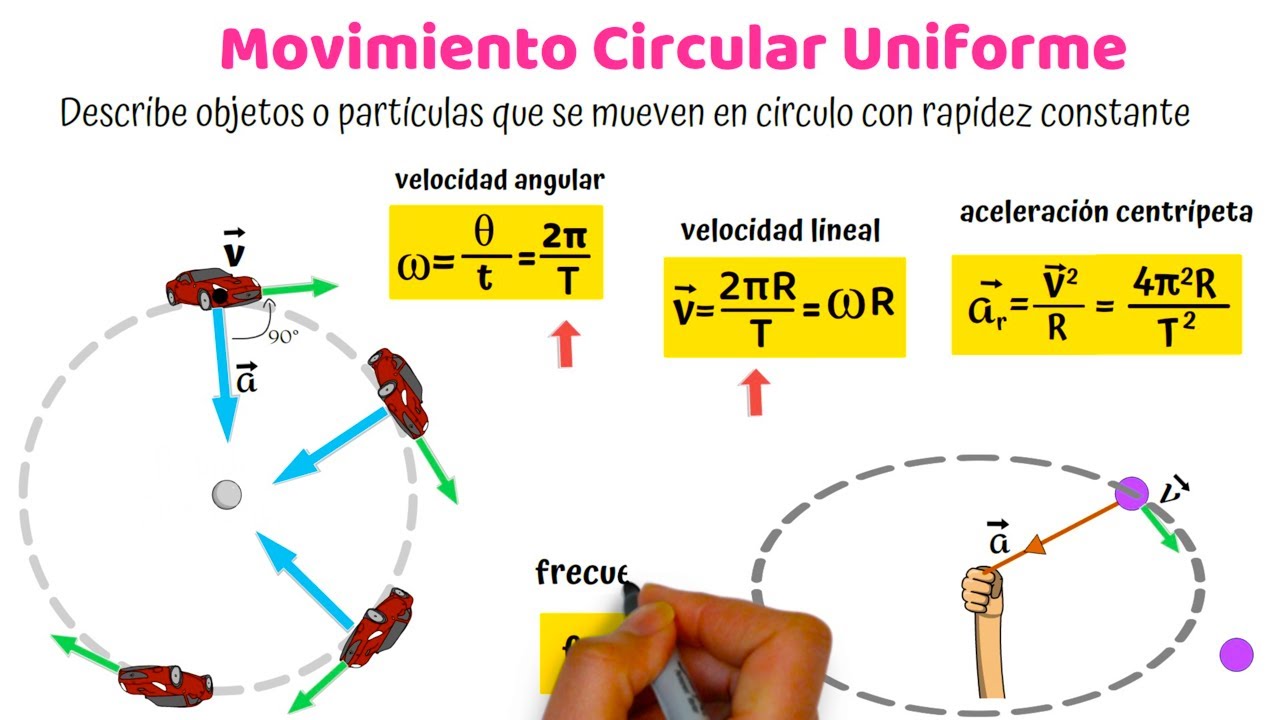
la geometría molecular la geometría molecular se refiere a la disposición tridimensional de los átomos es decir cómo está distribuida la molécula en el espacio la importancia de la geometría molecular tiene que ver con las propiedades físicas y químicas de las moléculas por ejemplo el punto de fusión de ebullición densidad y hasta el tipo de reacción en el que pueden participar tienen que ver con la geometría molecular aunque la distancia y los ángulos de los enlaces deben ser determinados de manera experimental existe un método simple el cual nos permite predecir la geometría molecular de las moléculas
conociendo las estructuras de lewis [Música] el fundamento de este método tiene que ver con el átomo central y su capa de valencia o sea su última capa de electrones este enfoque para estudiar la geometría molecular se llama modelo de la repulsión de los pares electrónicos de la capa de valencia representada por las siguientes siglas ya que se explica la distribución de los pares electrónicos que rodean al átomo central por medio de fuerzas de electrostáticas ya que los electrones tienden a repeler se lo más posible esto para ganar una mayor estabilidad [Música] por ejemplo si queremos
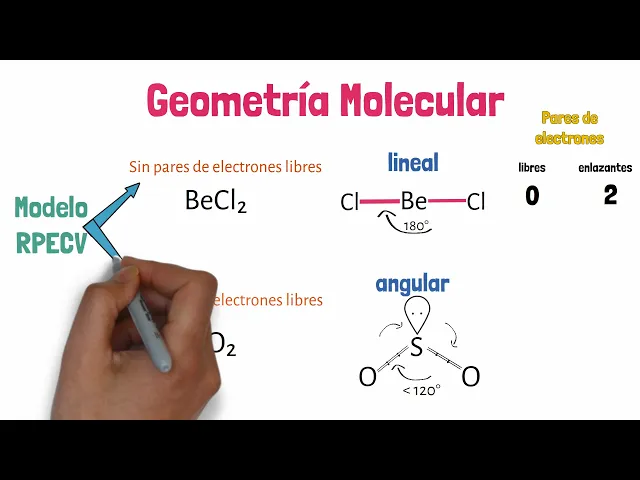
saber la geometría de esta molécula primeramente identificamos al átomo central que es el berilio esta molécula cuenta con dos enlaces hacia el átomo central si nosotros queremos representar la geometría de la molécula alejamos los pares de electrones que forman los enlaces quedando de la siguiente manera por la distancia tan alejada forman un ángulo de 180 grados y ahora sustituimos los electrones por los claros a esta geometría se le conoce como lineal [Música] algo importante a mencionar es que el átomo central de esta molécula no tiene pares de electrones libres ya que si lo estuviera la
geometría cambiaría [Música] vamos a poner un ejemplo para entender mejor lo que pasa cuando hay pares de electrones libres el dióxido de azufre aparentemente tiene la misma forma del ejemplo anterior sin embargo para esta molécula el átomo central cuenta con el par de electrones libres y lo que van a hacer estos electrones es ocupar a otra posición en el espacio además que el par de electrones libres ocupa un mayor espacio ocasionando una mayor repulsión hacia los padres de electrones en las antes formando entre ellos un ángulo menor de 120 grados y esta estructura se le
conoce como geometría angular entonces este modelo se divide en dos partes los átomos impares de electrones libres y los que sí lo tienen por lo tanto al predecir la geometría molecular de los compuestos primero debemos de tener en cuenta la estructura de lewis enfocándonos en el átomo central después vamos a contar los pares de electrones tanto libres como en las antes seguido de esto es distribuir los átomos laterales de tal manera que queden lo más alejados los unos de los otros recordando que si tenemos pares de electrones libres estos van a ejercer una mayor fuerza
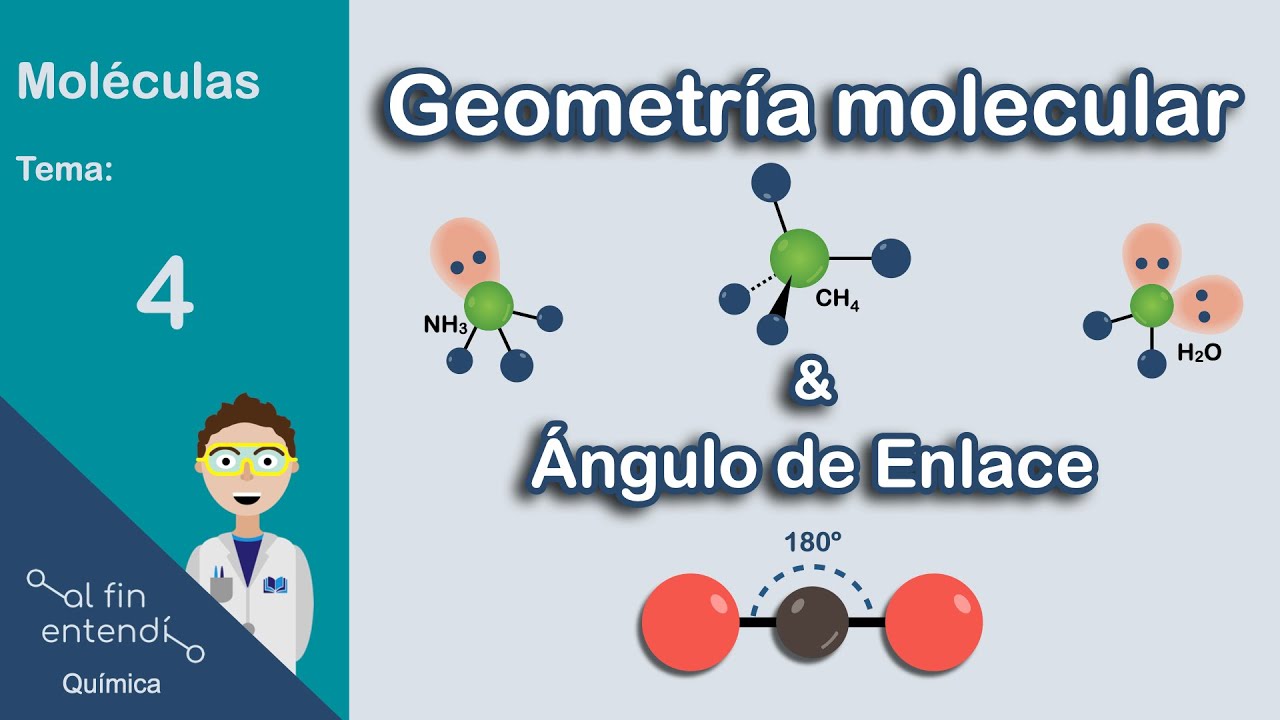
de repulsión hacia los padres de electrones en las antes i libras esto en caso de haber más de un par libre también vamos a considerar que si la molécula tiene un enlace doble o triple se van a tomar como enlaces sencillos en la siguiente tabla se encuentran algunos ejemplos de la geometría molecular para átomos centrales sin pares de electrones libres ya vimos el ejemplo lineal con dos pares de electrones en las antes que al separarlos entre sí forman un ángulo de 180 grados [Música] también está la geometría tribunal plana con tres pares de electrones en
las antes y entre ellos formando un ángulo de 120 grados [Música] conforme van aumentando los pares de electrones en las antes la distribución de electrones se vuelve más compleja [Música] como la tétrica [Música] vi piramidal tribunal con la ostra étnica [Música] para la geometría de las moléculas follones con pares de electrones libres en el átomo central van a cambiar su geometría como se muestra a continuación para estos ejemplos en especial solo tenemos un par de electrones libres pero hay moléculas con más de un par esto es muy importante y se especifica poniendo el tipo de
molécula como vemos en el primer caso que este tipo de moléculas se presentan como a b2 en donde la a se refiere al átomo central que se refiere a los pares de electrones en las antes y el subíndice 2 se refiere al número de pares de electrones en las antes y la es se refiere a cuántos pares de electrones libres hay si hubieran dos pares se específica con un subíndice en la letra [Música] aparte se cuentan los electrones tanto en las antes como libres y totales de la molécula para después hacer su distribución de electrones
para indicar la geometría que le corresponde que en este caso es angular entonces esto se va a hacer con todas las moléculas o iones para indicar su geometría [Música] para esta geometría con átomos libres la variedad de geometrías aumenta debido a que pueden haber más del par de electrones libres en el átomo central y esto ocasionará posiciones y ángulos diferentes esto dependerá del tipo de molécula [Música] si te gustó este vídeo dale like y suscríbete no olvides dejar tus comentarios ayúdanos a saber de qué temas quieres que hablemos nos vemos hasta el próximo vídeo [Música]










![[ QUIMICA FREE ] - TEORIA DE ENLACE COVALENTE I - Geometría molecular](https://img.youtube.com/vi/iDWi0z_7n1c/maxresdefault.jpg)