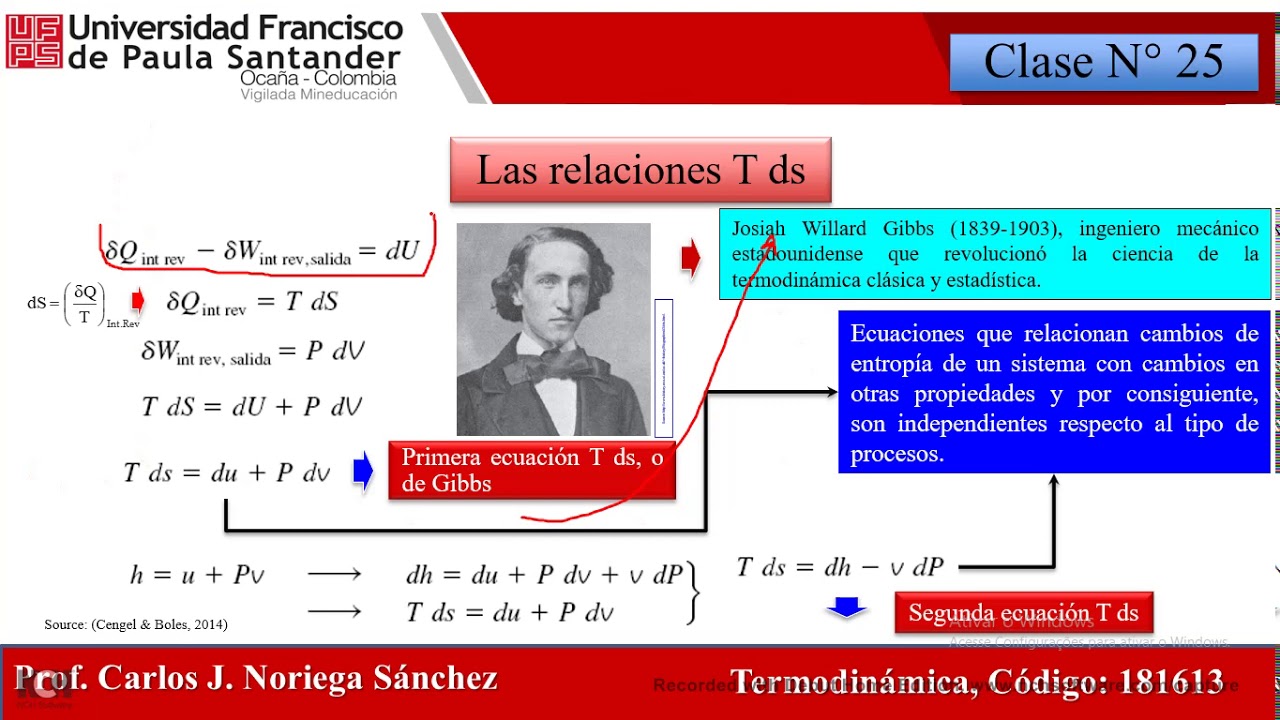
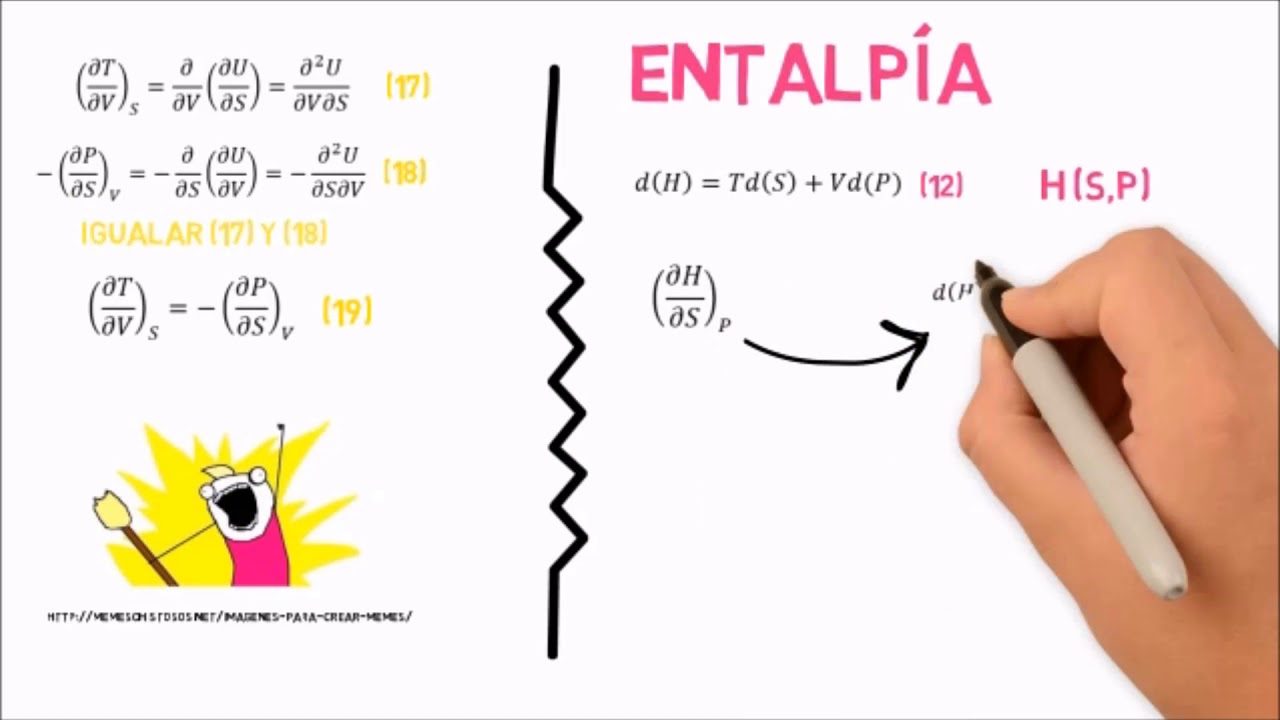
bueno en la continuación de los del contenido programático de la materia vamos a darle continuidad a esta introducción al concepto de entropía sus implicaciones y cómo vamos a determinar esa entropía y cómo éstas se generan durante un proceso listo para ello en este tema vamos a abordar la entropía como tal de donde se origina cuál es la formulación matemática postulado por rudof clausus el principio del incremento de entropía y vamos a cerrar este tema apasionante tema con algunas conclusiones relevantes con relación a la entropía y la generación de entropía entonces en la segunda ley de
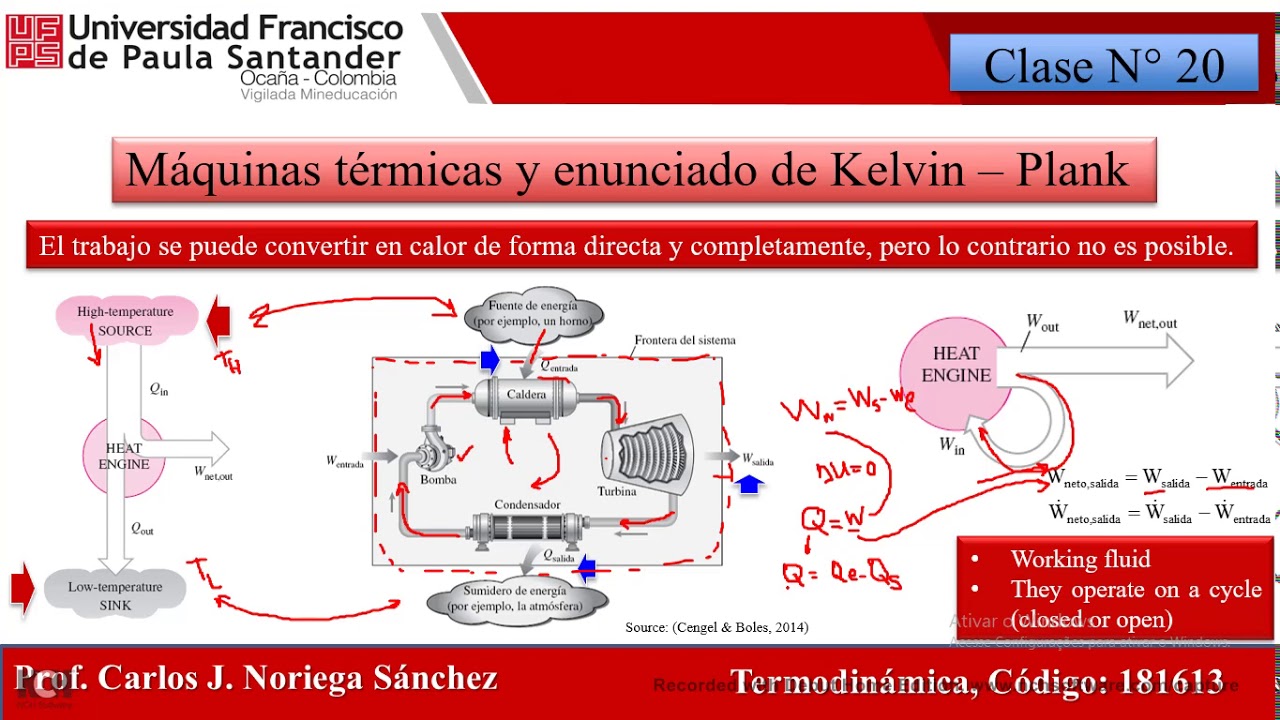
la termodinámica recordamos que hablamos que la energía tiene calidad y cantidad cierto pero los procesos reales tienden a disminuir la calidad de esa energía es cierto entonces frecuentemente en la segunda ley nos hemos encontrado igualdades por ejemplo detallamos cuando hacíamos la introducción a las máquinas térmicas que por ejemplo dos máquinas térmicas reversibles que operasen entre los mismos depósitos deben tener la misma eficiencia termodinámica listo y que una máquina térmica y reversible siempre tendrá una eficiencia térmica menor que una máquina térmica reversible es de hecho la segunda ley o en la definición de segunda ley ya
nos separamos con desigualdades precisamente otra desigualdad de gran relevancia fue aquella postulada por rudos clausus en 1865 en la que hablaba que la integral cíclica de la del calor cierto sobre la dividida entre la temperatura de la frontera era menor o igual a cero visto vamos a determinar que es que que implica eso y como como podemos demostrar que esta desigualdad aquí en el texto original de rudof klaus es cierto la indicaba como lo podemos determinar y como se comprueba esto entonces rudolf klaus es como lo observamos en el manifiesto en 1865 observaba que comentar
que la integral cíclica del calor sobre la temperatura absoluta de la frontera era igual al cambio de entropía es e inclusive clausus fue el primero aquí podemos detallar el primer en físico inclusive considerado el padre la termodinámica que comenzó o introdujo el término o el concepto el término de entropía listo entonces clausus definía esta cantidad como siendo menor o igual a 0 esto siendo recordemos que su calor y esta diferencia línea exacta representa la cantidad diferencial es cierto de calor recordemos que el calor no es una propiedad al igual que el trabajo cierto por eso
la diferencial es inexacta no exacta como el volumen o la energía interna la en tal cierto la temperatura representa la temperatura la frontera la temperatura del depósito de en los que opera la máquina térmica o opere el sistema como tal cierto y recordemos que el símbolo de esta integral nos hace recordar o aseverar o indica nos indica que está aplicada en un ciclo no ciclistas por eso hablamos de una integral cíclica entonces rudof clausus desea que se integral cíclica de esa relación calor temperatura era menor o igual a ser visto a través de este dispositivo
podemos que opera entre un depósito y un sistema podemos demostrar esta desigualdad listo entonces tenemos acá un dispositivo cíclico reversible que opera entre ese depósito térmico a una temperatura absoluta tr y un sistema cuya temperatura de la frontera esté listo que produce una cantidad de calor de trabajo perdón reversible porque es un dispositivo de cíclico irreversible y que parte de ese calor que recibe es cierto recordemos la finalidad de la máquina térmica parte de secarlos lo transforma el trabajo y otra parte la desecha a un depósito a baja temperatura en este caso el depósito es
este sistema está una temperatura de iu que esa transferencia de calor produce una cantidad diferencial de trabajo aquí simbolizaba como el diferencial de trabajo del sistema y esto si aplicamos el balance de energía a ese dispositivo cíclico reversible combinado junto al sistema vamos a tener estas fronteras listo y podemos observar qué calor y trabajo cruzan las fronteras de este sistema listo entonces por lo tanto podemos tenemos un sistema cerrado y del balance de energía tendremos esta expresión despejando el diferencial del trabajo tenemos diferencias de calor menos la derivada observen acá derivada cierto no inexacta como
el calor o como el trabajo sino la derivada que es exacta porque recordemos que estamos hablando de una propiedad energía interna visto que se deriva exacta de aquí siendo que este trabajo está diferencial de trabajo implica o ya está considerando los dos ciertos los trabajos producidos por el dispositivo en cíclico reversible y por el sistema como pues tenemos acá un dispositivo cíclico reversible es cierto y por ejemplo mientras este dispositivo experimenta experimenta un número equis de ciclos cierto es disponible de este sistema puede experimentar un ciclo entonces en total tenemos acá una un dispositivo un
sistema combinado que opera cíclicamente listo y sabemos qué los estados de energía para un sistema que es sometido un ciclo pues es cero o sea que la prueba la condición final es la misma la condición inicial es por lo tanto podemos decir que calor diferencial de calor es igual al diferencial de trabajo cierto conservante de trabajo recuerden recordando cierto es la suma tanto del trabajo producido por el dispositivo cíclico reversible como por el sistema esto como este dispositivo es cíclico reversible recordemos de la escala de temperatura termodinámica vamos a llegar a esta relación es el
calor igual a la razón de temperaturas de ahí que se pudo determinar la máxima eficiencia térmica tanto de una máquina térmica o de un refrigerador de bomba de calor entonces de aquí podemos despejar el diferencial de calor cierto igualando la tr veces el calor que recibe el sistema dividido entre la temperatura absoluta de la frontera poca como la temperatura tr pues la temperatura del depósito en este caso el depósito alta temperatura recordemos que las temperaturas son absolutas por lo tanto esta cantidad es positiva acá y observen aquí que este dispositivo cíclico opera en un depósito
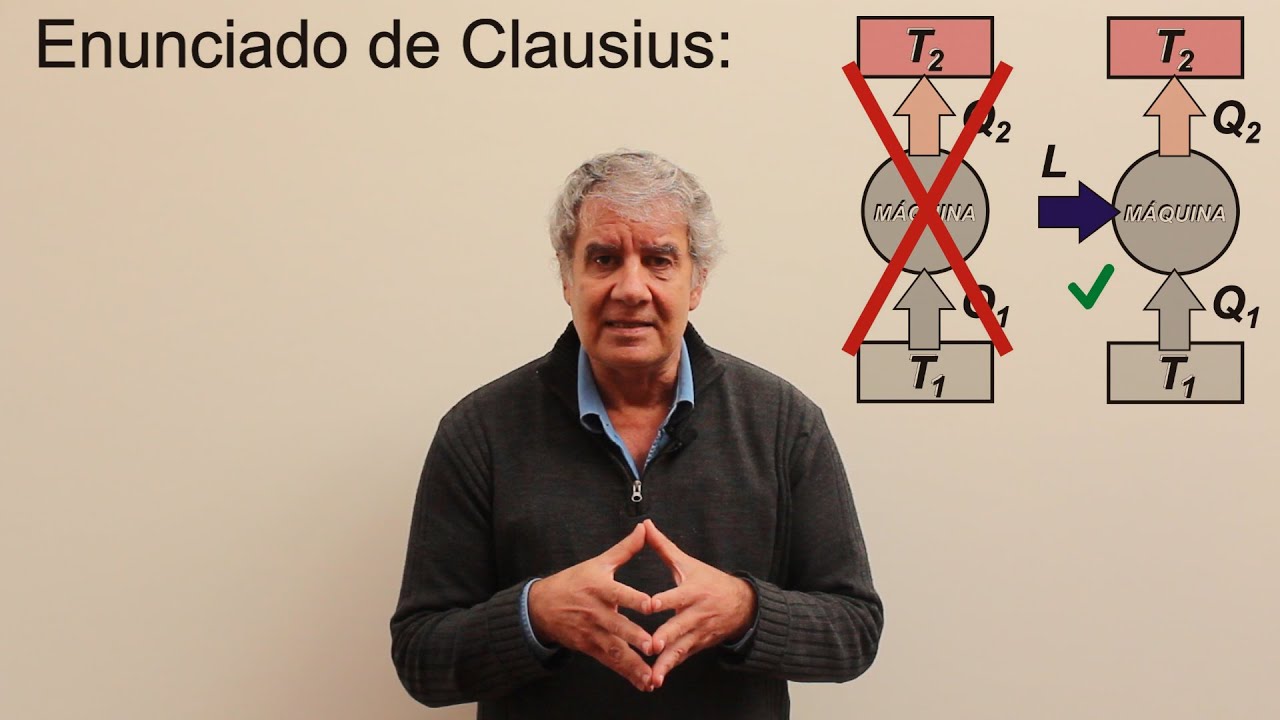
entre un depósito y transforma todo el calor en trabajo cierto entonces aparentemente pues estamos violando la desigualdad de que el implan que son los postulados digamos línea base digamos madres para la definición de entropía entonces no podemos tener un dispositivo que transforme todo el calor en trabajo cierto tampoco para tener una eficiencia de 100 por ciento entonces ahí estamos violando la desigualdad de kelvin plan para dispositivos cíclicos entonces por lo tanto este término que está dentro de esa e integral cíclica no puede ser mayor a 0 porque porque si es mayor a 0 pues tendremos
que el trabajo producido cierto ya integrado acá hacer tus recuerdos ya integré red como integre pues obviamente remuevo la diferencia línea exacta entonces si esta cantidad diferencial a esta relación calor temperatura este diferencial de calor la temperatura fuese positiva obviamente el trabajo sería positivo porque tener es positivo y si es positivo que decir que todo está saliendo y obviamente si estamos violando la desigualdad de que el vínculo pues esto no es posible por lo tanto este término que está al interior de la integral cíclica debe ser menor o máxima a lo sumo cierto sí igual
a cero entonces de aquí comprobamos esta desigualdad de kelvin plano es decir la integral cíclica de esa relación calor temperatura siempre es menor o igual a cero y es válido tanto para ciclos reversibles como irreversibles pero que implica a ello es cierto que implica cierto que esta integral cíclica del calor y temperatura sea menor o igual a cero entonces la igualdad quiere decir que se cumple tanto para ciclos reversibles total o sólo internamente reversibles cierto mientras que la desigualdad es en menor se mantiene para los irreversibles pero qué cantidad qué cantidad cuya integral cierto cíclica
es menor o puede ser igual a cero en el caso de los internamente reversibles qué cantidad qué variable tengo aquí que hace que su integral cíclica es decir fue y retornamos al muy serio al proceso y retornamos al mismo punto inicial donde partió es igual a cero entonces de esa conclusión cierto de esta representación de esta demostración matemática clausen descubrió que el término al interior de esa integral cíclica pues obviamente debe ser una propiedad porque porque recordemos que como ocurre con el volumen cierto el volumen en un ciclo pues es igual a cero si el
cambio de volumen en un ciclo es igual a cero porque el estado final es el mismo estado que inicial en pocas palabras la integral cíclica de una propiedad sea cual fuese es igual a cero listo de ahí que clausure descubre descubrió a través de esa representación una nueva propiedad que es la llamo entropía cierto cuya integral sí que pues es igual a cero entonces aquí lo representamos en este diagrama de temperatura entropía cuando tenemos absoluta 1 kilo yo lo que el incierto de los juliá unidades de calor que el vino unidades de temperatura absolutas listo
entonces observen acá que en este caso cierto si tenemos dos estados iniciales final estado inicial con una entropía de 0.3 y el estado final con 0.7 cierto el cambio de entropía de 12 pues tenemos acá el valor de 0.4 pero vamos de 2 a 1 pues nos daría 0 sea en la integral cíclica de esta propia en este proceso pues es igual a que a 0 listo en este en este proceso que sometido a un ciclo independiente de que se haga de forma irreversible es decir que el sistema experimento irreversibilidad es a la hora de
ejecutarse ciertas reversibles por ejemplo como la fricción o para procesos reversibles porque recordemos que las propiedades dependen única y exclusivamente del estado del estado es decir en el estado no tenemos el valor de una propiedad y en el estado tenemos el valor de otra propiedad sin importarnos la trayectoria cosa muy diferente que aplica para el calor y el trabajo porque recordemos que el calor y trabajo si dependen de la trayectoria del proceso entonces lo que tenemos acá es una propiedad y en la que clausuró llamo entropía listo la definición exacta y precisa aplica exclusivamente para
procesos internamente reversibles ciertos que aplicamos sacar bueno integramos ambos términos tenemos a que después es el cambio de entropía siendo igual al integral cierto del proceso de 12 aplica exclusivamente esa definición como tal para procesos internamente reversibles cierto pero el cambio el cambio el cambio de entropía cierto es el mismo ya sea para un proceso irreversible o e irreversible o reversible o internamente reversible recordemos que aquí la la la letra mayúscula cierto d se aplica lo mismo que para la energía interna o entalpía ciertas son unidades absolutas que en el caso de la entropía pues
era kilos julie sobre kelvin si hablamos del sistema internacional vtv sobre ranking cierta en el sistema inglés y también podemos hablar de entropía específica es decir que depende de la masa del sistema cierto una vez conocida la masa del sistema puede multiplicar la por la entropía y determinar la entropía absoluta del sistema entonces el cambio de entropía es cierto entre dos estados especificados como les comentaba es el mismo sin importar qué trayectoria sea reversible o irreversible se sigue durante el proceso porque recordemos que el cambio de esa propiedad cierta pues depende únicamente del estado de
la condición no del proceso visto entonces hay un caso especial para procesos isotérmicos de transferencia de calor visto procesos que pueden ocurrir entre depósitos deposite hacia una fuente de son sumidero porque consideramos que los depósitos pues son reservorios reservatorios grandes energía cierto cuya masa es tan elevada que las transferencias de calor cierto influencian mucho muy poco en el cambio de temperatura de estos depósitos cierto entonces a la hora pues de aplicar esa integral podemos que se puede esa temperatura de ese de ese depósito cierto puede ser considerada que constante listo de hecho que se procede
transferencia ocurre de forma que hizo térmica que podemos sacar esa temperatura de esa integral y para procesos internamente reversibles tenemos cierto que ese cambio de entropía en ese proceso de transferencia de calor hizo térmica es igual a calor sobre la temperatura absoluta ya sea de la frontera como tal o del depósito visto depósito ya puede ser sumidero o puede ser fuente y está o este cambio dentro pie puede ser positivo o negativo es decir el cambio de entropía medido única y exclusivamente como la transferencia de calor a un depósito cuya temperatura permanece constante puede ser
negativo o positivo depende de la trayectoria de ese calor recordemos que ese calor es considerado positivo cuando ingresa al sistema y negativo cuando sale del sistema listo entonces ese cambio de entropía en ese proceso de ese proceso de transferencia que parece positivo puede ser negativo dependiendo de la trayectoria de ese calor listo pero ahora vamos a identificar qué es el principio de incremento dentro que pareciese que siempre la entropía está aumentando está creciendo cierto nunca disminuye cierto a lo sumo puede ser 0 pero qué es ese principio de incremento de entropía entonces para demostrar ese
incremento de entropía vamos a valernos de dos procesos cierto tenemos dos estados el estado 1 y el estado 2 y vamos a llegar a esos estados de forma que el proceso cierto que ese proceso ocurra ya sea de forma reversible o irreversible recordemos irreversibles pues que en la en en el proceso ocurren o se presentan irreversibilidad es cierto fricción en reacciones químicas ciertos procesos súbitos etcétera espontáneos que hacen que se aumenta el desorden del proceso listo entonces si aplicamos esa integral cíclica de la relación calor y temperatura a lo largo de esas dos trayectorias cierto
vamos a determinar vamos a tener la sumatoria de estas dos de estas dos cantidades siendo que la primera pues ya puede ser aplicada a lo largo de una trayectoria reversible o irreversible y la segunda aplicada única exclusivamente para una trayectoria internamente reversible listo recuerdan en la que no hubo presencia de irreversibilidad es esto y esta segunda cantidad pues es precisamente la definición de entropía cierto de la definición del cambio de entropía listo la definición del cambio de entropía entonces si sustituimos ese cambio de entropía en la segunda cantidad menor o igual a cero que es
la desigualdad podemos despejar aquí esta cantidad y determinar y colocarla en forma de expresar esa relación en forma diferencial que el cambio de entropía siempre va a ser mayor o igual a esta relación listo entonces recordemos que esta relación puede ser para procesos reversibles o internas o reversibles perdón o irreversibles siempre aquí vamos a estar en este aspecto de segunda ley vamos está hablando de procesos reversibles o irreversibles y a veces eso se puede prestar para digamos a lograr pronunciarnos confundir un término con otro pero la pronuncia pero debemos tener claro que reversible hace referencia
a que no hay en fenómenos que hacen que la energía se degrade cierto se pierda pierda la calidad como una friki entonces en forma diferencial podemos se puede mostrar cierto que esta relación se puede expresar de esta forma sin que el cambio de entropía va a ser mayor hay que tenerlo claro el cambio de entropía es mayor o igual a la relación d el diferencial de calor sobre la temperatura listo entonces que no hay que confundir esta relación con esta desigualdad como tal visto recordemos que la integral cíclica del calor la y la temperatura esa
relación del diferencial de cambio de la temperatura es de menor o igual a cero esto pero que el cambio de entropía el cambio dentro pie es mayor o igual a la relación del diferencial de calor y la temperatura eso que implica esto qué quiere decir entonces para que antes de indicar le saca el de esa recogemos es el cambio de entropía y la relación del diferencial de calor y la temperatura es la transferencia dentro dentro vientos pareciese cierto qué siempre el ds es mayor y parece ser siempre en el peor de los casos es igual
en el menor de los casos y digamos es igual cierto pero sabemos que no es así porque siempre van a ver irreversibilidad es en los procesos reales entonces pareciese que el cambio de entropía es mayor que la transferencia de entropía por medio del calor listo entonces para los ciclos o para los procesos internamente reversibles la igualdad se cumple es decir de ese va a ser igual al diferencial de calor en la temperatura para procesos internamente reversibles y la desigualdad se cumple para procesos irreversibles entonces pareciese que en los procesos irreversibles algo dentro piense genera y
por qué se genera esa propiedad debida a las que a las irreversibilidad es entonces por ello aquí les aumentamos este término cierto qué da a entender que durante los procesos irreversibles algo de dentro pie se genera cierto algo dentro que se produce debido a la que a la presencia de irreversibilidad es entonces el cambio de entropía para procesos irreversibles es mayor que la transferencia de entropía entonces repito el cambio de entropía para los procesos irreversibles es mayor que la transferencia de entropía que lo hace mayor esta entropía generada listo aquí sólo para recordarles que esta
temperatura la temperatura de termodinámica de absoluta absoluta de la frontera cierta a través de la cual el calor diferencial se transfiere es entre el sistema entre el sistema y los alrededores esas temperaturas siempre la marca de que es una cantidad absoluta no lo observamos en las unidades de la entropía cierto hablamos de que el vino de rankin no de grado sentido ni grado fahrenheit entonces pareciera cierto que algo de entropía se genera a lo largo cuando estamos en presencia de procesos irreversibles cierto entonces por lo tanto esta cantidad de ese generada no es una propiedad
listo no es una propiedad del sistema depende de que del proceso es decir si el proceso se hace de forma reversible pues esto es sea esto es cero si lo hacemos si el proceso se hace de forma reversible es decir sin irreversibilidad es pero es mayor a cero cuando ese proceso pues se desarrolla de forma irreversible listo entonces hay esta cantidad se conoce como el principio de incremento de entropía es decir la entropía de un sistema aislados en el peor de los casos digamos en el caso base si fuese aislado pues no tenemos transferencia de
calor porque no hay pérdida de calor entonces en ese caso cierto en que el sistema es helado el proceso siempre la entropía durante se presiente se incrementa como mínimo es igual a cero pero en el caso límite de que ese proceso sea reversible permanece constante es decir igual a cero si no hay transferencia de calor si el proceso es irreversible pues la entropía el cambio de centro pier generada aumenta cierta si es irreversible y el cambio de entropía es en ese proceso a diabético cierto es decir aislado considerando que una pierde calor pues va a
ser igual a cero cuando el proceso sea que reversible porque en los procesos reversibles pues como mínimo la entropía va a permanecer que constante visto en otros términos nunca que disminuye mantiene disminuye entonces eso nos va a servir esa definición de entropía generada va a dar como un punto de partida para determinar qué tan bueno está haciendo mi proceso sí es decir en el mejor de los casos la entropía generada es cero cuando el proceso es reversible imposible sería un proceso cuya entropía generada sea menor a cero y en los procesos reales que son los
procesos irreversibles tendremos una generación de entropía es decir que es entropía generada va a ser mayor a cero y podemos considerar todo es entropía generada cierto como la suma de la entropía generada por el sistema que puede ser o la entropía el cambio de entropía del sistema puede ser negativa claro depende de la transferencia de calor cuando hablamos de cambio de entropía en función del calor sí pero el todo cuando consideramos sistema y alrededores debe ser mayor o igual a cero y esto nunca puede que disminuir visto la entropía generada nunca puede disminuir porque sería
hablar de un proceso que imposible listo entonces la igualdad se cumple para los procesos reversibles y la desigualdad para los irreversibles listo entonces podemos determinar acá y de hecho vamos a verlo en varios en problemas que se atrofia generada como ponderada o calculada como la suma de la entropía generada por el sistema y la entropía generada por la alrededor siempre va a ser mayor o igual a cero visto que repite repito ser igual a cero para el caso de procesos reversibles y mayor a ser mayor a cero para los procesos irreversibles entonces podemos tener es
sacar estas cuatro de estas tres conclusiones que las extranjera libros en el a propósito un libro bastante ilustrativo y práctico para hablar de esta parte introductoria de entropía de generación de entropía porque en la secuencia pues ya vamos a aplicar esa entropía para sustancias puras para grasas ideales pero es ésta esta parte básica digamos de concepto fundamental de entropía se encuentra bastante detallada en el libro de schengen de hecho pues lo destaca en las conclusiones y los procesos la primera conclusión podemos decir que sólo pueden ocurrir en una cierta dirección no en cualquiera y esa
dirección cuál es pues en el principio de incremento de entropía es decir el ser aquel en la que la entropía generada sea mayor a cero en el caso de procesos irreversibles o igual a cero como mínimo en el caso de los procesos reversibles cierta la entropía es una propiedad que no se conserva hay quien hablamos del principio de conservación de entropía no como si hablamos de la energía la energía se conserva visto entonces ésta se conserva sólo durante un proceso reversible idealizado es decir el cambio de entropía se mantiene constante s 2 menos s 1
es igual a 0 tenemos una entropía constante en un proceso reversible es cierto pero se va a incrementarse para todos los procesos reales porque porque en los procesos reales tenemos presencia de irreversibilidad gestión y el desempeño de los sistemas de ingeniería es degradado por la presencia de irreversibilidad es y la generación de entropía es una medida de la magnitud de reversibilidad presentes durante el proceso a mayor magnitud de reversibilidad es mayor generación de entropía por lo tanto esa entropía generada es un parámetro fundamental para mensurar que tan irreversible que tan malo que tan ineficiente está
haciendo mi proceso en función de centro pía de esa entropía generada que como mínimo es igual a cero como mínimo podemos llevar a un un proceso en cierto una actividad en el que la entropía general hacia cero se mantenga constante el cambio de entropía y la y lo ideal pues sabemos que no podemos tener de centro pi a generar igual a cero pues es llevarla disminuirla al máximo o joel apoyaban la cero pero vemos que no podemos porque los procesos reales siempre van a estar expuestos irreversibilidad es sí entonces esas tres conclusiones bastante relevantes alcalá
con relación a la entropía la generación de entropía listo nos dan pie para definitivamente concluir que los procesos ocurren en una dirección y esa dirección es el incremento de entropía por lo tanto la entropía del universo siempre está aquí aumentando aumentando debido a la presencia de irreversibilidad es en las actividades que se realizan en las irreversibilidad es que están amarradas a todo el proceso real gracias por la atención espero que haya podido esbozar o darles digamos conceptos o ideas acerca de la entropía y de la generación de entropía muchas gracias