A diluição é um processo de preparação de uma solução a partir de uma solução mais concentrada, chamada Solução Mãe, pela adição de um solvente. Então, se nós soubermos qual é o volume da solução mãe que nós pegamos, este volume dado em litros, e se nós soubermos qual é a concentração da Solução Mãe em mol por litro, se multiplicarmos 'concentração' e 'mol por litro' pelo volume em litro, nós temos o número de mols de soluto que nós retiramos da solução mãe. Este número de mols vai ser transferido para um segundo recipiente e este número de mols de soluto é constante, ele não é alterado.
Agora, neste segundo recipiente, nós vamos fazer a diluição. Nós vamos adicionar uma determinada quantidade de solvente de maneira que a solução agora apresenta-se mais diluída. Nós temos um volume de solução que é maior.
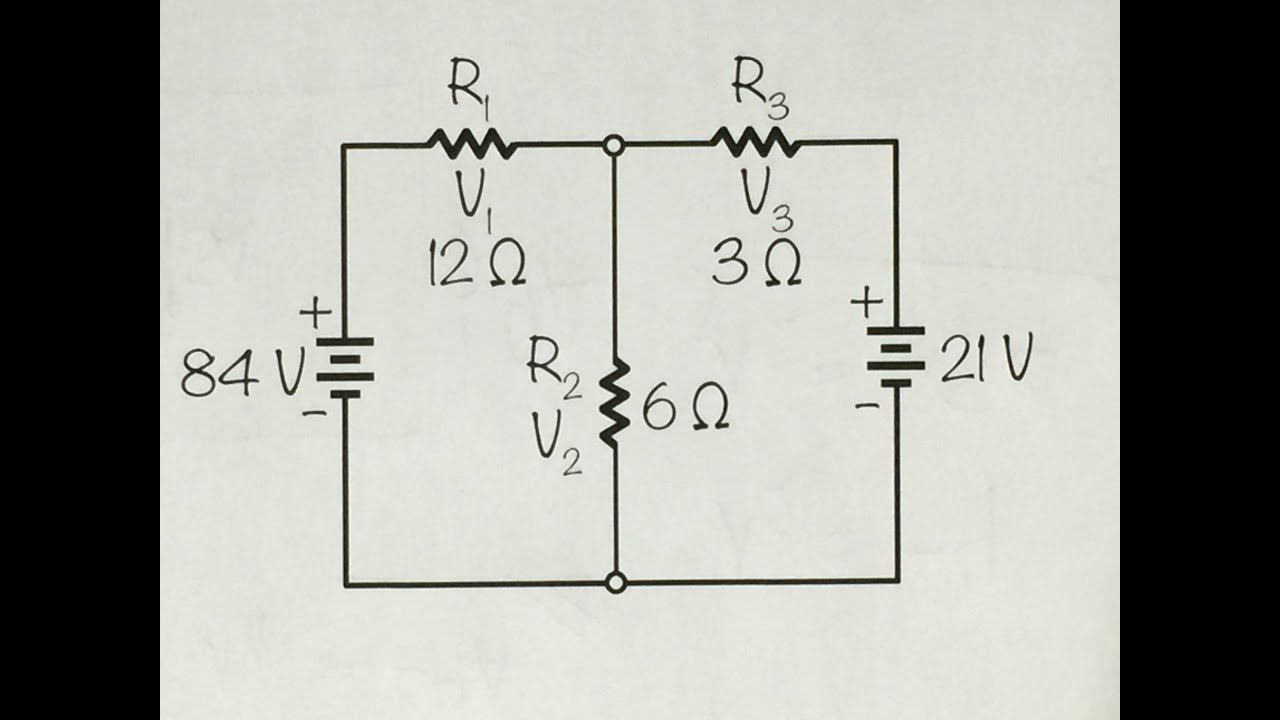
Mas a concentração em mol por litro multiplicada pelo volume em litro é igual ao número de mols que nós temos na nova solução que, por sua vez, é constante porque é igual ao que nós retiramos da solução mãe. Como o número de mols é constante e o volume é maior, na solução diluída a concentração é menor, e se nós relacionarmos a concentração da Solução 1 com o volume que tomamos da Solução 1 e a concentração da nova solução e o volume da nova solução, temos uma igualdade, que nos permitirá calcular qual é a concentração da solução diluída. Questão número 4: Uma solução aquosa de ácido sulfúrico H2SO4, para ser utilizado em baterias de chumbo de veículos automotivos, deve apresentar concentração igual a 4 mol por litro.
O volume total de uma solução adequada para se utilizar nessas baterias, que pode ser obtido a partir de 500 ml de solução de ácido sulfúrico, de concentração 18 mol por litro é igual a? Resposta: o volume inicial vezes a molaridade inicial é igual volume final vezes a molaridade final. Volume inicial (500ml) vezes 18 mol por litro é igual a o volume final, que não sabemos, vezes a molaridade final que é 4 mol/l Realizando a operação, temos o volume final 2,25 litros.