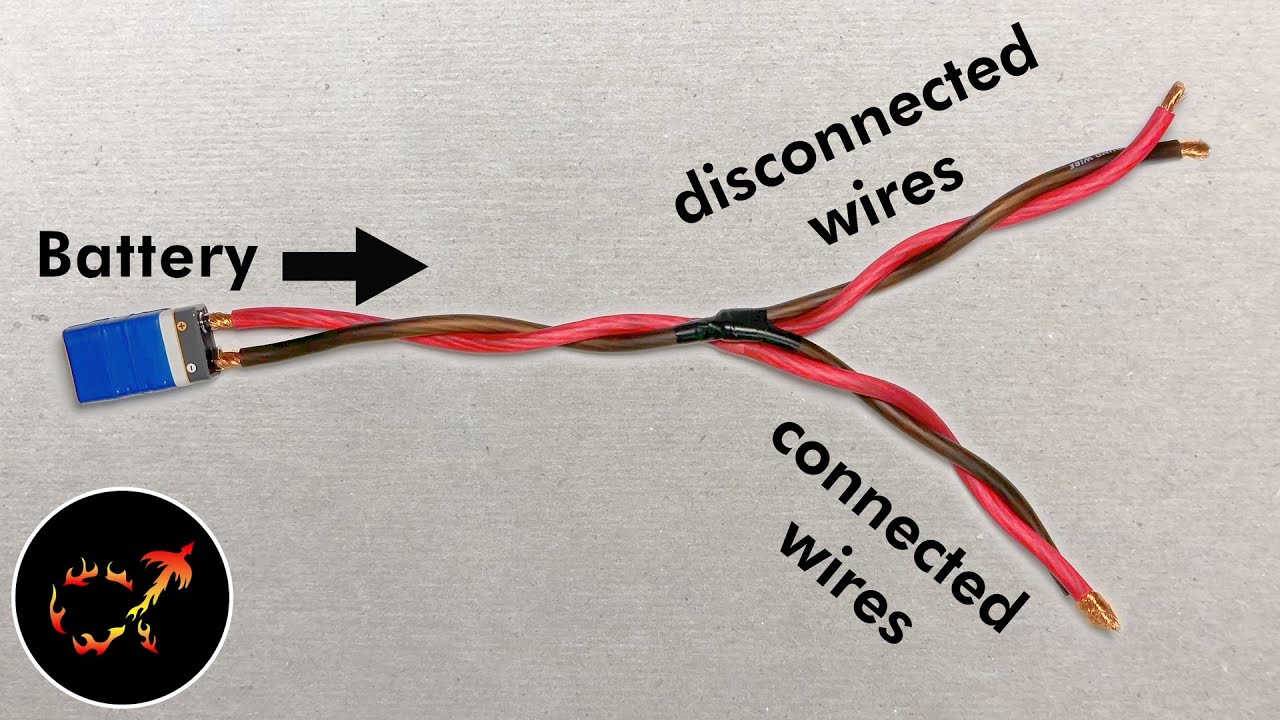
[Música] Hola Qué tal cómo les va bueno en este caso el objetivo acá cumplir es hablar un poquito sobre lo que son los procesos redox para entrar en el mundo de las oxidaciones biológicas y dar algunos aprovechar acá en esta misma este presentación dar algunos puntos centrales sobre metabolismo intermedio Sí así que nada vamos por ahí quiero que todo el mundo reconoce esto una pila posiblemente muchos no sepan pero básicamente en una pila lo que tenemos es especies químicas que se encuentran separadas en compartimento Y que cuando uno las conecta es decir cuando permite que
se establezca digamos lo que uno supone es un circuito que se da entre lo que llamamos el Polo positivo y el Polo negativo aparece un fenómeno que todo el mundo reconoce y es por el cual utiliza las pilas y es que las pilas me dan energía Así que si uno tuviera que pensar concretamente Cuál es el tema que vamos a charlar el tema que vamos a charlar se llama electroquímica la electroquímica es esta rama de la química que estudia la transformación entre la energía eléctrica y la energía química es con dos posibilidades poder generar energía
eléctrica a partir de energía química como se está planteando acá una pila e inclusive también a partir de la energía eléctrica poder generar cambios químicos vamos a definir lo que es un proceso entonces de óxido reducción que es el eje y centro de nuestro de nuestra charla nosotros hablamos de procesos redox o dióxido reducción cuando encontramos transferencia de electrones entre una especie que se define como dador y una especie que se define como aceptor es decir ponemos en el esquema a c de un electrón AB de tal manera que a se queda sin un electrón
y ve lo ha ganado esta especie que pierde el electrón es el que nosotros reconocemos como reductor esta especie que lo gana es el que conocemos como oxidante si lo ponemos en un ejemplo general en este caso fíjense esta reacción que ocurre entre el hierro y el cobre entre distintos estados fíjense como el hierro es más cede el electrón al cobre dos más de tal manera que el hierro es más pasa a estar como hierro tres más porque ha perdido un electrón con carga negativa y el cobre dos más pasa a estar como cobre más
porque ha ganado una carga negativa Sí eso lo vemos bien representado en estas dos en ecuaciones que responden a la ecuación original como el hierro sede un electrón electrón que es tomado por el cobre Sí para en tal caso reducirse Entonces nosotros acá lo que podemos observar es que cuando uno Define oxidación reducción lo que estás viendo está viendo Perdón es el movimiento de estos electrones a través de dos especies químicas yo puedo decir que una especie se oxida cuando está perdiendo o está cediendo electrones y en contraposición una especie se reduce cuando lo está
ganando es decir el hierro acá se oxidó el cobre acá se redujo sí de ahí viene químicamente la idea de el hierro el estado este ferroso se oxida férrico en el cupro el cúprico pasa a cuproso también puede decir que una especie se oxida cuando aumenta si ustedes se fijan la valencia del elemento en cuestión fíjense como acá el hierro dos más pasa hierro tres Y eso Define que sea oxidado de la misma manera por contraposición cuando se baja la valencia del elemento uno dice que la especie se está reduciendo como ocurre acá no el
cobre dos más pasa a cobre más siempre para casos procesos de robots necesito de ambos sistemas no existe la posibilidad de considerar un sistema redox sin uno de estos dos componentes tenemos otras formas de ver si algo se está oxidando o reduciendo a veces no siempre están los electrones tan evidentes la otra forma que tenemos es por ejemplo considerando la cantidad de oxígenos que pueda haber en una molécula Sí entonces fíjense acá si nosotros comparamos entre esta especie y esta especie que este es el esta especie de acá es el ácido acético y este es
el etanaldehído contando la cantidad de oxígenos yo puedo establecer cuál de estas está más oxidados Cuanto más oxígenos Tenga una molécula más oxidada está sí Entonces nosotros nos íbamos bastante sencillo fíjense como acá tenemos dos oxígenos acá Tenemos uno por lo tanto nosotros estamos diciendo que en este sentido lo que hubo fue una oxidación por contraposición oxidarse también significa perder hidrógenos sí Entonces yo cuento si la cantidad de oxígenos es exactamente la misma lo que puedo hacer es visualizar la cantidad de hidrógeno sí fíjense que en este lado Sí en el etanol Yo acá tengo
tres seis hidrógenos y en el etanaldehído Tengo cuatro hidrógenos por lo tanto perder hidrógenos significa también oxidarse así como nosotros podemos a través de la cantidad de oxígenos y de hidrógenos definir lo que es una oxidación podemos hacer exactamente lo mismo en cuanto a una reducción decimos que entonces que algo se reduce cuando pierde oxígenos al noce cuando aumenta la cantidad de hidrógenos entonces en resumen nosotros podríamos observar un proceso redes por comparación entre dos especies definiendo si se oxida o se reduce en función de ceder electrones aumentar la valencia aumentar la cantidad de oxígeno
disminuir la cantidad de hidrógenos para todos los procesos que signifiquen oxidación y reducción entonces podrá ser ganar electrones disminuir la valencia perder oxígenos o aumentar la cantidad de hidrógenos ahora cómo veo yo a estos electrones en estos procesos de transferencia muchos casos en electricidad está como bastante explícito como habíamos recién en las reacciones que involucran el hierro si una de las cosas por las cuales elegimos el hierro es porque el hierro es un elemento muy central en los procesos redos en nuestro organismo Entonces como lo vamos a ver muchas veces está bueno ya comenzar a
observar sus este su participación el tema es que a veces los electrones no vienen como electrones tan explícitos sino que vienen como electrones mimetizados o a través de otros sistemas qué es lo que eligió la naturaleza como sistemas de transportadores electrónicos al hidrógeno porque el hidrógeno cuando yo analizo el elemento hidrógeno el hidrógeno es y el elemento más sencillo del Universo tiene un núcleo con un protón y tiene un único electrón en su orbital más cercano de tal manera que si yo a ese hidrógeno le saco el electrón me quedo solamente con el protón con
una carga positiva y si yo hace hidrógeno le agrego un electrón me voy a quedar con un hidrógeno que tiene dos electrones con una carga negativa es decir que si yo te doy un hidrógeno con ese hidrógeno te estoy dando un electrón el tema es que el hidrógeno en la naturaleza lo tenemos como una molécula diatómica como h2 de tal manera que en realidad el hidrógeno lo que puede hacer es transferir electrones de dos formas diferentes puede ser que uno de los átomos de hidrógenos se quiere con los dos electrones dejando el Entonces el protón
y el hidruro como molécula o como elemento de transferencia de electrones y en este caso lo que va a transferir son dos electrones al mismo tiempo o puede ser que cada uno de los hidrógenos del hidrógeno molecular se quede con un electrón de tal manera que cada uno va a aportar ese electrón a la especie que corresponda entonces lo que les presento Yo acá a la izquierda son las especies transportadoras de electrones universales que aparecen a nivel celular y fíjense que son moléculas conocidas estamos hablando de la nicotinamina del indionucleótido la nicotinamina del nucleótidos fosfato
el flavin mononucleótido el flavin adherido nucleótido a lo que nosotros hemos visto cuando analizamos en encima el concepto de cofactor y observamos que un grupo importante de estos cofactores eran estas moléculas derivadas de vitaminas que participan en procesos es decir que estas funcionan como coenzimas o como grupos prostáticos de las enzimas que después por ahí comentamos algunas cosas Entonces en este análisis fíjense como el mar pasa nada pH más protón el Flamingo nucleótido pasa por un estado intermedio hasta alcanzar los dos hidrógenos lo mismo que el flavin adenine nucleótido todos los que nos podríamos preguntar
es por un lado Quién es la especie oxidada Quién es la especie reducida y Cuántos electrones son los que están puestos en juego digamos en cada una de estas reacciones siendo los electrones fíjense que en la reacción del nada a nadache son dos los electrones que están puestos en juego dado que hay dos hidrógenos y aparecen a mi derecha en la reacción claro de qué manera claramente a través del individuo por eso aparece el protón es decir que cuando la dupla no nada nada H participa de procesos de transferencia de electrones tiene la capacidad de
transferir de 2 al mismo tiempo ya sea tomándolos o ya sea cediéndonos de acuerdo a la dirección que tomemos Lo mismo sucede para el mal p el norte toma electrones a través del hidrógeno para generar más pH más protón o el pH cero dos electrones al mismo tiempo y quedará como nate es interesante diferenciar esta capacidad que tienen estos derivados la nicotini media en la transferencia de electrones con los derivados de flabina piense que en el caso del nucleótido al igual que en el flabina de nucleótido y la capacidad de tomar un electrón para formar
una especie que tiene un electrón desaparada desapareado perdón y luego tomar el segundo electrón para completar sí la forma flavismo mononucleótido h2 lo mismo en el caso contrario es decir que tanto para el clarismo monocleiótico como el flabina del indenucleótido los hidrógenos acá están funcionando como transportadores en este sentido es decir cada hidrógeno está aportando su propio electrón quiero remarcar si bien no lo vamos a analizar ahora la presencia de estas moléculas que tienen fíjense yo no le puse una carga negativa sino que lo que le puse es un puntito este punto indica que esta
especie es una especie que tiene un electrón en estado desapareado se hizo después más adelante vamos a considerar al respecto finalmente definimos De qué manera se van a transferir electrones a través de estos transportadores universales los que nos quedan por definir es Cuál es el estado reducido y Cuál es el estado oxidado de cada una de estas cofactores dijimos lo podemos hacer A través de la valencia acá se nos complica analizar la valencia Pues estamos hablando no de un elemento sino de una molécula compleja lo podemos hacer A través de oxígenos sí lo podemos hacer
pero el tema que tendríamos que abrir el juego a la fórmula digamos este fórmula molecular del lado del flavono nucleótido y la verdad que eso no vale la pena hacerlo si lo podemos hacer A través de saber si se excede o no sucede electrones y nos quedaría como alternativa a los hidrógenos creo que estrógenos en la forma más fácil de ver porque fíjense que hacia la derecha lo que observamos en cada una de las reacciones es ganancia de los hidrógenos ganancia de esos hidrógenos significa ganar electrones eso digamos de acuerdo a Los criterios que estuvimos
comentando nos permite definir que el nad el Nat t el esclavismo mononucleótido y el fad es decir lo que tenemos a la izquierda nuestras reacciones son las formas oxidadas y lo que tenemos a la derecha son las formas reducidas En conclusión nosotros decimos que al lunar oxidado se reduce al nevache más protón cuando acepta dos electrones o que el garaje se oxida a nada cuando cede dos electrones sufrimos la capacidad de poder medir si una especie química es fundador o una sector de electrones y con Qué característica lo hará frente a otros potenciales dadores y
actores eso se define como potencial redox y se lo identifica con la letra e lo hacemos a través de básicamente un aparato que tiene un electrodo de referencia el escritorio de referencias generales electrodo de hidrógeno que establece un valor de potencial cero contra el cual comparamos con un electrodo indicador la sustancia que nosotros queremos medir Y de esa manera podemos obtener valores de potencial redox cuya unidad de mediciones voltios así como habíamos comentado cuando hablamos de energía libre de gifs y de entalpía El concepto de estándar a capas Exactamente lo mismo no digamos cuando aparece
el super índice serito lo que estamos haciendo referencia es a un potencial reloj estándar definido por concentraciones establecidas las temperaturas phs etcétera entonces nosotros podemos encontrar básicamente dos grandes grupos que son aquellos especies que se comportan como aceptores versus aquellas especies que se transforman se comportan como dadores Cuanto más positivo es el valor de un potencial redox más acepto esas especies Cuanto más negativo es el potencial redox de un este de una especie más dadores es decir con los valores más negativos tenemos a los dadores de electrones con los valores dispositivos tenemos a los aceptores
de electrones entonces fíjense acá tenemos a la derecha una tabla que nos muestra algunos pares este químicos con sus correspondientes valores de potencial redox para poder analizar un poco estos fenómenos en realidad salvo en los extremos sí como observamos en la tabla en este caso el hidrógeno el oxígeno en el medio Tenemos un montón de posibilidades que nos permite definir entonces que alguien se comporta como un nador o como un aceptor dependiendo Contra quién lo esté comparando vamos a un ejemplo fumarato suxinato que tiene un valor positivo de más 0,03 voltios si yo lo comparo
con la dupla anterior O sea la acetatomalato que tiene un valor menos 0,17 y yo sé que los electrones van desde los dadores con valores negativos a sectores con valores positivos claramente los electrones en esta dupla Irán del oxalacitrato al fumarato ahora si yo tuvo el fumarato a esta dupla fumarato suxinato y digamos quiero analizar su comportamiento como dador o aceptor de electrones frente a esta dupla de citocromo B hay diferencias tiene un valor más positivo que el fumarato razón por la cual en este caso el fumarato ya no es un aceptor como en el
ejemplo anterior sino que ahora el fumarato se transforma en dador es decir que cuando nosotros nos movemos sí por afuera de los extremos los valores y aceptores de electrones van a de Contra quién estemos comparándolo ahora en esta tabla por un aparecen algunas cosas que son interesantes por un lado aparece la dupla nada llenar con un valor bastante negativo es decir que esta dupla uno tiende a pensar que es un fuerte dador de electrones Y en el otro extremo encontramos al oxígeno es difícil es difícil que podamos encontrar a nivel biológico una especie química que
tenga un potencial redox mayor al oxígeno esto quiere decir que el oxígeno se comporta al estar en este punto de la tabla como un acepto muy puro de electrones es decir que no importa Contra quién yo le estoy comparando el oxígeno siempre actúa como un actor de electrones es interesante comenzar a plantear este tipo de situaciones porque uno reconoce al oxígeno Quizá en otras dimensiones [Música] podemos estar sin comer durante meses podemos estar sin tomar agua durante días no podemos vivir más allá de cinco minutos sin oxígeno esa relación es algo en cualquiera la reconoce
Sí si uno deja de respirar y cuando deja de respirar y se deja de respirar oxígeno uno se mueve entonces simplemente el oxígeno debe tener un papel muy central en la condición de sobrevida de una célula y lo que estamos planteando acá es una participación del oxígeno en un proceso de transferencia de electrones y en donde él siempre se comporta como un aceptor de electrones Se los voy dejando como inquietud bien entonces creo que queda bastante explícito y sobre todo teniendo esta tabla acá adelante como el comportamiento de dadores receptores siempre están en relación contra
quien lo esté comparando analicemos un poco esta ecuación que tenemos acá la ecuación dice Delta G la variación de energía libre es igual a menos n es la cantidad de electrones estoy considerando en mi sistema por una constante que es la constante de faraday o sea es un valor definido por la variación de El potencial redox entre especies químicas es difícil que en esta ecuación tenemos dos términos que son reconocidos ya porque lo hemos visto porque Lo acabamos de comentar por un lado variación de energía libre que definimos como energía Útil para hacer trabajo y
la variación del potencial redox como la tendencia es Severo o aceptar electrones O mejor dicho digamos qué es lo que sucede cuando hay transferencia de electrones entre especies químicas todo lo que Les propongo es que analicemos esta relación que se establece entre fenómenos termodinámicos y procesos para eso vamos a tomar Esta dupla sí la dupla que habíamos visto en la diapa anterior de nuestra tabla en donde teníamos por un lado estos estas unidades de transferencia de electrones que nosotros las reconocemos como cofactores enzimáticos y por otro lado el oxígeno ya que de alguna manera tenemos
que empezar a desvelar el misterio de Por qué el oxígeno Parece ser tan bueno parece no es esencial no para la sobrevida de una célula Sí entonces básicamente lo que tenemos es el oxígeno que digamos el oxígeno se reduce agua y el nadache más protón se oxida a este anal lo que podemos preguntarnos es si esto que estoy planteando verdaderamente ocurre en el sentido planteado para eso Tendremos que saber cuál es el signo del valor de Delta G Si sabemos que son dos electrones los que están puestos en juego en este proceso robots dado que
hace un ratito analizamos sí la cantidad de electrones que había en la transferencia entre el Nat y el nadache entonces básicamente lo que hacemos Es reemplazamos los este los datos que tenemos en esta ecuación es decir en el valor 2 La constante de faraday tiene su valor que de acuerdo a las unidades yo elegí para que digamos las unidades sean en kilocalorías voltiomol sí hay otras unidades entonces pueden este aparecer otros números el valor de la constante de faraday es 23,061 kilocaloría Voltio mol y el potencial redox de la dupla oxígeno en agua más este
082 voltios lo tomé de la tabla anterior y el potencial redox de la dupla nada accionar también lo tomé la tabla anterior y tenía un valor de menos 0,32 se reemplazo estos datos en esta fórmula es decir -2 por 23,061 por la este resta entre el potencial del oxígeno y el potencial del este y obtengo un valor de Delta G igual a menos 52,6 kilocaloría mol Qué significa esto por un lado significa que el proceso es espontáneo tal cual como yo lo escribí Recuerden que definimos que un valor de Delta gm menor a 0 Define
a ese proceso como un proceso espontáneo es decir que va a ocurrir tal como está descrito por lo tanto es verdad que espontáneamente el oxígeno Sí el oxígeno toma los dos electrones provenientes del naranjo para reducirse agua y en la noche en consecuencia se oxidana y además este número me está diciendo que en este proceso de transferencia hay 52,6 kilocalorías disponibles porque Recuerden que El delta G establece la diferencia entre el estado final y el estado inicial Y como dice la primer ley de la termodinámica la energía No se crea ni se destruye sino que
se transforma la pregunta es estas 52,6 kilocalorías qué energía es bueno en principio quizás parte de la respuesta vuelve a ser nuestra pila original no cuando se Disculpen cuando se produce un proceso redondo es decir cuando en esta pila hay transferencia de electrones entre las especies químicas que están dentro de esa pila y se conectan a través de digamos la posibilidad de establecer la conexión valga la redundancia entre el Polo positivo el Polo negativo lo que nosotros estamos viendo Es la energía generada por la transferencia de electrones para eso nosotros utilizamos las pilas para poder
transformar esta energía química de transferencia de electrones en esta energía eléctrica que es lo que nos permite hacer funcionar el control del aire acondicionado La pregunta es a nivel biológico dado que a nivel biológico esta dupla existe consumimos oxígeno y nosotros ya sabemos que estas son cofactores enzimáticos O sea que son moléculas que están implicadas en los procesos metabólicos La pregunta es esta energía donde aparece una primera aproximación podría ser calor La pregunta es si considerando que El delta G es energía Útil para hacer trabajo y que sabemos que volvemos comentado que el calor es
muy importante pero desde el punto de vista de trabajo nosotros no nos sirve si la naturaleza ha ideado una estrategia similar a la que nosotros podemos observar en una pila para poder recuperar por lo menos digo parte de esta energía en los procesos de transferencias de electrones como una energía Útil para poder hacer funcionar a esa célula La pregunta sería nuestra forma de generar energía este tipo electroquímica bueno cosas para ir pensando [Música] vamos a hacer una mención para tenerlo para poder ya ir viendo cómo es que estos procesos de transferencia de electrones se van
a relacionar con algunos procesos metabólicos entonces un poco de Quiénes son las enzimas que están asociadas a estos procesos en la clasificación de enzimas esto forma parte del primer grupo sí por lo menos tenemos enzimas que digamos que participan de procesos de oxidación en estas enzimas que participan en el proceso de oxidación son las oxidasas la sociedad utilizan oxígeno como oxidante sí de tal manera que el oxígeno se reduce y la molécula en cuestión se va a oxidar el producto de la oxidación perdón el producto de la acción de estas oxidasas pueden ser agua o
puede ser peróxido de hidrógeno Sí y existe si ustedes quieren dentro de esta familia de oxidasas dos familias particulares que vale la pena Digamos como digamos tomarlas como su ítem para siempre tenerlas en consideración que son las peroxidasas y la catalasa Por qué Porque ambas participan de procesos de oxidación nada más que en el caso de las peróxidasas utilizan peróxido de hidrógeno como agente oxidante en vez del oxígeno utilizan peróxido de hidrógeno la catalasa es la enzima encargada de desdoblar esta agua oxigenada en agua más oxígeno acá tenemos una Acá hay un error en este
en esta ecuación si no es que se forma de nuevo agua oxigenada sino que acá es agua más oxígeno ahí tenemos la familia de las oxidasas Y esto es interesante Porque seguramente ustedes reconocen que en los peroxisomas celulares hay una alta actividad de periostias hay catalasa seguramente porque en esos orgánulos celulares hay muchos procesos de oxidación Entonces al haber mucho proceso de oxidación hay muchas generación de peróxido de hidrógeno y como veremos bastante más adelante ya hacia el final de digamos de todo este bloque de La Era uno vamos a analizar un poco el papel
del etéreo que puede llegar a tener estas especies derivadas del oxígeno otra familia de enzimas son las deshidrogenasas tienen como características sustancial que funcionan utilizando como cofactores nuestras transportadores universales de electrones el mononucleótido del flabina nucleótido sin que sean excluyentes es decir que Existen algunas deshidrogenasas que pueden utilizar al mismo tiempo varios de estos cofactores nada Como comentamos hace un rato digamos estos cofactores básicamente los que hacen es tener la capacidad de poder participar de los procesos de transferencia de electrones en forma directa porque son ellas mismas los que tienen la capacidad de poder tomar
el electrón o cederlo y como habíamos comentado antes dependiendo de cuál sea la especie podrá hacerlo de a uno O podrá hacerlo día 2 como es en el caso del nado en la sí acá lo que tenemos en esta imagen es el anillo flabina del flavismo mononucleoto y el flabina del indonucleótido en donde como habíamos comentado se encuentra el lugar por donde se puede tomar de a un electrón o ceder de algún Electro otra de las familias que participan en los procesos son las oxigenasas oxígenas es decir enzimas que participan de la oxigenación es decir
meter oxígeno en una molécula hay vamos a distinguir entre aquellas que llamamos mono oxigenasas que son las que catalizan los procesos de inclusión de un oxígeno en la molécula generando oxidrilos Sí hidroxilando al sustrato y las bioxigenasas que participan en procesos que digamos catalizando reacciones en donde lo que se incluye una molécula es el oxígeno diatómico sí van [Música] hacer algunas referencias importantes de estas mono oxigenasas cuando analicen en el último seminario los procesos de biotransformación Sí ahí van a encontrar una familia muy pero muy importante de enzimas mono oxigenasas conocidas como citocromos p-450 Sí
así que se los dejo para que cuando llegue el momento lo puedan analizar finalmente [Música] en contraposición tenemos los procesos de síntesis Sí el anabolismo los procesos anabólicos que parten de precursores moleculares sencillos para alcanzar complejidad molecular en la formación de macromoléculas acá vale la pena distinguir que no estamos hablando de los mismos productos simples que obtuvimos a través del catabolismo pero en realidad nosotros humanos somos organismos no autótrofos es decir nosotros no podemos construir nuestro propio alimento sino que tenemos que construir a partir de algo ya preformado es decir nosotros no podemos utilizar el
dióxido el agua y el amoniaco para formar nuestras aminoácidos nuestros monosacáridos o nuestras bases nitrogenadas cosa que hacen los organismos autótrofos lo que sí podemos es utilizar como precursores moléculas como monosacáridos ácidos grasos aminoácidos base nitrogenadas para conformar macromoléculas y podemos podemos tenemos la capacidad y utilizar moléculas sencillas como el acetato una molécula de carbonos para formar en algunos casos ácidos grasos aminoácidos sí tenemos algunas limitaciones pero en principio podríamos hacerlo cuando uno analiza la fase catabólica y la fase anabólica puede encontrar ciertas características distintivas por un lado evaluando la variación de energía libre que
ocurra que ocurre Perdón entre las moléculas complejas y sus productos finales claramente observamos que en el estadio final El delta G es menor que el estadio inicial razón por la cual los procesos catabólicos evolucionan a través de eventos exergónicos es decir que El delta G total Recuerden que los Delta g son aditivos Entonces yo analizo la sumatoria de los Delta G que puedan estar participando de cada uno de los eventos sí que me conectan las moléculas complejas con los productos finales el voltaje es menor a cero es decir este Delta G negativa me está diciendo
que el proceso metabólico es espontáneo en este sentido y con una variación de energía libre en donde hay energía disponible en el sistema por otro lado si yo tomo una molécula como la glucosa y analizo se encargó unos 6 hidrógeno 12 oxígeno 6 y lo comparo con seis moléculas de dióxido que voy a obtener lo que estoy observando es que digamos en los procesos catabólicos las moléculas sean oxidado es decir que catabolismo significa oxidación de esas moléculas en contraposición cuando ya analizo las vías anabólicas lo que observo es un proceso claramente endergónico no como hemos
charlado en en termodinámica construir es un proceso en principio no espontáneo que va a tener un Delta G positivo porque la energía final en el macromolécula es mayor a la energía inicial y que lo que voy a ver es que en general voy observando a través de estos procesos anabólicos procesos de reducción sí que van ocurriendo sobre estas moléculas eso pregunta por una de las fases catabólica pero el otro lado la fase anabólica Cómo pueden existir ambos procesos al mismo tiempo con características tan distintivas creo que parte de la respuesta se establece en función de
el ciclo energético que podemos encontrar que con esta la fase catabólica con la fase anabólica nosotros dijimos que el catabolismo es exergónico la energía recuperable a partir de los procesos catabólicos es la energía que puede conducir la fase anabólica del este del metabolismo sí la representación ATP como como moneda celular es una buena representación de cómo a través de la degradación de biomoléculas nosotros podemos recuperar energía bajo la forma ATP y el hidrólisis de ATP es la fuerza energética que conduce estos procesos anabólicos que son en sí mismo endergónicos sí algo que en termodinámica habíamos
definido aquellas procesos endergónicos ocurren en la dirección que a la célula le conviene acoplándose a reacciones de tipo exergónica y por el otro lado encontramos que entre esta fase catabólica y esta fase anabólica hay un evento redox y ese evento redox se establece en función de que el catabolismo genera coenzima digamos genera equivalentes de reducción bajo la forma de coenzimas que van a ser utilizadas por la fase anabólica también para conducir la fase redox correspondiente nuevamente nos queda acá una inquietud para develar y es lo que habíamos comentado hace un par de días Pues atrás
la relación entre procesos redox [Música] y procesos energéticos existe además de esta conexión entre el catabolismo y anabolismo en el ciclo energético el ciclo redox una relación directa entre el ciclo redes y la energía cosas que tenemos para develar en los próximos temas que vamos a abordar mapa metabólico algunos dice ya me lo voy a comprar y la verdad que no tiene ningún sentido no porque uno observa esto y en realidad lo que quiere es pegarse un corchazo no nada yo remarque algunas cosas en este temible mapa metabólico fíjense que por acá puse carbohidratos siento
este paquete de acá habla de carbohidratos por acá tengo todo un paquete de lípidos por acá tengo todo un paquete de proteínas de proteínas con aminoácidos por acá tengo todo un paquete de ácidos nucleicos y algo que es interesante que en este mapa metabólico Sí donde tengo las biomoléculas puestas sobre los sobre el entorno sobre la periferia encuentro por un lado representado una muy sencilla hace cinco a en realidad vinagre ácido acético nada más que un poquito activado si ustedes quieren y una vía metabólica muy este explícita cíclica que está en el centro de este
mapa metabólico sin que sea beneficiada Solamente porque créanme que esto está ocurriendo yo puedo conectar en el mundo de los carbohidratos la glucosa con esta molécula de acá pueden quitar los lípidos de ida y vuelta también con esta molécula de acá puede ver como esta molécula de acá se conecta con esta vía tan central del metabolismo intermedio veo como esta vía del metabolismo intermedio central también se conecta con aminoácidos Sí veo como nuestra vía se conecta con procesos en donde aparece el oxígeno a través de una transferencia de electrones que hay por acá entre coenzimas
citocromos y finalmente el oxígeno es decir que yo hacía grandes rasgos puede encontrar ciertas características de este mapa metabólico que puede definir a través de las vías catabólicas que nacen de moléculas muy diferentes entre sí son convergentes así intermediarios comunes del metabolismo intermedio y son algunos de esos intermediarios comunes del metabolismo intermedio los que a su vez pueden ser utilizados para la síntesis para los procesos anabólicos en este caso de una manera Divergente existen ciclos metabólicos que tienen una característica de poder comportarse tanto como vías catabólicas y como vías anabólicas estos ciclos metabólicos ciclos o
no ciclos dependiendo como lo quieran pero en donde yo encuentro ambas fases del metabolismo es decir veo el catabolismo y el anabolismo es lo que yo reconozco como ciclos o vías anfibólicas Sí entonces la verdad que este concepto de catabolismo convergente y anabolismo Divergente es un concepto muy interesante para trasladar porque nos va a ser muy útil para poder entender cómo se integra el metabolismo de los glúcidos como se integran el metabolismo de los lípidos como se integra el metabolismo de las aminoácidos en los procesos energéticos celulares y en los procesos de síntesis propiamente dichos
los organismos vivos dijimos que desde el punto de vista termodinámico son abiertos es decir que tiene la capacidad de poder intercambiar materia y energía con su entorno y que es intercambio lo hacen manteniendo un estado estacionario no un equilibrio con su entorno de hecho el equilibrio de una célula con su entorno no es nada más que la referencia de la muerte de esa célula podemos decir que en una vía metabólica Sí una vía metabólica definida como un conjunto de reacciones que comienzan y terminan un mundo determinado y está constituidas por una serie de intermediarios que
definen a esa digamos Ese Conjunto de reacciones que el flujo de esos intermediarios a través de una vida metabólica en general es bastante constante es decir que la velocidad en su síntesis y degradación de cada uno es intermediarios se mantiene de manera constante podemos decir que La regulación de ese estado estacionario que mantiene la sobrevida de esa célula lo que nosotros podemos decir homeostasis tiene que estar capacitada para poder hacerle frente a los cambios en el flujo de una vía metabólica en respuestas a los cambios en la demanda de esa vida podemos diferenciar dos términos
que a veces se utilizan de manera indiscriminada Qué es regulación metabólica y control metabólico hablamos de regulación metabólica cuando definimos el proceso por el cual se mantiene el estado estacionario el flujo de metabolismo a través de una vía en contraposición a control metabólico que es la influencia que se ejerce sobre las enzimas de una vía en cuestión en respuesta a una señal externa para alterar ese flujo de esos metabolitos Cuáles son esos mecanismos que entonces controlan el flujo de una vía mecanismos alostéricos que nosotros conocemos por ejemplo por retroalimentación positiva retroalimentación negativa mecanismos por modificación
covalente como hemos visto los fenómenos de fosforilación y despoforilación mecanismos a través de control de lo que llamamos ciclo de sustrato es decir control de sustrato en donde cuando yo tengo una reacción reversible pero catalizada por dos enzimas diferentes Sí una enzima hacia adelante y una enzima en reversa la velocidad de cada una de estas reacciones y el control sobre cada una de estas reacciones va a permitir establecer el control sobre los sustratos de las reacciones precedentes y posteriores estas estos ciclos de sustratos son muy importantes para poder mantener una cierta cantidad de un sustrato
y poder hacerle frente a una demanda inmediata cuando esta vía metabólica se apuesta en acción cuando veamos la vía glucolítica vamos a hacer una buena referencia a estos ciclos de sustrato y finalmente el último mecanismo Bueno ese es el último agregamos nuestro último mecanismo de control de flujo es el que opera a nivel génico es decir aquel que Define el control sobre la cantidad de las enzimas que están puestas en el juego que son las que controlan los los flujos metabólicos entonces pero Gustavo a ver Esto es lo que habíamos analizado salvo lo del ciclo
de sustrato había analizado como mecanismos que regulan la actividad enzimática Exacto porque cuando nosotros estamos hablando de mecanismos de control de flujo no de regulación sino de control de flujo dijimos que estamos haciendo referencia a cómo controlamos a las enzimas que catalizan los comprometidos centrales en estas vías metabólicas en resumen así como planteamos parabio energética nuestros objetivos sobre estas aproximaciones a los fenómenos dióxido reducción y de metabolismo intermedio en cuanto a su reducción poder definir lo que es una reacción redox distinguir entre lo que es oxidación y reducción en función de Digamos como pueda visualizar
este fenómeno de oxidación o reducción sí cantidad de electrones quien cede quién toma electrones oxígenos hidrógenos reconocer las distintas formas de transferencia de electrones entre especies químicas sin remarcar esto de los transportadores universales como son las este estos cofactores enzimáticos la presencia del hierro como una una especie que participa en los procesos de transferencia de electrones interpretar el valor del potencial redox y cómo lo relacionamos con los procesos de transferencia de electrones es decir potenciales positivos versus potenciales negativos interpretar esta relación que vimos entre variación de energía libre energía Útil para hacer trabajo y potencial
redes a nivel biológico y reconocer Cuáles son las distintas familias con las que nos vamos a encontrar que catalizan estas reacciones de óxido reducción en cuanto al metabolismo intermedio sencillo comenzar a distinguir las características de lo que significa el anabolismo y el catabolismo en función de los objetivos de cada una de estas fases y su relación con la variación de energía libre de los procesos redox es decir poder integrar el ciclo energético y ciclo redox a la fase catabólica y católica definir lo que es una vía católica convergente una anabólica Divergente una vía anfibólica para
tener claro Cuál va a ser el panorama central y el molde a través del cual funciona el metabolismo intermedio y reconocer en realidad volver a poner en acción a los mecanismos de regulación de las enzimas como parte de los mecanismos de control de flujo de una vía metabólica en fin fíjense que hemos analizado los procesos No desde el punto de vista matemático a través de ecuaciones sino que lo vamos a analizado sobre todo a través de extraer los conceptos que nos van a permitir comenzar a entender Cuáles son las estrategias de energéticas a nivel celular
Aunque parece en principio como sencillo Porque estamos solamente con conceptos van a ver qué importante cuando empecemos a trasladar estas cosas que estamos comentando a los temas que vienen sí así que bueno por ahora los dejo el próximo tema va a ser hablar un poquito sobre ese famoso acetilco a como punto central de ese metabolismo intermedio vamos a hacer una primera aproximación de como como sintetizamos ese acetil cual para poder meternos quizás en una de las vías más conocidas que tenemos que es el famoso ciclo de krebs Sí así que los dejo Cuídense Nos vemos
la próxima o nos escuchamos por ahí mejor dicho la próxima





![Upbeat Lofi - Deep Focus & Energy for Work [R&B, Neo Soul, Lofi Hiphop]](https://img.youtube.com/vi/THh4fT0O7IY/maxresdefault.jpg)
![Gravitation' by Richard Feynman [1080p HD Video with clear audio]](https://img.youtube.com/vi/q_edsSpDzHg/maxresdefault.jpg)