Hola cómo les va mi nombre es Gustavo bertot y en esta oportunidad vengo a presentarles los principales puntos a tener en consideración en relación a los contenidos que nos ocupan en esta unidad 2 sobre biocatálisis bien antes de comenzar a desarrollar los el contenidos De esta unidad me gustaría plantearles dos situaciones disparadoras a ver si podemos encontrar este respuestas a estas inquietudes En primer término si observamos la secuencia temporal en días de descomposición de esta hamburguesa Incluso como consecuencia de la presencia de microorganismos que claramente favorece en este proceso me pregunto esto significa que todavía
yo estoy descomponiendo la hamburguesa que me comía hace 15 días y este hecho se complica aún más y se hace más difícil de interpretar teniendo en cuenta que desde ese momento he seguido incorporando alimentos este a mi organismo con lo cual tengo como una idea de que estoy como estoqueando alimentos que se están descomponiendo en tiempos enormes por otro lado A partir de esta sencilla reacción una reacción que es bastante conocida la transformación de dióxido en bicarbonato es decir este lo que sucede cuando el dióxido de carbono como un gas se lo coloca en agua
y entonces se forma el bicarbonato una reacción que tiene una velocidad media de transformación de dióxido de bicarbonato de bicarbonato de dióxido que está en el orden de los minutos la pregunta en este caso es si el dióxido de carbono un producto este final del metabolismo de todas las células este que utilizan oxígeno para poder obtener energía que por el otro lado es una molécula que a partir de ciertas concentraciones Tiene efectos tóxicos muy severos si la velocidad media transformación está en el orden de los minutos la inquietud es tardamos minutos en transformar el dióxido
en bicarbonato como una forma de poder vehiculizarlo a través de la sangre y también tardamos minutos para poder volverlo a transformar a ese bicar bonato en dióxido para que como gas pueda difundir en los alveolos pulmonares y poder ser eliminado a través de la respiración son minutos y minutos hacia un lado hacia el otro y entonces La pregunta es cómo no estamos muertos no para tratar de encontrar alguna respuesta a estas inquietudes que Les acabo de plantear Les propongo que observemos un par de experimentos a partir de los cuales podamos entonces sacar algunas conclusiones en
este primer experimento vamos a ver nada tres eventos de reacciones químicas en principio muy clásicas en una digamos en una primera este reacción vamos a ver como el sodio reacciona con el agua luego vamos a ver cómo reacciona el cobre con el ácido nítrico y después en tercer término vamos a ver cómo el agua oxigenada reacciona con un óxido en este caso nos van a mostrar un óxido de manganeso sí veamos entonces este experimento en cuestión básicamente en la mayoría de las reacciones químicas cuando se pone contacto los reactivos los reactivos generan un producto y
una vez que los reactivos se consumen reacciones terminan sí esto lo estamos viendo con el sodio puesto en agua que genera hidróxido de sodio y con el cobre que nació nítrico forma el óxido cúprico [Música] cuando observamos sí la adición del óxido de manganeso en el peróxido de hidrógeno en el agua oxigenada vemos que también se produce una rápida reacción sin embargo sí sin embargo fíjense que no podemos observar que haya una disminución en la masa o en la cantidad de este óxido que hemos agregado al principio de hecho si nosotros pesamos ese óxido de
manganeso podemos corroborar que mantiene la misma masa que al comienzo de la reacción el agua oxigenada señala oxigenada es una molécula relativamente estable Sí con una este velocidad descomposición media este variable que puede estar en el orden de horas y lo que es interesante es que cada vez que nosotros volvemos a probar este óxido manganeso en agua oxigenada vemos como este se pone en evidencia esta reacción en donde se descompone generando agua y oxígeno como observamos recién acá vimos que se prendió una llama por la presencia de este oxígeno nuevamente volvemos a corroborar que sucede
con la masa de este óxido de manganeso y podemos volver a este definir que no ha cambiado su masa por lo tanto lo que es interesante que ha ocurrido en este tercer experimento respecto de los dos primeros es que tanto en presencia como en ausencia del óxido de manganeso la reacción que se verifica es la reacción de descomposición del agua oxigenada en agua más oxígeno sí sin haber observado ningún cambio ningún producto nuevo este y cambio como les decía en la masa de este óxido de manganeso en este segundo experimento volvemos a través a trabajar
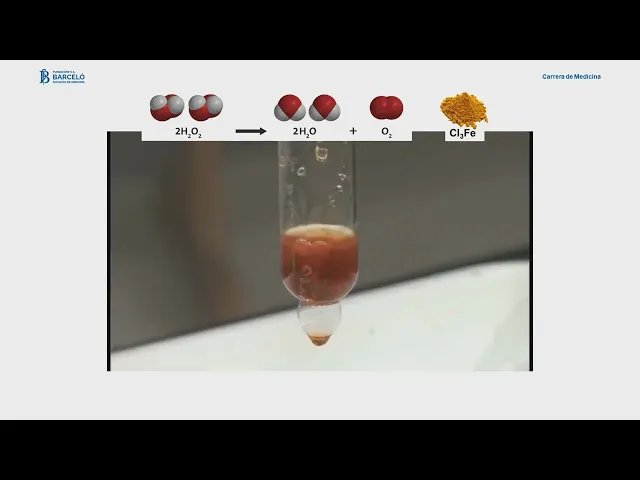
con la descomposición del agua oxigenada en agua más oxígeno nada más que en este caso en vez de utilizar un óxido lo que nos van a mostrar es qué es lo que sucede con la descomposición de la oxigenada en presencia de cloruro de hierro el químico tiene acá en este tubo de ensayo el agua oxigenada y lo que nos va a mostrar es con el agregado de una cantidad determinada de cloruro férrico que es lo que está sucediendo observemos ahí lo está agregando y fíjense lo que ha sucedido claramente hemos visto una reacción bastante violenta
Sí con vapor de agua e inclusive fíjense súper interesante que lo que nos está mostrando básicamente es el cloruro de hierro el cloruro férrico que se agregó al principio uno podía preguntarse qué fue lo que pasó con el peróxido de hidrógeno Qué pasó con el agua oxigenada que había en el tubo indudablemente la reacción fue lo suficientemente violenta lo suficientemente exotérmica ha liberado tanta energía tanto calor que ha digamos vaporizado el agua este y por eso digamos entre el oxígeno que es un gas liberado más el agua que se vaporizó por la energía liberada por
esta reacción ha quedado solamente como residuo el cloruro férrico el químico vuelve a colocar a oxigenada en el tubo ahora sobre el cloruro de hierro y veamos qué es lo que sucede nuevamente observamos la descomposición viene evidente bastante violenta en este caso también y por supuesto tomando consideración de que este experimento es semi cuantitativo fíjense que nuevamente podemos observar que el residuo seguramente hace referencia al cloruro férrico que hemos agregado entonces a partir de Las observaciones de ambos experimentos veamos si llegamos a conclusión similares en primer lugar el agregado del óxido de manganeso El agregado
del Cloruro férrico al agua esquinada solamente lo que hizo fue poner de manifiesto en forma evidente y rápida la reacción de descomposición del agua oxigenada podemos concluir que la presencia de el óxido y el cloruro férrico lo que hizo fue acelerar la reacción no crea la reacción la reacción de descomposición del peróxido de hidrógeno ocurría que en tal caso nosotros no pudiéramos ponerla en evidencia tiene que ver con el tiempo medio en la que el agua oxigenada se descompone otra conclusión fue interesante es que tanto para el óxido de manganeso como para el cloruro férrico
pudimos observar que no se perdió masa cuando digamos se puso en contacto con el peróxido de hidrógeno es decir no participó de la redacción ni como reactivo ni como producto en ambos casos se recuperó al final de la reacción tal cual como se había utilizado al comienzo de la misma por lo tanto claramente decimos no hubo un consumo de estas sustancias Y es más hemos visto cómo pudo ser reutilizado tanto en el caso del opcional maneso volviéndolo a poner en presencia del agua oxigenada como cuando el químico agregó nuevamente agua oxigenada al tubito que tenía
el residuo de cloruro férrico es decir que como sustancia en esta reacción no tuvo ningún tipo de participación de tipo estequiométrica es decir no hay una cantidad determinada ni de óxido de manganeso ni de cloruro férrico que fue necesario para que esta reacción se pusiera en evidencia otros digamos experimentos relacionados con la descomposición del agua oxigenada y en tal caso esta característica que comenzamos a observar de poder ver cómo el agua oxigenada acelera su descomposición en presencia de alguna sustancias en este caso lo que les muestro es el efecto de sales de hierro sobre una
sustancia llamada luminol en presencia de agua oxigenada veamos lo que sucede Entonces cuando se mezcla esta sustancia luminol con agua oxigenada y se agrega nuevamente una sal de hierro en este caso ferro cianuro de potasio cuando yo iluminó con un ultravioleta sí fíjense como veo los fotones liberados por la reacción Sí este de descomposición de este luminol esto seguramente ustedes lo han visto y es una de las herramientas y estrategias químicas para la búsqueda de manchas de sangre sobre todo desde el punto de vista forense sí la presencia de hierro como parte del grupo hemo
presente en la hemoglobina puede este de alguna manera acelerar sí como venimos diciendo la digamos este la transformación de este Lu en un producto que libere un fotón y que al ser eliminado por luz ultravioleta produce esta esta reacción tan característica Sí también es interesante un poco más divertido en este caso como nos está mostrando este digamos en este video acá lo que tenemos en ambos frascos es agua oxigenada con colorante para hacerlo más este más evidente y lo que van a hacer ahora es colocar detergente para qué detergente Para ver si estas burbujas que
nosotros veíamos en la descomposición del agua oxigenada las podemos atrapar de alguna manera y ponerlas más en evidencia en este caso lo que van a usar es una sal de yodo sí vimos un óxido vimos el cloro férrico vimos otras sal de hierro ahora lo que van a agregar es una sal de yodo sí veamos que nos sucede cuando se agrega una sal de yodo claramente pudimos poner de nuevo en evidencia la rapidez en la que se descompone el agua oxigenada generando agua y oxígeno sí las Burbujas de oxígeno se al ser atrapadas por este
por el el detergente genera esto este bastante divertido que se llama pasta de dientes de elefantes y finalmente finalmente me gustaría mostrarles que no todo parece ser este inorgánico no vimos óxido vimos sales de hierro vimos sales de yodo en este caso Les voy a mostrar una gota de sangre y qué es lo que sucede cuando sobre esta gota de sangre agregamos una gota de agua oxigena de nuevo observamos que la sangre acelera el proceso de descomposición del agua oxigenada hasta lo podemos observar a través de las burbujas que tenemos en el portaobjetos e inclusive
cualquiera que has utilizado oxigenada por ejemplo cuando tuvo algún sangrado de nariz ha sentido esas burbujitas que se forma cuando el agua oxigenada a digamos estado en contacto con con la sangre a principios de 1800 berselius uno de los químicos más renombrados de la historia de la química escribe se ha probado que algunas sustancias simples o compuestas solubles o insolubles tienen la propiedad de ejercer sobre otras sustancias un efecto muy diferente al de la afinidad química a través de este efecto ellas producen descomposición en los elementos de estas sustancias y diferentes recombinaciones de estos elementos
de los cuales ellas permanecen separadas esta nueva fuerza desconocida hasta hoy es común la naturaleza orgánica e inorgánica yo no creo que sea una fuerza completamente independiente de las afinidades electroquímicas por el contrario es una nueva manifestación de esa afinidad sin embargo como no podemos ver su conexión y mutua dependencia es más conveniente dar esta fuerza un nombre separado yo la llamaré fuerza catalítica y llamaré a la descomposición de sustancias por estas fuerzas catálisis de manera similar que a la descomposición de sustancias por la afinidad se la llama análisis Ahora sí oficialmente podemos entrar en
el mundo de los catalizadores Cuáles son los objetivos que planteamos para esta unidad podemos dividirlos en tres grandes objetivos sí los aspectos básicos de la catálisis y de los catalizadores analizando sobre todo a las enzimas como los catalizadores biológicos en este primer punto vamos a tratar de analizar un poco las características generales del proceso catalítico vamos a tratar de entender a las enzimas y las ribosimas como catalizadores biológicos Y dónde están sus características diferenciales de otro tipo de catalizadores vamos a hablar de algunas consideraciones estructurales respecto del proceso catalítico hablaremos particularmente del centro sitio activo
vamos a hablar de la participación de los cofactores en los procesos catalíticos y vamos a hablar de factores que modifican la actividad digamos este básicamente de estos procesos catalíticos en particular por otro lado vamos a tener también como como un segundo objetivo central este analizar un poco los fenómenos principales de la cinética enzimática y de los procesos de inhibición de la actividad enzimática Ahí vamos a trabajar sobre el modelo de micael y simenten vamos a tratar de poder interpretar como usar los parámetros cinéticos desde el punto de vista biológico vamos a definir un poco los
distintos tipos de inhibición que podemos encontrar y contrastar un poco las características de cada uno y en tercer término vamos a hablar y vamos a hacer un poco de análisis sobre los procesos de control y regulación de la actividad enzimática Sí ahí veremos los principales sistemas o mecanismos de regulación para tratar de ir construyendo un poco de este fundamento para todos los temas que vienen posteriormente retomando un poco lo que hablamos al principio volvamos a definir alguna de las propiedades principales que encontramos en el mundo de los catalizadores dijimos que los catalizadores aceleran reacciones no
crean reacciones es decir pueden actuar siempre sus reacciones que se definen como tales Sí permanecen inalterados al final de la reacción no se consumen durante la reacción no forman parte de la reacción y en consecuencia al no consumirse y permanecer inalterado pueden ser reutilizados tantas veces en principio como ese catalizador pueda permanecer en su estructura original hemos visto que al no formar parte de la reacción no actúa en relaciones tequiométricas es decir yo necesito tanta cantidad de catalizador para la reacción tal y una propiedad extra que digamos lo habíamos analizado pero que ahora la podemos
tener en consideración tiene que ver con digamos la constante de equilibrio para aquellas reacciones obviamente reacciones que están en equilibrio los catalizadores no crean reacciones solamente la acelera En consecuencia lo que harán es que las reacciones en equilibrio lleguen más rápido a esa situación de equilibrio por lo tanto los catalizadores no modifican la constante de equilibrio de una red ahora cómo hacen los catalizadores para hacer las reacciones a través de Qué mecanismo es que logran estos efectos si nosotros este analizamos Qué pasa cuando juntamos metano con oxígeno básicamente lo que veremos es una cierta estabilidad
sin una reactividad muy evidente para que realmente el metanio del oxígeno formen dióxido de agua lo que tenemos es que suministrar una cierta cantidad de energía para poder hacer que estas moléculas se vuelvan más reactivas y en consecuencia pasen a dar los productos determinados esta energía esta energía que necesitamos para que una reacción química ocurra es la que llamamos energía de activación en esta energía de activación sí se genera un estado si ustedes quieren intermedio entre reactivos y productos llamado estado de transición por lo tanto también podríamos definir a la energía de activación como la
energía necesaria para poder llevar a un reactivo al Estado de transición toda reacción química está obligada a adquirir una cierta cantidad de energía para poder alcanzar ese estado de transición y en consecuencia poder generar los productos determinados Qué pasa cuando nosotros analizamos sí esta misma reacción pero en presencia de un catalizador Sí por ejemplo una sustancia que permita que permita que ambos reactivos el metano y el oxígeno se unan se localicen se acerquen de tal manera de favorecer las interacciones entre ambas moléculas para que se genere el producto en presencia de un catalizador la energía
de activación ha disminuido y en consecuencia Al haber disminuido la cantidad de energía que yo necesito para llegar al Estado de transición la reacción es más rápida el producto final sigue siendo el mismo no cambia el fin de la reacción lo que cambió es lo que sucedió internamente para alcanzar ese producto los catalizadores disminuyen la energía de activación de la reacción Y de esa manera logran acelerar ya a mitad de 1800 se conocía la presencia de procesos catalíticos en el ámbito biológico de hecho virgen es el que propone por primera vez el término encima Para
estos procesos catalíticos asociados a fermentos Aunque pasó bastante tiempo hasta que se demostró la este naturaleza proteica de las enzimas en 1900 en la década de 1980 altman y sech son los que descubren que esta actividad catalítica también se encontraban en algunos ácidos nucleicos particularta particularmente ARN que fueron llamadas ribosimas en el contexto de las enzimas y las ribosimas como catalizadores biológicos lo que es el uso del término sustrato por reactivo como veremos en un ratito la interacción entre el sustrato y la enzima para formar un complejo encima sustrato en donde ocurre el proceso de
transformación la generación del producto la liberación de ese producto y la restitución de la enzima a su estado original como decíamos la naturaleza química de estos catalizadores biológicos es proteica en el caso de las enzimas y ARN en el caso de los ARN catalíticos o llamadas ribosimas lo que es sumamente interesante y a partir de la naturaleza de estas moléculas es que se abre una capacidad este muchísimo más este amplias en los procesos catalíticos respecto de los catalizadores inorgánicos dado que ambas estructuras pueden adquirir niveles de organizaciones estructural superiores estructuras secundarias estructuras terciarias inclusive estructuras
cuaternarias las interacciones ahora que se están dando entre el sustrato o los sustratos y la enzima este definen propiedades que son entre comillas muy especiales para este tipo de catalizadores una de las características estructurales más importantes que vamos a encontrar en las enzimas y en las ribosimas es la presencia de un sitio un centro un lugar en donde el sustrato interacciona con encima y en donde va a ocurrir el proceso catalítico eso es lo que conocemos como centroactivo Y en este centro activo formado por nada las interacciones de los aminoácidos de ciertos aminoácidos presentes en
la estructura proteica o de ciertos nucleótidos en el caso de los ARN conforma un lugar que permite acomodar permite unir al sustrato o a los sustratos de tal manera de poder orientar y favorecer los procesos químicos que van a ocurrir para la generación de los productos veamos como rápidamente esto se pone en evidencia cuando vemos en el centro activo como el sustrato experimenta los cambios químicos de alguna manera ayudado por las interacciones que se están dando por los aminoácidos del centro esta digamos interacción que se está dando entre sustratos y centroactivos permite entender el concepto
de especificidad tan característico de enzimas y de ribosimas y que es totalmente diferente a lo que uno podría observar lo que puede observar con los catalizadores de naturaleza inorgánica en donde digamos existe si ustedes quieren cierta especificidad dado que digamos una sustancia como actúa como catalizador podría llegar a catalizar más de una reacción pero en general digamos es muy muy diferente el concepto de especificidad en este caso sí acá es donde la naturaleza muestra toda toda su capacidad para poder lograr que estos procesos para hacerle las reacciones tomen una dimensión que en el plano biológico
son esenciales por otro lado dada la naturaleza de las enzimas y de las ribosimas es esperable que estén sujetas a alteraciones como consecuencia de las temperaturas estas estructuras normalmente que adquieren niveles de organización superior estructuras secundarias terciarias y cuaternarias sufren o experimentan mejor dicho los fenómenos de desnaturalización por lo tanto otra propiedad que es característica de las enzimas y ribosimas como catalizadores biológicos es la termolabilidad finalmente una tercer propiedad que también es característica de enzimas y ribosimas tiene que ver dada su naturaleza orgánica con la capacidad de poder Regular o controlar su actividad en el
caso digamos de las proteínas como cualquier otra proteína una enzima está sujeta a los mismos mecanismos de control que puede experimentar cualquier otro proteína y lo mismo sucede con los es interesante Sí tomar en consideración que además del centro activo en las enzimas podemos encontrar otros sitios otros sitios no catalíticos pero sí que pueden unir sustancias y al unir esas sustancias en tal caso modificar alterar la actividad enzimática a estos sitios si no catalíticos a donde se unen otro tipo de moléculas lo llamamos sitios alostéricos y veremos más adelante la importancia que en función de
Entonces cómo se establece las interacciones entre sustratos y el centro activo es que básicamente se definieron dos grandes hipótesis respecto de Cómo era el mecanismo y los modelos de interacción por un lado un típico modelo llave cerradura la enzima sería la cerradura perfecta para una llave llamada sustrato Este modelo si bien para algunas enzimas podía funcionar de manera adecuada mostró tener algunas incompatibilidades Sí el modelo más aceptado es el modelo en donde la enzima no tiene un centro activo tipo cerradura sino que la enzima tiene un centro activo que se adapta siempre y cuando el
sustrato sea el adecuado por eso el modelo llama modelo inducido o modelo de encaje Y entonces observemos como cuando ocurre cuando ocurre Mejor dicho las interacciones adecuadas entre el sustrato y el centro activo la enzima acomoda ese centro activo para poder permitir una Unión adecuada con ese sustrato y favorecer el proceso catalítico una manera de observar de una manera cotidiana Qué sería el modelo de encaje inducido es pensar en cuando uno se pone un guante por ejemplo un guante de látex sí como a medida que uno va este introduciendo la mano en el guante el
el guante se va adaptando nada a la forma de allá por mitad de casi a finales del 1800 sí Mitades pasadas Edward buschner este describe por primera vez que las actividades catalíticas de los fermentos asociados a la materia viva podían ocurrir independientemente de que existieran los organismos vivos básicamente lo que él demuestra es que puede hacer un extracto de este factores catalíticos derivados de levaduras sin tener las levaduras vivas sí a ese famoso extracto original él lo llama complejos y masa y es lo que posterior este digamos define un poco el concepto este de bushener
de las enzimas qué es lo que hizo jardín este como consecuencia de los trabajos sobre este complejo sin masa descubierto por puigner él demostró que para que este complejo libre de organismos pueda catalizar reacciones necesita de alguna sustancias sin las cuales no ocurría este proceso catalítico a esta sustancias que él demuestra que son termorresistentes que son dializables es decir que tienen tamaños muy pequeños él las denomina coenzimas nosotros reconocemos actualmente a toda esta familia de moléculas no proteicas de bajo peso molecular que son esenciales para la actividad de ciertas enzimas con el término cofactor de
tal manera el concepto es una enzima que requiere un cofactor para tener una parte proteica y los cofactores asociados de tal manera que cuando la coenzima se une a sus cofactores forma la enzima completa u olo encima para la mayoría de las enzimas que requieren con factor esos cofactores son esenciales para la actividad de enzima dentro de estos cofactores nosotros podemos reconocer como para poder organizar un poco la la información y el contenido podíamos distinguir a los factores según su naturaleza química es decir con factores de naturaleza orgánica o con factores de naturaleza inorgánica y
dentro dentro de los cofactores orgánicos vamos a hablar de grupos prostéticos o de coenzimas mientras que dentro de los cofactores inorgánicos podemos hablar de metal o enzimas o enzimas activadas por metales para nosotros sí creo que la organización de lo que es un cofactor más que por su naturaleza química nos conviene entenderlo Según como el cofactor se une a la enzima cuando los cofactores se unen covalentemente fuertemente a la enzima es decir permanecen continuamente Unidos a la enzima a esos cofactores los llamamos grupos prostéticos y son grupos prostéticos independientemente de si su naturaleza es orgánica
o su naturaleza es inorgánica por el otro lado si los cofactores tienen libertad y unión con la enzima es decir se unen a la enzima cuando la enzima cataliza reacciones y luego se separa a eso es lo que denominamos coenzimas Y nuevamente las coenzimas independientes de su naturaleza química las coenzimas también pueden ser de naturaleza orgánica o de naturaleza inorgánica una coenzima Entonces es un cofactor que se une a la enzima al momento en el que la enzima cataliza la transformación de un sustrato en un producto y en consecuencia la coenzima también se libera luego
del proceso catalítico un grupo prostético está permanentemente unido a la enzima y va a participar obviamente del proceso catalítico pero siempre siempre va a permanecer unida encima si durante el proceso catalítico tanto una coenzima como un grupo prostético son químicamente modificados deberán nuevamente volver a su estado original para que puedan seguir participando de los procesos catalíticos Esto es algo muy interesante no para ahora sino para más adelante la necesidad de entender este concepto si una enzima durante el proceso catalítico se modifica o su cofactor se modifica al final de la reacción deberán volver a su
estado original hay digamos que prácticamente todas las enzimas en sus centros catalíticos suelen tener algún metal sí asociado así que tenemos una enorme variedad de este metales que participan como cofactores en algunos casos participan como cofactores tipo grupo prostéticos en algunos casos participan como cofactores coenzimas es decir ingresan o salen sí sin magnesio manganeso molibdeno el hierro el cobre el calcio el selenio el níquel etcétera son cofactores de todo un conjunto de proteínas y por el otro lado los cofactores de naturales orgánica cuando uno analiza un poco Quiénes son Estos factores estos famosos cofactores encuentra
este un grupo de moléculas muy conocidas Quizá no con este papel vitamina B1 vitamina b2 nicotinamida ácido pa Vitamina b6 biotinas hidropónico vitamina B12 es decir todo el famoso complejo B funciona como cofactor enzimático ya sea porque Existen algunas vitaminas que son directamente con factores como es en el caso de la biotina o vitaminas que a través de un proceso de activación química funciona como cofactor como es el caso de la tiamina que actúa como pirofosfato de tiamina o porque la vitamina da parte de su molécula como precursor para la síntesis de esos cofactores como
observamos con la vitamina b2 la riboflavina que da origen Alfa o al fmn o la nicotinamida que de origen al nad y al Nat fosfato etcétera interesante en esta esta primera aproximación en la relación vitaminas con factores enzimáticos esenciales para la actividad de esa Ascensión la actividad enzimática no solamente Este es el resultado de la interacción entre los sustratos y el centro activo la actividad enzimática puede puede ser modificada por factores que pueden influir en esa relación obviamente la temperatura en primer término porque ya hemos hablado dada la naturaleza química de las enzimas de origen
proteico inclusive las ribosimas como arnés catalíticos están sujetas a los fenómenos de termolabilidad el pH la propia concentración de encima la concentración de sustrato y la presencia de sustancias que actúan como inhibidores son factores que afectan la actividad enzimática vamos a analizar un poco cada uno de estos en principio la temperatura si nosotros observamos un gráfico de variación de la actividad enzimática en función de la temperatura veremos esta representación como una representación común a la gran mayoría de las enzimas en donde hay este un punto en donde se observa su mayor actividad enzimática que es
lo que denominamos temperatura óptima podría ser una temperatura o un Rango de temperatura y hacia los extremos de esas temperaturas observamos Cómo se va perdiendo actividad enzimática interesante y lo dejo planteado para trabajar sobre la unidad porque este comportamiento a mayores temperaturas Y por qué este comportamiento a bajas temperaturas se los dejo como inquietud para que lo vayan pensando y que puedan este resolver alguna de las actividades que tenemos programadas para ustedes cuando analizamos el pH es decir la concentración de protones que se presenta en esa solución acuosa sí lo que observamos es un gráfico
en principio con estas características si ustedes quieren más bien universales sí en donde nuevamente observamos que hay un punto en donde hay una máxima actividad puedes tener evidencia que es lo que denominamos pH óptimo y que hacia digamos los lados de ese pH óptimo Se va perdiendo actividad enzimática Por supuesto que quizá diferencia lo que uno observa con la temperatura acá las curvas obtenidas pueden ser más variables Dado que los pH pueden estar en rangos y puede haber actividades a ph óptimos en distintos puntos de la escala de PH así podemos observar digamos enzimas con
pH óptimo cercanos a 7 enzimas con pH es óptimos más alcalinos enzimas con pH óptimo de rangos más amplios etcétera nuevamente van a tener una actividad para poder este interpretar Qué es lo que está sucediendo Sí en la medida que los phs se alejan del PH óptimo y que entonces la actividad enzimática Se va perdiendo concentración de encima cantidad masa de encima cuando yo analizo qué es lo que sucede con la actividad enzimática en función de la cantidad de enzima lo que observo es un gráfico con estas características básicamente lo que me está diciendo es
a medida que yo aumento la cantidad de encima aumento de manera proporcional la actividad enzimática sí algo que es bastante lógico más encima más actividad menos encima menos actividad cuando nosotros ponemos como eje de análisis qué es lo que sucede con la concentración de sustrato como un factor que afecta la actividad enzimática estamos poniendo en realidad como título de análisis a la cinética enzimática la cinética enzimática estudia la velocidad de las reacciones químicas que son catalizadas por las enzimas el estudio de cinética enzimática a través de modelos matemáticos es lo que permitió y siga permitiendo
tener una idea de cómo es el mecanismo catalítico de una idea de digamos la participación de esa enzima en un proceso metabólico determinado nos permite entender el control o La regulación que se puede establecer sobre la actividad de la cima a nivel celular nos permite entender la dinámica de digamos esa enzima en presencia de inhibidores de drogas de veneno este y en consecuencia poder este utilizarlas como estrategias de tipo terapéuticas a través de las modificaciones que puedan ser sobre su actividad este en cuestión algo que es interesante respecto de las enzimas y obviamente desde la
ribosimas tiene que ver con el concepto de centroactivo si yo Considero que una enzima tiene un centro activo obviamente hay un momento en donde para una cierta cantidad de enzima yo podré tener ocupado cada uno de esos centros activos por un sustrato Esa condición es la que nosotros definimos como saturación y es muy interesante porque una vez que una enzima está saturada no puede aumentar su capacidad catalítica porque ya está está toda la enzima en ese momento trabajando al máximo de su velocidad Así que es un concepto que también va a parecer más de de
uno en 1913 sí Leon micaellis Sí en Francia y madu-mente con una becaria este había ido a trabajar su laboratorio desde Estados Unidos escriben un trabajo que fue digamos este fundamental y fue el que definió lo que sucedió con el nacimiento enzimática para adelante Sí ellos plantean si plantean a través de una serie de experimentos y ciertas condiciones restrictivas que una enzima con un único sitio de Unión a sustrato cuando se une al sustrato forma un complejo encima sustrato caracterizado por la velocidad de formación y la velocidad de disociación de ese complejo enzima sustrato y
que en ese complejo enzima sustrato es donde ocurre el proceso catalítico que va de origen al producto y a la liberación de la enzima nuevamente a su estado original a través de una nueva velocidad de disociación del complejo encima producto encima más producto cuando ellos analizan sí en este contexto y algunas restricciones más que en este momento no vienen al caso ellos logran definir el comportamiento cinético de una enzima con estas características respecto de un sustrato y ellos demuestra que el comportamiento es una hipérbola cuadrada y logran definir entonces en la ecuación de la hipérbola
las dos constantes que definen un hipérbola por un lado la velocidad máxima la velocidad máxima definida como el punto de saturación de esa enzima es decir la concentración de sustrato necesaria para que la velocidad se mantenga constante esa sería la velocidad máxima Sí y hace referencia a la actividad Total que presenta Esa esa enzima sí por otro lado sí por otro lado definen a través de su ecuación matemática Sí una relación entre estas tres constantes que yo les comentaba sí la constante de formación del complejo enzima sustrato frente a las dos constantes de disociación del
complejo enzima sustrato Para volver a dar sustrato o para dar el producto sí matemáticamente esta relación de constantes termina siendo definida como constante de micael Y si mente y la podemos este definir diciendo que la constante de micaellis es la concentración de sustrato la concentración de sustrato que se necesita para alcanzar la mitad de la velocidad máxima de esa enzima cuando la enzima llega a la mitad de su velocidad máxima la concentración de sustrato que se necesitó para eso es lo que se define como constante de mi país es decir es una constante que tiene
como unidad la unidad del sustrato micromolar molar milivolar gramos la que esté considerándose Sí y ambas son constantes definidas en esa ecuación y le dan identidad es encima es decir Yo puedo aprovechar estas constantes para poder entender sí la identidad es encima y para poder a partir de estos dos parámetros analizar el comportamiento hacia encima respecto de varios sustratos el comportamiento de este es enzima respecto de otra enzima para un mismo sustrato etcétera hay una una forma de visualizar a la constante de micaellis en relación con el concepto de afinidad es decir la tendencia que
se forma el complejo encima sustrato o la tendencia a disociarse sí nuevamente a partir de deducción matemática uno lo que encuentre es una relación inversa entre constante de micaellis y afinidad podemos decir cuando los valores de la constante hídrica Deli son altos podemos hablar de una baja baja afinidad entre la enzima y el sustrato cuando los valores de la constante son bajos podemos hablar de una alta afinidad es decir si yo necesito poco sustrato para formar el complejo es porque realmente es encima Tiene alta afinidad por eso un sustrato y por eso rápidamente forma ese
complejo por otro lado y para terminar con este concepto de tenemos una tercer constante a tener en consideración que es muy interesante porque la constante de micaellis lo que me está diciendo es si ustedes quieren la afinidad para formar el complejo encima sustrato pero no me está diciendo cuánto producto se forma para poder entender la eficiencia catalítica es decir cuán entre comillas cuán buena es esa encima tenemos una tercera constante que es la que llamamos la constante catalítica la constante catalítica es como analizar un poco qué pasa con esta constante en donde el complejo enzima
sustrato o si ustedes quieren el complejo encima de producto termina generando el producto la constante catalítica nos dice el número de moléculas de sustrato convertidas por segundo Por eso habla de eficiencia catalítica Sí entonces a veces también es interesante porque yo puedo tener encima con mucha afinidad pero no tanta eficiencia catalítica enzimas con afinidad pero alta eficiencia catalítica Así es como digamos a través de la constante catalítica de la km y de la eficiencia catalítica porque una relación entre ambas yo puedo establecer las capacidades reales de los sistemas enzimáticos a nivel celular por ejemplo ya
que estuvimos Charlando hace un rato sobre el agua oxigenada la enzima encargada de acelerar la descomposición del peróxido de hidrógeno a nivel celular es la catalasa por eso es que cuando yo les mostré que colocábamos una gota de agua oxigenada sobre una gota de sangre se observaba cómo se aceleraba la reacción ahí podemos observar que el número de recambio es de 4 por 10 a las 7 es decir 40 millones 40 millones de moléculas de agua y oxígeno por segundo es lo que genera digamos la catalasa con una eficiencia catalítica dada su afinidad de 40
millones por segundo no lo mismo sucede con la nidrasacarbónica la enzima que se encarga de transformar Mejor dicho de transformar ser carga de acelerar la transformación de dióxido en bicarbonato Sí con una eficiencia catalítica que está en el orden de los entre dos y ocho millones de moléculas Sí este Y entonces permite entender digamos la capacidad de acelerar que tienen estas estas les planteo la siguiente situación una enzima que tiene la capacidad de poder catalizar la transformación de tres sustratos el sustrato 1 en el producto 1 el sustrato 2 en el producto 2 el sustrato
3 en el producto 3 Entonces desde el punto de vista biológico uno podría plantearse esta enzima Trabaja al azar con los tres sustratos si yo le oferto los tres sustratos o la enzima tiene alguna prioridad catalítica Cómo puede hacer para poder definir si hay un proceso azaroso o en realidad es un proceso catalítico preferencial uno de los instrumentos que tenemos es analizar la constante de micaellis Sí para cada uno de esos sustratos supongamos si supongamos que la constante de micaellis para el sustrato 1 es de 10 militar para el sustrato 2 es de 0 1
para el sustrato 3 es de uno lo que estaríamos diciendo es yo necesito 10 Mili molar de este sustrato para alcanzar el 50% de la actividad extensiva necesito 0,1 mínimo largo de este sustrato para alcanzar el 50% de la actividad catalítica y en el caso del sustrato 3 Necesito de uno mínimo molar con estos datos yo puedo predecir Cuál es el orden Entonces no azaroso sino el orden de preferencia catalítica cuando oferta estos tres sustratos claramente cuanto menos es la constante mcallis mayor es la afinidad y uno podría aún sin conocer la cantidad de catalítica
predecir que la preferencia va a estar sobre el sustrato 2 luego sobre sustrato 3 y en última instancia si hay realmente cantidad suficiente de sustrato 1 será el sustrato sí Entonces esto Me permite digamos por ejemplo interpretar cuando una enzima celular tiene más de un sustrato para catalizar si existe o no preferencia catalítica la segunda situación que les planteo es dos enzimas que pelean por el mismo sustrato nuevamente la inquietud es es un fenómeno al azar este sustrato puede ser tomado al azar por la enzima uno la enzima 2 o hay una preferencia de utilización
de ese sustrato de nuevo si yo les muestro que para la enzima 1 el km es de 10 y para el enzima 2 El km es de 01 nuevamente al igual que hicimos con el ejemplo anterior queda bastante en evidencia que la preferencia de reacción va a ser la de la enzima 2 al tener un menor km tiene mayor capacidad de poder a bajas concentraciones de sustratos catalizar las transformaciones de sustrato en el producto 2 Este es un interesante ejemplo de cómo nosotros vamos a poder utilizar esta información no vamos a trabajar en función de
los procesos matemáticos de la ecuación matemática de desarrollo matemático sino que lo que Nuestro objetivo es tratado por interpretar este este tipo de fenómenos a partir sí de estos parámetros cinéticos como el modelo micaellizmente es una curva y desde el punto de vista de el trabajo con curvas es muy complicado una vez que los trabajos de mililicementen fueron este considerados sí por el ámbito científico de los encimólogos comenzaron los trabajos para tratar de poder acomodar ese modelo a un modelo más es apto para poder a partir de los resultados obtenidos en el laboratorio piense que
estamos hablando de la década del 20 del 30 poder sacar toda esta información de los parámetros cinéticos Así es como uno varios y sigue habiendo este diseños matemáticos para poder hacer de este modelo un modelo más este apto para el trabajo la inmueble son los que plantean uno de los modelos más conocidos de transformación matemática del modelo de micalisismente la transformación matemática es una típica transformación para una hipérbola cuadrada y es hacer el doble recíproco es decir este aplicar uno sobre la velocidad 1 sobre la concentración de sustrato y entonces a partir de este desarrollo
matemático obtener la ecuación de una recta como yo para construir una curva necesito muchísimos puntos pero para poder construir una recta necesito solamente dos las transformaciones lineales lo que permiten es tener un número más reducido de puntos de análisis y la posibilidad de poder prolongar en el gráfico estas rectas de tal manera que en estos gráficos lineales también Sí también al igual que vimos en los gráficos originales de picanes y mente podemos encontrar representados ambos parámetros síndicos cuando la curva corta el eje y ahí Tenemos uno sobre la velocidad máxima cuando la recta corta el
eje x ahí tenemos el valor de -1 sobre caer por lo tanto experimentalmente yo si tengo una curva puedo perfectamente a partir de estos números obtener los datos de velocidad máxima y de km siempre siempre con la precaución de reconocer que estos son dobles recíprocos por lo tanto tendré que invertir el número para poder tener el número ahora no todas las enzimas cumplen con la cinética de micalecimiento recordemos que habíamos dicho que su modelo Que Tiene ciertas restricciones por ejemplo un solo sustrato una digamos única centro activo aquellas enzimas que no cumplen con esta cinética
micaelana las conocemos como enzimas de tipo alostéricas y estas enzimas de tipolostéricas suelen responder a dos modelos este en donde por ejemplo en un caso o un sustrato favorece la unión de un segundo tercer sustrato es decir interacciones de tipo homotrópicas Sí el sustrato trabaja sobre la interacción de otros sustratos o la presencia de otras sustancias que pueden favorecer o no favorecer la unión del sustrato en este caso lo que llamamos interacciones heterotrópicas así como no todas las enzimas siguen una cinética de mi calcimenten la gran mayoría de las enzimas utilizan más de un sustrato
por eso hablamos en general de reacciones multisustrato y estas reacciones multisustrato pueden ser reacciones de tipo secuencial es decir en donde los sustratos de manera ordenada o al azar van este uniéndose al centro activo para generar los productos correspondientes o a través de un sistema denominado de tipo ping pong en donde el ingreso de un sustrato genera un producto que permite a su vez el ingreso de un segundo sustrato para generar un este segundo producto etcétera Ahora sí creo que a esta altura ya tenemos algunas respuestas respecto a nuestra famosa hamburguesa indudablemente en nuestro tracto
digestivo la presencia de enzimas específicas son las que permiten catalizar y arreglarlas descomposición de las moléculas que constituye nuestros alimentos y en ese sentido permite la obtención de los nutrientes una manera sumamente eficiente y nos obliga a tener que de manera tan frecuente como reconocemos ingerir nuevos alimentos de acuerdo a las necesidades imperantes por el otro lado la enorme eficiencia catalítica que presenta la aniversasa carbónica eje las que nos permite entender Por qué razón no estamos intoxicados con el dióxido de carbono Sí su capacidad catalítica su constante catalítica su número de recambio es enorme Y
entonces permite que ese dióxido generado en forma continua y en grandes cantidades por todas nuestras células con metabolismo aeróbico rápidamente puede hacer este transformado en bicarbonato para que circule de una manera no tóxica por la sangre y que a nivel de los pulmones rápidamente puede hacer de nuevo este transformando en dióxido para que a través de la espiración este lo podamos eliminar de nuestro cuerpo Les propongo entonces que hagamos un racconto de los temas que estuvimos analizando a través de una serie de ideas claves los catalizadores aceleran la velocidad de una reacción porque disminuyen la
energía de activación entre otras propiedades permanecen en alterados al final de la reacción y no modifican la constante de equilibrio en aquella reacciones reversibles los catalizadores orgánicos son muy eficaces específicos y dadas su naturaleza proteica o de ácido ribonucleico termolábiles los factores sean coenzimas o grupos prostéticos orgánicos e inorgánicos son esenciales en la catálisis algunos con factores son vitaminas Como por ejemplo la biotina o vitaminas activadas por ejemplo el piro fosfato de tiamina otros son derivados de vitaminas del complejo b o en algunos casos parte de la estructura de una vitamina que es utilizada como
precursor para la síntesis del cofactor ahí encontramos la ripoplandia para el fad el fmn la niacina parednad etcétera cuando los sustratos se unen al sitio activo de una enzima inducen cambios conformacionales mutuos entre ambos que facilitan el reconocimiento del sustrato y del proceso catalítico la temperatura el pH la concentración de enzima la concentración de sustrato y los inhibidores como veremos en otras oportunidades afectan la actividad de las enzimas para el modelo de micales y mente la constante de micaellis y la velocidad máxima son los parámetros cinéticos que caracterizan el encima la constante catalítica o número
de recambio es el número máximo de molécula de sustrato que se transforman en producto las transformaciones de la web simplifica la determinación de cae y de máxima y permite para realizar análisis comparativo entre enzimas y sustratos los espero entonces para completar nuestro análisis sobre los contenidos de la unidad 2 básicamente inhibición enzimática y regulación de la actividad enzimática en el próximo encuentro hasta luego