fala pessoal que o professor tiago este é o canal físico químico em cinco minutos no vídeo de hoje vou falar sobre equilíbrio químico tão pessoal equilíbrio químico é um dos conceitos mais importantes da físico química e da química como um todo mas ele é freqüentemente mal compreendido é muito comum ver os alunos da área em definições que não estão corretas a respeito do equilíbrio para deixar bem claro já de início o pessoal estar em equilíbrio é não entender a mudança aqui é um ponto bem importantes quando se diz que uma reação está em equilíbrio o
que fazes estão em equilíbrio está dizendo que o sistema não tende a mudança ok um sistema equilíbrio não apresenta mudanças nas suas propriedades com o tempo a menos que variáveis como pressão e temperaturas sejam alteradas quem já estudou até mo dinâmica sabe que tendência a mudança tem a ver com a segunda lei da termodinâmica e é bem importante ter em mente que o conceito de equilíbrio equilíbrio químico deriva da segunda lei a gente pode resumir a segunda lei nessa equação delta essa do universo é maior ou igual a 0 aí boa vontade vale para processos
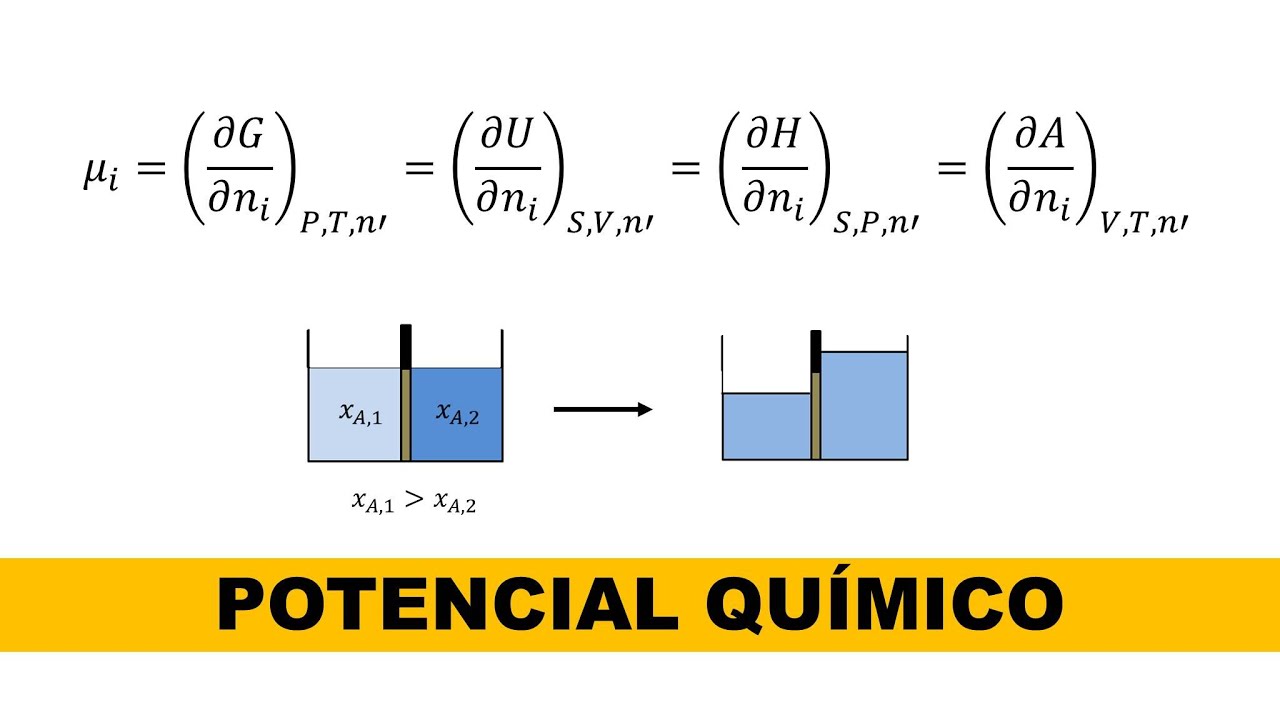
reversíveis que são ideais e de realizações todo o processo acontece com um aumento da entropia do universo sendo um universo à soma do sistema mais a vizinhança a gente pode interpretar essa equação dizendo que mudanças espontâneas ocorre na direção do aumento da entropia ok mas quando a gente está trabalhando pessoal um sistema químico muitas vezes é mais conveniente falar de espontaneidade em termos da energia livre de gipsy que eu representar aqui por g e daí a gente não precisa olhar pra entropia da vizinhança ok ea relação entre delta g e a entropia variação da entropia
do universo é dado pela equação mostrar aqui pessoal que a pt constantes processos espontâneos ocorrem com delta g negativo o processo espontâneo resulta no aumento de s a gente vai ter um delta g negativo em outras palavras mudanças espontâneas ocorre na direção da diminuição de g que essa definição fica clara e é muito didático de mostrar pessoal no estudo de equilíbrio de reações químicas vamos considerar por exemplo uma reação genérica de um gazza se decompondo formando um gás b ali o a menos que o minúsculo seriam os coeficientes de que o método quem então vamos
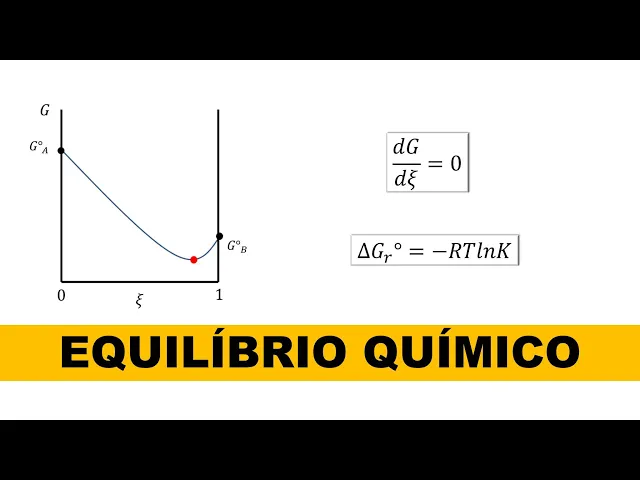
analisar como varia a energia livre de um sistema que inicialmente só têm um gás a com o avanço da reação o avanço da reação eu vou representar aqui por essa letra grega chamada alice por conveniência vamos considerar que a reação ocorre na pressão de um barco então esse diagrama que você tá vendo mostra e g em função do grau de avanço da reação que se como é que a gente interpreta esse grau de avanço quando o grau de avanço é zero eu tenho exclusivamente reagente então ali na reta sobre que sigo a 0 eu vou
ter a energia livre do gás a que a nossa reação ngassa formando b porque o outro lado quando o grau de avanço da reação é 100% quantia presente por um europeu o produto então sobre a reta que está ali sobre o que esse gol eu vou ter a energia livre do produto b aqui eu botei g grau a e o símbolo de grau indica que é o valor padrão na pressão de um bar que essa diferença pessoal do g patrão doha e do g padrão do b da o que a gente chama de bell tajra
e padrão da reação que é o que a gente calcula quando a gente faz a diferença entre delta g de formação do produto - o delta g de informação do reagente como mostrando aqui nessa equação a linha azul pessoal que o desenho que agora ela mostra como varia energia livre o sistema com um avanço da reação quando a gente segue a linha azul esse guazzelli apex igual a 1 ou seja está considerando que a reação está acontecendo a gente observa que já que diminui com grau de avanço da reação ok até chegar a um ponto
de mínimo estou aqui nesse exemplo que estou mostrando pessoal eu botei o valor db abaixo do valor de ar que isso é variável acho que assim ficou um pouco mais de idade contam com o transcorrer da reação pessoal a gente tem que o sistema vai mudando do ponto zero o ponto 1 ponto 2 e assim por diante até chegar no ponto 5 que eu marquei em vermelho ok então o sistema ele vai mudar espontaneamente decomposição até atingir esse ponto vermelho e ao chegar no ponto vermelho o sistema não mais mudará porque isso é o que
a gente viu que o processo espontâneo é sempre na direção de diminuir g se o sistema está em 5 no ponto 5 para qualquer lado que ele vá realmente então o sistema chega ali e não sai mais da le coq em outras palavras quando o sistema chega ao ponto vermelho ele se encontra o equilíbrio porque ele não tem demais a mudar ok daquele ponto inicial quando tenha puro até o ponto vermelho nós temos uma diminuição de g então o sistema vai entendendo até o mínimo e uma vez que ele chega no mínimo ele não tem
demais a mudança o que isso significa que se a pressão ea temperatura permanecer em constantes a quantidade de produto ea gente não vai mais alterar com o tempo então se você tem uma reação que está em equilíbrio se você não muda a pressão e temperatura a proporção de reagente o produto não vai mudar não adianta você esperar horas e horas que você não vai mais obter produtos e vai precisar ou alterar a temperatura ou remover o produto do equilíbrio e ponto bem importante pessoal dizer que uma reação está equilíbrio não significa dizer que é uma
mesma quantidade o duto tem gente no meio essa é uma confusão muito comum ok então nesse exemplo que odeia pessoal o sistema chega em equilíbrio com uma quantidade mostrar vale pela linha traz tracejada entre o produto ea gente ok então a língua o tempo ter um grau de avanço de reação de aproximadamente 90% ok então eu vou ter ali uma quantidade de produto e reagente é relativa a esse grau de avanço de reação ponto importante dependendo do valor do delta g padrão esse mesmo pode estar bastante deslocar inclusive isso delta g padrão for positivo um
menino pode estar bem próximo a um grau de avanço igual a zero que em uma maneira conveniente se expressar as quantidades de reagentes e produtos em determinado momento da reação é por meio do chamado consciente de reação que eu vou representar aqui por um que o consciente de reação tem a mesma forma da constante de equilíbrio que a gente usa esse termo consciente de reação como a gente vai escrever para o momento qualquer um para nossa reação pessoal de um gás à romano gaius b consciente da reação nada mais será consciente de reação será simplesmente
a razão entre a pressão parcial do produto elevado o seu coeficiente que o métrico sobre a pressão parcial do reagente também levaram seu coeficiente que o médico para cada momento da reação a gente pode escrever a equação destacado na caixa vermelha delta g é igual ao delta g padrão da reação mas rtl é de que sendo que o consciente da reação aqui outro ponto muito importante o que que é esse primeiro delta g que aparece ali que está o segundo delta g o delta g padrão a gente já viu naquele dia a grama é a
diferença entre o g do reagente e dos produtos ambos purus na pressão de um barco que esse primeiro belta jessen o símbolo do grau pessoal é a derivada de gekko grau de avanço da reação que os livros mais rigorosos inclusive escreve essa equação como dg desse igual a delta g padrão e etc o que significa ser elevada vamos pegar que a curva que a gente estava analisando se eu quero saber o valor de delta g num certo ponto chegamos àquele ponto preto ali eu passo uma reta tangente e à inclinação nessa reta tangente vai me
dar o valor de delta g observa que um ponto bem importante com o decorrer da reação o delta g que essa derivada muda logo mais quanto vale do itajaí e no equilíbrio mas esse bell tajra e padrão ele é constante o que o delta g padrão ele só muda se variar temperatura como a gente vai ver logo mais o que é importante observar pessoal que no equilíbrio o delta g que é derivada é igual a zero ok isso porque no ponto de mínimo a reta tangente tem inclinação nua e nesse ponto a gente pode escrever
aí começa mostrando a língua slide que rearranja para essa equação que é muito importante delta g padrão de reação é igual a menos a retê lnd caac o substituiu que pelo cá porque como eu falei antes o consciente de rede reação no equilíbrio é a constante de equilíbrio aqui essa equação destacado na caixa preta é muito importante porque o valor da constante kahn pode ser obtido teoricamente a partir dos valores de energia livre de formação que são tabelados se você pega o livro doático por exemplo você tem no final uma sessão de dados com valores
de delta g de informação a gente pode utilizar a aplicar aquela forma de produto - é agente calcular o delta g padrão da reação e calcular o valor ficar ok então se você gostou desse vídeo de um like se inscreva no canal ativo as notificações e fique ligado nas novidades se você tiver dúvida deixe suas perguntas nos comentários valeu pessoal