fala galerinha do Miss salva estamos começando mais uma aula do nosso módulo de ligações químicas e nessa aula a gente vai falar um pouquinho melhor sobre os compostos que fazem ligações covalentes Então vamos falar um pouquinho melhor na verdade das formas que a gente pode representar esses compostos covalentes ou seja nessas formas de representação a gente chama elas de fórmulas e a gente tem alguns tipos aí diferentes de fórmulas de maneiras de representar então esses compostos covalentes Mas antes a gente tem que entender um pouquinho como é que esses compostos se comportam Ou pelo menos
os átomos que fazem essas ligações se comportam a gente tem que lembrar um pouquinho que bom se a gente olhar a tabela periódica né a gente sabe que ã os compostos covalentes eles ã são formados por ligação entre ametais Então são esses elementos que estão aqui ó tá vendo esse tracejados ametais estão para cima e os metais para baixo certo lembrar que os gases nobres eles geralmente não fazem ligações químicas né só em condições bem extremas aí e aí a gente tem por exemplo fluor cloro bromo iodo aqui são halogênios Então os elementos aqui do
grupo 17 a gente chama eles de halogênios como cloro bromo iodo aí que vocês viram fluor os halogênios eles se ligam compartilhando Um elétron isso quer dizer que em geral eles fazem apenas uma ligação certo Por isso que a gente diz que eles são monovalentes eles têm apenas um elétron Zinho lá na última camada na camada de valência por isso que a gente chama eles de monovalente eles vão compartilhar aquele único elétron por isso vão fazer apenas uma ligação se a gente observar né do ladinho esquerdo dos halogênios a gente tem o oxigênio o enxofre
o selênio que são os elementos do grupo 16 esses elementos são chamados de calcogênios então eles são do grupo 16 e eles vão compartilhar Quando forem fazer ligações dois elétrons certo nas ligações covalentes ou seja ligações com outros metais né não esqueçam disso portanto em geral eles fazem duas ligações é por isso que a gente diz que eles são bivalentes certo eles vão fazer lá duas ligações bivalentes se a gente olhar novamente mais à esquerda né a gente vai encontrar ali o grupo do nitrogênio ou a família do nitrogênio tem baixo fósforo e assim por
diante bom esses elementos quando eles fizerem ligações covalentes eles vão compartilhar três elétrons por isso que em geral eles fazem três ligações e eles são chamados de trivalentes por conta disso e por fim mas não menos importante nós temos né então o nitrogênio que era do grupo 15 nós temos o grupo 14 que é o grupo ou a família do Carbo que a gente olha aqui né o carbono silício e esses elementos eles vão Quando fizerem ligações covalentes compartilhar quatro elétrons então em geral eles fazem quatro ligações e é por isso que nós chamamos eles
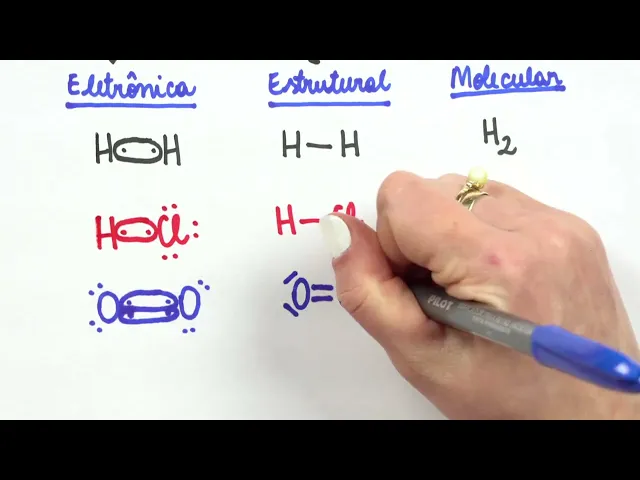
de tetra Valentes Lembrando que isso em relação ao carbono vai ser muito importante quando vocês estudarem né química orgânica que fala muito sobre carbono bom dito isso né a gente tem que entender um pouquinho como representar esses elementos essas substâncias formadas por eh átomos de ametais né que vão fazer ligações covalentes a gente tem três maneiras de representar a gente tem a fórmula eletrônica a fórmula estrutural e a fórmula molecular então vocês viram que na aula na outra aula por exemplo a gente tava representando o hidrogênio né o hidrogênio que vai fazer ali uma ligaçãozinha
só ele vai ser que nem os halogênios né vai ser monovalente representar eletronicamente o hidrogênio o hidrogênio ele fica estável com dois elétrons né é um dos poucos elementos que fica estável aí só com dois elétrons na última camada e lembrando como eles fazem ligação covalente eles compartilham esses dois elétrons certo então essa seria a representação eletrônica como que eu represento estruturalmente eu coloco os dois hidrogênios e só faço um tracinho que representa a única ligação que existe entre eles já a fórmula molecular é H2 né como a gente escreve geralmente certo vou dar aqui
mais alguns exemplos se a gente por exemplo observar o hcl o hcl ele é formado então né Por um hidrogênio o hidrogênio que tem um eletroninho só na última camada e o cloro que tem sete elétrons mas que é monovalente que vai compartilhar apenas um elétron e assim então eu represento a fórmula eletrônica do ácido clorídrico do hcl certo o cloro fica estável com oito sete que ele já tinha mais um que ele compartilhou ali com o hidrogênio e o hidrogênio fica estável com dois o que ele já tinha e o que ele compartilhou ali
com o cloro a fórmula estrutural ó só uma ligação é bem parecida né com H2 e a fórmula molecular é hcl bom até que tranquilo né Mas agora vamos representar então por exemplo o O2 o O2 né que a fórmula molecular é como vocês conhecem O2 o oxigênio gente o oxigênio Ele tem seis eletron zinhos lá na última camada então ele vai ter seis elétrons e quando ele se ligar a outro oxigênio que também tem seis elétrons lembrando né que o oxigênio ele é da família dos calcogênios então ele vai ele é bivalente ele vai
fazer duas ligações então ele vai compartilhar cada oxigênio vai compartilhar dois eletron zinhos certo Ficou ali meio ruim Ó mas tá ali os elétrons Então essa seria a representação eletrônica com todos os elétrons quando eu desenho a fórmula estrutural bom agora né eu tenho duas ligações covalentes portanto eu tenho que colocar aqui dois tracinhos alguns eh alguns autores alguns pesquisadores Também Gostam de representar os elétrons não ligantes E daí eles desenham assim ó por exemplo Como o oxigênio tem dois pares não ligantes cada tracinho representa um par não ligante então pode encontrar desenhado assim também
com os pares de elétrons não ligantes certo a gente a gente poderia desenhar aqui no cloro também ó se a gente quisesse os três pares de elétrons não ligantes do cloro bom continuando né a gente também tem por exemplo a água h2oo mundo sabe que a fórmula molecular da água é h2oo a fórmula eletrônica da água bom eu tenho lá um hidrogênio um oxigênio e mais um hidrogênio são dois hidrogênios né cada hidrogênio tem um eletroninho e vai fazer uma ligação né e o oxigênio ele tem lá o seu seis elétrons e ele faz duas
ligações ele compartilha dois dos seus elétrons então a representação da Fórmula eletrônica da água fica exatamente assim ó o oxigênio compartilhando cada um dos seus elétrons né com um hidrogênio e o hidrogênio também compartilhando cada hidrogênio compartilhando um elétron ali com o oxigênio a representação estrutural fica assim né nesse formato aqui certo podemos desenhar ali os pares de elétrons não ligantes no oxigênio se a gente quiser outra molécula que aparece bastante em prova eu sempre dou Exemplo né das substâncias que aparecem bastante é o CO2 que contribui lá né pro aquecimento global o aumento da
concentração de CO2 contribui para o efeito estufa o agravamento do efeito de estufa como é que eu faço né o desenho da Fórmula eletrônica do CO2 bom pessoal a gente viu ali que o oxigênio vai ter seis elétrons né na última camada e o carbono tem quatro mas o que a gente tem que saber aqui é que cada oxigênio compartilha dois e cada carbono carbono é tetravalente se o oxigênio é bivalente o carbono é tetravalente então o carbono vai fazer quatro né ligações e vejam Como isso acontece ó aqui né então o carbono faz duas
ligações com esse oxigênio que já fez as suas duas ligações já está estável e o carbono ainda faz mais duas ligações com o outro oxigênio que também precisava de duas ligações né e agora de fato a gente tem o carbono fazendo quatro ligações e o oxigênio duas compartilhando seus dois elétrons cada né portanto a entação estrutural do CO2 fica exatamente assim vou dar aqui um último exemplo Zinho de uma substância que cai bastante também que é a amônia o nh3 o nh3 a gente tem que lembrar né Para dar um exemplo de um elemento trivalente
a gente tem que lembrar que o nitrogênio ele vai fazer três ligações ele compartilha três elétrons enquanto cada um dos hidrogênios faz apenas uma ligação né compartilha apenas um elétron e assim isso acontece ó o nitrogênio vai fazer uma ligação com cada um desses hidrogênios E aí ele faz aqui as suas três ligações enquanto cada hidrogênio ali faz as suas duas ligações então por exemplo a gente tem que lembrar que os elétrons compartilhados eles pertencem tanto a o átomo de hidrogênio aqui nesse caso quanto ao nitrogênio então por exemplo esse hidrogênio ele tem dois elétrons
esse também esse também o nitrogênio ele tinha 1 2 3 4 5 mais 6 7 8 de cada ligação que ele fez e aí a representação né da fórmula estrutural da amônia do nh3 é assim Lembrando que a gente pode fazer ali o tracinho para representar os pares de elétrons não ligantes aqui também o oxigênio ó do CO2 a gente poderia ter colocado bom Pessoal espero que tenha ficado Claro para vocês e dica no módulo de forças intermoleculares é que a gente vai falar sobre polaridade e sobre geometria molecular e aí vocês vão entender Por
que as fórmulas estruturais também ficam inclinad dinhas às vezes ou em linha certo espero que tenha ficado Claro e até a próxima aula