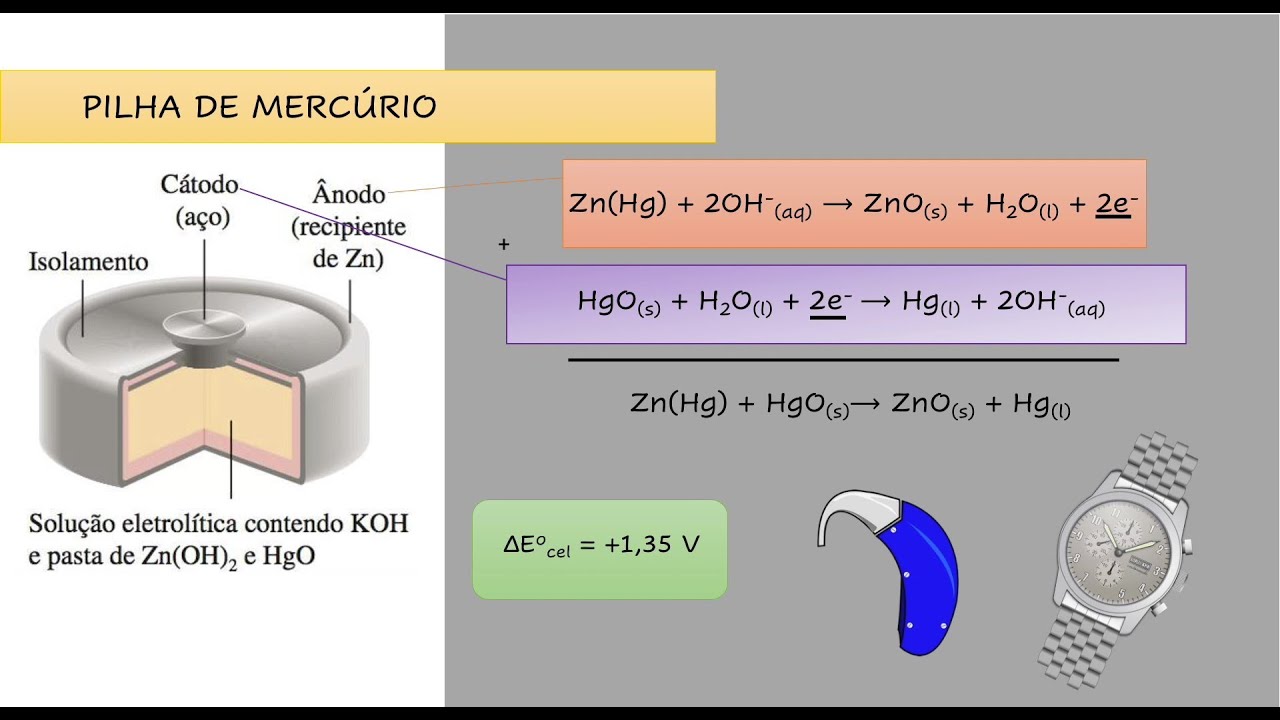
E aí [Música] o Olá no vídeo anterior Vimos um pouco sobre a história das pilhas e como elas foram evoluindo com o passar dos anos Hoje iremos tratar especificamente de células galvânicas e não deixam de ser o caso de pilhas e baterias dessa forma iremos construir uma famosa célula galvânica passo a passo com base em alguns conceitos já vistos na temporada de introdução eletroquímica e ao final da vídeo aula aprenderemos um pequeno macete com algumas palavras-chave que pode auxiliar Em algumas ocasiões as é uma célula galvânica consiste na produção de corrente elétrica ou seja energia
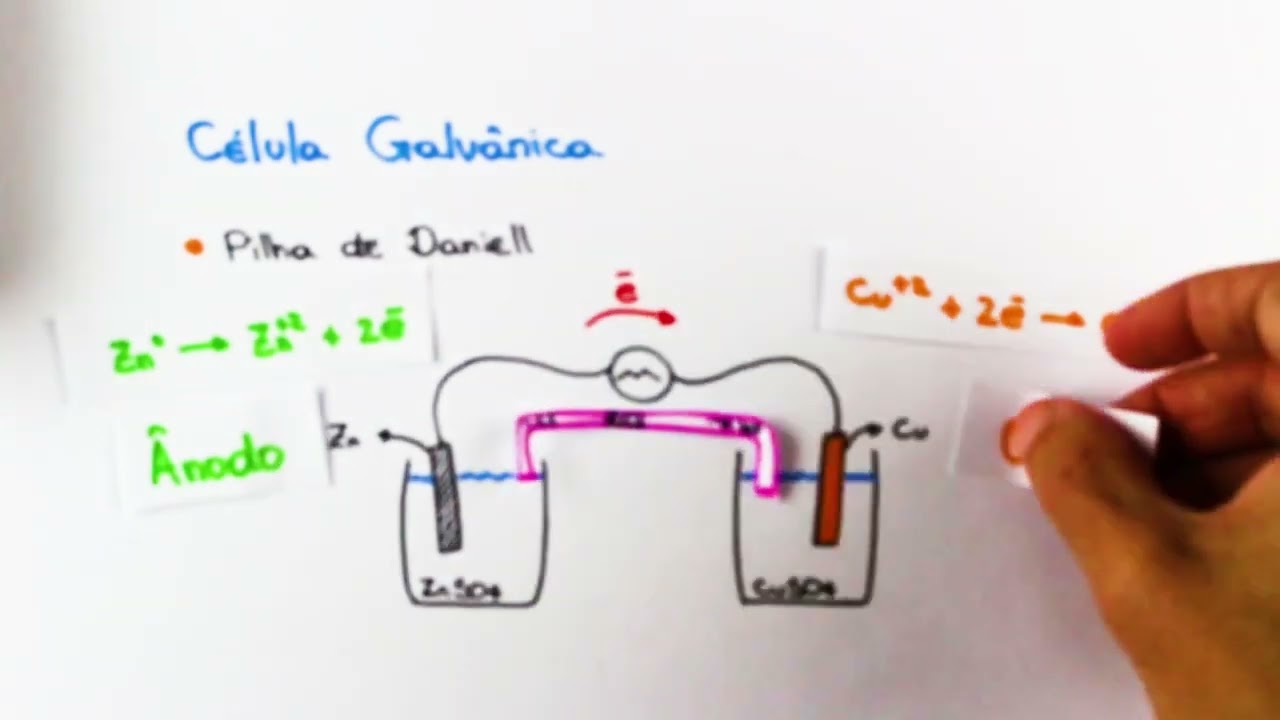
elétrica a partir de reações de oxirredução espontânea um exemplo clássico desse tipo de célula é a pele Daniel tem muito cobrado em diversas avaliações no Brasil portanto é com base nela queremos estudar as células galvânicas e a pilha de daniell é constituída por duas placas metálicas chamadas de eletrodos um de zinco e o outro de cobre e eles são ligados externamente por um fio condutor o eletrodo de zinco está imerso em uma solução de sulfato de zinco e o eletrodo de cobre em uma solução de sulfato de cobre essas soluções estão ligadas através de uma
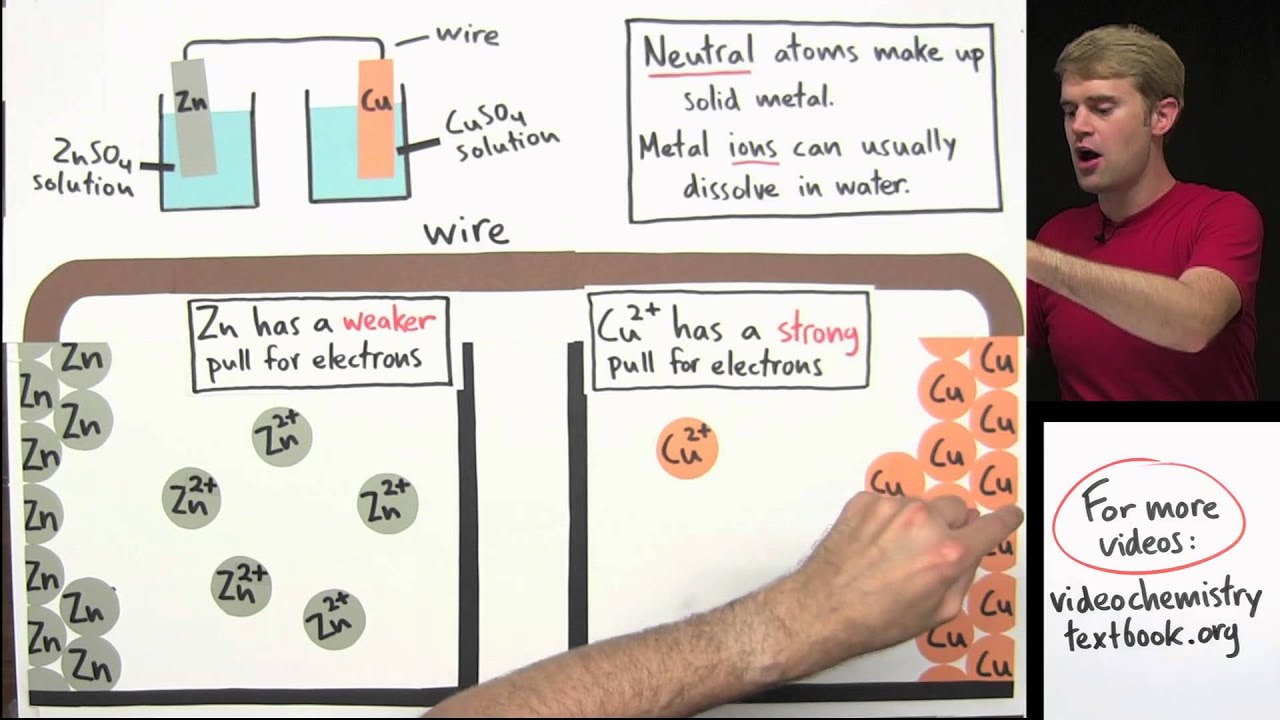
ponte Salina e consiste em um tubo contendo uma solução de um sal como cloreto de potássio Este é um Panorama geral da pilha de de neon com uma célula galvânica para podermos introduzir novos conceitos e construir uma linha de raciocínio bacana para aula vamos começar analisando o potencial padrão de redução dos eletrodos em questão e você lembra o que essa grandeza nos indica isso mesmo a tendência com que o eletrodo tem em reduzir o oxidar dessa forma como potencial de redução do cobre é maior que o dos zinco podemos afirmar que o cobre é espécie
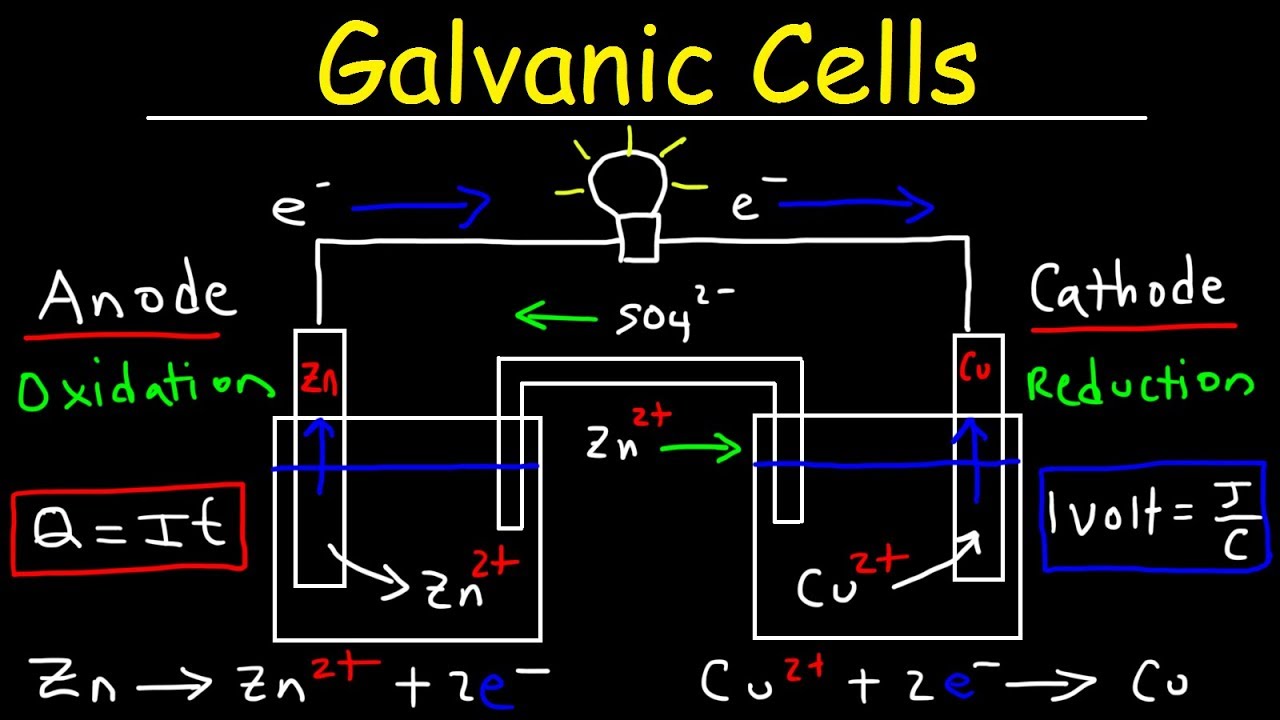
que reduz e o zinco é quem oxida sem que haja a aplicação de uma fonte externa de energia e agora para melhor compreendermos alguns conceitos podemos separar essa célula eletroquímica em duas semicélulas assim teremos assim célula do cobre EA semi-célula do cinco Então como acabamos de ver na semi-célula do cobre ocorre a redução e nascendo célula do 5 a oxidação para facilitar os estudos foi convencionado para células galvânicas que o eletrodo em que ocorre a redução é chamado de Cá tudo e ele é o pólo positivo por outro lado o eletrodo que sofre oxidação é
denominado ando que ao pólo negativo da célula nesta forma na pilha de daniell o eletrodo de cobre é o caso do e o eletrodo de Zinco é o ânodo e como já sabemos o 5 a oxidar perde elétrons e esses são recebido pelo cobre essa transferência de elétrons ocorre através do Fio condutor ligado ao sistema esse movimento ordenado de portadores de carga elétrica nada mais é do que a corrente elétrica que é ocasionada pela diferença de potencial a ddp entre os eletrodos ou seja através de um processo espontâneo a produção de energia elétrica que é
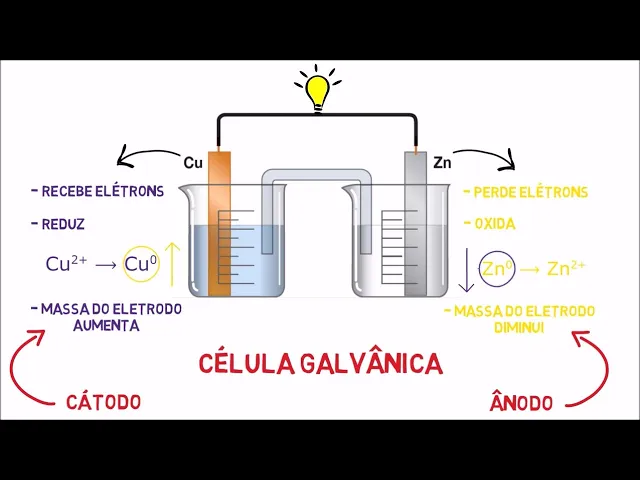
capaz de acender uma lâmpada como mostra a figura perceba também que esse movimento de elétrons acontece do 5 para o cobre ou seja do polo negativo para o positivo que o sentido real da corrente elétrica e agora vejamos o que ocorre com os eletrodos em questão o cobre como vimos recebe os elétrons perdidos pelo 5 e reduz ou seja ele passa de cobre dois mais para cobre zero assim é formado cada vez mais cobre metálico que é o cobre fizeram Esse cobre metálico é depositado então na própria placa de cobre logo você deve concordar comigo
que a massa do eletrodo de cobre aumenta por outro lado o zinco perde os elétrons e sofre oxidação passando de 50 para 52 mais isto é o 5 que antes era metálico passa para a solução na forma de íons zinco dois mais dessa forma o eletrodo de zinco sofre corrosão e portanto farmácia diminui com isso pode-se dizer que em uma célula galvânica a massa do eletrodo aumenta no catodo e no ano do a massa do eletrodo diminuem é a figura a seguir serve para ajudar a visualizar o aumento e diminuição das massas dos eletrodos bom
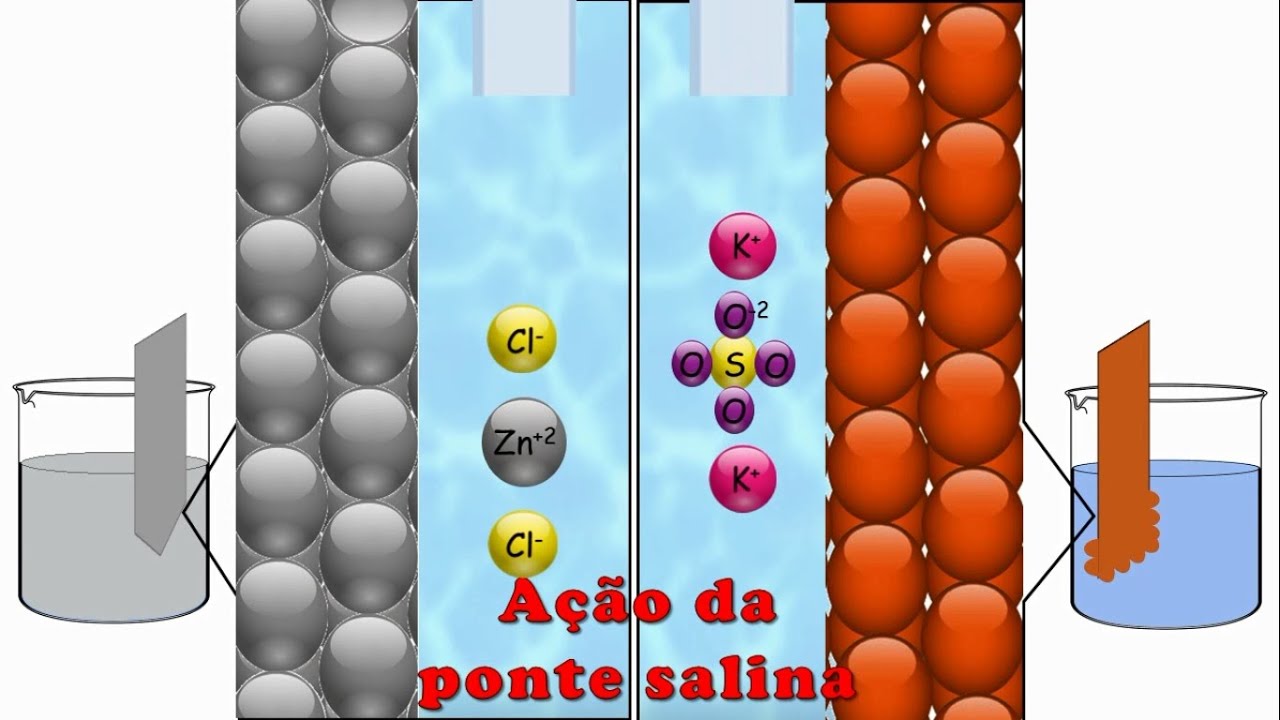
e para que serve a ponte Salina como acabamos de ver nós temos célula do cobre usei uns cobres dois mais que estavam inicialmente de solução faça uma ser cobre metálico dessa forma começará a ter um excesso de um sulfato em solução já nasceram célula do zinco o zinco que inicialmente era metálico passa a solução como 52 Março o que ocasionará em um excesso de 15 em solução se permanecesse dessa maneira atrapalha o fluxo de elétrons no fio condutor da célula fazendo com que a pilha parasse de funcionar então para solucionar esse problema é ligado uma
ponte Salina as soluções o sal dissociado vai fazer com que a quantidade de cátions e ânions em solução fique em equilíbrio prolongando o funcionamento da pilha é bom aqui terminamos de construir conceituar a pilha de daniell perceba que quando se cria uma linha de raciocínio não é difícil de memorizar traz conceitos Pois é só uma questão de exercício mental diz que foram realmente aprendido as suas definições agora vamos supor que deu aquele branco durante uma prova importante uma seita a seguir pode ajudar com palavras-chave e Serviu de estopim para você relembrar o funcionamento de uma
célula galvânica teorema da dona porca O amido é o polo negativo é onde ocorre a oxidação EA massa do seu eletrodo diminui o cátodo é o pólo positivo é aonde ocorre a redução e a massa do seu eletrodo aumenta é isso Você pode escrever Dona porca e treinar o preenchimento das palavras a partir da Letra Inicial assim vai ser difícil você esquecer os principais conceitos no entanto isso é apenas uma sente estude como realmente funciona uma célula galvânica que você irá compreender o conteúdo com mais facilidade e essa foi o vídeo aula de hoje no
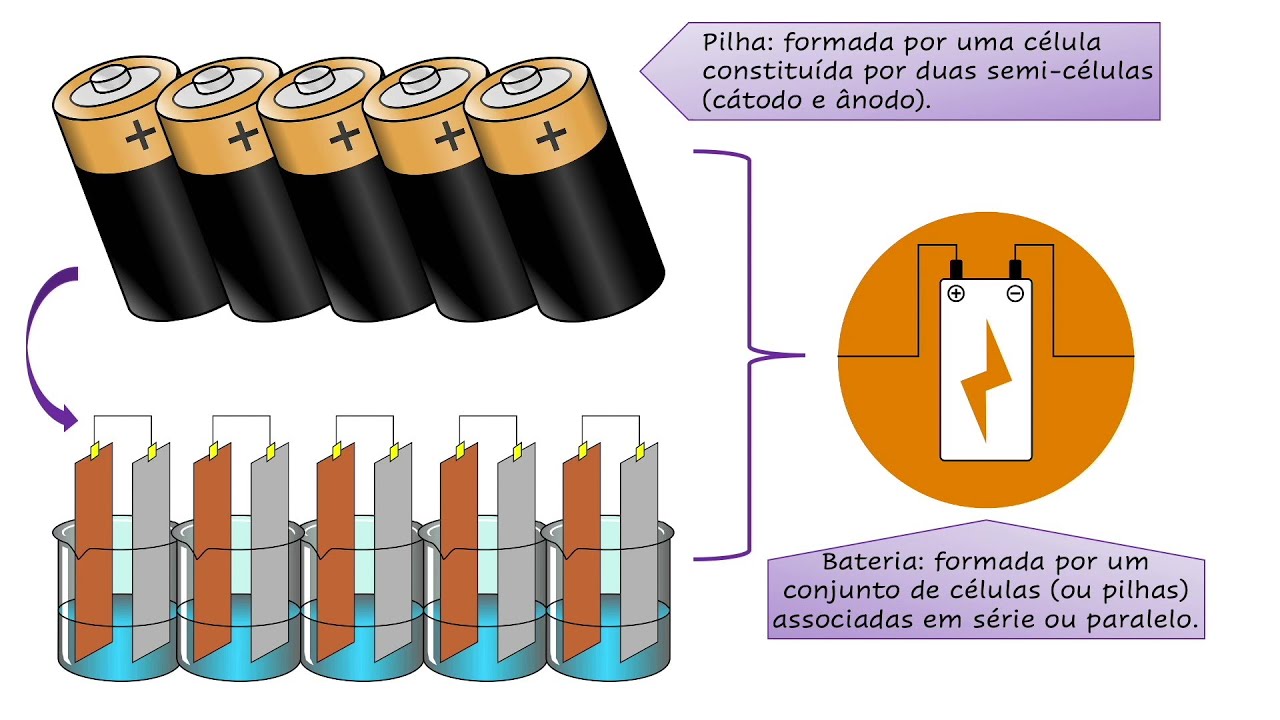
próximo episódio iremos ver como funciona as baterias Será que elas podem ser utilizadas como sinônimo de pilhas Qual a relação entre elas o sistema na semana que vem aqui no canal do cliente até mais E aí [Música]










![Pilhas ou célula galvânica [Módulo 16 - Aula 03]](https://img.youtube.com/vi/ahzLUFVTugg/maxresdefault.jpg)